Тактика вакцинации детей с хроническими заболеваниями
СтатьиОпубликовано в журнале:
Практика педиатра
Март, 2007
С.М. Харит, Е.А. Лакоткина, Т.В. Черняева, ФГУ «НИИ детских инфекций» Росздрава, г. Санкт-Петербург
Вакцинация имеет более чем двухсотлетнюю историю, и за это время международный опыт показал, что прививки – самое эффективное и экономически оправданное средство, позволяющее контролировать инфекции.
Однако периодически появляются публикации, в которых подвергается сомнению безопасность и эффективность прививок. Действительно, вакцинный препарат вызывает сложную цепь реакций, результатом которых является создание специфического иммунитета, но возможна и активация «побочных» иммунологических процессов, характер и интенсивность которых зависят от типа вакцины (живая или неживая), иммуногенетических особенностей привитого. Для того чтобы оценить, существуют ли проблемы при вакцинации детей с различным состоянием здоровья, и определить меры их профилактики, в ФГУ «НИИ детских инфекций» Росздрава проводились вакцинация и наблюдение за разными группами детей.
Объект и методы исследования
Под наблюдением находилось 673 ребенка (табл.1) в возрасте от 3-х месяцев до 7 лет, которых прививали в соответствии с календарем прививок и наставлениями к вакцинам АКДС (АДС) и коревой. За привитыми детьми осуществляли клиническое наблюдение: в течение месяца ежедневно и далее 1-2 года – периодически.
Таблица 1
Характеристика состояния здоровья привитых против кори и дифтерии детей
| Группы детей по состоянию здоровья | Всего детей | Привиты | |
|---|---|---|---|
| АКДС/АДС | против кори | ||
| Аллергические заболевания (бронхиальная астма, атопический дерматит) | 105 (33/72) | 32 (8/24) | 73 (25/48) |
| Органические поражения ЦНС, в том числе болезнь Дауна | 154 21 | 63 10 | 91 11 |
| Судорожный синдром, эпилепсия | 95 | 41 | 54 |
| Детский церебральный паралич (ДЦП) | 38 | 12 | 26 |
| Системные заболевания соединительной ткани (АИЗ) | 30 | 30 | 28 |
| Часто болеющие (ДЧБ) | 129 | 18 | 111 |
| Онкологические заболевания (солидные опухоли, острый лимфобластный лейкоз) | 42 (18/24) | 42 (18/24) | 42 (18/24) |
| ВИЧ-инфицированные (В-23) | 34 | 34 | 34 |
| С перинатальным контактом по ВИЧ (R-75) | 115 | 115 | 42 |
| Здоровые | 64 | 16 | 48 |
Поствакцинальный период оценивали по общепринятым критериям как гладкий, при котором выделяли бессимптомное течение, слабые, средней силы и сильные нормальные вакцинальные реакции; и осложненный (наслоение интеркуррентных инфекций или обострение основного заболевания в течение месяца после прививки).
До прививки, на 14-й и 45-й дни после нее изучали титр коревых (в РТГА) и дифтерийных (в РПГА) антител, число лимфоцитов с помощью теста микролимфоцитотоксичности (CD3+, CD4+, CD8+, CD20+, CD16+, CD25+, CD95+) и четырех классов иммуноглобулинов (IgA, IgM, IgG, IgE) в стандартной реакции иммунодиффузии.
После введения АКДС (АДС) вакцинальный процесс у большинства привитых детей (67-100 %) протекал гладко (рис.1), при этом в 90-100% бессимптомно или в виде слабых вакцинальных реакций. Различий в проявлениях гладкого вакцинального процесса в зависимости от кратности вакцинации не отмечено.
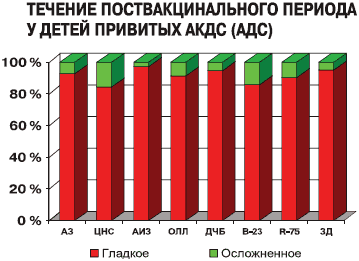
Рисунок 1
Наслоение интеркуррентных инфекций отмечалось в основном на 3-14-й дни после прививки в виде острых респираторных инфекций, причем после первых двух введений вакцины чаще, чем при последующих. Обострения основного заболевания были выявлены в первые две недели после прививки у 10 из 340 (2,9%) человек: у 3 детей из группы с поражением ЦНС (у 2 – в виде ночных страхов, возбуждения, головокружения, у 1 ребенка с ДЦП – галлюцинаторного синдрома); у 4 детей с аллергией – обострение атопического дерматита; у 1 ребенка из группы АИЗ, с нестабильным течением процесса, через 10 дней после введения АДС анатоксина – обострение ревматоидного увеита; в группе детей с онкологическими заболеваниями после введения АДС анатоксина у 1 ребенка отмечали обострение аллергического дерматита и у 1 – с первичным раком печени в анамнезе – лейкопения на 7-й день вакцинального процесса, которая возникала периодически и ранее без видимых причин. У всех детей обострения были кратковременными и купировались в течение 1-2 недель применением противорецидивной терапии.
У большинства детей, привитых против кори (рис. 2), вакцинальный процесс также был гладким и бессимптомным. Наиболее частыми клиническими проявлениями вакцинального процесса были: температура (55,7%), ринит (37,5%), кашель (23,9%). Сроки появления симптомов варьировали: у детей с аллергическими заболеваниями – на 5-12-е сутки, с поражением нервной системы – на 6-13-е, у часто болеющих детей и ВИЧ-инфицированных – на 4-12-е сутки, у здоровых – на 5-6-е сутки, что, видимо, ассоциировано со скоростью репликации вируса вакцины у детей разных групп.
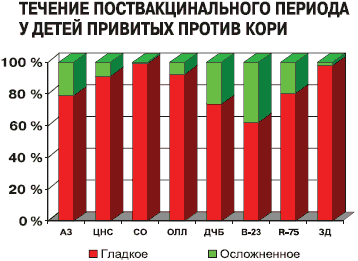
Рисунок 2
Наслоение интеркуррентных заболеваний чаще отмечалось в группах детей с аллергическими заболеваниями, у ВИЧ-инфицированных и детей с перинатальным контактом по ВИЧ.
В структуре осложненного течения преобладали сочетанные вирусно-бактериальные и бактериальные инфекции (64,5%). Обострения регистрировали у 12 из 493 детей (2,4%): у 7 детей с аллергией; у 3 из группы ДЧБ (два случая обострения пиелонефрита в виде лейкоцитурии на 7-8-е сутки после прививки, один случай обострения сопутствующего атопического дерматита). У 1 ребенка из группы детей с поражением ЦНС также наблюдалось обострение атопического дерматита. У 1 пациента с сахарным диабетом отмечен однократный подъем сахара крови до 19,5 ммоль/л на третий день после прививки. В целом обострения хронической патологии отмечались в 1,7 раза реже, чем при введении АКДС (АДС) (9,4 и 15,3% соответственно).
Таким образом, дети с различным состоянием здоровья могут прививаться наравне со здоровыми как неживыми, так и живыми вакцинами. Традиционное опасение развития обострений хронических заболеваний после иммунизации является преувеличенным. Наблюдение в катамнезе не выявило изменений течения основного заболевания.
Анализ антителообразования (рис. 3) показал, что у всех детей уровень противодифтерийных антител зависит от кратности введения препарата. Однако в период между законченной вакцинацией и ревакцинацией происходит снижение среднегеометрической величины титров антител на 30%. Это определяет важность своевременного введения ревакцинирующих доз для поддержания антитоксического иммунитета. У детей с аллергическими заболеваниями имела место тенденция к замедленному антителообразованию, но к 30-му дню среднегеометрическая величина титров антител достоверно не отличалась от здоровых. После третьей вакцинации в группе детей-аллергиков и с поражением ЦНС оставалось 5% серонегативных пациентов. После полного комплекса прививок (вакцинация и ревакцинация) у 2,5% детей этих групп не было защитного титра антител.
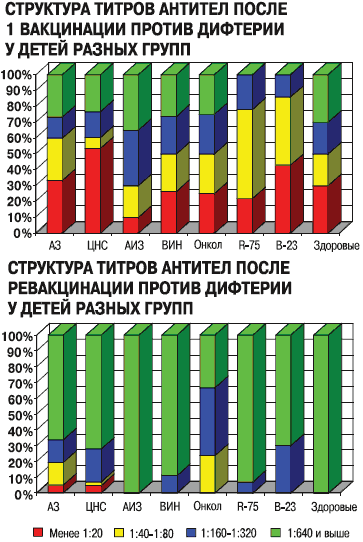
Рисунок 3
В группе детей с АИЗ, напротив, синтез антител был быстрым и сопоставим только с группой здоровых.
У ВИЧ-инфицированных детей среднегеометрическая величина титров противодифтерийных антител после ревакцинации был в 1,5-2 раза ниже, чем у здоровых, а в группе детей с перинатальным контактом по ВИЧ не отличалась от здоровых. Наслоение интеркуррентных заболеваний или развитие обострения не влияло на специфическое антителообразование.
Анализ титров противокоревых антител выявил сходные закономерности (рис. 4). Наиболее интенсивная выработка антител отмечалась у детей с АИЗ. Дети, страдающие аллергическими заболеваниями и дети, имеющие поражение ЦНС после ревакцинации, в 13,7% случаев оставались серонегативные, а дети с онкологическими заболеваниями в анамнезе – в 30,0%. Среди ВИЧ-инфицированных пациентов после вакцинации 24,4% оставалось серонегативными. Детей с ВИЧ-инфекцией, оставшихся серонегативными, через 6 месяцев после вакцинации привили повторно, и у них у всех выработались антитела, что может быть перспективным методом иммунизации для этой группы.
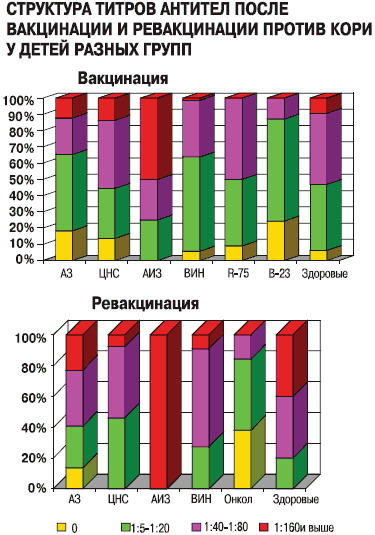
Рисунок 4
Основные принципы иммунизации детей с различными хроническими заболеваниями в анамнезе
- Иммунизацию следует проводить планово, с соблюдением интервалов между вакцинирующими дозами, так как полноценный иммунитет формируется после полного комплекса прививок; для поддержания защитного уровня антител необходимы своевременные ревакцинации.
- Плановые прививки проводят не ранее чем через месяц после начала полной или частичной стойкой клинико-лабораторной ремиссии, а для детей с онкологическими заболеваниями – через 6 месяцев после окончания терапии.
- Экстренная иммунизация (по эпидемическим показаниям) при любом заболевании может быть проведена в отсутствии ремиссии при продолжающейся активной терапии.
- Перед прививкой ребенка осматривает медицинский работник: проводит термометрию, уточняет данные анамнеза, оценивает стабильность ремиссии, уточняет, планово или экстренно прививается ребенок.
- Для всех детей используют сочетанное введение всех необходимых вакцин (за исключением БЦЖ).
- Минимальное лабораторное обследование проводят до и после прививки для определения эффективности использованной медикаментозной терапии. В случае выявления декомпенсации процесса, последующие прививки проводят с назначением других медикаментозных средств.
Дополнительные рекомендации для детей с поражением нервной системы
- Использование медикаментозных средств для предотвращения обострения в разгаре вакцинального периода (сосудистых, некоторых ноотропов, мочегонных, противосудорожных). Нежелательно вводить АКДС в момент приема церебролизина, актовегина и других препаратов, усиливающих судорожную готовность. Необосновано введение антигистаминных препаратов.
- Детям с прогрессирующей патологией, афебрильными судорогами в анамнезе, вместо цельноклеточной коклюшной вакцины вводят бесклеточную, при невозможности – только анатоксины.
Дополнительные рекомендации для детей с аллергическими заболеваниями
- Гипоаллергенный быт и диета в момент иммунизации: не вводить новые смеси, прикормы за 5 дней до и 10-14 дней после прививки.
- Плановые прививки не проводят в момент СИТ, а детям с поллинозом – в момент цветения значимых растений.
- Детям с атопическим дерматитом назначают биопрепараты, ферменты за 7 дней до и 7-14 дней после прививки (в зависимости от вакцины). Возможно назначение антигистаминных средств II-III поколения на тот же период времени.
- Детям с бронхиальной астмой: при легкой форме БА прививки проводят без назначения терапии; при средней и тяжелой формах – на фоне базисной терапии. При гормонозависимой астме с использованием ингаляционных ГКС можно вводить все вакцины, но доза ГКС должна быть стабильной в течение двух-трех месяцев.
- Детей с острыми аллергическими заболеваниями и реакциями (крапивница, отек Квинке и др.) прививают, одновременно применяя антигистаминные препараты (АГ). АГ I поколения назначают за 2-3 дня до и 4-14 дней после прививки (в зависимости от вакцины). АГ II-III поколения назначают с первого дня вакцинации на 4-14 дней. Дополнительно за 30 минут до вакцинации может назначаться АГ препарат парентерально. Пациентам с анафилактическим шоком в анамнезе можно вводить не АГ, а преднизолон – 1 мг/кг веса.
Дополнительные рекомендации для детей с аллергическими заболеваниями
- Для профилактики наслоения интеркуррентных инфекций применяют различные препараты: при преобладании бактериальных инфекций в анамнезе – стимуляторы макрофагального звена и В-клеточного ответа (Ликопид, Полиоксидоний, Рибомунил, бактериальные лизаты и др.); при преобладании вирусных инфекций – индукторы интерферонов (Циклоферон, Анаферон и др.), стимуляторы клеточного звена иммунитета.
Дополнительные рекомендации детям с иммунодефицитными состояниями
- Используются все неживые вакцины без ограничения.
- Живые вакцины противопоказаны лицам с первичным гуморальным, клеточным или комбинированным иммунодефицитом, детям с хронической гранулематозной болезнью, в момент иммуносупрессивной терапии, пациентам после тимэктомии.
- При решении вопроса о вакцинации детей с иммунодефицитом не требуется исследований иммунного статуса.
- До иммунизации проводят санацию хронических очагов инфекции.
- Через 6 месяцев после ревакцинации целесообразно контролировать уровень антител и при их отсутствии вводить дополнительную дозу вакцины.
- Детям, рожденным от ВИЧ-инфицированных матерей, и при всех стадиях ВИЧ-инфекции можно вводить все неживые вакцины.
- Детям с перинатальным контактом живые вакцины вводят наравне со здоровыми детьми.
- ВИЧ-инфицированным детям живые вакцины вводят при отсутствии клеточного иммунодефицита (число CD4+ – не менее 25% от возрастной нормы), т.е. с определением числа CD4+ до прививки.
- ВИЧ-инфицированным детям рекомендуется контроль титров антител через 6 месяцев после законченного курса АКДС (АДС) или вакцинации живыми вакцинами. При отсутствии защитного титра – дополнительная бустерная доза вакцины.
Сведения об авторах:
Сусанна Михайловна Харит, руководитель отдела иммунопрофилактики ФГУ «НИИ детских инфекций» Росздрава, главный внештатный специалист по вакцинопрофилактике детей Комитета здравоохранения Санкт-Петербурга, профессор, д-р мед. наук
Евгения Александровна Лакоткина, ведущий научный сотрудник отдела иммунопрофилактики ФГУ «НИИ детских инфекций» Росздрава, профессор, д-р мед. наук
Татьяна Владимировна Черняева, старший научный сотрудник отдела иммунопрофилактики ФГУ «НИИ детских инфекций» Росздрава, канд. мед. наук
Комментарии
ПРАКТИКА ПЕДИАТРА

