Простое слепое рандомизированное плацебо-контролируемое исследование эффективности применения тразодона для коррекции аффективных расстройств у больных с алкогольной зависимостью в ремиссии
Статьи Опубликовано в журнале:«ОБОЗРЕНИЕ ПСИХИАТРИИ И МЕДИЦИНСКОЙ ПСИХОЛОГИИ»; № 1; 2012; стр. 29-37.
Е.М. Крупицкий, С.М. Ериш, К.В. Рыбакова, А.С. Киселев, В.А. Бернцев, М.Н. Торбан, С.П. Ерошин, О.Ф. Ерышев
Санкт-Петербургский научно-исследовательский психоневрологический институт им. В.М. Бехтерева
Резюме.
Введение. Результаты исследований применения антидепрессантов (АД) для лечения алкоголизма оказались противоречивыми, возможно в силу того, что в эти исследования включались как больные с коморбидными аффективными расстройствами, так и пациенты без таковых, а также в силу использования АД с различными механизмами действия.
Цель исследования. Изучить эффективность применения антидепрессанта тразодона, относящегося к группе SARI, механизм действия которого включает ингибирование обратного захвата серотонина и блокаду 2А-подтипа рецепторов серотонина, для купирования аффективных расстройств депрессивного круга и стабилизации ремиссии у больных алкоголизмом.
Методы. Больные алкоголизмом (61 человек) с коморбидными депрессивными расстройствами — депрессивным эпизодом (F32.0), умеренным депрессивным эпизодом (F32.1) или рекуррентным депрессивным расстройством (F33.x) — случайным образом были распределены на две группы. Больные первой группы (30 человек) получали тразодон (150 мг/сут) в течение трех месяцев. Больные второй группы (31 человек) получали идентично выглядящее плацебо. Все больные еженедельно должны были посещать клинику для контроля ремиссии (потребления алкоголя), оценки выраженности аффективных расстройств и комплайенса приема препаратов (по подсчету не принятых таблеток). Для оценки депрессии и тревоги использовали шкалы Гамильтона, Монтгомери-Ашберг, Зунга и Спилбергера. Влечение к алкоголю оценивали с помощью обсессивно-компульсивной, Пенсильванской и визуальной аналоговой шкал. Для контроля потребления алкоголя применяли методику ретроспективного анализа и определение активности гамма-глутамилтранспептидазы (ГГТП). Для общей оценки эффективности терапии использовали шкалу общего клинического впечатления. Исследование проводилось простым слепым методом.
Результаты. Результаты данного исследования показали, что тразодон значимо превосходил плацебо в отношении купирования аффективных расстройств (депрессии и тревоги), антикрэйвингового эффекта, а также стабилизации ремиссии при алкоголизме. Количество побочных эффектов было несколько выше в группе тразодона.
Выводы. Тразодон продемонстрировал высокую эффективность и хорошую переносимость в лечении больных, страдающих алкогольной зависимостью с коморбидными аффективными расстройствами.
Ключевые слова: алкогольная зависимость, ремиссия, тревога, депрессия, тразодон.
SINGLE BLIND PLACEBO CONTROLLED RANDOMIZED CLINICAL TRIAL OF TRAZODON FOR ALCOHOLISM COMORBID WITH AFFECTIVE DISORDERS
E.M. Krupitsky, S.M. Yerish, K.V. Rybakova, A.S. Kiselev, V.A. Berntsev, M.N. Torban, S.P. Eroshin, O.F. Eryshev
St. Petersburg V.M. Bekhterev Research Psychoneurological Institute
Summary. Introduction: Results of clinical trials of antidepressants for alcohol dependence are controversial possibly due to inclusion patients with and without co-morbid affective disorders, as well as by the use antidepressants with different mechanisms of action.
Aim: To study efficacy of SARI — group antidepressant trazodone for treatment of alcoholics with co-morbid affective disorders (mild to moderate depression).
Methods: 61 patient with mild to moderate depression had been randomized to one of two treatment groups. Patients of the first group were treated with trazodone (150 mg/day) for 3 months while patients of the 2nd one received identically looking placebo. All the study subjects were scheduled to come to the clinic on the weekly basis for psychiatric evaluation (severity of depression and anxiety, and craving for alcohol), control of alcohol use and compliance with the study medications (by calculation of the missed tabs). To assess depression and anxiety used Hamilton scales, Montgomery-Ashberg scale, Spielberger state-trait inventory, and Zung scale. Craving for alcohol assessed with Obsessive-Compulsive Drinking scale, Penn Alcohol Craving scale, and Visual Analog Scale of Craving for alcohol. Alcohol use evaluated with the Time Line Follow Back technique and gamma-glutamiltranspeptidase activity in blood. Overall treatment effect assessed with the Clinical Global Impression scale. The study design was single blind.
Results: Trazodone was significantly superior to placebo in treating affective disorders (depression and anxiety), craving for alcohol and also preventing a relapse to heavy drinking: The number of side-effects in trazodone group was higher.
Conclusion: Trazodone is effective medication for alcohol dependence with co-morbid affective disorders.
Key words: alcohol dependence, stabilization, anxiety, depression, trazodone.
Введение
Алкоголизм является важной медико-социальной проблемой, актуальность которой обусловлена как стабильно высоким уровнем распространенности этого заболевания [3], так и его негативными социальными последствиями.
Антидепрессанты широко используются в лечении зависимости от алкоголя [5, 11]. Клинические и нейрохимические исследования представляют убедительные свидетельства того, что расстройства тревожно-депрессивного спектра, являясь широко распространенным психопатологическим феноменом при алкоголизме, патогенетически обусловлены и нередко являются одним из проявлений патологического влечения к алкоголю [2, 27].
Полученные в ряде исследований противоречивые данные относительно эффективности селективных ингибиторов обратного захвата серотонина при алкоголизме [4, 18, 22, 24] определили целесообразность изучения эффективности тразодона — антидепрессанта бициклической структуры, представителя группы SARI (ингибитора обратного захвата серотонина и антагониста 2А-рецепторов серотонина). Исследований эффективности данного препарата при алкогольной зависимости с коморбидной аффективной патологией, отвечающих критериям доказательной медицины, в литературе мы не нашли. Результаты зарубежных исследований структурно близкого к тразодону и обладающего тем же механизмом действия антидепрессанта нефазодона оказались неоднозначными. C.A. Hernandez-Avila et al. [17] и E.S. Brown et al. [9] выявили снижение уровня депрессии и тревоги у пациентов, получающих нефазодон, а также сокращение дней потребления алкоголя у зависимых от него пациентов с коморбидной депрессивной патологией.
В исследовании P.P. Roy-Byrne et al. [26] нефазодон, с одной стороны, проявил себя как безопасный и эффективный антидепрессант, снижающий уровень депрессии у коморбидных больных, однако с другой — не оказывал статистически значимого влияния на потребление алкоголя, по сравнению с группой плацебо.
В некоторых других исследованиях эффективность нефазодона при алкоголизме также была поставлена под сомнение [16, 19, 30].
Следует отметить, что негативные результаты были получены в исследованиях нефазодона, для которых больные алкоголизмом были рекрутированы из общей популяции без учета наличия коморбид-ных аффективных расстройств.
Некупированные коморбидные депрессия и тревога, а также повышенная импульсивность и эмоциональная лабильность, являясь ведущими симптомами периода становления ремиссии, провоцируют наступление рецидива алкогольной зависимости. В связи с этим использование антидепрессантов с седативным компонентом действия, в частности тразодона, представляется перспективным.
Вышесказанное обусловило целесообразность исследования тразодона как средства коррекции аффективных нарушений и профилактики рецидивов алкоголизма.
Материал и методы
Общий дизайн исследования. В рамках одинарного (простого) плацебо-контролируемого исследования больные с алкогольной зависимостью (61 человек) с коморбидными аффективными расстройствами были в случайном порядке распределены на 2 группы: больные основной группы (30 человек) получали тразодон однократно вечером 150 мг/сут, больные группы сравнения (контрольной группы) (31 человек) получали идентично выглядящее плацебо. Исследуемый препарат назначался на 3 месяца (12 недель), в течение которых испытуемые еженедельно должны были посещать исследовательский центр для контроля ремиссии, комплайенса приема препаратов (по подсчету не принятых таблеток), а также для психометрических оценок.
Испытуемые. В исследование включались мужчины и женщины в возрасте от 18 до 50 лет с отрицательным тестом на алкоголь в выдыхаемом воздухе, имевшие диагностированную согласно критериям МКБ-10 алкогольную зависимость в сочетании с аффективными расстройствами — депрессивным эпизодом (F32.0), умеренным депрессивным эпизодом (F32.1) или рекуррентным депрессивным расстройством (F33.x); воздерживавшиеся от употребления алкоголя не менее 7 дней (купированный алкогольный абстинентный синдром). В исследование включались только больные с депрессией легкой или средней степени выраженности (от 8 до 18 баллов по шкале депрессии Гамильтона). Критерием включения для женщин было также отсутствие текущей беременности и согласие использовать адекватные способы контрацепции в период участия в исследовании. Все больные включались в исследование при условии наличия контактного номера телефона — для осуществления катамнестического наблюдения (соблюдения еженедельного графика визитов в клинику).
В исследование не включали больных, использующих какие-либо иные психотропные препараты. Кроме того, в исследование не включали больных с выраженным органическим поражением головного мозга, выраженной соматической патологией (патология печени, почек, сердечно-сосудистой, нервной систем), психотическим состоянием или тяжелым психическим заболеванием в анамнезе (шизофрения, эпилепсия, биполярное аффективное расстройство и т. п.), с какой-либо иной химической зависимостью, кроме зависимости от алкоголя и табака, а также получающих какую-либо иную фармако- или психотерапию в связи с зависимостью от алкоголя, в том числе так называемую «плацебо-опосредованную суггестию» («химзащиту»), «кодирование» и т. п.
Набор участников и клиническая база. Исследование проводилось на базе отдела наркологии НИПНИ им. В.М. Бехтерева. После подписания информированного согласия больной включался в исследование.
Методы оценки. Для оценки состояния здоровья больных перед включением в исследование были использованы данные клинического и биохимического анализов крови и общего анализа мочи.
Всем больным проводили физикальный осмотр, определяли концентрацию алкоголя в выдыхаемом воздухе с помощью газоанализатора, осуществляли ретроспективный анализ употребления алкоголя за последние три месяца («Time Line Follow Back») [28] для оценки количества дней пьянства и количества потребленного алкоголя, подтверждали диагнозы алкогольной зависимости и аффективного расстройства по МКБ-10, собирали анамнестические данные с помощью специально разработанного клинического структурированного интервью, а также выполняли психометрические оценки с помощью батареи психометрических инструментов. Использовались следующие инструменты: индекс тяжести зависимости (ИТЗ) [20], шкала оценки общего функционирования (ШООФ) (дополнительная шкала DSM-IV) [12], шкала общего клинического впечатления (ОКВ) [10], краткая шкала психиатрической оценки (КПШ) [23], шкалы тревоги [15] и депрессии [14] Гамильтона, шкала депрессии Монтгомери-Ашберг (MADRS) [21], самооценочные шкалы депрессии Зунга [6, 31] и тревоги Спилбергера-Ханина [7, 29], а также Пенсильванская [13], обсессивно-компульсивная [8] и визуальная аналоговая шкалы оценки патологического влечения к алкоголю (ПВА) (табл. 1). Все вышеприведенные обследования повторялись в течение трех месяцев исследования с периодичностью, указанной в табл. 1.
Таблица 1.
Общая схема исследования
| Мероприятие | При вступлении в исследование | Еженедельно | Ежемесячно (или при выписке) | Конечная точка |
| Критерии МКБ-10 | X | |||
| Критерии включения/исключения | X | |||
| Алкоголь в выдыхаемом воздухе | X | X | X | |
| Анамнез и физикальное обследование | X | |||
| Индекс тяжести зависимости | X | X | ||
| Шкала общего клинического впечатления | X | X | ||
| Методика ретроспективного анализа потребления алкоголя | X | X | X | |
| Краткая шкала психиатрической оценки | X | X | X | |
| Шкала оценки общего функционирования | X | X | ||
| Пенсильванская шкала ПВА | X | X | X | |
| Обсессивно-компульсивная шкала ПВА | X | X | X | |
| Визуальная аналоговая шкала ПВА | X | X | X | |
| ГГТП | X | X | X | |
| Контроль комплайенса с лечением и психотерапией | X | X | ||
| Шкала депрессии Монтгомери-Ашберг (MADRS) | X | X | X | |
| Шкала Гамильтона (тревога) | X | X | X | |
| Шкала Гамильтона (депрессия) | X | X | X | |
| Шкала депрессии Зунга | X | X | X | |
| Шкала тревоги Спилбергера-Ханина | X | X | X | |
| Психотерапия | X | |||
| Опросник регистрации побочных эффектов | X | X | ||
| Форма контроля ремиссии | X | X | ||
| Форма выбывшего из исследования | X |
Кроме того, для объективизации сообщаемых больными данных о потреблении алкоголя еженедельно при каждом визите проводилось определение в крови активности гамма-глутамилтранспептидазы (ГГТП) — фермента, являющегося маркером массивного потребления алкоголя [1].
Для оценки наличия побочных эффектов проводимой терапии на всех больных при каждом из визитов заполнялась специальная регистрационная форма.
Комплайенс с приемом тразодона оценивали методом подсчета не принятых таблеток на каждом визите.
Всем больным (независимо от вида терапии — тразодон или плацебо) на каждом из еженедельных визитов проводился стандартизированный курс рациональной (когнитивно-поведенческой) психотерапии в соответствии с руководством по консультированию больных алкоголизмом [25].
Общая схема проведения исследования, мониторинга состояния больных и оценки клинически значимых параметров приведена в табл. 1.
Рандомизация и ослепление. Рандомизация была проведена при помощи генератора случайных чисел на базе электронных таблиц Ехсе1. Препараты (тразодон и плацебо) выдавались пациентам с соблюдением принципов одинарного ослепления при каждом визите один раз в неделю на протяжении трех месяцев таким образом, чтобы у них всегда был трехнедельный запас препарата (на случай пропуска 1-2 визитов). Пациенты не знали о своей принадлежности к той или иной группе лечения.
Исключение из исследования. Больные исключались из исследования в случае рецидива алкоголизма, в качестве которого рассматривалось возобновление массивного ежедневного (запойного) пьянства — три и более дней «тяжелого пьянства» подряд (согласно международным стандартам, «тяжелое пьянство» — heavy drinking — 5 и более стандартных порций алкоголя в день для мужчин, 4 и более — для женщин), а также в случае пропуска трех и более визитов подряд.
Статистическая обработка. Для ведения базы данных с информацией обо всех пациентах и о каждом их визите использован статистический пакет SPSS. Статистический анализ данных осуществлялся также с помощью статистического пакета SPSS. В целях соблюдения конфиденциальности вся информация о пациентах в базе данных была закодирована и их имена и фамилии нигде не упоминались. Различия рассматривали как статистически значимые при р < 0,05. Статистические характеристики количественных показателей представлены в виде среднее ± ошибка среднего.
Условно статистический анализ может быть разделен на 3 части: анализ анамнестических данных, анализ показателей, измеренных в динамике, и анализ побочных эффектов.
Анализ анамнестических данных осуществляли для доказательства однородности исследуемых групп. Группа анамнестических показателей состояла из 94 переменных, характеризующих пациента: пол, возраст, биографические данные, показатели, характеризующие его социальное положение, и клинические данные. Для анализа однородности по каждому показателю, в зависимости от его вида (шкала измерения, соответствие нормальному распределению), были использованы: точный критерий Фишера, тесты Колмогорова-Смирнова и Манна-Уитни, а также Т-тест. Анализ показал, что по всем измеренным показателям группы следует считать однородными.
Для анализа показателей, измеренных в динамике, использовался многофакторный дисперсионный (ковариационный) анализ с тестом Бонферрони в качестве апостериорного (post-hoc) теста. В качестве независимых переменных выступали вид терапии (тразодон или плацебо) и время (неделя) с момента включения в исследование, а в качестве зависимых — показатели психометрических шкал и потребления алкоголя. Для сравнения групп по таким показателям, как причина завершения программы, количество дней пьянства, количество употребленного алкоголя (в граммах чистого этанола), наличие и количество срывов и пропусков визитов, были построены таблицы сопряженности и использовался точный критерий Фишера. Для сравнения групп по общей продолжительности ремиссии в исследовании и по времени до первого приема алкоголя применялся тест Манна-Уитни. Также был проведен анализ выживаемости Каплана-Мейера (межгрупповые сравнения по методу хи-квадрат Мантеля-Кокса) по событию выбывания из исследования.
Для анализа побочных эффектов были построены таблицы частот по их наличию и количеству, продолжительности, количеству испытуемых с побочными эффектами, и применен точный критерий Фишера для оценки значимости межгрупповых различий.
Этические аспекты. Исследование было одобрено в этическом комитете НИПНИ им. В.М. Бехтерева. Информированное согласие было подписано каждым больным до включения в исследование. Больные, получавшие плацебо, тем не менее не оставались без лечения, так как всем без исключения пациентам проводился стандартизированный курс психотерапии в соответствии с руководством [25].
Конфиденциальность данных об участвовавших в исследовании больных обеспечивалась использованием защищенных кодами компьютеров и баз данных, а также отсутствием фамилий и имен больных на каких-либо документах, кроме информированного согласия.
Результаты
Анамнестические данные. Анамнестические данные (демографические и клинические) приведены в табл. 2. Как видно из таблицы, исследуемые группы больных значимо не различались по основным показателям, таким, как возраст, пол, давность формирования зависимости и др. Не отмечалось также статистически значимых различий между группами по другим анамнестическим и клиническим показателям, включая показатели ИТЗ и КПШ.
Таблица 2.
Характеристика групп больных
| Переменные | Группы больных | ||
| Тразодон | Плацебо | ||
| Число больных | 30 | 31 | |
| Возраст (годы) | 41,3 ± 1,6 | 40,9 ± 1,3 | |
| Пол | Муж. | 21 (70%) | 25 (81%) |
| Жен. | 9 (30%) | 6 (19%) | |
| Трудоустройство (% работающих) | 60 | 71 | |
| Давность формирования ААС (годы) | 9,8 ± 1,2 | 9,9 ± 1,3 | |
| Давность утраты количественного контроля (годы) | 11,6 ± 1,7 | 9,5 ± 1,4 | |
| Давность утраты ситуационного контроля (годы) | 11,8 ± 1,9 | 10,6 ± 1,7 | |
Динамика психометрических показателей. Шкала депрессии Монтгомери-Ашберг (ШДМА). Исходно повышенные показатели депрессии постепенно и значимо снижались в обеих группах больных (табл. 3). По данным дисперсионного анализа, статистически значимое снижение депрессии по ШДМА в основной группе больных произошло уже к 3-й неделе исследования, в то время как в группе сравнения — только к 11-й неделе. Уровень депрессии по ШДМА в основной группе оставался статистически значимо ниже исходных значений с 3-й по 12-ю неделю исследования, в то время как в контрольной группе — только на 11-й и 12-й неделях исследования (табл. 3). Уровень депрессии по данной шкале в основной группе был значимо ниже, чем в группе сравнения: статистически значимые различия между основной и контрольной группами отмечались на 5-й, а также 9-12-й неделях исследования (табл. 3).
Таблица 3.
Динамика психометрических показателей в процессе лечения
| Шкалы | Вид терапии | Значения психометрических показателей по неделям исследования (M ± SE) | ||||||||||||
| 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | ||
| ШДМА | Тразодон | 16,5±0,7 | 15,3±0,7 | 13,1±0,8 | 11,6+±0,9 | 11,8+±1,1 | 10,0+*±1,0 | 9,6+±1,2 | 10,2+±1,4 | 7,9+±1,2 | 5,0+*±1,5 | 6,6+*±1,3 | 5,1+*±1,3 | 4,6+*±1,3 |
| 16,0±0,7 | 15,4±0,7 | 14,4±0,8 | 13,2±0,9 | 12,9±1,0 | 13,3*±1,1 | 12,1±1,2 | 11,9±1,4 | 10,1±1,8 | 11,3*±1,8 | 11,5*±1,6 | 9,6+*±1,6 | 9,5+*±1,6 | ||
| Плацебо | 15,3±0,6 | 14,5±0,6 | 12,7±0,7 | 11,3+±0,8 | 10,4+±0,9 | 9,8+±0,9 | 9,1+±1,1 | 10,0+±1,2 | 8,3+±1,0 | 5,1+*±1,3 | 6,2+±1,1 | 4,9+±1,1 | 3,8+*±1,1 | |
| 15,2±0,6 | 14,4±0,6 | 12,5±0,7 | 12,5±0,7 | 11,5+±0,9 | 12,0±1,0 | 11,6±1,1 | 10,2+±1,2 | 10,4±1,6 | 9,7*±1,6 | 8,8+±1,4 | 8,1+±1,4 | 7,6+*±1,4 | ||
| ШДГ | Тразодон | 13,8±0,6 | 13,0±0,6 | 11,0±0,7 | 9,8+±0,8 | 10,2±1,0 | 10,2±0,9 | 9,8±1,1 | 9,3±1,3 | 8,0+±1,1 | 5,7+±1,4 | 6,3+±1,2 | 6,1+±1,2 | 5,4+±1,2 |
| 12,9±0,6 | 12,5±0,6 | 11,9±0,7 | 11,3±0,8 | 11,3±0,9 | 11,8±1,0 | 11,0±1,1 | 10,9±1,3 | 9,9±1,7 | 9,9±1,7 | 8,7±1,5 | 8,5±1,5 | 7,3+±1,5 | ||
| Плацебо | 43,6±1,1 | 42,1±1,1 | 40,3±1,3 | 37,5±1,4 | 36,2+±1,7 | 34,9+±1,6 | 33,4+±1,9 | 31,7+±2,2 | 31,0+±1,9 | 27,1+±2,4 | 29,8+±2,1 | 28,6+±2,1 | 29,3+±2,1 | |
| 42,6±1,1 | 39,9±1,1 | 38,5±1,2 | 38,4±1,3 | 37,6±1,6 | 35,2+±1,9 | 35,2±2,0 | 34,1+±2,2 | 29,7+±2,9 | 29,6+±2,9 | 32,8+±2,6 | 34,0±2,6 | 30,5+±2,6 | ||
| ШТГ | Тразодон | 47,1±1,2 | 47,3±1,2 | 46,3±1,3 | 45,4±1,5 | 46,3±1,8 | 43,6±1,7 | 41,6±2,1 | 38,0+±2,4 | 39,5±2,0 | 34,5+±2,6 | 37,6+±2,2 | 37,4+±2,2 | 36,9+±2,2 |
| 46,8±1,1 | 45,8±1,2 | 43,0±1,3 | 44,9±1,4 | 43,3±1,7 | 41,2±2,0 | 42,1±2,1 | 42,5±2,4 | 40,5±3,2 | 40,4±3,2 | 41,8±2,8 | 41,7±2,8 | 41,8±2,8 | ||
| Плацебо | 48,9±1,2 | 48,8±1,2 | 47,0±1,4 | 43,5±1,6 | 43,6±1,9 | 43,0±1,8 | 38,2+±2,2 | 36,8+*±2,4 | 36,4+±2,0 | 33,5+±2,6 | 35,9+±2,3 | 34,4+±2,3 | 32,6+*±2,3 | |
| 48,0±1,2 | 47,6±1,2 | 45,3±1,4 | 45,3±1,5 | 43,3±1,7 | 42,7±2,0 | 40,6±2,2 | 44,1*±2,5 | 40,5±3,2 | 40,9±3,2 | 39,9±2,9 | 39,4±2,9 | 40,0*±2,9 | ||
| ШДЗ | Тразодон | 7,7±0,7 | 6,7±0,7 | 5,4±0,8 | 4,0±0,9 | 5,3±1,1 | 4,9±1,0 | 2,3+±1,2 | 0,7+±1,4 | 1,2+±1,2 | 0,0+±1,5 | 1,1+±1,3 | 0,0+±1,3 | 0,5+±1,3 |
| 7,2±0,7 | 5,8±0,7 | 5,1 ±0,8 | 5,0±0,8 | 3,9±1,0 | 6,2±1,1 | 3,2±1,2 | 4,1±1,4 | 3,3±1,8 | 3,9±1,8 | 3,7±1,7 | 3,7±1,6 | 2,6±1,6 | ||
| Плацебо | 17,2±1,2 | 14,1±1,2 | 11,3±1,4 | 10,3+±1,5 | 11,3±1,8 | 10,3±1,8 | 4,8+±2,1 | 2,4+±2,4 | 3,8+±2,0 | 1,8+±2,6 | 3,6+±2,2 | 2,5+±2,2 | 2,8+±2,2 | |
| 15,4±1,1 | 10,9±1,2 | 9,3+±1,3 | 9,7±1,5 | 7,4+±1,7 | 10,5±1,9 | 6,5+±2,1 | 8,8±2,4 | 7,5±3,2 | 8,4±3,2 | 8,0±2,8 | 5,3±2,8 | 4,1+±2,8 | ||
| ЛТ С-Х | Тразодон | 2,1±0,3 | 2,1±0,3 | 1,4±0,3 | 1,0±0,3 | 1,1±0,4 | 1,6±0,4 | 0,9±0,5 | 0,2±0,5 | 0,6±0,4 | 0,5±0,5 | 0,6±0,5 | 0,7±0,5 | 0,4±0,5 |
| 2,1±0,3 | 1,5±0,3 | 1,5±0,3 | 1,5±0,3 | 1,3±0,4 | 1,6±0,4 | 1,1±0,5 | 1,3±0,5 | 1,3±0,7 | 1,1±0,7 | 1,2±0,6 | 1,3±0,6 | 0,6±0,6 | ||
+ Статистическая значимость различий показателей на разных сроках лечения от исходных (ANCOVA, T-тест с поправкой Бонферрони для post hoc сравнений): р < 0,05.
Шкала депрессии Гамильтона (ШДГ). Статистически значимое снижение депрессии в основной группе больных по данной шкале произошло к 3-й неделе исследования, и в дальнейшем уровень депрессии оставался значимо ниже на протяжении всего периода исследования (табл. 3). В контрольной группе депрессия по ШДГ статистически значимо снизилась к 4-й неделе, но затем достоверно отличалась от исходных значений только на 7-й и 10-12-й неделях исследования. Статистически значимо более низкий уровень депрессии по ШДГ в основной группе по сравнению с контрольной регистрировался на 9-й и 12-й неделях исследования (табл. 3).
Шкала тревоги Гамильтона (ШТГ). Уровень тревоги в основной группе снижался и статистически значимо отличался от исходных значений на 3-й и 8-12-й неделях исследования, в то время как в контрольной группе — только на 12-й неделе. Статистически значимых межгрупповых различий выявлено не было (табл. 3).
Шкала депрессии Зунга (ШДЗ). Уровень депрессии по самооценочной шкале Зунга снижался и статистически значимо отличался от исходных значений на 4-12-й неделях в основной группе больных и на 5-й, 7-10-й и 12-й неделях — в группе сравнения. Межгрупповые различия не были статистически значимыми (табл. 3).
Шкала реактивной тревоги Спилбергера-Ханина (РТ С-Х). Уровень РТ в основной группе снижался и статистически значимо отличался от исходных значений на 6-12-й неделях лечения. В группе сравнения статистически значимых различий выявлено не было. Уровень тревоги в основной группе больных был статистически значимо ниже, чем в группе сравнения, на 7-й и 12-й неделях исследования (табл. 3).
Шкала личностной тревоги Спилбергера-Ханина (ЛТ С-Х). Статистически значимое снижение ЛТ в основной группе больных по данному тесту выявлено на 7-й и 9-12-й неделях лечения. В контрольной группе статистически значимых различий по отношению к исходному уровню не выявлено. Значимых различий между группами по данным показателям также выявлено не было (табл. 3).
Шкалы оценки патологического влечения к алкоголю (ПВА). По данным Пенсильванской шкалы ПВА (ПШПВА), в основной группе интенсивность ПВА снижалась и статистически значимо отличалась от исходных значений на 6-12-й неделях исследования. В контрольной группе изменения не были статистически значимыми. Достоверных различий в выраженности ПВА между основной и контрольной группами выявлено не было (табл. 3).
В основной группе по обсессивно-компульсивной шкале (ОКШПВА) значимое снижение интенсивности ПВА по сравнению с исходными значениями происходило на 3-й и 6-12-й неделях исследования. В контрольной группе снижение уровня ПВА отмечалось на 2-й, 4-й, 6-й и 12-й неделях. Статистически значимых межгрупповых различий выявлено не было (табл. 3).
В динамике ПВА по данным визуальной аналоговой шкалы (ВАШПВА) достоверных межгрупповых и внутригрупповых различий выявлено не было.
Динамика биохимических показателей. Гамма-глутамилтранспептидаза (ГГТП). Уровень ГГТП в крови больных обеих групп постепенно снижался — практически в 2 раза, однако значимые межгрупповые и внутригрупповые различия отсутствовали из-за большой дисперсии параметров (табл. 4).
Таблица 4.
Активность гамма-глутамилтранспептидазы (ГГТП)
| Вид терапии | Значения ГГТП по неделям исследования (M ± SE) | ||||||||||||
| 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | |
| Тразодон | 103,6±8,4 | 99,3±9,2 | 84,5±14,5 | 75,9±12,6 | 79,8±13,5 | 92,7±11,9 | 49,3±14,5 | 93,2±17,8 | 71,5±15,9 | 52,7±15,9 | 52,4±17,8 | 71,9±20,6 | 48,2±17,8 |
| Плацебо | 117,0±6,9 | 84,2±10,9 | 85,4±12,1 | 86,3±11,8 | 61,7+±11,8 | 82,3±15,9 | 79,1±15,9 | 58,0±20,5 | 86,3±20,5 | 76,6±17,8 | 74,5±20,5 | 55,0±20,5 | 58,2±25,2 |
Показатели потребления алкоголя и выбывания из исследования. Выбывание из программы исследования. В основной группе больных программу лечения закончили в ремиссии 8 человек (27%), у 7 больных (23%) наступил рецидив алкоголизма, и еще 15 больных (50%) выбыли из исследования по другим (не связанным с основным заболеванием) обстоятельствам. В контрольной группе закончили исследование в ремиссии всего 5 человек (16%), выбыли по рецидиву алкоголизма — 9 (29%), и 17 больных (54%) выбыли из исследования по другим обстоятельствам. Статистически значимые различия между группами отсутствуют.
Результаты анализа выживаемости Каплана-Мейера продемонстрировали значимо лучшее удержание в программе лечения в группе больных, получавших тразодон (рис. 1). Различия между основной группой и группой сравнения по критерию хи-квадрат Мантеля-Кокса статистически значимы (р < 0,05).
Рис. 1. Результаты анализа выживаемости Каплана-Мейера. Различия статистически значимы: р = 0,01 (хи-квадрат Мантеля-Кокса)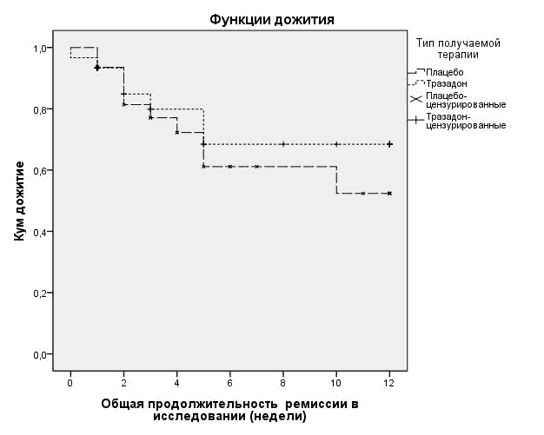
Показатели ремиссии и употребления алкоголя. Суммарное количество дней употребления алкоголя, верифицированное методом ретроспективного анализа, в основной группе больных (30 дней) было статистически значимо меньше, чем в контрольной группе (46 дней) (р < 0,05; точный критерий Фишера). Относительно небольшое число дней употребления алкоголя в группах обусловлено тем, что при расчете данного показателя учитывались только срывы без рецидивов (то есть больные, у которых наступал рецидив, исключались из исследования первым днем рецидива). Средняя продолжительность ремиссии в основной группе (5,30 ± 0,84 недели) была несколько выше, чем в контрольной (4,74 ± 0,71 недели), однако эти различия не были статистически значимыми. Время до первого употребления алкоголя («срыва ремиссии») между группами достоверно не различалось: 3,43 ± 0,53 недели в основной группе против 4,33 ± 0,99 недели в контрольной.
Общие показатели эффективности терапии. Шкала общего клинического впечатления (ШОКВ). К концу исследования «очень значительное» или «значительное» улучшение в основной группе отмечалось у 23,3% испытуемых, а в контрольной — у 6,4%. При этом статистически значимых различий выявлено не было (р = 0,364).
Шкала оценки общего функционирования (ШООФ). Исходно группы имели примерно одинаковые оценки по ШООФ (59,23 ± 1,46 в основной группе и 61,38 ± 1,08 в контрольной). Через 1,5 месяца (середина исследования) показатели общего функционирования в основной группе были выше, чем в контрольной (70,00 ± 2,26 против 62,22 ± 4,34), но статистически значимых различий выявлено не было. Примерно такая же разница между основной и контрольной группами сохранялась к концу лечения (77,78 ± 3,64 в основной группе и 71,67 ± 6,54 в контрольной), однако она также не достигала уровня статистической значимости.
Показатели переносимости терапии. Побочные эффекты. В основной группе больных побочные эффекты отмечались у 16 испытуемых (53%), в то время как в контрольной группе — у 9 (29%) (p = 0,071, точный критерий Фишера). Появлявшиеся побочные эффекты были легкой степени выраженности и не требовали какой-либо терапии. Наиболее частыми нежелательными явлениями в основной группе были ощущение заторможенности, вялость, сонливость, усталость, отсутствие энергии, слабость. По причине побочных эффектов в основной группе отказались от участия в исследовании 5 пациентов (16,7%), а в контрольной — 1 (3,2%). Серьезных нежелательных явлений зарегистрировано не было.
Обсуждение
Данное исследование является первым одинарным слепым рандомизированным клиническим исследованием эффективности тразодона для купирования аффективных расстройств депрессивного круга и стабилизации ремиссии у больных с алкогольной зависимостью. Общая эффективность 12-недельного курса терапии тразодоном была изучена на выборке из 61 пациента. Первичными показателями эффективности являлись динамика депрессии и тревоги у испытуемых, в то время как выраженность влечения к алкоголю, а также показатели, характеризующие устойчивость ремиссии, рассматривались как вторичные.
Результаты данного исследования свидетельствуют об эффективности тразодона как средства купирования аффективных нарушений начального периода ремиссии у больных алкоголизмом. При этом тразодон продемонстрировал отчетливый антидепрессивный и умеренный анксиолитический эффект. Данные шкалы депрессии Монтгомери-Ашберг выявили статистически значимое снижение уровня депрессии в основной группе больных уже к 3-й неделе исследования. Аналогичная динамика уровней депрессии и тревоги была зарегистрирована по шкалам Гамильтона, снижение показателей по которым оставалось стабильным до 12-й недели исследования. Выраженность реактивной и личностной тревоги, оцениваемая соответствующими шкалами Спилбергера-Ханина, в группе испытуемых, получавших тразодон, значимо снижалась в середине исследования и оставалась статистически значимой до его конца. В контрольной группе по этим шкалам снижение уровня депрессии и тревоги происходило только в конце исследования и не носило устойчивого характера.
Более быстрая и существенная редукция тревоги и депрессии в группе больных, получавших тразодон, сопровождалась достоверной редукцией интенсивности патологического влечения к алкоголю по отношению к исходным показателям, что демонстрирует оценка ПВА по Пенсильванской и обсессивно-компульсивной шкалам. В основной группе интенсивность ПВА по Пенсильванской шкале статистически значимо снижалась начиная с 6-й недели исследования и достоверно отличалась от исходных значений до конца исследования. По данным обсессивно-компульсивной шкалы, в основной группе значимое снижение ПВА происходило уже на 3-й и 6-12-й неделях исследования. При этом достоверные изменения ПВА в контрольной группе практически отсутствовали. Таким образом, тразодон обнаружил также определенное антикрэйвинговое действие у больных с алкогольной зависимостью. Следует отметить, что, несмотря на более частое развитие побочных эффектов у больных основной группы (ощущение заторможенности, вялость, сонливость, усталость, слабость), их выраженность была невысокой и не требовала какой-либо терапии, то есть переносимость тразодона может быть оценена как удовлетворительная. Серьезных побочных эффектов по результатам исследования не было зарегистрировано.
Таким образом, в данном исследовании были получены результаты, свидетельствующие о клинической эффективности и безопасности тразодона, схожие с результатами исследований близкого к нему по механизму действия антидепрессанта нефазодона, полученными C.A. Hernandez-Avila et al. [17] и E.S. Brown et al. [9]. Полученные данные, в частности, продемонстрировали снижение выраженности депрессии и тревоги, а также сокращение дней потребления алкоголя у зависимых от него пациентов. Результаты проведенного нами исследования тразодона хорошо соотносятся также с данными многоцентрового двойного слепого исследования нефазодона, выполненного P.P. Roy-Byrne et al. [26], в котором была показана эффективность данного класса АД в отношении купирования депрессии у больных алкоголизмом.
Заключение
Таким образом, проведенное простое слепое рандомизированное плацебо-контролируемое исследование выявило высокую эффективность и хорошую переносимость тразодона в лечении больных, страдающих алкогольной зависимостью, сочетающейся с коморбидными аффективными расстройствами, способствуя редукции депрессии и тревоги, стабилизации ремиссии и профилактике рецидивов.
Продемонстрированная нами в данной работе определенная эффективность тразодона в отношении стабилизации ремиссий при алкоголизме и его умеренное антикрэйвинговое действие, возможно, обусловлены тем, что в настоящее исследование включались только коморбидные больные, у которых зависимость от алкоголя сочеталась с депрессией легкой или средней степени выраженности.
Сведения об авторах
Крупицкий Евгений Михайлович — руководитель отдела наркологии НИПНИ им. В.М. Бехтерева, д.м.н., профессор.
Ериш Софья Михайловна — аспирант отделения лечения больных алкоголизмом НИПНИ им. В.М. Бехтерева.
Рыбакова Ксения Валерьевна — старший научный сотрудник отделения лечения больных алкоголизмом НИПНИ им. В.М. Бехтерева, к. м. н.
Киселев Алексей Сергеевич — специалист по биомедицинской статистике, отдел научномедицинской информации НИПНИ им. В.М. Бехтерева.
Бернцев Владимир Александрович — врач психиатр-нарколог отделения лечения больных алкоголизмом НИПНИ им. В.М. Бехтерева.
Торбан Михаил Наумович — младший научный сотрудник отдела терапии больных с аддиктивной патологией НИПНИ им. В.М. Бехтерева.
Ерошин Сергей Петрович — старший научный сотрудник отделения лечения больных алкоголизмом НИПНИ им. В.М. Бехтерева, к. м. н.
Ерышев Олег Федорович — главный научный сотрудник отделения лечения больных алкоголизмом НИПНИ им. В.М. Бехтерева, д. м. н., профессор.
1. Винницкая Е.В. Алкогольная болезнь печени: клиническое течение, терапия // Гастроэнтерология. 2007. № 13. С. 53-58.
2. Иванец Н.Н., Анохина И.П., Коган Б.М. Эффективность и механизмы действия леривона при алкоголизме // Журн. невропатол. и психиат. им. С.С. Корсакова. 1996. Т. 96, № 5. С. 52-58.
3. Кошкина Е.А., Спектор Ш.И., Сенцов В.Г., Богданов С.И. Медицинские, социальные и экономические последствия наркомании и алкоголизма. M.: ПЕР СЭ, 2008. 288 с.
4. Крупицкий Е.М., Илюк Р.Д., Ерышев О.Ф., Цой-Подосенин М.В. Современные фармакологические методы стабилизации ремиссий и профилактики рецидивов в наркологии // Обозрение психиатрии и медицинской психологии им. В.М. Бехтерева. 2009. № 1 (Наркология). С. 12-27.
5. Малин Д.И., Янкин Е.В., Медведев В.М., Ковалев А.В. Депрессии у больных алкоголизмом // Психиатрия и психофармакотерапия. 2004. Т. 6, № 5. С. 243-245.
6. Рыбакова Т.Г., Балашова Т.Н. Клиникопсихологическая характеристика и диагностика аффективных расстройств при алкоголизме: метод. реком / НИПНИ им. В.М. Бехтерева; сост.: Т.Г. Рыбакова, Т.Н. Балашова. Л., 1988.27с.
7. Ханин Ю.Л. Краткое руководство по применению шкалы реактивной и личностной тревожности Ч.Д. Спилбергера / Ю.Л. Ханин. Л.: ЛНИИФК, 1976.18 с.
8. Anton R.F., Moak D.H., Latham P.K. The obsessive compulsive drinking scale // Arch. Gen. Psych. 1996. Vol. 53, № 3. Р. 225-231.
9. Brown E.S., Bobadilla L., Nejtek VA. Open-label nefazodone in patients with a major depressive episode and alcohol dependence // Prog. Neuropsychopharmacol. Biol. Psychiatry. 2003. Vol. 27, № 4. P. 681-685.
10. Busner J., Targum S.D., Miller D.S. The Clinical Global Impressions Scale: Errors in Understanding and Use // Compr. Psychiatry. 2009. Vol. 50, № 3. Р. 257-262.
11. Crocq M.A. Depression and alcohol // Depression and addiction: WPA Bulletin on Depression. — 2001. Vol. 5, № 23. P. 1-4.
12. Diagnostic and Statistical Manual of Mental Disorders: Fourth Edition (DSM-IV) / А. Frances, H.A. Pincus, M.B. First (eds.). Substance Related Disorders. 1994. P. 325-346.
13. Flannery B.A., Volpicelli J.R., Pettinati H.M. Psychometric properties of the Penn alcohol craving scale // Alc. Clin. Exp. Res. 1999. Vol. 23, № 8. P. 1289-1295.
14. Hamilton M. A rating scale for depression // J. Neurol. Neurosurg. Psychiatry. 1960. Vol. 23. P. 56-62.
15. Hamilton M. Development of a rating scale for primary depressive illness // Br. J. Soc. Clin. Psychol. 1967. Vol. 6. P. 278-296.
16. Hautzinger M., Wetzel H., Szegedi A. et al. Combination treatment with SSRI and cognitive behavior therapy for relapse prevention of alcohol-dependent men. Results of a randomized, controlled multicenter therapeutic study // Nervenarzt. 2005. Vol. 76, № 3. P. 295-307.
17. Hernandez-Avila C.A., Modesto-Lowe V., FeinnR., Kranzler H.R. Nefazodone treatment of comorbid alcohol dependence and major depression // Alcohol. Clin. Exp. Res. 2004. Vol. 28, № 3. P. 433440.
18. Kranzler H.R., Burleson J.A., Korner P. et al.Placebo-controlled trial of fluoxetine as an adjunct to relapse prevention in alcoholics // American Journal of Psychiatry. 1995. Vol. 152. P. 391-397.
19. Kranzler H.R., Modesto-Lowe V., Van Kirk J. Naltrexone vs. nefazodone for treatment of alcohol dependence. A placebo-controlled trial // Neuropsychopharmacology. 2000. Vol. 22, № 5. P. 493-503.
20. McLellan A.T., Luborsky L., Woody G.E., O'Brien C.P. An improved diagnostic evaluation instrument for substance abuse patients. The Addiction Severity Index // J. Nerv. Ment. Dis. 1980. Vol. 168, № 1. P. 26-33.
21. Montgomery S.A., Asberg M.A new depression scale designed to be sensitive to change // Br. J. Psychiatry. 1979. Vol. 134. P. 382-389.
22. Naranjo C.A., Bremner K.E. Clinical pharmacology of serotonin-altering medications for decreasing alcohol consumption // Alcohol. Alcohol. 1993. Vol. 2. (Suppl.). P. 221-229.
23. Overall J.E., Gorham D.R. The brief psychiatric rating scale // Psychological Reports. 1962. Vol. 10. P. 799-812.
24. Pettinati H.M., Volpicelli J.R., Kranzler H.R. et al. Sertraline treatment for alcohol dependence: interactive effects of medication and alcoholic subtype // Alcoholism: Clinical and Experimental Research. 2000. Vol. 24. P. 1041-1049.
25. Pettinati H.M., Weiss R.D., Miller W.R., Dundon W. Medical Management Treatment Manual: A Clinical Research Guide for Medically Trained Clinicians Providing Pharmacotherapy as Part of the Treatment for Alcohol Dependence. Bethesda, MD: US Department of Health and Human Services, 2004. — NIAAA COMBINE Monograph Series, Vol. 2.
26. Roy-Byrne P.P., Pages K.P., Russo J.E. et al. Nefazodone treatment of major depression in alcohol-dependent patients: a double-blind, placebo-controlled trial // J. Clin. Psychopharmacol. 2000. Vol. 20, № 2. P. 129-136.
27. Salloum I.M., Daiey D.C., Thase M.E. Male depression, alcoholism and violence. UK: Martin Dunitz Ltd., 2000. 97p.
28. Sobell M.B., Sobell L.C., Klajner F. et al. The reliability of a timeline method for assessing normal drinker college students' recent drinking history: utility for alcohol research // Addict. Behav. 1986. Vol. 11, № 2. P. 149-161.
29. Spielberger C.D., Gorsuch R.L., Lushene R.E. Manual for the state-trait anxiety inventory. Palo Alto, CA: Consulting Press, 1970.
30. Wetzel H., Szegedi A., Scheurich A. et al. Combination treatment with nefazodone and cognitive-behavioral therapy for relapse prevention in alcohol-dependent men: a randomized controlled study // J. Clin. Psychiatry. 2004. Vol. 65, № 10. P. 1406-1413.
31. Zung W.W.K. A self-rating depression scale // Arch. Gen. Psych. 1965. Vol. 12. P. 63-70.
Комментарии
ПРАКТИКА ПЕДИАТРА
