Роль клопидогреля в лечении и профилактике сердечно-сосудистых заболеваний
Статьи Опубликовано в журнале:«CONSILIUM MEDICUM»; ТОМ 11; № 10; стр. 130-137.
Г.А.Барышникова
Кафедра семейной медицины
ФГХ Учебно-научный медицинский центр, Москва
Ежегодно в России от сердечно-сосудистых заболеваний (ССЗ) умирают более 1 млн человек, т.е. примерно 700 человек на 100 тыс. населения. Хорошо известно, что причиной развития тяжелых сердечно-сосудистых осложнений, прежде всего инфаркта миокарда (ИМ) и инсульта, является повреждение поверхности атеросклеротической бляшки с формированием внутрисосудистого тромбоза (атеротромбоз) [1]. Именно клинические проявления атеротромбоза - ведущая причина смертности населения в экономически развитых странах, в том числе в России. В 2000 г. в мире в структуре общей смертности 52% составила смертность от осложнений атеротромбоза, существенно опередив онкологическую патологию (24%) [2]. Первыми на разрыв атеросклеротической бляшки реагируют тромбоциты, «прилипая» к открывающимся субэндотелиальным структурам (адгезия). Происходящая при этом активация тромбоцитов ведет к вовлечению в адгезивный процесс все новые кровяные пластинки и экспрессии на их поверхности IIb/IIIa гликопротеиновых (ГП) рецепторов, которые на завершающем этапе агрегации тромбоцитов играют ключевую роль в процессе тромбообразования, образуя «мостики» между тромбоцитами и адгезивными белками, прежде всего фибриногеном. Активация тромбоцитов может происходить под влиянием нескольких веществ, важнейшим из которых является аденозиндифосфат (АДФ). АДФ в высоких концентрациях содержится в плотных внутритромбоцитарных гранулах и, высвобождаясь из них, способен инициировать и усиливать процесс агрегации [3]. Активация АДФ-рецепторов ведет к изменению формы тромбоцитов, возрастанию внутриклеточной концентрации кальция, экспрессии ГП IIb/IIIa рецепторов и высвобождению β-селектина -мембранного гликопротеина, способствующего взаимодействию тромбоцитов с другими клетками [4].
Ведущая роль в профилактике осложнений атеросклероза принадлежит антитромбоцитарным препаратам (антиагрегантам), ингибирующим функцию тромбоцитов. Классификация антитромбоцитарных средств (антиагрегантов) представлена в табл. 1. Перечисленные антиагреганты блокируют агрегацию тромбоцитов посредством разных механизмов действия. Аспирин блокирует циклооксигеназу, предотвращая образование тромбоксана А2; дипиридамол увеличивает концентрацию циклических нуклеотидов и влияет на концентрацию АДФ, тромбина, арахидоновой кислоты; производные тиенопиридина (тиклопидин, клопидогрель) необратимо ингибируют АДФ-индуцированную агрегацию тромбоцитов, блокируя аденозиновые рецепторы тромбоцитов; антагонисты ГП рецепторов тромбоцитов GP IIb/IIIa предотвращают образование межтромбоцитарных фибриногеновых мостиков.
Таблица 1.
Основные классы антиагрегантных препаратов
| Аспирин Курантил Тиклопидин (Тиклид) Клопидогрель (Плавикс, Лопирел) Абсиксимаб (Рео Про) Эптифибатид Тирофибан |
Поскольку в первую очередь, вызывается и усиливается агрегация тромбоцитов тромбоксан А2 и АДФ, неудивительно, что с целью профилактики атеротромботических осложнений стали широко применять антиагреганты, влияющие на образование ТхА2 (аспирин) или блокирующие АДФ-рецепторы тромбоцитов (тиенопиридины). Дипиридамол используется преимущественно после перенесенного ишемического инсульта в комбинации с аспирином. Ингибиторы IIβ/IIIα ГП-рецепторов (прежде всего абсиксимаб) с успехом применяются (парентерально!) при проведении ангиопластики, однако попытка использовать эти препараты длительно перорально не увенчалась успехом.
В течение многих лет «золотым стандартом» антиагрегантной терапии оставалась ацетилсалициловая кислота (аспирин), имеющая очень хорошую доказательную базу. Доказана эффективность аспирина при всех формах ишемической болезни сердца (остром коронарном синдроме - ОКС, остром ИМ, после перенесенного инфаркта, стабильной стенокардии, после аортокоронарного шунтирования и ангиопластики), при ишемическом инсульте и после перенесенного ишемического инсульта, при поражении периферических артерий. По данным метаанализа 287 исследований, включивших более 200 тыс. пациентов высокого риска сердечно-сосудистых осложнений, проведенного группой экспертов Antithrombotic Trialists' Collaboration, 2002 г. [5], длительный прием аспирина (75-325 мг/сут) снижает суммарную частоту ИМ, инсульта и сердечно-сосудистой смерти на 23%. При остром ишемическом инсульте аспирин вообще является единственным (безальтернативным) антиагрегантом, эффективность которого доказана. Кроме того, только аспирин рекомендован для первичной профилактики сердечно-сосудистых осложнений. Во многом благодаря именно аспирину показания к применению антиагрегантов после 2-го метаанализа, проведенного группой экспертов Antithrombotic Trialists' Collaboration, значительно расширились (табл. 2). К середине 1990-х годов аспирин вошел в качестве обязательного препарата практически во все рекомендации по лечению и профилактике клинических проявлений атеротромбоза.
Таблица 2.
Расширение показаний к применению антитромбоцитарных препаратов по итогам метаанализа 2002 г. [5]
| Показания к применению антитромбоцитарных препаратов | 1994 г. | 2002 г. |
| Острый ИМ | + | + |
| Нестабильная стенокардия | + | + |
| Перенесенный ИМ | + | + |
| Перенесенный ишемический инсульт | + | + |
| Острый ишемический инсульт | + | |
| Перемежающаяся хромота | + | |
| Стабильная стенокардия | + |
Но при всех его достоинствах аспирин не лишен ряда недостатков. Хорошо известны его побочные эффекты: диспепсия (в 20-30% случаев при длительном применении), эрозивно-язвенные поражения желудочно-кишечного тракта (ЖКТ), бронхоспазм, острый приступ подагры (из-за нарушения экскреции мочевой кислоты); аллергические реакции. Развитие аспирининдуцированных осложнений со стороны слизистой оболочки ЖКТ требует отмены аспирина и назначения наиболее эффективных в данной ситуации ингибиторов протонной помпы. Снизить риск неблагоприятного воздействия аспирина на ЖКТ можно, используя таблетки с кишечнорастворимой оболочкой, например Аспирин Кардио [6]. При непереносимости аспирина альтернативой ему согласно большинству европейских и отечественных рекомендаций является клопидогрель.
Следует также указать, что в последние годы привлечено внимание клиницистов к возможности резистентности больных к аспирину (неспособность аспирина угнетать синтез тромбоксана А2 и подавлять агрегацию тромбоцитов). По данным разных исследований, частота резистентности к аспирину колеблется в широких пределах от 1 до 61% [7-9], однако надежных тестов для выявления аспиринорезистентности нет [10]. Сложилось мнение, что у пациентов с высоким риском тромботических осложнений целесообразно сочетать аспирин с другими антитромбоцитарными средствами (клопидогрелем - у больных ишемической болезнью сердца - ИБС, с синдромом перемежающейся хромоты, цереброваскулярной недостаточностью; дипиридамолом - после перенесенного ишемического инсульта).
В связи с этим понятен интерес клиницистов к сравнительно новому классу антиагрегантов - тиенопиридинам (тиклопидин, клопидогрель), уменьшающим агрегацию, блокируя АДФ-рецепторы тромбоцитов. После аспирина клопидогрель является одним из наиболее изученных антитромбоцитарных препаратов, эффективность и безопасность которого подтверждены в крупных рандомизированных контролируемых плацебо исследованиях.
Одним из первых исследований, в которых сравнивалась эффективность клопидогреля и аспирина, было исследование CAPRIE (Clopidogrel versus Aspirin in Patients at Risk of Ischaemic Events). В него были включены 19 185 больных с поражением одного из сосудистых бассейнов: больные, недавно перенесшие ИМ или ишемический инсульт либо страдающие атеросклерозом сосудов нижних конечностей и, соответственно, имеющие высокий риск развития повторной сердечно-сосудистой катастрофы. Половина больных в течение 1-3 лет (средняя длительность наблюдения 1,9 года) получали аспирин 325 мг/сут, половина - клопидогрель 75 мг/сут.
Частота регистрируемых ишемических событий (ИМ, ишемический инсульт, ампутация конечностей, сердечно-сосудистая смерть) составила 5,32% в группе рандомизированных к приему клопидогреля и 5,83% - в группе рандомизированных к приему аспирина (рис. 1). Относительное снижение риска возникновения этих событий при использовании клопидогреля составило 8,7% (р=0,043) [11]. Мнение экспертов, по результатам исследования, заключалось в том, что появился новый антиагрегант с отличающимся от аспирина механизмом действия, который не менее эффективен, чем аспирин, а у больных, перенесших ИМ, инсульт и страдающих перемежающейся хромотой, даже более эффективен. При сравнении эффективности клопидогреля и аспирина отдельно по подгруппам больных были обнаружены его наибольшие преимущества у лиц, страдающих перемежающейся хромотой. Возможно, это связано с тем, что у больных с перемежающейся хромотой АДФ как индуктор агрегации имеет большее значение, чем тромбоксан А2, на содержание которого преимущественно влияет аспирин. Кроме того, в исследовании CAPRIE в группе клопидогреля отмечено меньшее число осложнений со стороны ЖКТ (рис.2).
Рис. 1. Сравнительная эффективность аспирина и клопидогреля в исследовании CAPRIE [11].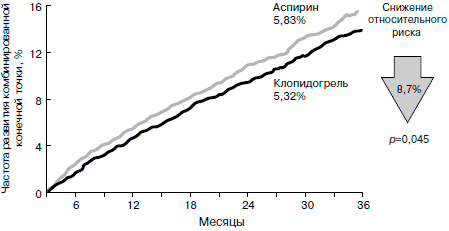
Рис. 2. Риск осложнений со стороны ЖКТ в исследовании CAPRIE [12].
Клопидогрель по сравнению с аспирином вызывает меньше осложнений со стороны ЖКТ 
После подведения итогов исследования CAPRIE возникла идея оценить эффективность одновременного назначения аспирина и клопидогреля у больных с показаниями к антитромбоцитарной терапии, тем более что имелись экспериментальные данные, указывающие на синергизм антитромботического действия аспирина и клопидогреля. В дальнейшем клопидогрель уже не противопоставляется аспирину, а используется в комбинации с аспирином. Так, в исследовании CURE (Clopidogrel in Unstable Angina to Prevent Recurrent Events) оценивается эффективность комбинации клопидогреля с аспирином и монотерапии аспирином при ОКС без стойких подъемов сегмента ST [13]. В исследование были включены 12 562 больных, 61% - с нестабильной стенокардией, а 39% - с мелкоочаговым ИМ. Подавляющее большинство больных получали гепарин (96% больных) и β-блокаторы (78% больных), около 50% больных получали ингибиторы ангиотензинпревращающего фермента (ИАПФ) и статины.
Все больные были рандомизированы в группу монотерапии аспирином (75-325 мг/сут; 6303 человека) или в группу терапии аспирином в комбинации с клопидогрелем (в 1-е сутки нагрузочная доза 300 мг, в дальнейшем - 75 мг/сут; 6259 больных). Нагрузочная доза клопидогреля (300 мг) позволила ускорить действие препарата: различия в сравниваемых группах начали проявляться уже через 2 ч. Через 12 мес количество главных конечных точек (смерть от сердечных причин, ИМ и инсульт) в группе больных, получавших комбинацию клопидогреля и аспирина, оказалось на 20% меньше, чем в группе аспирина (9,3 и 11,4% в группах соответственно, p=0,001; рис. 3). Относительный риск развития ИМ с зубцом Q в группе комбинированной терапии снизился на 40%! Уже к концу 1-х суток лечения количество сердечно-сосудистых смертей, ИМ, инсультов и эпизодов рефрактерной ишемии в группе клопидогреля было на 34% меньше, чем в группе плацебо (1,4 и 2,1% соответственно, p<0,003) [14]. На рефрактерной ишемии следует остановиться особо, поскольку ее уменьшение означает уменьшение числа пациентов с выраженным болевым синдромом, требующим коронарной реваскуляризации, проведения тромболизиса и др. (рис. 4). Однако следует отметить достоверно более высокую частоту больших кровотечений в группе комбинированной антиагрегантной терапии.
Рис. 3. Эффективность комбинированной антиагрегантной терапии при ОКС без ST: исследование CURE [13, 14].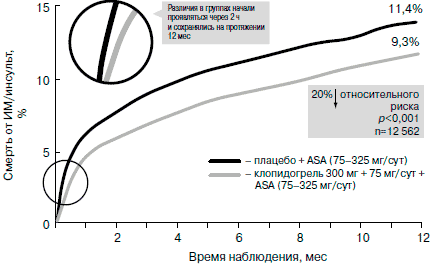
Рис. 4. Симптоматические эффекты комбинации аспирина с клопидогрелем в исследовании CURE [13].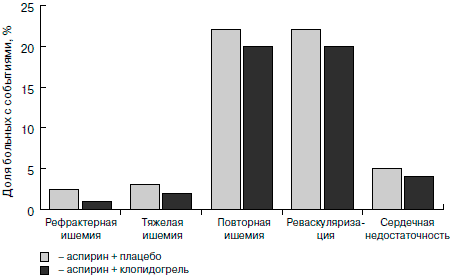
Результаты исследования CURE оказались столь впечатляющими, что комбинация аспирина и клопидогреля была включена в рекомендации по лечению больных ОКС без ST на электрокардиограмме (ЭКГ). Клопидогрель следует назначать вместе с аспирином немедленно после установления диагноза ОКС без ST (в 1-й день нагрузочная доза составляет 300 мг, в дальнейшем - по 75 мг ежедневно в течение 9-12 мес). При возникновении потребности в проведении аортокоронарного шунтирования клопидогрель следует отменить за 5 дней до операции [15-17].
В исследовании CURE более чем у 20% больных было выполнено чрескожное внутрикоронарное вмешательство (ЧКВ), в большинстве случаев со стентированием коронарной артерии. В рамках субисследования CURE-PCI (Clopidogrel in Unstable angina to prevent Recurrent Events - Percutaneous Coronary Intervention) планировалось оценить роль раннего назначения клопидогреля больным, подвергнутым ЧКВ. Для этого половине больных (n=1313) назначили клопидогрель в день поступления в стационар (в среднем за 10 дней до ЧКВ). Остальным больным (n=1345) клопидогрель был назначен в день выполнения ЧКВ (до этого они получали плацебо). Затем обе группы больных в течение 28 дней получали комбинацию аспирин + клопидогрель в «открытом» режиме, после чего 1-я группа продолжила комбинированную антитромбоцитарную терапию, 2-я вернулась к приему аспирина с плацебо. Частота неблагоприятных исходов (сердечная смерть, ИМ и необходимость в экстренной реваскуляризации) в течение 30 дней после ЧКВ в группе больных, получавших клопидогрель до ЧКВ, была достоверно ниже, чем в группе больных, начавших прием клопидогреля в день выполнения ЧКВ (4,5 и 6,4% соответственно, p=0,03) [18]. У больных, получавших клопидогрель до ЧКВ и продолживших его прием по окончании 28дневного периода «открытого» использования клопидогреля после ЧКВ, частота неблагоприятных исходов (сумма смертей и ИМ) в период от ЧКВ до окончания наблюдения была достоверно ниже (6%), чем в группе плацебо (8%; p=0,047). Если же за точку отсчета взять не ЧКВ, а момент рандомизации, то различие между группами будет более выраженным (частота смерти и ИМ составит 8,8% в группе клопидогреля и 12,6% - в группе плацебо; p=0,002); относительное снижение риска смерти и/или ИМ составило 31%. Преимущество клопидогреля перед плацебо отмечено не только в случае стентирования, но и в случаях, когда вмешательство ограничивалось обычной баллонной ангиопластикой коронарных артерий. При этом снижение риска смерти, ИМ и инсульта было даже более выраженным (44%), чем при ангиопластике со стентированием (27%). По завершении исследования CURE-PCI стали очевидными преимущества назначения клопидогреля в нагрузочной дозе минимум за 6 ч до ЧКВ с длительным последующим приемом, но и целесообразность применения препарата по такой схеме не только при стентировании коронарных артерий, но и у больных, подвергнутых обычной баллонной ангиопластике.
Доказательства эффективности длительной (около 1 года) терапии клопидогрелем после ЧКВ, полученные у больных с ОКС в исследовании CURE-PCI, послужили основанием для организации нового крупномасштабного исследования CREDO (Clopidogrel for the Reduction of Events During Observation trial), целью которого было изучение эффективности 12-месячной терапии клопидогрелем в дозе 75 мг/сут на фоне стандартной терапии, включающей аспирин, в сравнении с плацебо [19].
В исследование включали больных ИБС с показаниями к ЧКВ (53% имели клиническую картину нестабильной стенокардии). Все больные с 1-го дня после выполнения ЧКВ получали клопидогрель по 75 мг ежедневно в течение 28 дней. Рандомизация осуществлялась в две группы: больные в 1-й группе получали нагрузочную дозу клопидогреля 300 мг за 3-24 ч до ЧКВ, а затем по 75 мг ежедневно в течение 12 мес, во 2-й - вместо нагрузочной дозы клопидогреля было плацебо, и после 28-го дня до окончания времени наблюдения (12 мес) назначалось плацебо. Больные обеих групп на протяжении всего исследования получали аспирин. Оказалось, что длительный прием клопидогреля больными после ЧКВ приводит к снижению риска развития смерти, ИМ и инсульта на 27% (рис. 5). В соответствии с результатами исследований PCI-CURE и CREDO рекомендуется прием клопидогреля начинать с нагрузочной дозы 300 мг за 6 ч до выполнения ЧКВ и продолжать прием 75 мг клопидогреля ежедневно в течение 3-12 мес. При необходимости сократить время, требующееся для максимального подавления агрегации тромбоцитов, до 2 ч рекомендуется увеличить ударную дозу клопидогреля до 600 мг [20-22].
Рис. 5. Эффективность монотерапии аспирином и комбинированной терапии аспирином и клопидогрелем при ОКС без подъема ST: данные исследования CURE [13].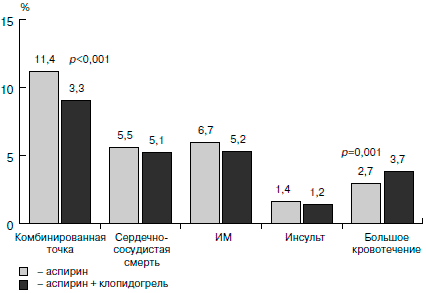
В 2007 г. E.Eisenstein и соавт. [23] опубликовали сообщение о необходимости более продолжительного, чем было рекомендовано ранее, приема клопидогреля после ЧКВ с установкой стентов, высвобождающих антипролиферативные препараты. В течение 2 лет осуществлялось наблюдение за больными, перенесшими ЧКВ с установкой обычных металлических стентов (3165 больных) или стентов, обработанных сиролимусом или паклитакселем (1501 больной). В той и другой группе больных учитывались такие исходы, как смерть, развитие острого ИМ или необходимость повторной реваскуляризации в зависимости от типа стента и приема в дополнение к аспирину клопидогреля или плацебо. У пациентов с освобождающими лекарства стентами без перечисленных событий через 6 мес после стентирования использование клопидогреля ассоциировалось со значительным снижением риска осложнений (смерть, смерть + острый ИМ), в то время как у больных, которым были установлены обычные стенты, влияние клопидогреля на риск осложнений было недостоверным (рис. 6). В настоящее время тип установленного стента учитывается при определении продолжительности приема клопидогреля после ЧКВ (рис. 7).
Рис. 6. Эффект длительного (до 1 года) приема клопидогреля после ЧКВ: данные исследования CREDO [19].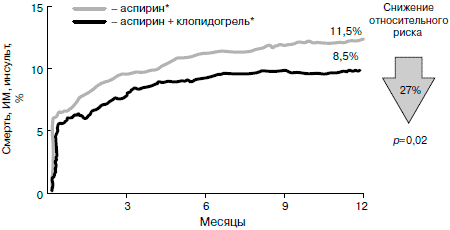
Рис. 7. Влияние длительной терапии клопидогрелем на частоту осложнений после ангиопластики со стентированием в зависимости от типа стента [23]. 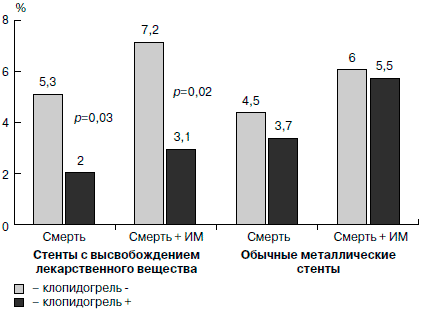
Исследование CLARITY (CLpidogrel as Adjunctive ReperfusIon TherapY) открыло новые возможности применения клопидогреля. Известно, что проводимый согласно стандартам лечения острого ИМ с подъемом сегмента ST тромболизис оказывается успешным немногим более чем у половины больных, причем у части больных даже после успешного тромболизиса развивается реокклюзия инфарктсвязанной коронарной артерии. Полагают, что это может быть связано с повышением активности тромбоцитов под действием тромболитиков. В исследование CLARITY были включены больные (n=3491), доставленные в стационар в течение 12 ч от появления симптомов со стойким подъемом сегмента ST. Половине больных в дополнение к аспирину и тромболитику назначался клопидогрель (нагрузочная доза 300 мг, затем - 75 мг/сут), половине - плацебо. Через несколько дней всем больным проводили коронарную ангиографию. Первичная комбинированная конечная точка включала в себя зарегистрированную при коронарографии окклюзию инфарктсвязанной артерии, смерть, рецидив ИМ. Частота достижения первичной конечной точки в группе плацебо составила 21,7%, в группе клопидогреля - 15%, т.е. в группе клопидогреля события, составляющие конечную точку, развивались на 36% реже (p<0,001). На 30-й день в группе клопидогреля такие неблагоприятные события, как сердечнососудистая смерть, повторный ИМ и повторная ишемия, потребовавшая реваскуляризации, развивались на 20% реже, чем в группе плацебо. Больные, получавшие клопидогрель, значительно реже подвергались экстренной коронарографии в первые 2 сут (15,4% против 18,6%, p=0,01) и неотложной реваскуляризации (19,5% против 23,3%, p=0,005). Частота крупных кровотечений и геморрагических инсультов в обеих группах достоверно не различалась [24].
Доказательства эффективности клопидогреля при остром ИМ также были получены в крупномасштабном исследовании COMMIT/CCS-2 (ClOpidogrel & Metoprolol in Myocardial Infarction Trial) [2]. В исследование COM-MIT/CCS-2 были включены 45 852 пациента с подозрением на острый ИМ. Больные были рандомизированы на две группы: получавших клопидогрель 75 мг/сут (без нагрузочной дозы) в течение 2-4 нед и получавших плацебо. Кроме того, все больные получали аспирин, и более чем половине больных была проведена тромболитическая терапия. Комбинированную конечную точку составили смерть, рецидив ИМ и инсульт; частота ее развития у больных, получавших клопидогрель, в течение 28 дней наблюдения оказалась на 9% ниже, чем у больных, получавших плацебо. Кроме того, отмечено достоверное (на 7%) снижение смертности. Было рассчитано, что клопидогрель, назначенный 1000 больных с подозрением на острый ИМ дополнительно к аспирину, предотвратит 3 рецидива ИМ (p=0,01), 1 инсульт (p=0,3) и 5 смертельных исходов (p=0,03). Следует отметить, что действие клопидогреля на конечную точку оказалось статистически значимым у больных, получивших тромболитик, но недостоверным у больных без тромболитического лечения.
Таким образом, в двух независимых друг от друга исследованиях, включавших почти 50 тыс. больных с ИМ, показана способность клопидогреля снижать риск осложнений преимущественно при проведении тромболитической терапии. Предполагается, что в основе благоприятного действия клопидогреля у этой категории больных лежит его способность предотвратить ретромбоз коронарной артерии после успешного тромболизиса.
В 2006 г. в США Управление по контролю за пищевыми продуктами и лекарственными средствами (Food and Drug Administration -FDA), основываясь на результатах исследований COMMIT и CLARITY (50 тыс. пациентов), одобрило использование клопидогреля (совместно с аспирином) в лечении пациентов с острым ИМ с подъемом сегмента ST на ЭКГ, которым не планируется выполнение ангиопластики.
Таким образом, комбинация аспирина и клопидогреля в острой ситуации (ОКС, острый ИМ, выполнение ЧКВ с последующим стентированием коронарных артерий) может обеспечить более высокую эффективность в предупреждении серьезных кардиоваскулярных событий, чем монотерапия аспирином. Однако большой интерес вызывали также перспективы комбинирования разных антитромбоцитарных препаратов, прежде всего аспирина и клопидогреля, для вторичной и первичной профилактики у пациентов с низким риском (при стабильном течении существующего ССЗ, при наличии факторов риска ССЗ). Попытка изучить эффективность комбинированной антитромбоцитарной терапии у таких пациентов была предпринята в международном контролируемом плацебо исследовании CHARISMA [26]. В этом исследовании, включавшем 15 603 пациента, изучали эффективность комбинированной антитромбоцитарной терапии клопидогрелем и аспирином в сравнении с монотерапией аспирином у лиц с уже имеющейся кардиоваскулярной патологией (документированные ИБС, цереброваскулярная патология и/или облитерирующий атеросклероз нижних конечностей) и у лиц без ССЗ, но с множественными факторами риска атеротромбоза. Первая подгруппа, соответственно, называлась симптомной, или группой вторичной профилактики атеротромботических событий, вторая - бессимптомной, или группой первичной профилактики. Средняя длительность наблюдения в этом исследовании составила 28 мес.
По результатам исследования, частота первичной конечной точки (сердечно-сосудистая смерть, нефатальные ИМ и инсульт) составила 7,3% в группе монотерапии аспирином и 6,8% в группе комбинированной антитромбоцитарной терапии (уменьшение относительного риска - 7,1%; p=0,22). Однако при оценке эффективности комбинированной терапии отдельно у больных с ССЗ (симптомная подгруппа) отмечены ее явные преимущества (6,9% в группе комбинированной терапии против 7,9% в группе монотерапии аспирином; относительное уменьшение риска составило 12,5%, p=0,046). Риск тяжелых геморрагических осложнений при этом возрос по сравнению с монотерапией аспирином недостоверно (1,7% против 1,3%, p=0,09). Однако у больных с множественными факторами риска ССЗ, но без диагностированного ССЗ, в случае комбинированной антитромбоцитарной терапии риск наступления сердечно-сосудистой смерти оказался достоверно выше, чем при монотерапии аспирином (3,9% против 2,2%, p=0,01). Таким образом, исследование CHARISMA продемонстрировало, что у больных с множественными факторами риска, но без установленных ССЗ, т.е. в качестве средства первичной профилактики, проведение комбинированной антитромбоцитарной терапии нецелесообразно, тогда как у больных с установленной кардиоваскулярной патологией риск сердечно-сосудистых осложнений снижается без значимого увеличения частоты тяжелых кровотечений. Результаты исследования CHARISMA явились «холодным душем» для приверженцев агрессивной антиагрегантной терапии [27]. Выводы из исследования CHARISMA представлены в табл. 3.
Таблица 3.
Антиагреганты при ангиопластике и стентировании коронарных артерий в зависимости от лекарственного покрытия стентов и использованного для покрытия препарата (Федеральное руководство по применению лекарственных препаратов, 2007)
| Продолжительность терапии после ЧКВ: 1) при использовании металлических стентов без покрытия - 2-4 нед; 2) при использовании стентов, покрытых сиролимусом, - не менее 3 мес; 3) при использовании стентов, покрытых пакликтакселом, - не менее 6 мес; 4) ОКС без подъема ST + покрытый стент - 1 год |
Рис. 8. Кривые концентрация-время при назначении здоровым добровольцам Лопирела и Плавикса. 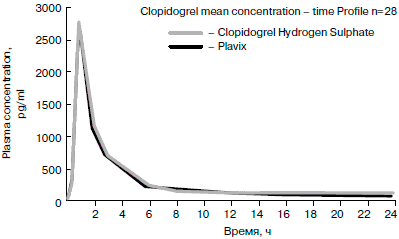
Наиболее обоснованным представляется использование комбинации клопидогреля и аспирина в тех случаях, когда имеется выраженное атеросклеротическое поражение сонных и других мозговых артерий у пациентов, перенесших транзиторную ишемическую атаку или инсульт, при сочетанном поражении артерий, а также при возникновении повторных сердечнососудистых событий на фоне приема аспирина [28].
Таким образом, в крупных клинических исследованиях (CAPRIE, CURE, CREDO) почти у 35 тыс. больных получены доказательства того, что клопидогрель является эффективным и безопасным средством профилактики тромботических осложнений атеросклероза. Клопидогрель признан обязательным элементом антитромботического лечения при стентировании коронарных артерий. Причем данные исследований исследования PCI CURE, CREDO указывают на необходимость начала лечения клопидогрелем не менее чем за 6 ч до внутрикоронарного вмешательства.
Главным недостатком оригинального клопидогреля остается его высокая стоимость, поэтому появление его генериков может только приветствоваться при условии их биоэквивалентности оригинальному препарату. Одним из генериков клопидогреля является препарат Лопирел, (компания «Актавис») недавно появившийся в России, доказательства фармакокинетической биоэквивалентности которого были получены при проведении исследования в Канаде (рис. 8). Лопирел выпускается в таблетках по 75 мг. Препарат хорошо всасывается из ЖКТ независимо от приема пищи. Торможение агрегации тромбоцитов наблюдается через 2 ч после приема нагрузочной дозы (300 мг), максимальный эффект - через 4-7 дней постоянного приема в дозе 75 мг/сут. Применение Лопирела показано у больных с ОКС (в комбинации с аспирином) и у больных, перенесших ИМ, ишемический инсульт, с синдромом перемежающейся хромоты (дозы и режим применения представлены в табл. 4). Лопирел хорошо переносится. К числу его наиболее часто встречающихся побочных эффектов относятся диспепсия, диарея. Подобно другим антитромбоцитарным препаратам, Лопирел следует с осторожностью назначать больным с повышенным риском кровотечения. Его назначение противопоказано при остром кровотечении, язвенной болезни желудка и двенадцатиперстной кишки в стадии обострения, беременности, тяжелой печеночной недостаточности. Перед оперативным вмешательством прием Лопирела следует прекратить за 5-7 дней. В случае необходимости эффект Лопирела может быть устранен переливанием тромбоцитной массы. Более низкая по сравнению с оригинальным клопидогрелем стоимость Лопирела позволяет надеяться на более широкое применение этого высокоэффективного антиагреганта как у больных с непереносимостью аспирина, так и в составе комбинированной антиагрегантной терапии.
Таблица 4.
Показания к применению Лопирела
| Контингент больных | Профилактика атеротромбоза | |
| начальная доза | поддерживающая доза | |
| Больные, перенесшие ИМ, ишемический инсульт, с диагностированным заболеванием периферических артерий | 75 | 75 |
| Больные с ОКС без подъема сегмента ST (нестабильная стенокардия или ИМ без зубца Q на ЭКГ), в комбинации с аспирином | 300 | 75 |
ЛИТЕРАТУРА 1. Fuster V, Fallon JT, Badimon JJ, Nemerson Y. The unstable atherosclerotic plaque: clinical significance and therapeutic intervention. Thrombosis and Hemostasis 1997; 78 (1): 247-55.
2. The World Health Report 2001. Geneva: WHO; 2001.
3. George JN. Platelets. Lancet 2000; 355: 1531-9.
4. Daniel JL, Dangelmaier C, Jin J et al. Molecular basis for ADP-induced platelet activation: I. Evidence for three distinct ADP receptors on human platelets. J Biol Chem 1998; 273: 2024-9.
5. Collaborative meta-analysis of randomized trials of antiplatelet therapy for prevention of death, myocardial infarction, and stroke in high risk patients. BMJ 2002; 324: 71-86.
6. Kubler W, Darius HZ. Kardiol 2005; 94 (suppl. 3): 66-73.
7. Gum PA, Kottke-Marchant K, Welsh PA et al. A prospective, blinded determination of the natural history of aspirin resistance among stable patients with cardiovascular disease. J Am Coll Cardiol 2003; 41: 961-5.
8. Mueller MR, Salat A, Stangl P et al. Variable platelet response to low-dose ASA and the risk of limb deterioration in patients submitted to peripheral arterial angioplasty. Thromb Haemost 1997; 78: 1003-7.
9. Eikelboom JW, Hirsh J, Weitz JI et al. Aspirin resistance and the risk of myocardial infarction, stroke, or cardiovascular death in patients at high risk of cardiovascular outcomes. Circulation 2002; 105: 1650-5.
10. Ушкалова Е.А. Аспиринорезистентность: механизмы развития, методы определения и клиническое значение. Фарматека. 2006; 13: 35-41.
11. CAPRIE Steering Committee. Lancet 1996; 348: 1329-39.
12. Harker LA et al. Drug Safety 1999; 21: 325-35.
13. The Clopidogrel in Unstable Angina to Prevent Recurrent Events trial investigators. Effects of clopidogrel in addition to aspirin in patients with acute coronary syndromes without ST.segment elevation. New Engl J Med 2001; 345:494-502.
14. Yusuf S, Mehta SR, Zhao F et al on Behalf of the CURE (Clopidogrel in Unstable angina to prevent Recurrent Events) Trial Investigators. Early and Late Effects of Clopidogrel in Patients With Acute Coronary Syndromes. Circulation 2003; 107: 966-72.
15. Bertrand ME, Simoons ML, Fox KAA et al. Management of acute coronary syndromes in patients presenting without persistent ST.segment elevation. The Task Force on the Management of Acute Coronary Syndromes of the European Society of Cardiology. EurHeart J 2002; 23: 1809-40.
16. Braunwald E, Antman EM, Beasley JW et al. ACC/AHA guideline update for the management of patients with unstable angina and non-ST.segment elevation myocardial infarction: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines (Committee on the Management of Patients With Unstable Angina). J Am Coll Cardiol 2002; 40: 1366-74.
17. Всероссийское научное общество кардиологов. Рекомендации по лечению острого коронарного синдрома без стойкого подъема сегмента ST на ЭКГ. М., 2007.
18. Mehta S, Yusuf S, Peters R et al. Effects of pretreatment with clopidogrel and aspirin followed by longterm therapy in patients undergoing percutaneous coronary intervention: the PCI CURE study. Lancet 2001; 358: 527-33.
19. Beinart S, Kolm P, Veledar E et al. «Short and Long.Term Cost Effectiveness of Early and Sustained Dual Oral Antiplatelet Therapy with Clopidogrel following Percutaneous Coronary Intervention: Results from CREDO» Circulation 2003; 108 (Suppl. 4; 17): iv-775 (abstract) 3495.
20. Seyfarth Hf, Koksch M, Roethig G et al. Effect of 300- and 450-mg clopidogrel LDs on membrane soluble P-selectin in patients undergoing coronary stent implantation. Am Heart f 2002; 143: 118-23.
21. Muller I, Seufarth M, Rudiger S et al. Effect of high LD of clopidogrel on platelet function in patients undergoing coronary stent placement. Heart 2000; 85: 92-3.
22. Angiolillo Df, Fernandez-Ortiz A, Bernardo E et al. High clopidogrel loading dose during coronary stenting: effects on drug response and interindividual variability. Eur Heartf 2004; 25: 1903-10.
23. Eisenstein EL, Anstrom Kf, Kong DF et al. Clopidogrel use and long-term clinical out-comes after drug-eluting stent implantation. JAMA 2007; 297 (2): 159-68.
24. Sabatine MS, Cannon CP, Gibson CM et al. Addition of clopidogrel to aspirin and fibrinolytic therapy for myocardial infarction with ST-segment elevation N Engl J Med 2005; 352: 1179-89.
25. COMMIT collaborative group. Addition of clopidogrel to aspirin in 45852 patients with acute myocardial infarction: randomized placebo-controlled trial. Lancet 2005; 366: I607-21.
26. Bhatt DL, Fox K.A, Hacke W et al CHARISMA Investigators. Clopidogrel and aspirin versus aspirin alone for the prevention of atherothrombotic events. N Engl J Med 2006; 354 (16): 1706-17.
27. Serebruany VL. Aggressive antiplatelet strategies: time to reconsider. Eur Heart J 2007; 28: 2183-4.
28. Ушкалова Е.А. Добавление клопидогреля к аспирину может быть полезно больным с симптоматическим атеротромбозом, но не рекомендуется для пациентов с множественными факторами риска: результаты исследования CHARISMA Фарматека. 2006; 13: 16-9.
