Диагностика и лечение при нарушениях функции щитовидной железы
СтатьиОпубликовано в журнале:
Клиническая и экспериментальная тиреоидология »» 2008, том 4, № 2
Muller A.F., Berghout A., Wiersinga W.M., Kooy A., Smit J.W.A., Hermus A., working group Thyroid Function Disorders of the Netherlands Association of Internal Medicine. Thyroid function disorders – Guidelines of the Netherlands Association of Internal Medicine// Neth. J. Med. 2008. V. 66. P. 134–142.
Перевод и комментарии В.В. Фадеева
Review of the Guidelines of the Netherlands Association of Internal Medicine for Thiroid Function Disorders
Предисловие к переводу
Уважаемые коллеги! Перед вами перевод (несколько адаптированный) рекомендаций Медицинской ассоциации Нидерландов по диагностике и лечению заболеваний щитовидной железы. Цель публикации данного материала – ознакомление российских эндокринологов с формой клинических рекомендаций в западных странах. На многочисленных конференциях во многих регионах нашей страны часто возникают вопросы, есть ли какие либо приказы Минздрава или других структур или некие стандарты, регламентирующие информацию, доводимую до сведения слушателей на лекциях и семинарах. (Например, что коллоидные узлы размером более 3 см далеко не всегда нужно оперировать или что беременность при гипотиреозе не нужно прерывать, а нужно назначить женщине заместительную терапию). Не хотелось бы переходить на обсуждения вопроса о том, нужны или нет эти так называемые стандарты, или оценивать качество имеющихся. Российская ассоциация эндокринологов в области патологии ЩЖ пошла по пути создания клинических рекомендаций, которые носят именно рекомендательный характер. Такие рекомендации существуют во многих западных странах. На мой взгляд, по сравнению с приказами и стандартами функционирование таких рекомендаций отражает более высокий уровень развития медицинской помощи и более высокий уровень культуры в этой области.
В представленных рекомендациях, которые датированы 2008 г., вы вряд ли найдете для себя какие-то незнакомые вещи: почти все их положения хорошо известны и получили проверку многолетней практикой. Тем не менее эти рекомендации в простой и лаконичной форме представляют серьезные вопросы и в полной мере отражают современное состояние тиреоидологии (среди соавторов экс-президент Европейской тиреоидной ассоциации Вильмар Вирсинга). Именно это обстоятельство и обусловило необходимость перевода этого документа, и это как раз та самая ситуация, когда перевод доставил не меньше удовольствия, чем чтение оригинала. Достаточно обширный список литературы к этим рекомендациям мы решили не публиковать, поскольку он занимает столько же места, сколько и сама статья.
Председатель секции по патологии щитовидной железы и околощитовидных желез Российской Ассоциации Эндокринологов
В.В. Фадеев
Введение
Заболевания щитовидной железы (ЩЖ) встречаются достаточно часто, причем у женщин в 4 раза чаще по сравнению с мужчинами. Распространенность первичного гипотиреоза и тиреотоксикоза среди взрослых женщин составляет соответственно 3,5 и 0,8 случая на 1000 населения. Представленные рекомендации в первую очередь адресованы специалистам, работающим во вторичных звеньях медицинской помощи, особенно интернистам, но могут быть интересны для врачей общей практики и для гинекологов. Рекомендации подготовлены авторским коллективом, в который вошли врачи многих специальностей. Положения рекомендаций отбирались из литературы на основе принципов доказательной медицины. Представленный документ является сокращенным вариантом рекомендаций, который ориентирован практическим врачам.
Диагностика и лечение нарушений функции щитовидной железы
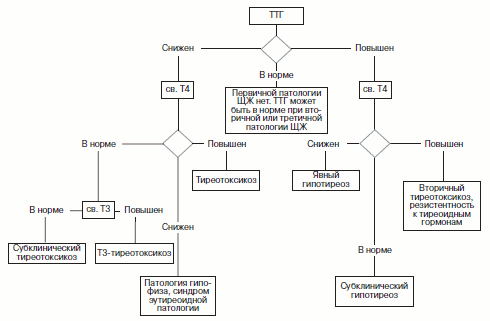
При оценке функции ЩЖ самым важным тестом является определение уровня ТТГ. На рис. 1 представлен алгоритм диагностики нарушений функции ЩЖ. Важно отметить, что в процессе лабораторной диагностики могут возникать различные аналитические проблемы, большинство которых связано с приемом различных лекарственных препаратов (табл. 1). Представленный алгоритм наиболее оправдан в амбулаторной практике. В случае тяжелой нетиреоидной патологии при оценке функции ЩЖ зачастую выявляются транзиторные изменения ряда параметров, которые нормализуются после компенсации основного заболевания. Таким образом, у тяжелых пациентов оценка функции ЩЖ должна проводиться только при очень высоком подозрении на ее заболевания. После оценки функции ЩЖ осуществляется нозологическая диагностика, в которой может помочь определение уровня антител или сцинтиграфия ЩЖ. Наиболее важно это при тиреотоксикозе.
| Подавление продукции ТТГ | Допамин, глюкокортикоиды, аналоги соматостатина |
| Подавление секреции Т4 | Амиодарон, литий |
| Стимуляция секреции Т4 | Йод, амиодарон |
| Нарушение абсорбции ТТГ | Желчные кислоты, железо, антациды, карбонат кальция, гидрохлорид алюминия, сукральфат |
| Стимуляция синтеза тироксинсвязывающего глобулина (ТСГ) | Эстрогены, опиоиды |
| Подавление синтеза ТСГ | Андрогены, глюкокортикоиды |
| Подавление 5' дейодиназы | Амиодарон, β-блокаторы, глюкокортикоиды |
| Диссоциация ТСГ и Т4 | Фуросемид, гепарин |
 |
Лечение тиреотоксикоза
Можно выделить 3 основные причины тиреотоксикоза: болезнь Грейвса (БГ), узловой и многоузловой токсический зоб и тиреоидиты. К методам лечения относятся консервативная терапии, терапия радиоактивным йодом и хирургическое лечение. Предпочтительный метод лечения определяется причиной тиреотоксикоза, в связи с чем принципиально важно установить правильный нозологический диагноз. Зачастую причина тиреотоксикоза очевидна, как, например, в случае выраженной эндокринной офтальмопатии. Однако в ряде случаев для дифференциальной диагностики может понадобиться сцинтиграфия ЩЖ; ее проведение рекомендуется в большинстве случаев тиреотоксикоза.
| Болезнь Грейвса: тиреостатики, радиоактивный йод, хирургия Узловой токсический зоб: радиоактивный йод, хи рургия Деструктивный тиреотоксикоз (подострый, после родовый тиреоидит и др.): активное наблюдение, симптоматическое лечение |
Лечение болезни Грейвса
За исключением случаев, когда речь идет об очень большом зобе или тиреотоксикозе значительной тяжести, медикаментозная терапия предпочтительна для большинства пациентов. Хирургическое лечение наиболее оправдано при зобе очень большого размера и/или при очень тяжелом тиреотоксикозе. Высокий уровень антител к рецептору ТТГ ассоциирован с низкой вероятностью стойкой ремиссии БГ. На основании анализа литературы можно сделать вывод о том, что пропилтиоурацил (ПТУ) и тиамазол являются одинаково эффективными тиреостатическими средствами. При этом на фоне их приема побочные реакции развиваются с одинаковой частотой (сыпь, артралгия, желудочно кишечные расстройства, изменение вкусовых ощущений). С другой стороны, более тяжелые, но весьма редкие побочные эффекты, такие как гепатит или васкулит с антинейтрофильными цитоплазматическими антителами, несколько чаще ассоциированы с приемом ПТУ. Важно отметить, что тиамазол можно принимать 1 раз в день, что повышает приверженность пациента к лечению. Следует помнить, что как ПТУ, так и тиамазол может способствовать развитию агранулоцитоза, а в случае возникновения ангины с лихорадкой тиреостатик должен быть отменен до тех пор, пока будет исключен агранулоцитоз. Поэтому мы рекомендуем тиамазол как препарат выбора тиреостатической терапии у взрослых за исключением беременных женщин.
Проведенный недавно метаанализ показал, что эффективность тиреостатической терапии в плане развития в перспективе стойкой ремиссии одинакова для режима «блокируй и замещай» (высокие дозы тиреостатиков в сочетании с L-Т4) и режима «блокируй». После курса лечения продолжительностью 6–18 мес вероятность рецидива тиреотоксикоза составила 51% для схемы «блокируй и замещай» и 54% для схемы «блокируй». Вероятность побочных эффектов в случае использования схемы «блокируй и замещай» была лишь погранично выше, чем на схеме «блокируй». Следует отметить, что отличия были обнаружены в отношении только легких, но не тяжелых побочных эффектов. В результате мы преимущественно рекомендуем проведение тиреостатической терапии болезни Грейвса по схеме «блокируй и замещай» на протяжении 12–18 мес, которая позволяет надежнее контролировать эутиреоидное состояние и предотвращать медикаментозный гипотиреоз, что выгодно отличает эту схему от титрационного режима («блокируй»); исключением в этом случае являются беременные женщины.
Тиамазол: стартовая доза 30 мг 1 раз в день
|
Если после курса тиреостатической терапии у пациента развивается рецидив тиреотоксикоза, предпочтительным методом лечения является тера пия 131I. Молодым пациентам, у которых нет сердеч но сосудистых заболеваний 131I может быть назначен без предварительного достижение эутиреоза на фоне терапии тиреостатиками. У пожилых пациентов и при сердечно сосудистых заболеваниях 131I назна чается после подготовки тиреостатиками. Тиамазол при этом необходимо отменить за 3–5 дней, а ПТУ как минимум за 15 дней до назначения 131I. У таких пациентов тиреостатики лучше вновь назначить примерно через 4 дня после приема 131I и продолжать на протяжение как минимум 3 мес, чтобы предот вратить выраженный тиреотоксикоз вследствие дес трукции ЩЖ. Риск стойкого рецидива тиреотокси коза зависит от введенной активности 131I. Примерно у 10% пациентов гипотиреоз, развившийся в бли жайшие сроки после назначения 131I, оказывается транзиторным. В связи с этим через полгода после начала заместительной терапии целесообразно отме нить L-Т4, чтобы оценить реальную функцию ЩЖ. Терапию 131I следует рассматривать уже как лечение первого выбора при БГ и при большом зобе и/или тяжелом тиреотоксикозе.
|
Хирургическое лечение БГ следует обсуждать в случае тяжелых аллергических реакций на тиреостатики, при сочетании БГ с опухолями ЩЖ, а так же в том случае, когда радикального излечения нужно добиться в максимально быстрые сроки (например, при выраженной компрессионном синдроме). Оперативное лечение состоит в предельно субтотальной резекции ЩЖ или тиреоидэктомии. Перед операцией необходимо достичь эутиреоидного состояния. Возможными осложнениями (вероятность развития которых определяется опытом хирурга) являются гипопаратиреоз и повреждение возвратного гортанного нерва.
|
Лечение эндокринной офтальмопатии
Эндокринная офтальмопатия (ЭОП) встречается у 87% пациентов с БГ. Примерно у 3% пациентов с ЭОП определяется гипотиреоз, а у 10% – эутиреоз. В последнем случае у пациентов, как правило, выявляются антитела к рецептору ТТГ и в 25% случаев в течение нескольких лет развивается тиреотоксикоз. При обычном для БГ сочетании ЭОП и тиреотоксикоза последний предшествует ЭОП в 20% случаев, развивается одновременно с ЭОП в 40% и манифестирует после ЭОП еще в 40% случаев. С другой стороны, только у 5–15% пациентов с болезнью Грейвса и тиреотоксикозом развивается тяжелая ЭОП и у 30–40% пациентов – ЭОП умеренной тяжести. ЭОП обычно носит двусторонний характер, но в 15% случаев развивается унилатерально. Более того, ЭОП является самой частой причиной одностороннего экзофтальма. Качество жизни пациентов с ЭОП значительно снижено. Восстановление эутиреоидного состояния чаще приводит как минимум к некоторому облегчению ЭОП. По своему влиянию на течение ЭОП тиреостатическая терапия и хирургическое лечение одинаково безопасны. Тем не менее терапия 131I может привести к утяжелению (манифестации) ЭОП примерно у 15% пациентов с БГ. Такое утяжеление обычно происходит в течение первых нескольких месяцев после назначения 131I. При этом в двух третях случаев речь идет лишь о легких изменениях со стороны глаз, которые, как правило, транзиторны. Назначение глюкокортикоидов может предотвратить утяжеление ЭОП после терапии 131I, в связи с чем оно рекомендуется пациентам с уже имеющейся активной офтальмопатией в сочетании с тяжелым тиреотоксикозом (общий Т3 более 5 нмоль/л), высоким уровнем антител к рецептору ТТГ, особенно у курящих.
| 1–4 нед: преднизолон 30 мг/сут 5–8 нед: преднизолон 20 мг/сут 9–12 нед: снижать дозу преднизолона на 5 мг в неделю до отмены |
Всем пациентам с ЭОП необходимо рекомендовать отказ от курения, поскольку оно ассоциировано с более тяжелым течением ЭОП и снижением эффективности лечения. Для решения задачи о назначении иммуносупрессивной терапии и хирургического лечения ЭОП последнюю необходимо классифицировать по тяжести и активности. С этой целью рекомендуется использовать классификацию NOSPECS.
|
|
При ЭОП умеренной тяжести может быть применена радиотерапия на ретробульбарную область. Она наиболее эффективна по влиянию на такие проявления ЭОП, как болевой синдром и нарушение подвижности глаз, но не оказывает влияния на проптоз. При более тяжелой офтальмопатии могут быть использованы препараты с иммуносупрессивной активностью (предпочтительно глюкокортикоиды внутривенно). Оптическая нейропатия и изъязвление роговицы являются наиболее тяжелыми проявлениями ЭОП. Для их лечения должны использоваться высокие дозы глюкокортикоидов или декомпрессия орбиты. Лечение настоятельно рекомендуется проводить в специализированных центрах, которые имеют опыт иммуносупрессивной терапии и хирургической декомпрессии орбиты.
Йодиндуцированный тиреотоксикоз
Избыточное поступление йода может привести к развитию тиреотоксикоза. Нидерланды относятся к региону с нормальным потреблением йода (150–300 мкг в день). При ряде заболеваний ЩЖ, в частности БГ в анамнезе и при многоузловом зобе, избыток йода может привести к развитию тиреотоксикоза, который с определенным допущением можно обозначить как йодиндуцированный тиреотоксикоз (ЙТ). Наиболее частыми источниками йода при ЙТ являются: йодсодержащие рентгеноконтрастные вещества, амиодарон, келп, йодсодержащие поливитамины, японские блюда в большом количестве. ЙТ вследствие введения йодсодержащих рентгеноконтрастных веществ и амиодарона будет обсуждаться более детально.
ЙТ после введения йодсодержащих рентгеноконтрастных веществ развивается у 0–1,2% пациентов без предсуществующей патологии ЩЖ. У пациентов с патологией ЩЖ это происходит значительно чаще – в 5,2% случаев. Факторами риска являются пожилой возраст, узловой зоб и подавленный ТТГ. Такой тиреотоксикоз, как правило, выражен умеренно и спонтанно разрешается. Для его предотвращения может быть использован тиамазол (20 мг 1 раз в день) и перхлорат натрия (300 мг 3 раза в день). Тем не менее такая терапия не может полностью предотвратить развитие тиреотоксикоза. В то же время она не лишена побочных эффектов. Таким образом, ее, вероятно, имеет смысл назначать только пациентам с высоким риском развития тяжелых аритмий сердца.
|
Амиодарон оказывает большое влияние на обмен тиреоидных гормонов и функцию ЩЖ. Он на 39,3% состоит из йода, в связи с чем ежедневное назначение 200–400 мг препарата приводит к значительному избытку йода, который может подавить органификацию йода в ЩЖ (эффект Вольфа – Чайкова), в результате чего может произойти некоторое повышение уровня ТТГ обычно в пределах 5–15 мЕд/л – примерно через 3 мес за счет «ускользания» от эффекта Вольфа Чайкова ТТГ нормализуется. Периферические эффекты амиодарона на обмен тиреоидных гормонов в сумме приводят к тому, что может произойти повышение уровня Т4 и св. Т4 при сохранении нормального уровня ТТГ. Если пациент получает амиодарон, при интерпретации у него уровня Т4 и св. Т4 следует исходить из того, что верхний референсный предел для этих показателей нужно повысить примерно на 25%. В Нидерландах амиодарониндуцированный тиреотоксикоз (АмИТ) развивается у 12,1% пациентов, получающих этот препарат. Его клиническая картина широко варьирует. При этом зачастую она выражается утяжелением аритмии сердца. Риск развития АмИТ не зависит откумулятивной дозы препарата; он развивается непредсказуемо и в достаточно короткие сроки. Есть два типа АмИТ. При этом результаты лечения в значительной мере зависят от их тщательной дифференциальной диагностики. АмИТ 1-го типа – тиреотоксикоз с гиперфункцией ЩЖ, развивающийся у пациентов с многоузловым зобом или БГ. Нередко выявляются антитела к ЩЖ. Поскольку ЩЖ при АмИТ 1-го типа гиперфункционирует и развивается ее гиперваскуляризация, для лечения может быть использован радиоактивный 131I. В основе патогенеза АмИТ 2 го типа лежит деструктивный тиреотоксикоз, который является результатом цитотоксического эффекта амиодарона на фолликулярные клетки ЩЖ. Лечение 2-го типа АмИТ может оказаться достаточно сложным. Предпочтительным вариантом лечения АмИТ 1-го типа является терапия тиамазолом (30 мг в день) в комбинации с перхлоратом калия (500 мг 2 раза в день). В этом случае применение только тиамазола не столь эффективно, и он незначительно сокращает продолжительность тиреотоксикоза (если он транзиторен), поскольку в организме присутствует значительный избыток йода. Если это возможно, рекомендуется прекратить прием амиодарона, но, к сожалению, у большинства пациентов тиреотоксикоз сохраняется на протяжении еще примерно 6 мес, несмотря на отмену амиодарона. В ряде случаев при АмИТ 1-го типа захват радиоактивного йода оказывается достаточным для того, чтобы использовать в лечении 131I. При АмИТ 2-го типа лечением выбора является назначение преднизолона: 30 мг ежедневно на протяжении 2 нед с последующим снижением дозы и отменой препарата в течение 3 мес. При АмИТ 2-го типа продолжение терапии амиодароном в большинстве случаев возможно. При стойкой и непреодолимой невозможно сти контроля тиреотоксикоза и его рецидивах при попытке отмены преднизолона как альтернатива выполняется тиреоидэктомия.
|
Субклинический тиреотоксикоз
Субклинический тиреотоксикоз характеризуется подавленным уровнем ТТГ при нормальных св. Т4 и св. Т3. После того как будут исключены такие причины подавления ТТГ, как медикаменты (глюкокортикоиды, допамин), синдром эутиреоидной патологии, заболевания гипофиза и гипоталамуса, можно говорить о том, что у пациента есть небольшой избыток тиреоидных гормонов в организме, который превышает некий индивидуальный порог. Распространенность эндогенного субклинического тиреотоксикоза составляет 0,7–1,9%, экзогенного – 1,3–2,0%. Причиной эндогенного субклинического тиреотоксикоза являются узловой зоб, БГ и тиреоидиты. Субклинический тиреотоксикоз ассоциирован с фибрилляцией предсердий: среди участников Фрамингемского кардиологического исследования, у которых уровень ТТГ был менее 0,1 мЕд/л, 10 лет няя кумулятивная частота ее новых случаев составила 28% по сравнению с контрольной популяцией с нормальным уровнем ТТГ. Эти данные недавно были подтверждены в исследовании Capolla et al., которые у лиц с уровнем ТТГ менее 0,4 мЕд/л, наблюдавшихся на протяжении 13 лет, обнаружили вдвое большую частоту новых случаев фибрилляции предсердий по сравнению с лицами без нарушений функции ЩЖ. Помимо нарушений ритма, субклинический тиреотоксикоз ассоциирован с рядом неблагоприятных эхокардиографических изменений. У женщин в постменопаузе субклинический тиреотоксикоз является фактором риска остеопороза. В связи с этим был сделан вывод о том, что у женщин с подавленным ТТГ выше риск переломов, чем у женщин с эутиреозом. Наконец, по некоторым данным при субклиническом тиреотоксикозе в 3 раза выше риск развития деменции. Тем не менее вопрос о том, что при субклиническом тиреотоксикозе повышена смертность, не столь однозначен. В результате всего вышесказанного можно сделать вывод, что субклинический тиреотоксикоз требует коррекции как минимум у пациентов с симптоматикой тиреотоксикоза, фибрилляцией предсердий и остеопенией. Вне зависимости от наличия каких либо симптомов или проявлений субклинический тиреотоксикоз требует коррекции у лиц старше 60 лет, у женщин в постменопаузе, особенно если ТТГ при этом ниже 0,1 мЕд/л.
Тиреоидиты
Причиной воспалительных заболеваний ЩЖ могут быть внешние воздействия, микроорганизмы и аутоиммунный процесс. Здесь мы кратко расскажем о подостром гранулематозном тиреоидите и подостром лимфоцитарном тиреоидите. О послеродовом тиреоидите речь пойдет отдельно.
Распространенность подострого гранулематозного тиреоидита (ДеКервена) в 5 раз меньше, чем таковая для БГ, причем значительно чаще он встречается среди женщин. Предполагается, что заболевание обусловлено вирусной инфекцией или воспалением, развившимся после вирусной инфекции. Клинически подострый тиреоидит представлен болью в области ЩЖ, часто иррадиирущей в уши, в сочетании с мышечными болями, слабостью и симптомами тиреотоксикоза. При физикальном исследовании выявляется болезненный зоб. В острую фазу определяется повышение СОЭ (как правило, более 40 мм) в сочетании с легкой анемией и лимфоцитозом. При исследовании функции ЩЖ выявляется тиреотоксикоз, который продолжается от 2 до 10 нед и спонтанно прекращается. Тиреотоксикоз при подостром тиреоидите имеет деструктивную природу, в связи с чем носит самолимитирующийся характер. Лечение симптоматическое: аспирин (600 мг от 3 до 6 раз в день) и β адреноблокаторы. В редких случаях для купирования болевого синдрома необходимо назначение глюкокортикоидов (40 мг преднизолона – 1 нед, далее – 30 мг с постепенным снижением дозы на протяжении 5 нед). У пациентов, перенесших подострый тиреоидит, риск развития стойкого гипотиреоза в отдаленной перспективе не повышен.
| Аспирин: 600 мг от 3 до 6 раз в день β-адреноблокаторы: пропранолол 40–120 мг в день или атенолол 25–50 мг в день |
Подострый лимфоцитарный тиреоидит и послеродовый тиреоидит в большинстве случаев рассматриваются как варианты тиреоидита Хашимото (АИТ). И в том и в другом случае речь идет о деструктивном тиреотоксикозе аутоиммунного генеза. В отличие от подострого гранулематозного тиреоидита при подостром лимфоцитарном тиреоидите отсутствует болевой синдром (безболевой или «молчащий» тиреоидит). Кроме того, изменение функции ЩЖ при нем чаще носит двухфазный характер – за тиреотоксической фазой следует гипотиреоидная. Тирео токсикоз самолимитируется, поскольку он имеет деструктивный генез. С другой стороны, сменяющий его гипотиреоз в 6% случаев оказывается необратимым. При этом важно отметить, что он может развиться спустя достаточно длительный период эутиреоидного состояния. В связи с этим у таких пациентов реко мендуется ежегодная оценка функции ЩЖ.
Лечение первичного гипотиреоза
Явный гипотиреоз
Первичный гипотиреоз, причиной которого являются заболевания ЩЖ, характеризуется повышенным уровнем ТТГ и сниженным св. Т4. Симптомы гипотиреоза весьма неспецифичны и значительно варьируют по выраженности. К ним относятся: зябкость, запоры, сухость кожи, брадикардия, охриплость голоса, снижение памяти. Крайним и казуистически редким осложнением гипотиреоза является гипотиреоидная кома. У детей гипотиреоз может обусловить ментальную ретардацию. Кроме того, она может развиться вследствие гипотиреоза у матери в условиях тяжелого йодного дефицита. Общая распространенность гипотиреоза составляет 0,3–0,4%, причем она нарастает с возрастом и значительно выше среди женщин. В большинстве случаев гипотиреоз имеет аутоиммунный генез. Кроме того, он может быть ятрогенным (после лечения токсического зоба), медикаментозным (амиодарон, литий) или врожденным. Лечение гипотиреоза подразумевает заместительную терапию левотироксином (L-Т4). Вне зависимости от причины гипотиреоза, заместительная доза L-Т4 назначается исходя из веса и составляет около 1,8 мкг/кг при гипотиреозе в исходе АИТ и около 2,0 мкг/кг при гипотиреозе после тотальной (предельно субтотальной) тиреоидэктомии. При этом межиндивидуальная вариация дозы очень высока. У молодых пациентов и при отсутствии сопутствующей патологии полная заместительная доза L-Т4 может быть назначена сразу, тогда как у более пожилых (ориентировочно старше 60 лет), а также при сопутствующей сердечно сосудистой патологии рекомендуется постепенное начало заместительной терапии (25 мкг с постепенным повышением дозы каждые 4–6 нед под контролем ТТГ). Важно отметить, что отличия в качестве жизни у пациентов, у которых повышение дозы L-Т4 проводилось медленно и быстро, выявлены не были. Доза L-Т4 подбирается в соответствии с уровнем ТТГ, но не св. Т4. При этом целью лечения является поддержание уровня ТТГ в норме. L-Т4 должен приниматься ежедневно утром натощак. Ряд лекарственных препаратов, таких, как соли желчных кислот, железо, антациды, карбонат кальция, гидрохлорид алюминия, сукральфат, нарушают всасывание L-Т4. Эти препараты рекомендуется принимать через 2–4 ч после L-Т4. Фенитоин, карбамазепин, фенобарбитал и рифампицин усиливают клиренс L-Т4, в связи с чем на фоне их приема может понадобиться увеличение дозы L-Т4.
Сохранение симптомов гипотиреоза несмотря на компенсацию:
комбинированная терапия Т4 + Т3
У существенной части пациентов с гипотиреозом, несмотря на достижение нормального уровня ТТГ, сохраняются некие неспецифические симптомы. Возможным объяснением этого является недостаточность Т3, который частично продуцируется ЩЖ, но не восполняется на фоне монотерапии L-Т4. В недавнем метаанализе 11 исследований, в который в общей сложности вошли 1216 рандомизированных пациентов, значимых отличий в плане выраженности различных болевых ощущений, депрессии, тревожности, качества жизни и показателей липидного спектра, между монотерапией L-Т4 и комбинированной терапией L-Т4 + L-Т3 выявлено не было. В крупном голландском исследовании пациенты с гипотиреозом нашли предпочтительной комбинированную терапию с соотношением L-Т4 : L-Т3 = 5 : 1. Следует отметить что, это субъективное предпочтение не удалось никак объективизировать при помощи большого количества нейрокогнитивных тестов. Пациентам импонировало снижение веса на фоне комбинированной терапии. При использовании терапии с указанным соотношением L-Т4 : L-Т3 у 51% пациентов определялись подавление ТТГ, большая ЧСС и повышение маркеров костной резорбции.
На основании всего сказанного комбинированная терапия L-Т4 + L-Т3 не рекомендуется в качестве стандартной заместительной терапии при гипотиреозе. При стойком сохранении симптомов гипотиреоза на фоне заместительной терапии L-Т4 рекомендуется небольшое повышение дозы препарата с целью достижения низконормального уровня ТТГ. При этом следует учесть, что у этой рекомендации отсутствует достаточная доказательная база. Кроме того, важно исключить наличие у пациентов сопутствующих заболеваний, которые могут быть причиной плохого самочувствия, в том числе аутоиммунных, таких, как сахарный диабет 1-го типа, надпочечниковая недостаточность, дефицит витамина В-12 и целиакия.
|
Субклинический гипотиреоз
Под субклиническим гипотиреозом (СГ) подразумевается феномен, при котором уровень ТТГ повышен, а св. Т4 в норме. Помимо гипотиреоза, такого рода изменения могут развиваться при синдроме эутиреоидной патологии, восстановлении функции ЩЖ после перенесенного тиреоидита, а также на фоне лечения рекомбинантным человеческим ТТГ. Распространенность СГ в популяции варьирует между 4 и 8,5%. Риск развития явного гипотиреоза у пациентов с СГ напрямую зависит от уровня ТТГ и наличия антител к тиреоидной пероксидазе (АТ ТПО). При уровне ТТГ менее 6 мЕд/л кумулятивный риск развития явного гипотиреоза, при отсутствии АТ ТПО близок к нулю, если ТТГ оказывается от 6 до 12 мЕд/л, он составляет 42,8%, а при ТТГ более 12 мЕд/л кумулятивная частота новых случаев явного гипотиреоза составит 76,9%. Наличие АТ ТПО может увеличить имеющийся риск развития явного гипотиреоза, особенно если ТТГ находится в пределах 6 и 12 мЕд/л. В этом случае носительство АТ ТПО увеличивает риск развития явного гипотиреоза до 80%. При ТТГ меньше 6 мЕд/л носительство АТ ТПО увеличивает риск развития явного гипотиреоза до 40%.
В настоящее время есть результаты только одного исследования, которое при проспективном наблюдении пациентов с СГ на протяжении 20 лет не обнаружило у них увеличения смертности от сердечно сосудистых заболеваний. С другой стороны, 2 недавно опубликованных метаанализа свидетельствуют о том, что СГ ассоциирован с ИБС. К сожалению, пока не выполнялось интервенционных исследований достаточно высокого качества, которые бы показали эффективность назначения L-T4 при СГ в плане предотвращения сердечно сосудистого риска. Несмотря на это, то есть на отсутствие прямых и высококачественных доказательств эффективности, представляется вполне резонным назначение как минимум на 3 мес заместительной терапии L-T4 пациентам с субклиническим гипотиреозом и такими проявлениями, как необъяснимая слабость и когнитивная дисфункция. Следует отметить, что у лиц старше 85 лет субклинический гипотиреоз ассоциирован с меньшей смертностью даже по сравнению с эутиреоидным состоянием.
Литий индуцированный гипотиреоз
Зоб развивается примерно у 50% пациентов, получа ющих препараты лития. Наиболее вероятно, это обусловлено повышением уровня ТТГ, поскольку субклинический и явный гипотиреоз выявляется у 20–40% и в 4,4% случаев соответственно. В связи с этим у пациентов, получающих препараты лития, мы рекомендуем определение уровня ТТГ каждые 6–12 мес, а с целью предотвращения развития зоба – назначение L-Т4 в том случае, если уровень ТТГ превышает 4 мЕд/л.
Заболевания щитовидной железы во время беременности и в послеродовом периоде
Во время беременности происходят существенное изменение обмена тиреоидных гормонов и увеличение потребности в йоде вследствие его трансплацентарного транспорта к плоду. Ежедневная потребность в йоде во время беременности и лактации составляет не менее 250 мкг. Под влиянием эстрогенов значительно увеличивается уровень тироксинсвязывающего глобулина (ТСГ), что, в свою очередь, приводит к увеличению уровня общего Т4 и общего Т3. В первом триместре беременности уровень хорионического гонадотропина (ХГЧ) быстро и значительно повышается. Поскольку ХГЧ структурно гомологичен ТТГ, уровень последнего снижается опосредованно стимулирующему действию ХГЧ на ЩЖ (ТТГ менее 0,4 у 10% женщин). Кроме того, существенная часть тироксина транспортируется через плаценту и метаболизируется в ней, что еще более увеличивает потребность в тиреоидных гормонах во время беременности. Поскольку фетальная система «гипофиз – ЩЖ» начинает функционировать только около 12-й нед. беременности, до этого времени развитие плода полностью зависит от тиреоидных гормонов матери.
Гипертиреоз во время беременности наиболее часто обусловлен гестационной транзиторной гипертиреоксинемией. Она развивается у 2–3% европейских и у 11% азиатских женщин. Распространенность БГ среди беременных женщин составляет 0,01–0,02%. Нелеченный или плохо леченный тиреотоксикоз при БГ ассоциирован с акушерскими осложнениями (выкидыши, низкий вес плода, преэксампсия, возможно, врожденные аномалии).
Гестационный транзиторный гипертиреоз, как правило, развивается в первом триместре и в 50% случаев ассоциирован со рвотой у беременных. При гестационном транзиторном гипертиреозе чаще всего отсутствует зоб, никогда не бывает эндокринной офтальмопатии, не определяются антитела к рецептору ТТГ (АТ рТТГ); тиреотоксикоз, как правило, весьма умеренный и в большинстве случаев спонтанно разрешается до 18 нед беременности. БГ следует подозревать при обнаружении диффузного зоба, офтальмопатии, дермопатии и АТ рТТГ. У женщин с БГ, которые планируют в ближайшем будущем беременности, предпочтительным методом лечения являются радикальные методы, целью которых должна быть аблация ЩЖ: терапия радиоактивным йодом или тиреоидэктомия. Следует отметить, что на протяжении полугода после терапии 131I планирование беременности противопоказано, так как за такой строк не всегда удается достичь стойкого эутиреоидного состояния. При выявлении БГ во время беременности показано проведение консервативной тиреостатической терапии, которая подразумевает монотерапию тиреостатиками в минимально возможной дозе, позволяющей поддерживать уровень св. Т4 на верхней границе нормы. В связи с тем, что было опубликовано несколько сообщений о развитии у детей, матери которых во время беременности принимали тиамазол, аплазии кожи, атрезии хоан и пищевода, предпочтение следует отдавать пропилтиоурацилу. Функцию ЩЖ рекомендуется оценивать не реже чем каждые 6–8 нед. В крайне редких случаях, когда тиреотоксикоз не удается контролировать тиреостатиками, во втором триместре беременности может быть предложено проведение тиреоидэктомии. Во время грудного вскармливания малые дозы тиреостатиков безопасны для ребенка: тиамазол менее 20 мг или ПТУ менее 300 мг в день. Для оценки риска фетального и неонатального тиреотоксикоза должно использоваться определение уровня АТ рТТГ у матери. Эти антитела рекомендуется определять у всех женщин с БГ, в том числе в анамнезе. Особенно это касается женщин, которые в прошлом получали аблативную терапию БГ. АТ рТТГ могут быть определены в первом или втором триместре беременности, а в случае их выявления тест необходимо повторить еще раз в третьем триместре. Если же эти антитела определяются и в третьем триместре, необходим адекватный мониторинг плода и новорожденного на предмет неонатального тиреотоксикоза.
По имеющимся данным литературы даже легкая, как правило, нераспознанная гипотиреоксинемия у беременной женщины (например, сниженный св. Т4 при нормальном ТТГ) ассоциирована со стойкими нейрофизиологическими нарушениями у детей. К сожалению, в настоящее время отсутствуют проспективные исследования по влиянию заместительной терапии L-Т4 на неврологическое развитие детей в более или менее отдаленном периоде. Важно отметить, что определение уровня св. Т4 во время беременности сопряжено с серьезными аналитическими проблемами. В связи с этим до настоящего времени остается неясным, как относится к ситуации, когда у беременной женщины снижен уровень св. Т4, а уровень ТТГ – в норме. Для ситуаций повышенного уровня ТТГ (например, более 4,0 мЕд/л) доказано увеличение вероятности развития акушерских осложнений. В связи с этим субклинический гипотиреоз во время беременности (ТТГ более 4,0 мЕд/л) требует назначения заместительной терапии. Данные о том, имеет ли преимущества лечение субклинического гипотиреоза у женщин с бесплодием неясного генеза и с привычным невынашиванием, в настоящее время отсутствуют. Тем не менее, принимая во внимание сказанное выше, L-Т4 в таких ситуациях рекомендуется назначать.
При выявлении явного гипотиреоза (повышенный ТТГ, сниженный св. Т4) во время беременности необходимо сразу назначить полную заместительную дозу L-Т4. У женщин, которые до наступления беременности получали заместительную терапию L-Т4, потребность в препарате обычно увеличивается примерно на 50%. Если женщина с субклиническим гипотиреозом не получает заместительную терапию, оценку функции ЩЖ ей необходимо провести сразу после наступления беременности. Женщин, которые получают L-Т4 по поводу гипотиреоза, нужно проинструктировать о необходимости увеличения дозы препарата примерно на 30% сразу после наступления беременности, после чего доза L-Т4 будет корригироваться на основании данных оценки функции ЩЖ. Как и в случае лечения во время беременности тиреотоксикоза, при лечении гипотиреоза оценка функции ЩЖ необходима каждые 6–8 нед, при этом уровень ТТГ необходимо поддерживать ниже 2 мЕд/л.
|
|
Послеродовый тиреоидит
Послеродовый тиреоидит (ПТ) – синдром транзиторного или стойкого нарушения функции ЩЖ, развившегося на протяжении первого года после родов, причиной которого является аутоиммунное воспаление ЩЖ. В Нидерландах распространенность ПТ у женщин составляет 5,2–7,2%. Классически заболевание имеет двухфазное течение: за тиреотоксической фазой следует гипотиреоидная. Послеродовый тиреоидит может развиться и после прерывания беременности на сроках 5–20 нед. Причиной тиреотоксикоза при ПТ является выход тиреоидных гормонов в кровь из разрушающихся тиреоцитов. В этом случае такой тиреотоксикоз самолимитируется. Наиболее важна дифференциальная диагностика тиреотоксической фазы ПТ с БГ, которая базируется на сцинтиграфии и определении АТ рТТГ. Гипотиреоидная фаза обычно развивается через 4–8 мес после родов и обычно протекает с большим количеством симптомов, чем тиреотоксическая. Стойкий гипотиреоз развивается в 12–61% случаев. При этом он может развиться после неопределенного по продолжительности периода эутиреоидного состояния. В связи с этим женщинам с ПТ в анамнезе рекомендуется ежегодное определение уровня ТТГ.
Экстренные состояния
Тиреотоксический криз
Тиреотоксический криз – клинический синдром, который характеризуется угрожающим жизни тиреотоксикозом. Для диагностики основное значение имеет клиническое подозрение. Burch и Wartofsky предложили схему, которая может помочь в постановке диагноза. Тахикардия, лихорадка, желудочно кишечная симптоматика и нарушения со стороны центральной нервной системы – наиболее частые клинические проявления тиреотоксического криза. Смертность при тиреотоксическом кризе высока (10–75%), и его лечение должно начаться немедленно в условиях реанимационного отделения. Лечение направлено на гиперфункцию ЩЖ и симптоматические мероприятия. Последние подразумевают лечение гиперпирексии ацетаминофеном (назначение аспирина может привести к повышению уровня Т4 и Т3), контроль гемодинамики, лечение инфекционных заболеваний и других сопутствующих заболеваний и осложнений. Целью воздействия на ЩЖ является снижение уровня тиреоидных гормонов в крови и ослабление их действия на ткани мишени. Из тиреостатиков могут назначаться как ПТУ (200–250 мг каждые 4 ч), так и тиамазол (30 мг каждые 6 ч). Подавление высвобождения тиреоидных гормонов из ЩЖ достигается назначением препаратов йода: раствор Люголя (10–15 капель каждые 8 ч) или йодид натрия (калия), которые можно назначить внутривенно (0,5–1,0 г каждые 12 ч). Для предотвращения использования йода в качестве субстрата для синтеза тиреоидных гормонов он назначается не раньше чем через 1 ч после первого назначения тиреостатика. Подавление конверсии Т4 в Т3 на периферии достигается внутривенным назначением глюкокортикоидов (например, гидрокортизон 200–300 мг исходно, затем 100 мг каждые 8 ч). Кроме того, с этой целью могут быть назначены β-ад реноблокаторы: пропранолол 0,5–1,0 мг внутривенно, в дальнейшем – через 10 мин, по 1–3 мг каждый час с последующим переходом на пероральный прием (60–80 мг каждые 6–8 ч).
|
Микседематозная кома
Микседематозная кома – тяжелый гипотиреоз, осложнившийся нарушением сознания, дыхательной недостаточностью и гипотермией в сочетании с другими типичными симптомами гипотиреоза. Обычно микседематозную кому провоцируют сопутствующие острые заболевания (инфекции, инфаркт миокарда, гипотермия, прием седативных препаратов), которые развиваются на фоне длительно нелеченного или неадекватно леченного гипотиреоза. При лабораторном исследовании выявляются: гипонатриемия, анемия, гипогликемия, гиперхолестеринемия, повышение уровня ЛДГ и КФК. Если есть подозрение на вторичный гипотиреоз, пациенту в начале необходимо назначить гидрокортизон. Для подтверждения диагноза необходимо определение уровня ТТГ и св. Т4. При этом следует иметь в виду, что уровень ТТГ вследствие общего тяжелого состояния может быть повышен достаточно умеренно. Лечение необходимо проводить в отделении реанимации. Назначение заместительной терапии не следует откладывать до получения результатов оценки функции ЩЖ. Мы рекомендуем назначение комбинации Т4 и Т3. Вначале назначается 200–250 мкг L-T4 внутривенно, после чего через 24 ч вводится еще 100 мкг, в дальнейшем доза снижается до 50 мкг ежедневно (предпочтительно перорально). L-T3 назначается в дозе 10 мкг каждые 8 ч, вплоть до нормализации витальных функций.
|
Комментарии
ПРАКТИКА ПЕДИАТРА
