Иммуногенность и реактогенность живой и инактивированной полиовакцин при различных схемах применения
СтатьиВакцинация, №6 (24) Ноябрь - декабрь 2002 г.
В.И. Задорожная, А.В. Моисеева, С.И. Доан
ГП "Центр иммунобиологических препаратов" г. Киев, Украина
40-летнее применение в Украине оральной полиомиелитной вакцины (ОПВ) позволило преодолеть эпидемическое распространение заболевания и полностью исключить случаи полиомиелита, вызванные "дикими" полиовирусами. Однако в последнее время особую тревогу вызывает увеличение количества регистрируемых случаев вакциноассоциированного паралитического полиомиелита (ВАПП) после использования ОПВ (в 1998 г. - 2 случая, в 1999 г. - 8 случаев, в 2000 г. - 5, в 2001 г. - 2).
Учитывая, что больше половины всех ВАПП возникли в ответ на 1-ю и 2-ю вакцинацию, и то, что причиной развития ВАПП у половины привитых был полиовирус 3-го типа, можно предположить, что применение ОПВ на определенном этапе несет риск осложнений больший, чем риск заболевания той инфекцией, которую она предупреждает.
В последние годы в ряде стран, где достигнуты определенные успехи в эрадикации "диких" полиовирусов с целью исключения риска возникновения ВАПП для профилактики полиомиелита используют инактивированную полиомиелитную вакцину (ИПВ)[3].
Генетическая нестабильность полиовируса 3-го типа, неудовлетворительное состояние популяционного иммунитета населения Украины к полиовирусу этого типа (удельный вес серонегативных в 2001 г. составил 13%), тенденция к росту заболеваемости ВАПП и ОВП, связанных по времени с вакцинацией, требовали изучения возможности рутинного применения ИПВ в условиях Украины [1].
Для определения реактогенности и иммуногенности ИПВ 300 детей (по 100 детей в каждой группе) получали ИПВ в 3, 4 и 5 мес. жизни (1-я группа, 1-я схема иммунизации); дети, которые получали ИПВ в 3 мес. жизни, а в 4 и 5 мес. - ОПВ (2-я группа, 2-я схема иммунизации). Контрольную группу составляли дети, которых в 3, 4 и 5 мес. жизни прививали ОПВ (3-я группа, 3-я схема иммунизации). Для проведения иммунизации использовались следующие вакцины: "Имовакс Полио" (инактивированная вакцина для профилактики полиомиелита компании "Авентис Пастер", Франция) и две живые пероральные вакцины для профилактики полиомиелита (производства той же компании и Института полиомиелита и вирусных энцефалитов им. М.П.Чумакова РАМН, Россия).
С целью оценки реактогенности за детьми велось наблюдение на протяжении 4-х недель после каждой прививки. Все местные и общие реакции (табл.) регистрировались в дневниках наблюдения. В соответствии с национальным календарем прививок Украины одновременно с полиомиелитной вакциной дети получали АКДС-вакцину. В отличие от ИПВ, при введении ОПВ местные реакции не учитывались в связи с оральным путем введения вакцины.
Частота поствакцинальных реакций
при сочетанной вакцинации АКДС и ИПВ или ОПВ
| Реакции | Первая прививка, % | Вторая прививка, % | Третья прививка, % | |||
| ИПВ | ОПВ | ИПВ | ОПВ | ИПВ | ОПВ | |
| Местные | ||||||
| Слабые | 6,5+1,7 | - | 7,0+2,6 | - | 5,0+2,2 | - |
| Сильные | 3,5+1,3 | - | - | - | - | - |
| Общие | ||||||
| Слабые | 11,0+2,2 | 6,0+2,4 | 9,0+2,9 | 10,0+3,0 | 7,0+2,6 | 5,0+2,2 |
| Сильные | 1,0+0,7 | - | - | - | - | - |
ИПВ вводилась внутримышечно. После 1-й дозы у 10% детей были зафиксированы местные реакции (гиперемия в месте введения), в дальнейшем их количество снизилось до 7% (после 2-й дозы) и до 5% (после 3-й дозы). Большинство реакций были кратковременными и проходили в течение 1-2 дней. Удельный вес общих реакций (повышение температуры тела более 37,20С) на 1-е введение ИПВ в сочетании с АКДС составил 12%, против 6% - в случае ОПВ. В дальнейшем их количество снизилось и составило на 2-ю прививку - 7%, на 3-ю - 5%.
Из приведенных данных видно, что после первой сочетанной прививки АКДС + ИПВ показатели реактогенности были более высокими, чем при применении ОПВ. Данный факт, скорее всего, может быть связан с парентеральным путем введения вакцины. В то же время, при широкомасштабном использовании ИПВ в практическом здравоохранении для плановой иммунизации в 2001 г. из регионов не было получено сообщений о каких-либо необычных реакциях или осложнениях на данную вакцину.
Для изучения напряженности иммунитета через 1 мес. после 2-й прививки и через 6 мес. после окончания вакцинации у детей были взяты пробы крови для определения содержания вируснейтрализующих антител к полиовирусам трех типов (соответственно 63, 51 и 52 ребенка из каждой группы).
Через 1 мес. после 2-й прививки самые высокие значения средних геометрических титров (СГТ) антител к полиовирусу 1-го типа были при 2-й схеме иммунизации, самые низкие -при 3-й (рис. 1), хотя в целом эти показатели были достаточно высокими. Удельный вес серонегативных имел близкие значения и составил соответственно 1,6%, 2,0% и 1,9% среди детей 1, 2 и 3-й групп. Антитела в высоких титрах 1:512 и 1:1024 к полиовирусам 1-го и 2-го типов почти с одинаковой частотой выявляли у детей 1-й и 2-й групп (соответственно 17,5-17,6% и 7,8-7,9%). Среди детей 3-й группы антитела в высоких титрах наблюдали только к полиовирусу 1-го типа (7,7%). Самый высокий уровень СГТ антител к полиовирусу 2-го типа во время 1-го обследования определялся во 2-й группе (1:182,0), самый низкий - в 3-й группе (1:128,0). Полученные результаты подтверждают данные литературы о более высоком уровне специфических антител при комбинированной схеме иммунизации (ИПВ+ОПВ) [2,4].
Уровни СГТ гуморальных антител к полиовирусам трех типов
через 1 месяц после 2-ой дозы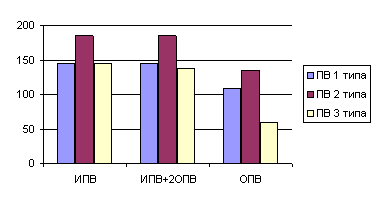
К полиовирусу 3-го типа самые высокие значения СГТ антител выявлены через 1 мес. после двух доз ИПВ (1:193,7) (рис. 1). При двух других схемах иммунизации этот показатель был значительно ниже и составлял: после 2-й прививки ОПВ - 1:84,5, после ИПВ+ОПВ - 1:104,0. При комбинированной схеме иммунизации большинство детей имели антитела к полиовирусу 3-го типа в титрах 1:64-1:256 (15,7-21,6%). В 3-й группе был высоким удельный вес детей с титрами 1:128 (38,5%).
Несмотря на то, что перед 3-й прививкой состояние специфического иммунитета оценивалось как удовлетворительное при всех схемах иммунизации, следует отметить, что более эффективными оказались те, которые предусматривают использование ИПВ. В отношении полиовируса 3-го типа наиболее эффективной оказалась первая схема (трехкратное введение ИПВ).
Через 6 мес. после завершения вакцинации самые высокие значения СГТ антител среди всех групп детей зафиксированы к полиовирусу 2-го типа, самые низкие - к полиовирусу 3-го типа (рис. 2).
Уровни СГТ гуморальных антител к полиовирусам трех типов
через 6 месяцев после 3-й дозы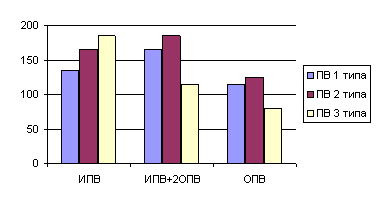
К полиовирусу 1-го типа уровни СГТ антител имели сопоставимые значения в группах с использованием комбинированной схемы иммунизации и 3 доз ИПВ (1:157,6). У тех детей, которые получали только ОПВ, этот показатель составил 1:84,0.
К полиовирусу 2-го типа среди детей 1-й группы детей наблюдалось увеличение уровней СГТ антител с 1:157,6 до 1:182,0. В группе детей, которые получали ОПВ, значения СГТ антител не изменились (1:120,0).
К полиовирусу 3-го типа СГТ антител среди детей 1 и 2-й групп соответственно составляли 1:147,0 и 1:128,0, а в контрольной группе - 1:59,7. Все дети после завершения вакцинации имели антитела ко всем типам полиовируса.
Полученные результаты позволили сделать вывод, что схемы иммунизации, которые предусматривают применение ИПВ как для проведения полного цикла вакцинации, так и первой прививки, более эффективны по сравнению с традиционной схемой (три дозы ОПВ). Осуществление двух первых прививок с использованием ИПВ обеспечивает высокий уровень иммунитета против полиовируса 3-го типа и снижает до минимума риск возникновения такого осложнения как ВАПП.
В 2001 г. в Украине для проведения вакцинации впервые использовалась как моновакцина ИПВ ("Имовакс Полио"), так и ее комбинация с дифтерийно-столбнячно-коклюшной вакциной ("Тетракок" компании "Авентис Пастер", Франция). Несмотря на то, что всего было использовано лишь около 100 тыс. доз ИПВ (в основном, иммунизировались дети, имевшие противопоказания к ОПВ - 8% от общего числа прививок первичного вакцинального комплекса), мы наблюдали снижение регистрируемых ВАПП до двух случаев.
В настоящее время полный отказ от применения ОПВ в Украине в силу экономических обстоятельств невозможен. Однако использование комбинированной схемы иммунизации на фоне отсутствия циркуляции "дикого" полиовируса даст возможность практически избежать случаев ВАПП среди детей, которые в дальнейшем будут привиты ОПВ, а также значительно уменьшить интенсивность циркуляции вакцинных полиовирусов [5].
Литература:
- Облапенко Г.П. Ликвидация полиомиелита в Европе. Основные материалы ВОЗ по вопросу ликвидации полиомиелита. - 1995 - стр.59.
- Faden H., Modlin J.F., Thoms M.L., et al. // J. Infect. Dis. 1990. - №162. р.1291-7.
- John T.J. // N. Еngl. J. Med. 2000. V.343, №11. р.806-7.
- Swennen B, Levy J. // Vaccine. - 2001. - №19. р.2262-7.
- WHO Global overview: Progress towards the Global Eradication of poliomyelitis. 1-2 May 1996, Geneva.
© 2002, В.И. Задорожная, А.В. Моисеева, С.И. Доан
Комментарии
ПРАКТИКА ПЕДИАТРА

