Иммуномодулирующая терапия сепсиса: неожиданные эффекты макролидов
СтатьиОпубликовано в издании: "ИНФЕКЦИИ В ХИРУРГИИ", №4, 2009, с. 31-34 E.J. Giamarellos-Bourboulis, Греция
Резюме
Несмотря на многочисленные усилия проникнуть в суть воспалительных реакций, лежащих в основе патогенеза сепсиса, ряд клинических исследований по модулированию иммунного ответа с использованием антиэндотоксиновых антител, антител к фактору некроза опухоли-α (ФНО-α) и растворимых ФНО-рецепторов не смогли продемонстрировать клинические преимущества. Аналогичные результаты наблюдали при использовании гидрокортизона или интенсивном контроле уровня глюкозы путем постоянной инфузии инсулина.
Иммуномодулирующий эффект макролидов был продемонстрирован у больных хроническими легочными заболеваниями - диффузным панбронхиолитом и муковисцидозом. Благоприятные клинические исходы внебольничной пневмонии при лечении β-лактамными антибиотиками в комбинации с макролидами также объясняются иммуномодулирующим действием последних. Эффективность макролидов в отношении грамотрицательных микроорганизмов в экспериментальных моделях сепсиса послужила основанием для инициации клинического исследования иммуномодулирующего действия кларитромицина у 200 больных вентилятор-ассоциированной пневмонией и сепсисом.
Сепсис занимает 10-е место в списке ведущих причин смерти в США. Сепсис развивается у 11-12% больных отделений интенсивной терапии (ОИТ) с показателями смертности 48,4-55,2% (в ОИТ и госпитальной). Несмотря на своевременную постановку диагноза и раннее начало антибиотикотерапии, смертность у больных сепсисом по-прежнему высока. Очевидно, это объясняется вовлечением других механизмов, в частности избыточного иммунного ответа, которые приводят к развитию полиорганной недостаточности (ПОН) с неблагоприятным исходом для больного. Поэтому одним из ключевых направлений в лечении сепсиса является воздействие на иммунный ответ.
Индукторами септической реакции считаются определенные компоненты/метаболиты микробной клетки - эндотоксины (липополисахарид - ЛПС), липотейхоевая кислота, зимозан и бактериальная ДНК, которые активируют моноциты, прикрепляясь к толл-рецепторам клеточной стенки, и таким образом стимулируют внутриклеточные сигнальные пути. Это приводит к активации ядерного фактора NF-κΒ, генной экспрессии про- и противовоспалительных цитокинов, среди которых наиболее изученными являются ФНО-α и интерлейкины (ИЛ) - ИЛ-1β, ИЛ-6, ИЛ-8, ИЛ-10. Гиперпродукция этих цитокинов может привести к развитию ПОН, синдрому диссеминированного внутрисосудистого свертывания и гипергликемии.
Можно предположить, что подавление некоторых компонентов этого воспалительного каскада позволит улучшить клинический исход. Были предприняты попытки подавления: 1) ЛПС - антиэндотоксиновыми антителами; 2) ФНО-α - антителами и растворимыми рецепторами; 3) гиперкоагуляции - дротрекогином-α (Зигрис); 4) гипергликемии - интенсивной инсулинотерапией; 5) надпочечниковой недостаточности - введением малых доз гидрокортизона. Проведено 11 рандомизированных исследований эффективности антиэндотоксиновых и анти-ФНО-α антител и растворимых рецепторов (этанерцепт, ленерцепт) с участием 3000 пациентов, но с однотипным заключением об отсутствии у этих препаратов каких-либо преимуществ перед плацебо в улучшении показателя 28-дневной выживаемости.
Интерес к теме возобновился после публикации результатов исследования PROWESS с участием 1690 пациентов с симптомами недостаточности одного и более органов, в котором 4-дневная инфузия дротрекогина-α (человеческого рекомбинантного активированного С-протеина) улучшила показатели 28-дневной выживаемости по сравнению с плацебо, особенно в группе с исходным значением APACHE II >25. Впрочем, этот результат не удалось воспроизвести у больных тяжелым сепсисом (APACHE II Учитывая гетерогенность септических больных по инфекционному возбудителю и отсутствие четких данных об эффективности антибактериальной терапии в проведенных исследованиях, было решено обратиться к антибактериальным препаратам с иммуномодулирующим эффектом. Макролиды были выбраны в силу демонстрируемой ими в течение 20 лет эффективности при воспалительных заболеваниях легких, в частности, макролиды значительно увеличивают продолжительность жизни у больных диффузным панбронхиолитом1. В 4 исследованиях показана эффективность азитромицина у больных муковисцидозом, в том числе за счет снижения продукции слизи респираторным эпителием, подавления quorum sensing P. aeruginosa, стимуляции фагоцитоза альвеолярными макрофагами и снижения воспаления за счет подавления продукции провоспалительных цитокинов клетками респираторного эпителия. Эти эффекты наблюдались у пациентов с хроническим воспалением.
В эксперименте показано подавление кларитромицином высвобождения ИЛ-8 клеточной культурой человеческих моноцитов после их предварительной стимуляции клеточными лизатами P. aeruginosa и Escherichia coli благодаря ингибированию транскрипции ядерного фактора NF-κΒ и активатора протеина 1. Иммуномодулирующее действие макролидов при остром воспалении подтверждается данными ретроспективного анализа результатов лечения внебольничной пневмонии у 1518 больных в Испании: смертность 6,9% - при лечении комбинацией β-лактама и макролида, 13,3%- при лечении только β-лактамом. Анализ 409 случаев пневмонии, вызванной S.pneumoniae, показал снижение макролидами риска смерти в 2,5 раза, исключив влияние макролидов на исход за счет подавления атипичных патогенов. Эти данные подтвердились в ретроспективном анализе 2349 больных пневмонией.
Предпочтение кларитромицину отдано в силу того, что азитромицин не обеспечивает достаточные сывороточные концентрации, необходимые для подавления продукции провоспалительных цитокинов моноцитами. В экспериментальной модели сепсиса, вызванного полирезистентными штаммами P. aeruginosa, Klebsiella pneumoniae и E. coli (не относящимися к спектру активности кларитромицина), кларитромицин вводили внутривенно одновременно с инокуляцией бактерий либо уже после появления симптомов сепсиса (для максимального приближения к клиническим условиям). При отсутствии подавления роста бактерий кларитромицин в значительной мере ослабил воспалительную реакцию, что подтверждалось меньшей инфильтрацией тканей нейтрофилами и лимфоцитами, снижением сывороточной концентрации ФНО-α и сывороточного оксидантного стресса, а также повысил выживаемость. Максимальные сывороточные концентрации кларитромицина в этом исследовании варьировали в диапазоне 5-10 мкг/мл и достигались через 30 мин после введения.
Клиническая эффективность кларитромицина у больных сепсисом и вентилятор-ассоциированной пневмонией (ВАП)
Двести больных ВАП, осложненной нозокомиальным сепсисом, были рандомизированы в группы лечения кларитромицином и плацебо (100 пациентов в каждой группе), кларитромицин вводили в дозе 1 г/сут в виде внутривенной 1-часовой инфузии в течение 3 дней подряд с намерением достичь сывороточных концентраций 5-10 мкг/мл. Дополнительная антибактериальная терапия назначалась по усмотрению лечащего врача. В исследовании использовались международные критерии сепсиса, тяжелого сепсиса и септического шока.
Группы кларитромицина и плацебо были сопоставимы по возрасту, половой принадлежности, сопутствующим заболеваниям, тяжести сепсиса и степени органной недостаточности у пациентов, равно как и степени респираторной дисфункции (значению отношения парциального давления кислорода к фракции вдыхаемого кислорода -рО2/FiO2) и спектру используемых дополнительно иммуномодулирующих препаратов (низких доз гидрокортизона и инфузии инсулина для поддержания уровня глюкозы в пределах 80-110 мг/дл).
Этиологию сепсиса определяли посевом трахеобронхиального секрета с последующим бактериологическим исследованием до начала лечения кларитромицином, а затем на 5 и 10-е сутки. В группах плацебо и кларитромицина культуры грамотрицательных патогенов (105 КОЕ) выделены у 68 и 66% пациентов соответственно (разница статистически незначима), в том числе Acinetibacter baumannii (63,2%), P. aeruginosa (17,6%), K. pneumoniae (8,8%). Частота выделения указанных возбудителей в группе кларитромицина составила 54,5, 25,8 и 7,6% соответственно.
Для исключения влияния других антибактериальных препаратов на интерпретацию эффектов кларитромицина и клинических исходов среди выделенных патогенов определили пропорцию чувствительных микроорганизмов к одному или более используемым в группе антибиотикам. Таковых оказалось 62,5% в группе плацебо и 75,4% - в группе кларитромицина (р=0,44). Эрадикация патогена к 5-му дню была достигнута у 37,3% пациентов из группы плацебо и 42,6% пациентов из группы кларитромицина (р=0,31), а к 10-му дню - у 41,4 и 46,2% соответственно (р=0,82).
Обе группы сравнивали по следующим клиническим исходам/параметрам: резолюция ВАП, время до отключения от аппарата искусственной вентиляции легких (ИВЛ) (экстубации), риск смерти. Среднее время резолюции ВАП составило 15,5 сут в группе плацебо и 10,0 сут в группе кларитромицина (р=0,011). Средний период времени до экстубации составил 22,5 и 16,0 сут соответственно (р=0,047). Полученные данные согласовались с результатами оценки по шкале легочной инфекции CPIS (Clinical Pulmonary Infection Score): исходные значения составили 7,92 и 7,62 балла в группах плацебо и кларитромицина соответственно (р=0,29), на 5-е сутки - 6,10 и 5,23 балла, на 10-е - 5,88 и 5,09 (р=0,032).
Показатель выживаемости зависел от развития у пациентов септического шока в сочетании с ПОН -основной причины смерти. В группе плацебо относительный риск смерти ввиду указанных причин составил 19,0, а в группе кларитромицина он был снижен до 3,78 (р=0,043).
В целом, ПОН развилась у 22 пациентов, не имевших симптомов органной недостаточности на момент включения в исследование. Средний период времени до проявления симптомов органной недостаточности составил 3,38 сут в группе плацебо и 5,78 - в группе кларитромицина (р=0,006).
В группе кларитромицина не выявили риска развития каких-либо серьезных побочных эффектов в связи с введением препарата.
Полученные результаты могут послужить основанием для назначения кларитромицина внутривенно больным сепсисом и ВАП. Предлагаемые показания к применению кларитромицина: 1) ВАП - ввиду обеспечения кларитромицином более раннего разрешения пневмонии и более раннего отключения от ИВЛ; 2) септический шок с ПОН -ввиду существенного снижения риска смерти.
Могут рассматриваться разные гипотезы о механизме действия кларитромицина. Исходя из накопленных данных (у больных с хроническими воспалительными заболеваниями дыхательных путей и в модели экспериментального сепсиса), механизм действия кларитромицина включает модулирование иммунного ответа хозяина и инструмента общения бактерий - quоrum sensing, о чем свидетельствует пролонгирование кларитромицином промежутка времени до развития ПОН у септических больных.
Заключение
Сепсис и септический шок остаются одной из основных причин гибели больных в ОИТ. Попытки использовать ряд препаратов с разным механизмом действия с целью модулирования иммунного ответа хозяина практически не изменили показатели смертности у этой категории больных (см. рисунок).
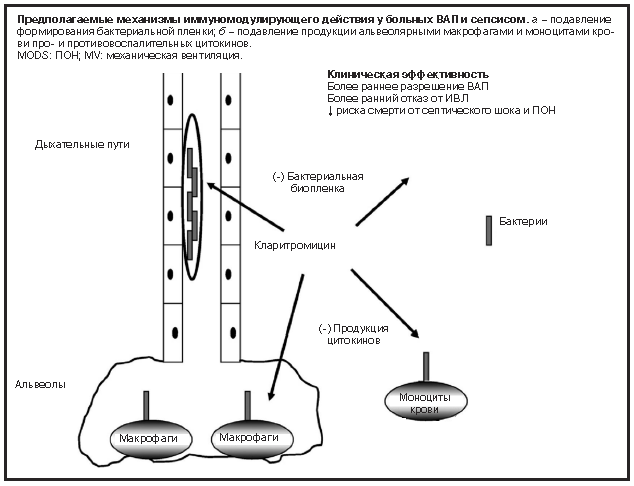
Наблюдаемые в двойном слепом рандомизированном клиническом исследовании эффекты внутривенного лечения кларитромицином больных ВАП и сепсисом позволяют смотреть в будущее с оптимизмом. Необходимы дополнительные клинические исследования для четкого определения показаний к применению кларитромицина в качестве иммуномодулятора при сепсисе.
Комментарии
ПРАКТИКА ПЕДИАТРА
