Интестамин: Научный информационный бюллетень
СтатьиНаучный отдел компании «Фрезениус Каби», Германия. Научное и техническое редактирование д.м.н. А.В.Дмитриев
- 1. Основные положения
- 1.1 Кишечная защитная система: Кишечные барьеры
- 1.1.1 Люминальная и эпителиальная поверхностная защита (внешние механизмы)
- 1.1.2 Защита с помощью слизистой (внутренние механизмы)
- 1.1.2.1 Защитные механизмы эпителия слизистой оболочки кишечника
- 1.1.2.2 Лимфатическая ткань кишечника (GALT)
- 1.2 Определения и инциденты SIRS (синдром воспалительной системной реакции), сепсисом и MODS (синдром множественной дисфункции органов)
- 1.2.1 Определения
- 1.2.2 Частота заболеваний
- 1.3 Метаболизм SIRS и нутритивные осложнения
- 1.3.1. Метаболическая реакция на SIRS ^стресс1] и голод
- 1.3.2. Нутритивные последствия вызванного стрессом катаболизма
- 1.4. Желудочно-кишечный тракт в критических состояниях
- 1.4.1 Ишемия и реперфузионное повреждение
- 1.4.2. Чрезмерное развитие бактерий
- 1.4.3. Кишка как триггер и/или мотор полиорганной недостаточности (MOF)
- 1.4.4. Уменьшение подвижности
- 1.4.5. Нарушение всасывания
- 1.5 Окислительный стресс
- 1.5.1 Развитие окислительного стресса при критических состояниях
- 1.5.2. Воспалительная реакция на окислительный стресс
- 1.5.3. Антиоксидантные механизмы
- 1.5.3.1. Антиоксидантные энзимы
- 1.5.3.2. Глутатион
- 1.5.3.3. Витамины С, Е и [3-каротин
- 1.6. Истощение ключевых питательных веществ
- 1.6.1 Глутамин
- 1.6.2 Антиоксиданты
- 1.6.2.1. Почему для критически больных пациентов особенно опасен недостаток антио ксиданта?
- 1.6.2.2. Развитие во времени дефицита антиоксидантов у критически больных пациентов
- 1.6.2.3 Шкала дефицита антиоксидантов у критически больных пациентов
- 2. Питание критически больных пациентов
- 2.1. Раннее введение субстрата в кишечник (раннее энтеральное питание) 2.1.1. Почему энтеральное введение?
- 2.1.2 Почему и как рано?
- 2.1.3 Возможно ли очень раннее энтеральное питание и безопасно ли оно у критически больных пациентов?
- 2.1.4. Сколько и какого энтерального питания должны получать пациенты
- 2.2 Недостатки современного имму но питания
- 2.2.1. Ограниченная переносимость объема энтерального питания убольных в критических состояниях
- 2.2.2. Неадекватное снабжение глутамином тяжело больных пациентов
- 2.2.3 Недостаточное поступление антиоксидантов
- 2.2.4. Недостаточность короткоцепочечных жирных кислот (SCFA)
- 2.2.5. Поступление высокомолекулярных питательных веществ при нарушенном пищеварении и всасывании
- 2.2.6. Прием аргинина с условно противовоспалительными эффектами
- 3. Новое фармакопитание с помощью Интестамина
- 3.1 Показания
- 3.2. Оптимальный объём для эффективности субстрата
- 3.2.1. Оптимальное количество очень рано подаваемого энтерального субстрата
- 3.2.2. Оптимальное количество очень ранней энтеральной подачи субстрата
- 3.3. Фармакопитание с помощью Интестамина
- 3.3.1. Глутамин дипетиды
- 3.3.1.1. Глутамин в номальном и катаболическом метаболизме
- 3.3.1.2 Важность глутамина для критически больных пациентов
- 3.3.1.3 Глутаминовая терапия у критически больных пациентов
- 3.3.1.4 Обоснование для использования глутамин дипептидов
- 3.3.2. Антиоксидантные витамины и микроэлементы
- 3.3.2.1. Сколько антиоксидантов должны получить критически больные пациенты?
- 3.3.2.2. Какие дозы антиоксидантов безопасны у критически больных пациентов?
- 3.3.2.3. Почему энтеральные антиоксиданты?
- 3.3.3. Бутират / Трибутирин
- 3.3.3.1. Преимущества бутирата
- 3.3.3.2. Как добавить бутират к Интестамину?
- 3.3.3.3. Характеристики и производство трибутирина
- 3.3.3.4. Метаболизм трибутирина
- 3.3.3.5. Исследования с энтерально подаваемым трибутирином для процессов питания
- 3.3.3.6. Другие исследования с трибутирином
- 3.3.4 Глицин
- 3.3.4.1. Основы глицина
- 3.3.4.2. Благоприятные эффекты глицина на функцию печени в критических заболеваниях
- 3.3.4.3. Благоприятные эффекты глицина на кишечную функцию в критических заболеваниях
- 3.4. Дозировка и применение Интестамина
- 3.4.1. Дозировка Интестамина
- 3.4.2. Интестамин - место и время применения
- 3.5. Режимы кормления Интестамином
- 3.5.1. Выбор питательных растворов
- 3.5.2. Интестамин, дополняющий ЭП, ПП или оба случая
1.1 Кишечная защитная система: Кишечные барьеры
Желудочно-кишечный тракт обычно рассматривается как орган, предназначенный для приема пищи, переваривания пищи и её усвоения.
Существует, однако, другая чрезвычайно важная роль желудочно-кишечного тракта, - это его выдающаяся роль в общей защите организма человека.
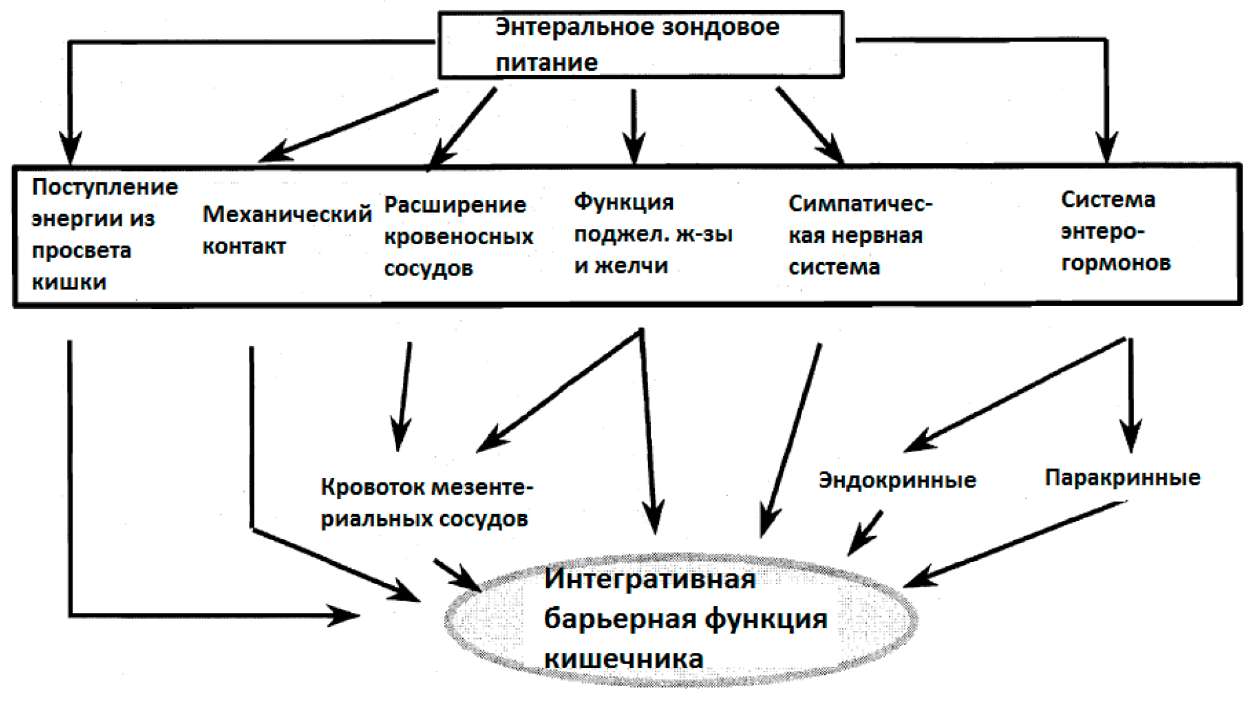
Ниже будут описаны множественные структуры и функции пищеварительного тракта, дающие вклад в защиту от болезнетворного типа бактерий и эндотоксинов (рис.1). Это должно помочь понять угрожающие жизни последствия в результате частичного или полного нарушения кишечных барьеров, возникающего в случае серьезных заболеваний.
Рис. 1: Наиболее важные компоненты кишечной защиты
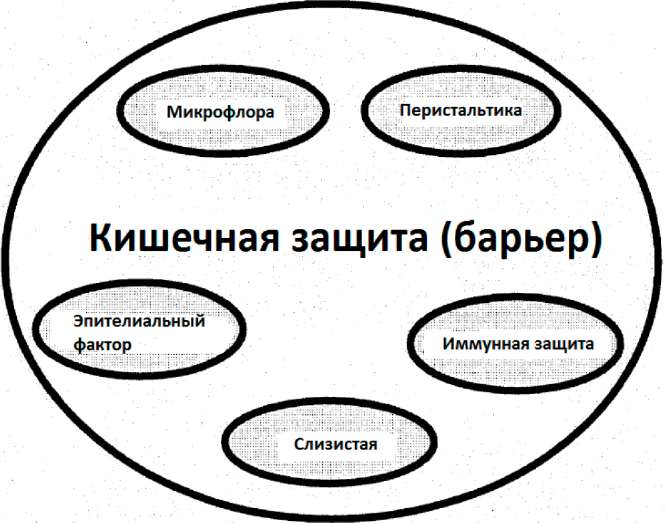
Вначале большинство болезнетворных организмов попадают на слизистую поверхность кишечника, респираторного и мочеполового трактов. В целом эта поверхность составляет примерно 400 квадратных метров, что более чем в 200 раз больше, чем поверхность кожи. 300 квадратных метров - т.е. 80% всей слизистой поверхности - занято желудочно-кишечным трактом (Таканаши и др. 1999, Джонсон и др. 1999).
Вследствие такой большой поверхности желудочно-кишечного тракта эффективные барьеры очень важны для защиты тела от внедрения патогенов (антигенов). Врождённые (неспецифичные для антигена) и приобретённые (специфичные для антигена) механизмы образуют сетку кишечной системы защиты. И те и другие действуют совместно на временной оси. Врождённая система обеспечивает защиту немедленно в ответ на вторжение, в то время как специфичной для антигена системе требуется от 3 до 4 дней для полной активации клеток иммунной компоненты (Сталлмах и др. 1998) - что подчеркивает важность наличия всей неповреждённой сети. Кишечный защитный барьер выстроен из внешних и внутренних механизмов. Внешние защитные механизмы действуют в кишечной люминальной и эпителиальной поверхности. Внутренние защитные механизмы состоят из структурных и функциональных свойств самой слизистой (Джонсон и др. 1999).
1.1.1 Люминальная и эпителиальная поверхностная зашита (внешние механизмы)
В принципе все внешние механизмы ограничивают количество антигенов (патогенов), которые могут достичь поверхности слизистой, уменьшая тем самым опасность внедрения в кишечный эпителий.
Перистальтика, которая определяет время кишечного прохождения, ограничивает контакт патогенов с кишечным эпителием и последующее возможное сцепление патогенов.
Слизистая оболочка состоит из муцина, слизистого секрета, который является очень вязким протеином. Кроме того, её вязкостная природа предотвращает прикрепление микроорганизмов к кишечному эпителию.
Физиологическая кишечная микрофлора защищает от болезнетворных бактерий путем
а) прикрепления к кишечному эпителию и тем самым уменьшению площади поверхности, доступной для крепления патогенных бактерий,
б) создания противомикробных веществ, таких как жирные кислоты, а также
в) путем стимулирования эпителиального клеточного роста.
Иммуноглобулин IgA является главным иммунологическим компонентом механизмов внешней кишечной защиты. IgA транспортируется из лежащей под кишкой связанной с ней лимфоидной ткани (GALT) в кишечный просвет. Это предотвращает внедрение патогенов путём захвата микроорганизмов, получаемых из окружающей среды и пищи (образование антиген - антитело - комплексов) в слизистой оболочке. Другие факторы, такие как врождённые гуморальные факторы (лактоферрин, лизозимы, пероксидазы), или расщепляющие белок GI выделения, также вносят свой вклад в эти множественные внешние механизмы.
1.1.2 Зашита с помощью слизистой (внутренние механизмы)
Патогены, которые успешно минуют внешние защитные механизмы, сталкиваются с внутренними защитными барьерами, которыми являются слизистый эпителий и GALT, связанная с кишкой лимфоидная ткань.
1.1.2.1 Защитные механизмы эпителия слизистой оболочки кишечника
Эпителий слизистой обеспечивает различные защитные механизмы. Межклеточные связи прочно скрепляют клетки эпителия вместе, обеспечивая эффективный механический барьер для патогенов. Специальные эпительные клетки производят слизь (см. выше), противомикробные вещества или пептидные гормоны вносят свой вклад в кишечную иммунную реакцию.
1.1.2.2 Лимфатическая ткань кишечника (GALT)
GALT («связанная с кишкой лимфоидная ткань») является объединяющим термином для всех лимфоидных тканей, расположенных в кишечнике. Лимфоидные клетки GALT ответственны за примерно 80% производства иммуноглобулинов организма, что количественно подчеркивает важность кишки для общей иммунной реакции. GALT состоит из нескольких уникальных иммунологических структур (таблица 1). Она играет выдающуюся роль в антиген специфичной иммунной реакции - для ввода и обработки антигенов (патогенов), а также секреции антител, в частности IgA 9.
Таблица 1: Уникальные иммунологические структуры GALT
|
Лимфатическая ткань кишечника (GALT) |
|
|
Организованная лимфоидная |
Неорганизованная лимфоидная |
|
ткань в собственной оболочке |
ткань |
|
- Пейеровы очаги |
- Интраэпителиальные лимфоциты |
|
- Аппендикс |
- Лимфоциты собственной оболочки |
|
- Кишечные лимфоузлы |
(первичное место производства IgA) |
|
- Одиночные лимфоидные узлы |
|
В пределах GALT пейеровы очаги являются тем местом, где инициируется антиген специфичная иммунная реакция. GALT - лимфоциты служат затравкой, чтобы в конце концов стать - после сложного процесса созревания клетки - либо выделяющими Ig клетками, либо производить цитокины, регулирующие секрецию IgA из клеток плазмы. (Обзоры: Сталлмах и др. 1998, Брандтцэг 1998, Джонсон и др. 1999, Таканаши и др. 1999, МакВэй и др. 1996, Дачмэн и др. 1997)
Заключение
Данный очерк количественных и качественных аспектов кишечной защиты ясно демонстрирует главную роль, которую кишка играет в общей защите организма. Сложная сеть врождённых и приобретённых иммунологических и неиммунологических защитных механизмов успешно защищает тело от проникновения патогенов при существующих физиологических условиях.
Разрушение кишечного барьера в патологических условиях, как это, например, случается при критических состояниях, может иметь губительный эффект. Таким образом становится очевидно, что необходимо предпринять все усилия, чтобы предотвратить нарушение кишечных защитных барьеров. Для этого наиболее важным оказываются адекватный путь питания и тип питания (Джонсон и др. 1999). Более подробные сведения о механизмах приводятся в следующих разделах.
1.2 Определения и инциденты SIRS (синдром системной воспалительной реакции), сепсиса и MODS (синдром множественной дисфункиии органов)
Интестамин показан для критически больных пациентов с опасностью или наличием у них SIRS, сепсиса и MODS.
1.2.1 Определения
Термины SIRS и сепсис относятся к определениям в том виде, как они были согласованы Американской корпорацией врачей, специалистов в области грудной клетки (Согласительной конференцией Общества медицинской помощи тяжелобольным, август 1991 (АССР, SCCM 1992, Bone и др. 1992). На этой конференции термин SIRS был предложен для того, чтобы определить системную воспалительную реакцию на любое серьезное повреждение, как инфекционное, так и неинфекционное. Так как подобные или даже идентичные метаболические реакции могут возникать как от инфекционных, так и от неинфекционных повреждений, конференция предложила использовать термин SIRS независимо от типа повреждения. Неинфекционные серьезные повреждения могут включать панкреатит, ишемию, множественные травмы и повреждения ткани, геморрагический шок или ожоги. Сепсис был определён как воспалительная реакция на инфекцию, таким образом представляя собой частный случай SIRS. Сепсис - это SIRS от инфекционного повреждения. Взаимосвязь между SIRS, сепсисом и инфекциями показана на рис.2
Рис.2: Взаимоотношение между синдромом системной воспалительной реакции (SIRS), сепсисом и инфекцией ( Бон и др. 1992)
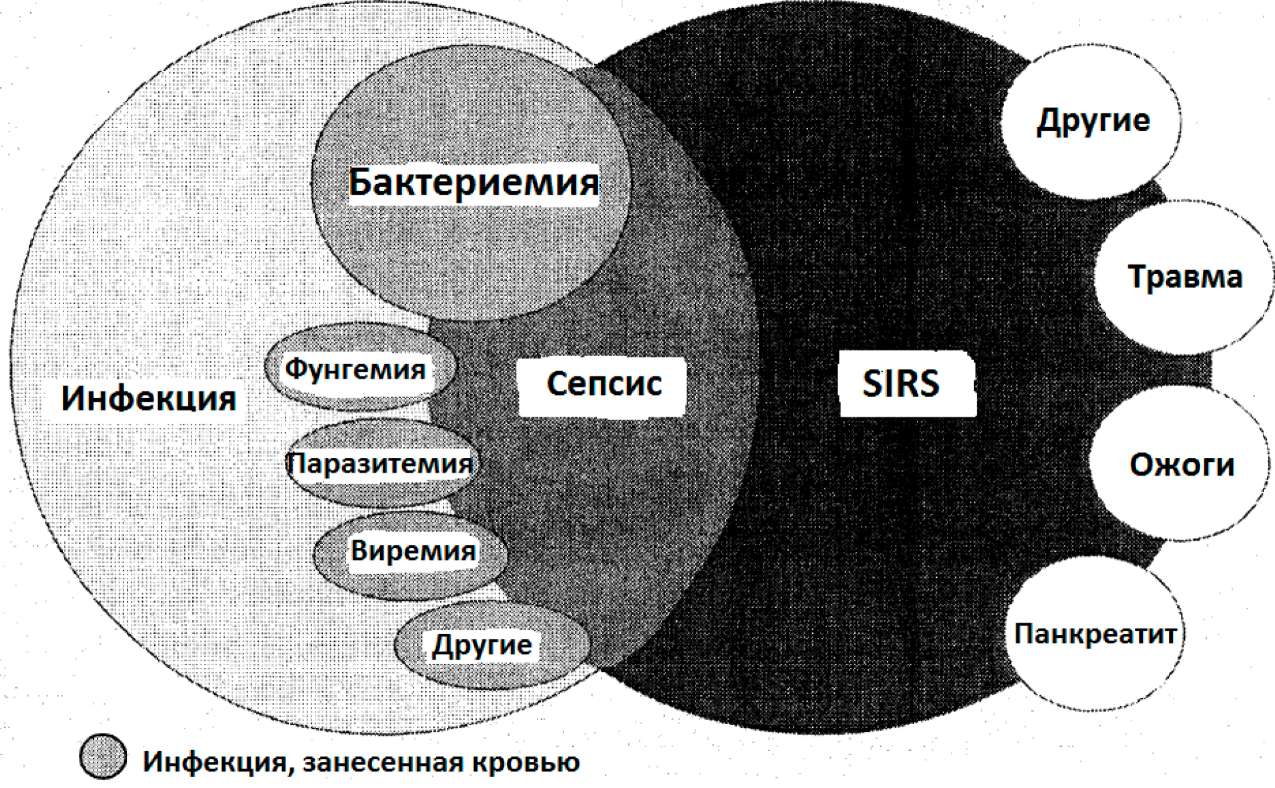
SIRS/острый сепсис и септический шок (для подробного определения каждого смотрите рис.3) представляют континуум клинической и патофизиологической тяжести, который коррелирует с возрастающей дисфункцией органа и смертностью (Бон и др. 1992, Матот и др. 2001).
MODS - Синдром множественной дисфункции органа - является термином, который должен применяться к тяжело больным пациентам с переменными нарушениями функции органа, не способного поддерживать метаболический гомеостаз.
Рис.3: Динамический процесс от SIRS и СЕПСИС до MODS, установленный согласительной конференцией 1991 года (Бон и др., Брун_Буиссон 2000, Мато и др. 2001)
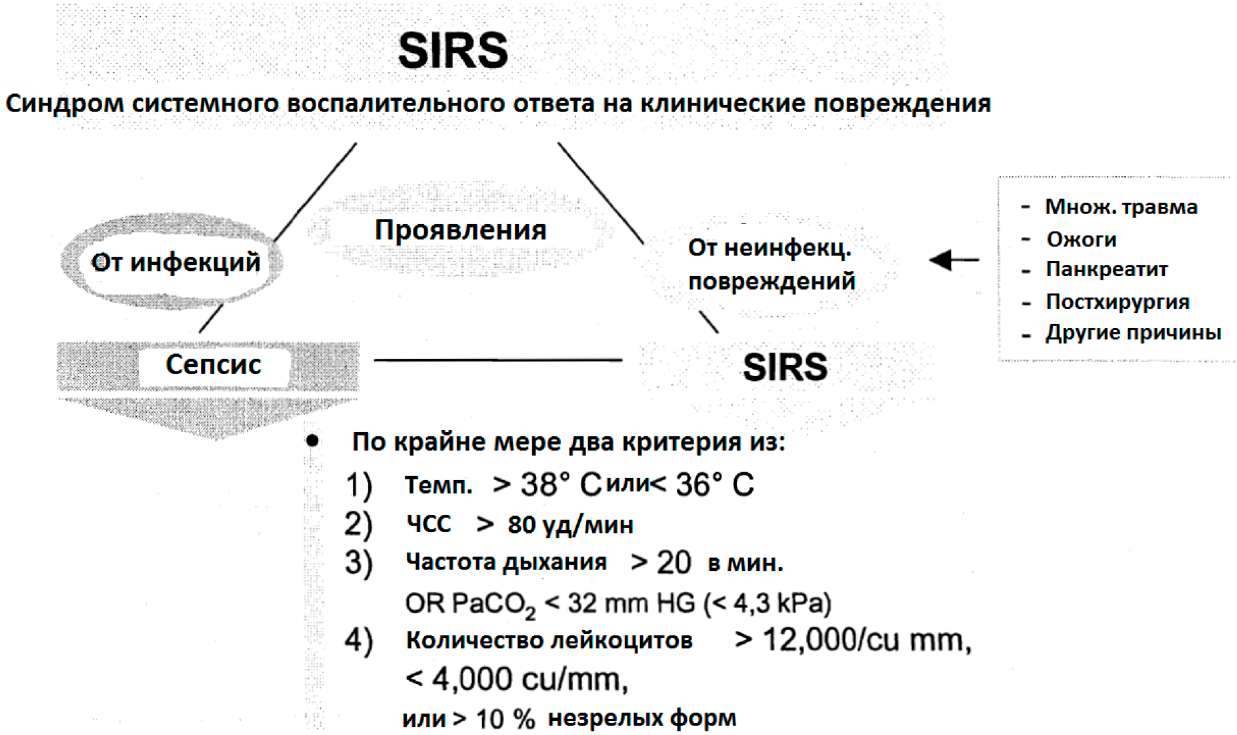
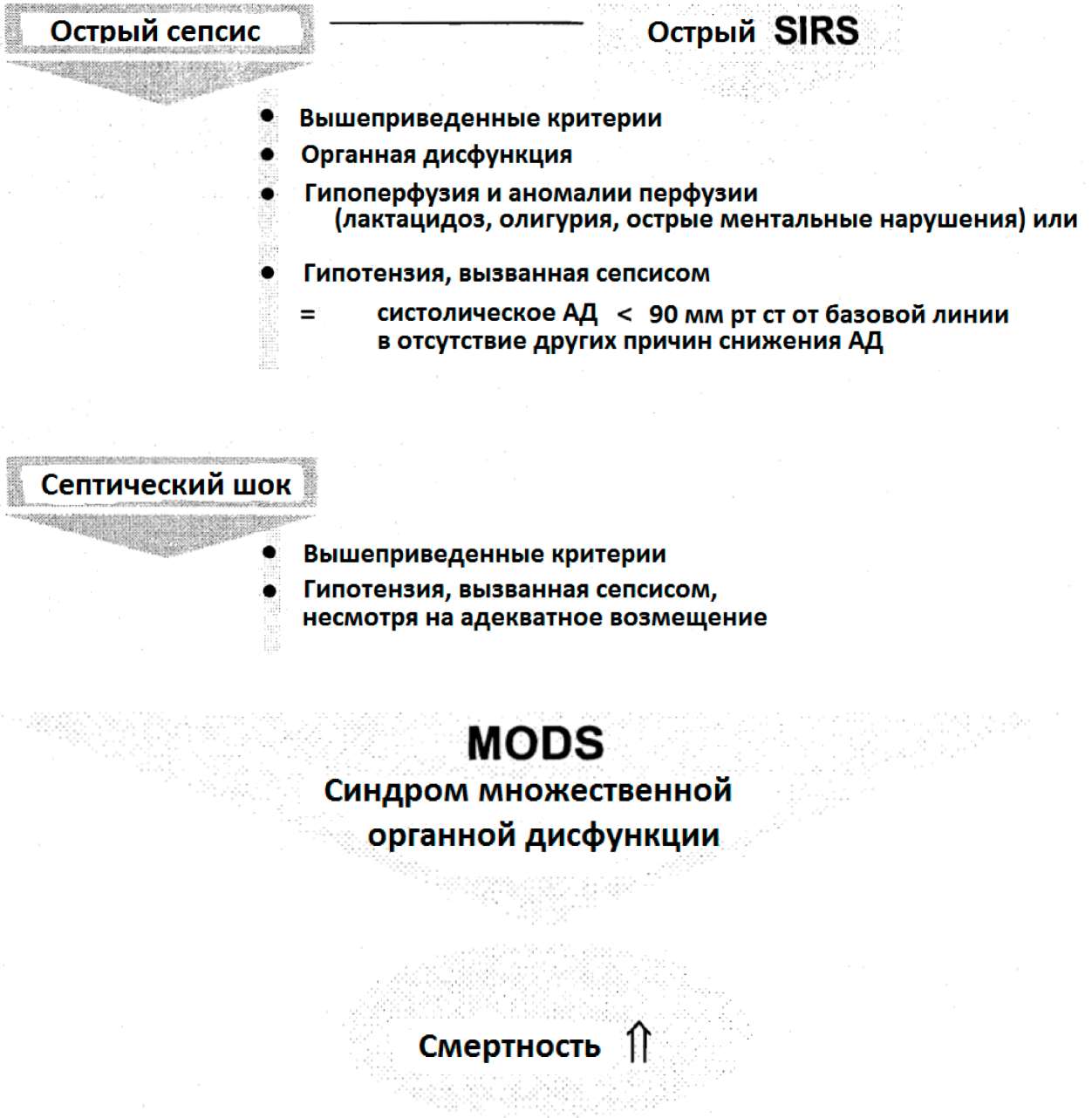
MODS представляет - аналогично SIRS - континуум физиологических отклонений от нормальной работы. Он описывает динамический процесс возрастания остроты патологических нарушений. Термин «органная дисфункция», следовательно, должен заменить термин «органная недостаточность», который просто указывает на статичное состояние в виде наличия или отсутствия (Bone и соавт., 1991).
До сих пор, однако, научная литература (Фэст и др. 1998, Бау и др. 1998, Паттерсон и др. 2000, Маршал 2000 - мы приводим лишь несколько примеров) и клинические врачи продолжают использовать этот термин «множественная органная недостаточность» (MOF), который, следовательно, является приемлемым также и в следующих разделах.
MODS часто является усложнением SIRS, что может быть понято как более серьезное окончание SIRS и сепсиса (Бон и др. 1991). Это выглядит так, как будто усложнение SIRS и сепсиса следует предотвратить вместо того, чтобы лечить болезнь (Маршалл, 2000).
Синдром МультиОрганной Дисфункции (MODS) может быть описан либо как первичный, либо как вторичный ( Бон и др. 1991) (рис.4)
Рис.4: Различные случаи и результаты первичного и вторичного синдрома множественной дисфункции органа (MODS)
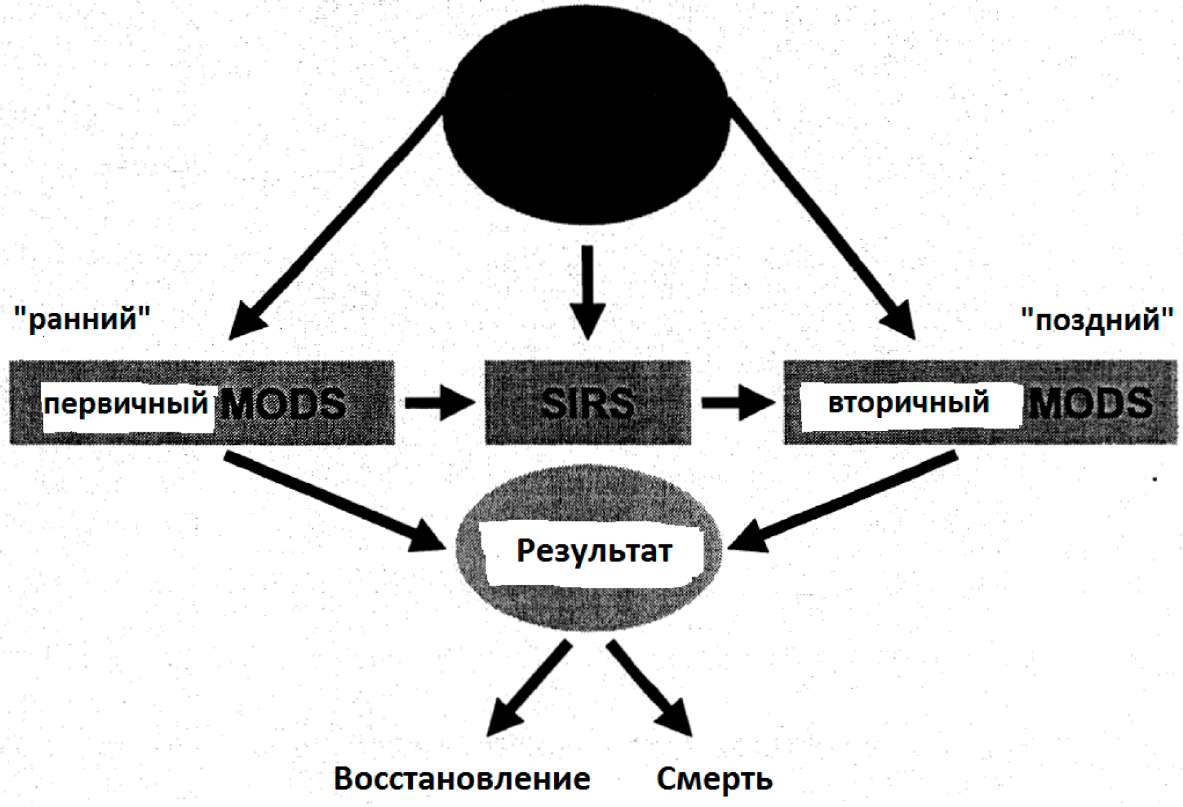
Первичный MODS следует немедленно из первичного повреждения, например, легочной контузии, в то время как вторичный MODS возникает значительно позже от SIRS или сепсиса.
Хотя определения сепсиса и его клинических проявлений остается предметом споров, определения SIRS и сепсиса, предложенные на согласительной конференции 1991 года, пока принимаются в принципе (Матот и др. 2001). 1.2.2. Частота заболеваний
Частота заболеваний SIRS и сепсиса ещё очень велика в ОРИТ (рис.5,6) и коррелирует с высокой смертностью. Ретроспективное исследование Брун-Буиссона (2000) изучило острый сепсис и шок у 10 - 15% всех пациентов в ОРИТ. Единственное недавно опубликованное проспективное когортное исследование Альберти и др. (2002) пришло к следующим результатам. У 25% всех пациентов, которые оставались более 24 часов в интенсивной терапии, развился острый сепсис и септический шок.
Рис.5: Эпидемиология SIRS и сепсиса: обзор 6 опубликованных исследований из Франции, США, Нидерландов, Италии и Швейцарии с использованием определений согласительной конференции 1991 года (Брун-Буиссон 2000).
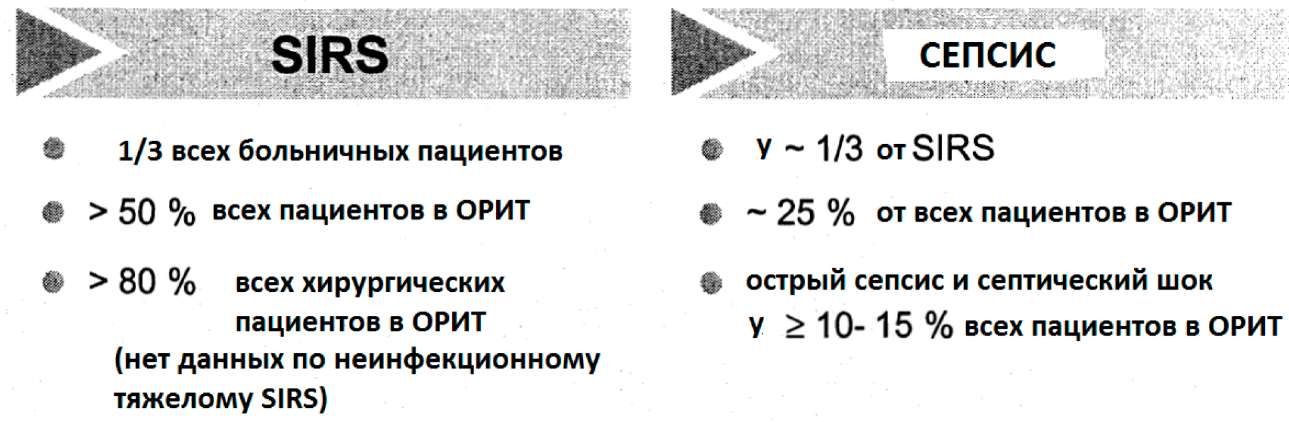
Исследованы 8 353 пациентов интенсивной терапии длительного пребывания (более 24 часов)
Рис.6: Эпидемиология сепсиса у пациентов интенсивной терапии: Международное проспективное когортное исследование в 6 европейских странах (Франция, Дания, Польша, Великобритания, Бельгия, Испания), Канаде и Израиле, использующее определения согласительной конференции 1991 года (Альберти и др. 2002).

28- дневная частота смертности при остром сепсисе составляет примерно 20-40%, а для септического шока - 40-60% (Брун - Буиссон 2000). Благодаря колоссальному прогрессу в начальном лечении пациентов с серьезной травмой, ранняя смертность может быть впечатляюще снижена в последние годы. Поздняя смертность, однако, ещё высока и связана с высокой заболеваемостью сепсисом и MODS. Отсюда очевидна необходимость новых перспективных подходов в лечении, лучшем предотвращении SIRS, сепсиса и его последствий (Сухнер и др. 2000)
Основываясь на имеющихся научных данных, Интестамин может принадлежать к этим новым многообещающим подходам.
1.3 Метаболизм SIRS и нутритивные осложнения
Интестамин является энтеральной добавкой, обеспечивающей ключевые компоненты как можно раньше у больных в критических состояниях для поддержания барьерной функции кишечника.
Сопровождающее применение парентерального или энтерального питания должно быть тщательно адаптировано к индивидуальным потребностям пациента в отношении количества и качества питательных веществ.
Нутритивная концепция Интестамина совсем не фокусируется на раннем обеспечении большим количеством энергии и питательных веществ.
Целью данного раздела является выяснение того, почему «слишком много калорий и неправильная комбинация калорийных веществ может принести больше вреда, чем пользы» во время SIRS и MODS (Беал 1994). Обзорные статьи Senftleben и соавт. (1998) и Kim и соавт. (2000) послужили главными источниками объяснений и выводов, приведенных ниже.
1.3.1. Метаболическая реакция на SIRS [=стресс}1 и голод
Катаболизм является метаболической реакцией как на стресс, так и на голод, во время стресса обычно называемой гиперметаболизмом. Между стрессом и голодом, однако, имеется глубокое различие в отношение того, в какой степени вещества могут быть утилизированы.
Так как обе метаболические ситуации могут возникнуть у критических больных, важно знать:
• в чём заключаются различия между метаболизмом стресса и голода, а также
• каковы диетологические последствия этого?
Во время голода утилизация питательных веществ не нарушена. Использование веществ адаптируется к их доступности. В результате повышенное поступление питательных веществ может инвертировать вызванный голодом катаболизм. Во время стресса, однако, использование веществ нарушено. Катаболизм, т.е. повышенная мобилизация эндогенной энергии и запасов протеина, не может быть инвертирован или остановлен, а только понижен подачей эндогенного вещества. Общая цель вызванного стрессом катаболизма -это использовать эндогенный жир и запасы протеина для адекватного обеспечения организма:
- энергией,
- глюкозой
для зависящих от глюкозы тканей, таких как
- мозг,
- эритроциты и
- иммунные клетки, а также
- аминокислотами и азотом
для синтеза новых функционирующих протеинов, особенно в острой фазе патологического процесса, вовлечённых в иммунную реакцию.
Обе ситуации, стресс и голод, дают в конечном итоге дисбаланс между инсулином и противорегуляторными гормонами в пользу последних, что приводит к катаболизму (рис.7).
Рис.7: Картина изменений метаболизма гормонов и воспалительных медиаторов в состоянии стресса и голода
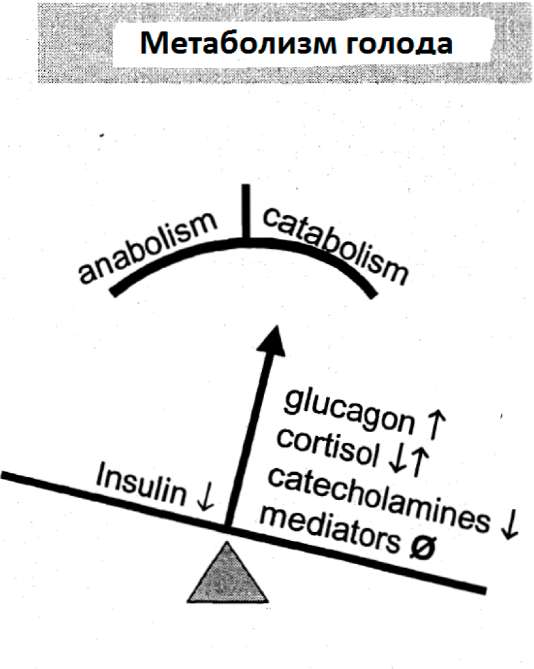
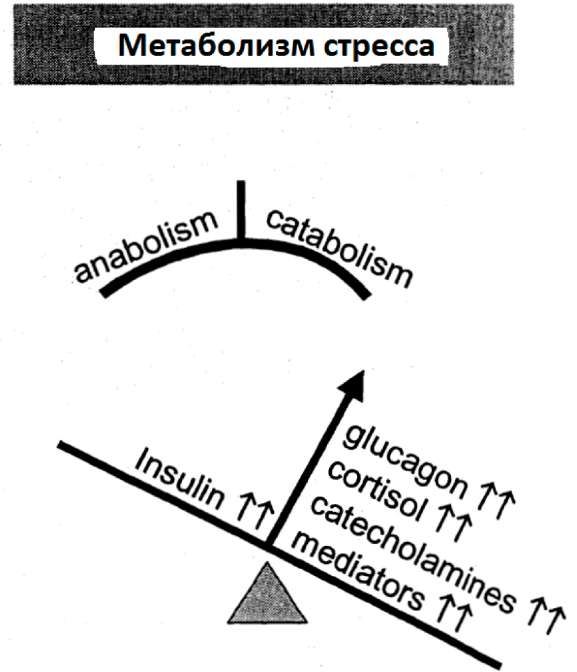
Во время стресса - в отличие от метаболизма при голодании - этот дисбаланс создан, несмотря на повышенное высвобождение инсулина, сопровождающееся намного более высоким возрастанием контррегуляторных гормонов катаболического инсулина, таких как глюкагон, кортизол и катехоламины.
Это один из главных регуляторных механизмов для утилизации различных веществ во время голода и стресса. Другое отличие лежит в повышенном высвобождении воспалительных медиаторов во время стресса, усиливающего катаболизм, что отличается от ситуации во время голода.
Характерные черты вызванного стрессом гиперметаболизма, как было определено по неврологической и гормональной реакции на стресс, суммированы на рис.8.
Рис.8: Характерные черты гиперметаболизма, определённые по неврологической и гормональной реакции на стресс
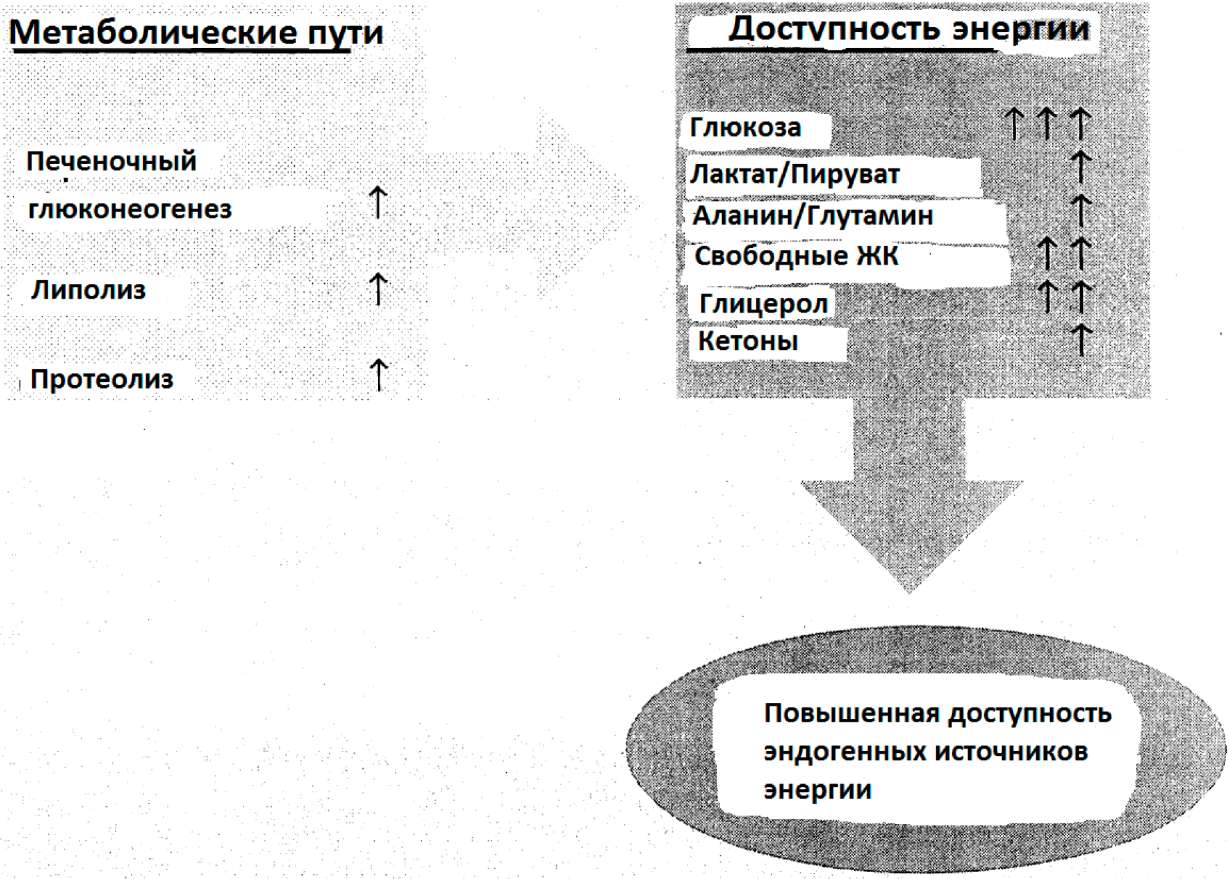
1.3.2. Нутритивные последствия вызванного стрессом катаболизма
Вызванный стрессом катаболизм, как описано выше, определённый по неврологическим и гормональным реакциям на стресс, который онтогенетически имел смысл для выживания человечества, не может быть реверсирован путём подачи экзогенных веществ. Следовательно, питание должно быть адаптировано к фактической метаболической ситуации. Первой задачей питания во время стрессового метаболизма является поддержание функций органов и систем, в особенности функций кишечника, печени, легких и иммунной системы. Не может ставиться в качестве задачи поддержание или восстановление тощей массы тела.
По этой причине, при стрессовых условиях питание было также названо «метаболической поддержкой» (Сегга, 1987).
Разумное поступление экзогенных веществ должно рассматриваться как функция, определяемая вычитанием из повышенных потребностей организма эндогенной мобилизации веществ, и зависящая от степени метаболического стресса.
Потребность в подаче питательных веществ может быть явно ниже интенсивности обмена веществ в покое из-за мобилизации эндогенных субстратов (рис.9).
Рис.9: Адекватное поступление экзогенных веществ, определенное через изменение интенсивности метаболизма и мобилизации эндогенных веществ (в отношении определений дляфазы отлива и прилива - см. ниже).
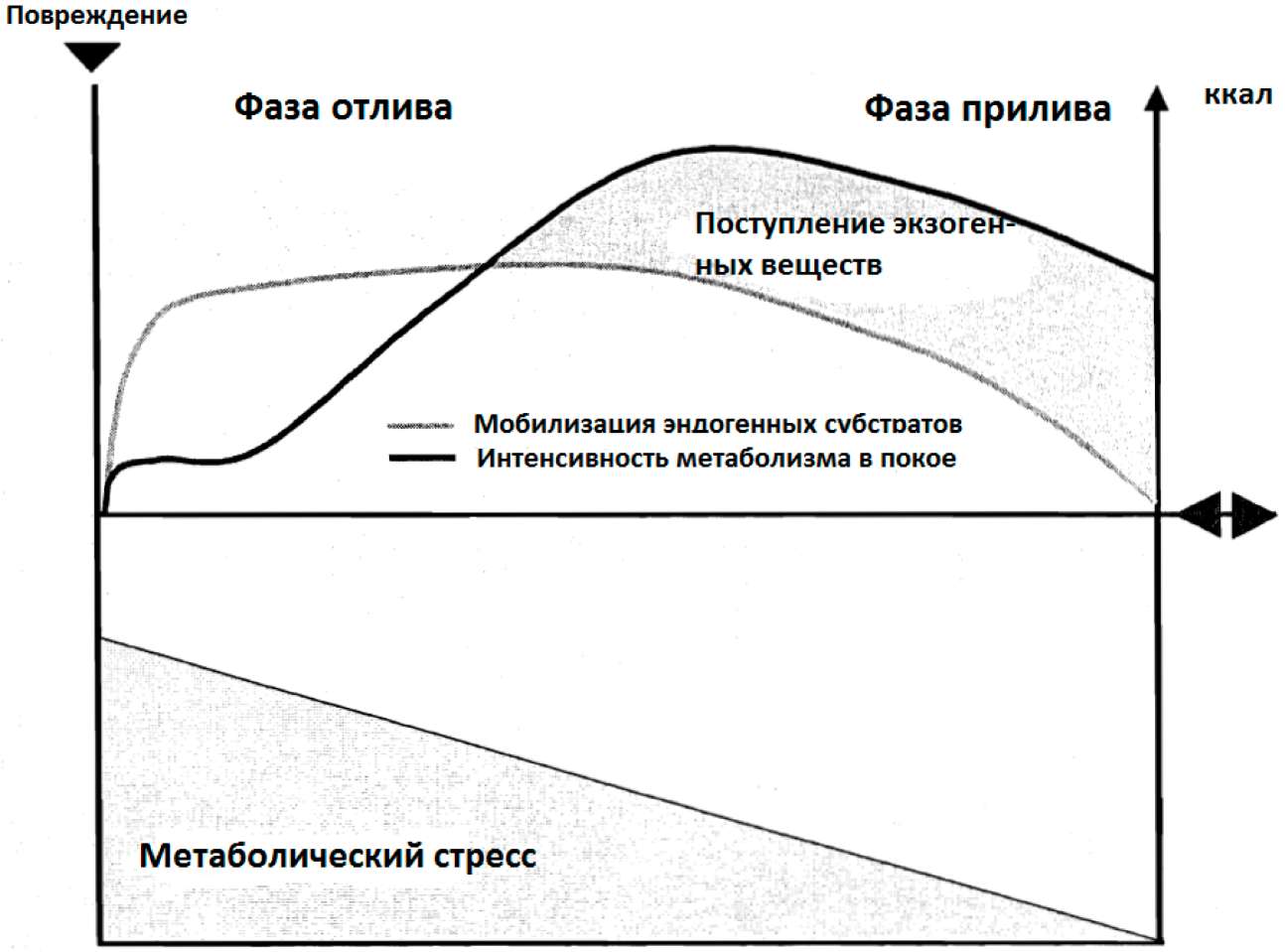
Доза энергии, жира и углеводов должна быть адаптирована к фактической метаболической способности использования и выведения вещества. На практике это может быть выполнено с помощью регулярных контролей мочевины плазмы, триглицеридов плазмы, сахара крови, регулярного вычисления скорости образования мочевины и регулярного определения дыхательного коэффициента. Это поможет распознать метаболические изменения и предотвратить гипералиментацию, которая, как было показано, увеличивает заболеваемость и смертность в условиях стрессового метаболизма. Это приводит нас к вопросу о том, какая питательная стратегия должна быть применена в случаях:
- нет питания;
- «метаболическая поддержка», либо
- питание для достижения положительного баланса энергии и азота - чтобы восстановить тощую массу тела.
3 фазы стрессового метаболизма, как они введены Катбертсоном (Cuthbertson, 1978), пока очень помогают при определении правильной стратегии питания. Они описаны как:
1. фаза отлива
2. фаза прилива и
3. фаза выздоровления (рис.10).
Рис.10: Фазы стрессового метаболизма по определению Катберстона и соответствующие стратегии питания.
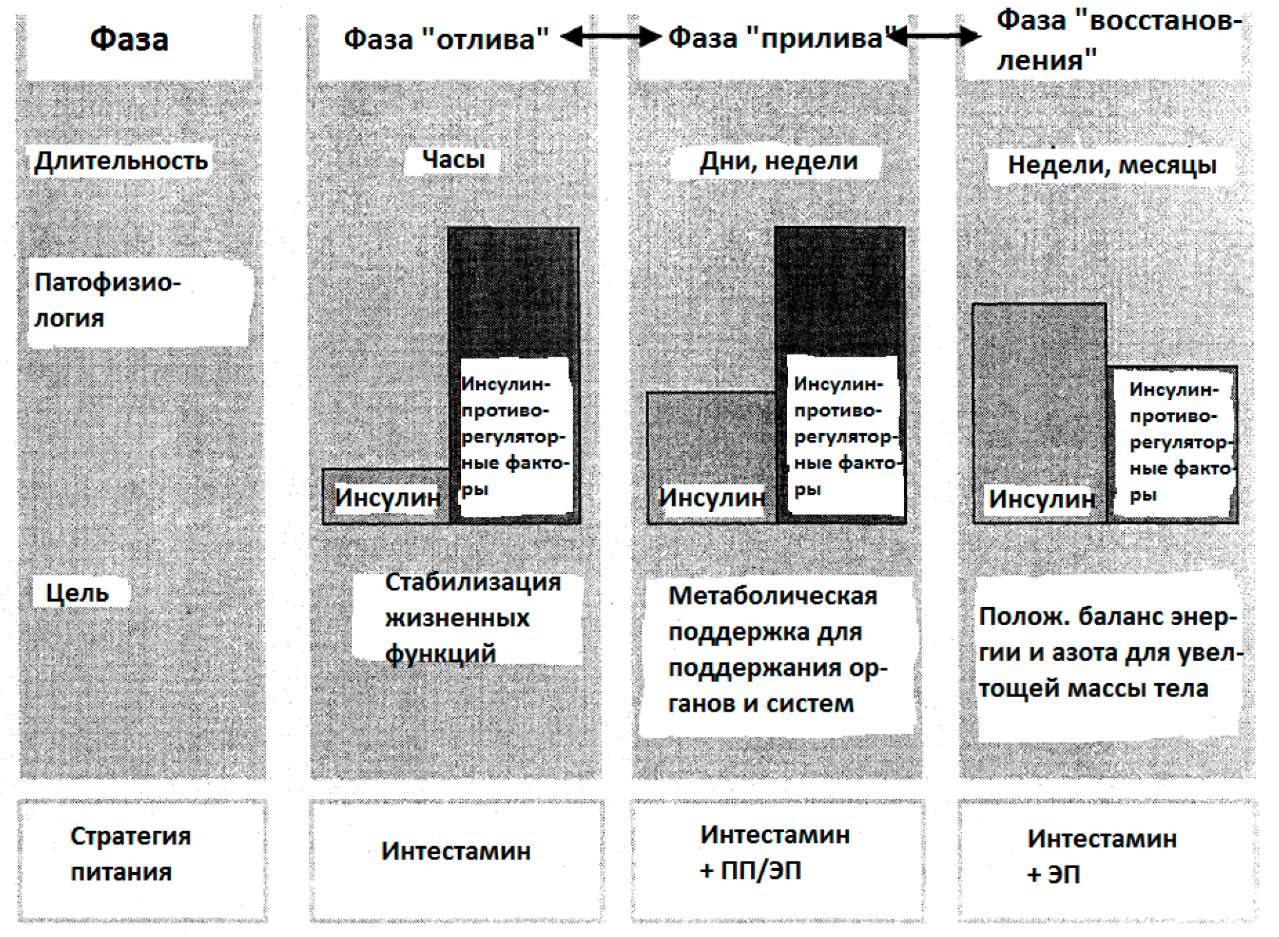
1. Фаза отлива
Фаза отлива (=шоковая фаза) следует сразу за травмой или после начала серьезных инфекций. Она обычно сохраняется в течение нескольких часов. В зависимости от времени реанимации, т.е. респираторной поддержки и гемодинамической стабилизации пациента, она может длиться от минут до примерно 24 часов после повреждения. Противорегуляторные факторы инсулина доминируют. Стабилизация жизненных функций - дыхание, кровообращение и поддержание функций органов - абсолютный приоритет лечения.
Питание не показано в течение фазы отлива! НО:
Интестамин может быть дан сразу, как только макрогемодинамическая ситуация стабилизируется.
2. Фаза прилива
Когда восстановлен адекватный объём циркулирующей крови, доминирует фаза прилива. Благодаря прогрессу интенсивной терапии, пациенты в наше время выдерживают очень критические ситуации и, в результате, фаза прилива может длиться в течение нескольких дней или даже недель. Это фаза стрессового [=SIRS] метаболизма, как описано выше. Серьезность её зависит от величины повреждения и SIRS.
Метаболическая поддержка является стратегией питания, которая должна быть применена: поступление нутриентов должно быть тщательно адаптировано к утилизации и выведению питательных веществ, как подчеркнуто выше.
3. Фаза восстановления
Переход в фазу восстановления будет достигнут только после того, как патофизиологические проявления, вызванные стрессом, будут устранены. Только тогда анаболический инсулин превалирует над противорегуляторными факторами. Утилизация нутриентов восстанавливается до нормальных величин. Положительный баланс энергии и азота может быть достигнут для увеличения массы тела, как и в случае метаболизма при голодании.
Эти 3 фазы могут, однако, не обязательно следовать одна за другой. Если вызывающие реакцию организма стресс факторы не были устранены и SIRS обостряется, пациент может опять впасть в фазу прилива или даже отлива. Это может случиться повторно и, конечно, требует адаптации стратегии питания к соответствующей метаболической ситуации.
Таким образом, рациональное применение Интестамина во время фазы отлива является обязательным и показано только после макрогемодинамической стабилизации. В фазе прилива доза обычного PN и EN должна быть «точно подстроена» согласно метаболической способности использования и выведения нутриентов. Для Интестамина эта «точная подстройка» не нужна, так как она не обеспечивает соответствующие количества энергии или другие главные питательные вещества.
Таким образом, полная доза Интестамина может быть обеспечена независимо от метаболической фазы и требуемой стратегии питания.
1.4. Желудочно-кишечный тракт в критических состояниях
Желудочно-кишечный тракт играет решающую роль в критических состояниях (заболеваниях) из-за его выдающейся иммунологической, а также механической
барьерной функции (смотрите раздел 1.1.). Обычно считается, что дисфункция кишки происходит рано в результате шока, сепсиса и вслед за травмой, и что отказ кишки и повреждение слизистой оболочки является неблагоприятным прогностическим фактором у критически больных пациентов (Хэглунд 1996). Что входит в понятие «дисфункции кишки»?
- повреждение слизистой
- повышенная проницаемость кишечника
- нарушенная иммунная функция GALT
- чрезмерно быстрый рост бактерий
- нарушения подвижности
- илеус (нарушение прохождения содержимого по кишечнику)
- нарушение всасывания
1.4.1. Ишемия и уепеуфузионное повреждение
Кишке была предназначена роль «осведомителя тела», что означает, что это сторожевой орган, который особенно восприимчив к расстройству потока крови или кислорода и к поступлению нутриентов (Данцкер 1993, Трэгер и др. 2001). Перфузия слизистой желудочно-кишечного тракта является первым процессом, подвергающимся изменениям при снижении кровотока, и последним, который будет восстановлен до нормальных величин в реанимации (Валет и др. 1996). Кишечная гипоперфузия (+ишемия) обычна для многих пациентов интенсивной терапии как последствие хирургии, геморрагического, кардиогенного или септического шока с последующей потерей крови или перераспределением крови к жизненно важным органам (мозг или сердце), что вызывает существенное падение потока крови к печени и кишечнику (Шмидт и Мартидейл, 2001). Желудочно-кишечная перфузия может быть также отягощена механической вентиляцией или отлучением от вентиляции (Трагер и др. 2001). Кроме того, местный поток крови в кишке уменьшается при голодании. Отсутствие кислорода и питательных веществ в клетках слизистой вызывает морфологические и функциональные изменения. Серьезность этого клеточного повреждения зависит от продолжительности данной ишемии (Сухнер и др. 2000).
Восстановление нормального потока крови к кишечнику называется «реперфузией». Реперфузия может ухудшить повреждение кишечных клеток из-за избытка свободных кислородных радикалов. Эти высоко реакционные радикалы не могут быть блокированы антиоксидантными энзимами, потому что эти защитные механизмы нарушены во время ишемии (Шварц и др. 1999).
Вот почему шок, кишечная ишемия и реперфузионное повреждение быстро создают характерное гипоксическое повреждение кишечной слизистой (Рис.11).
Рис.11: Механизмы, вызывающие повреждение слизистой ЖКТ во время критического состояния (заболевания) (взято из Хэглунд, 1996).
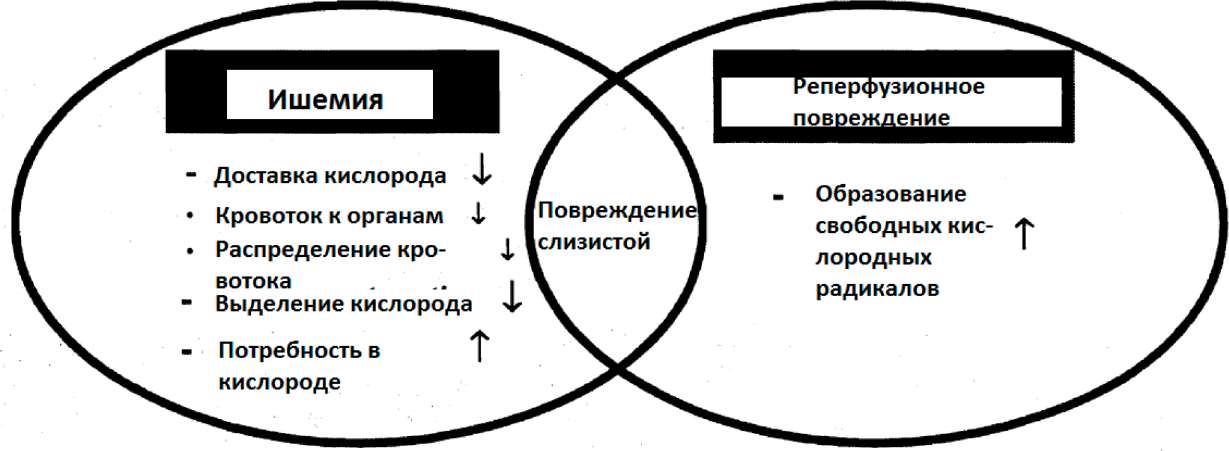
Повреждение слизистой может привести к повышенной кишечной проницаемости и/ или к высвобождению воспалительных или других токсичных веществ из повреждённой слизистой (Хэглунд 1996).
Вслед за ишемией и реперфузионным повреждением функция кишки как барьера может ослабнуть!
1.4.2. Чрезмерное развитие бактерий
Следующей проблемой у критически больных пациентов, кроме «протекающей кишки» (повышенная проницаемость), является колонизация верхней части желудочно-кишечного тракта бактериями и/или грибками, которое называется «чрезмерным развитием бактерий» (Маршалл 1999). Не только локализация, но также состав флоры часто бывает изменён во время критического заболевания. Основные причины показаны на рисунке 12.
Рис.12: Главные причины избыточного роста бактерий у критически больных пациентов (Маршалл 1999).

Колонизация верхней части желудочно-кишечного тракта осуществляется теми же штаммами микроорганизмов, которые превалируют в случае нозокомиальной инфекции. Часто трудно определить, является ли патологическая колонизация причиной или следствием системных нарушений (Маршалл, 1999). Предположено, что избыточный рост бактерий является фактором риска для приобретённой в интенсивной терапии инфекции путем аспирации или переноса (Маршалл 1991, 1999). В пользу этого предположения говорит факт благоприятного влияния профилактического избирательного обеззараживания пищеварительного тракта, который предотвращает нозокомиальные респираторные инфекции и снижает смертность в ОРИТ (Д'Амико и др. 1998, Маршалл, 1999). Другими последствиями бактериального избыточного роста могут быть:
- Подавление иммунологических функций слизистой оболочки кишки (GALT) и печени.
- Активация провоспалительных медиаторов в стенке слизистой токсическими факторами.
- Нарушение усвоения нутриентов (Маршалл, 1991, Харари и др. 2000).
Избыточный рост бактерий с указанными вредными эффектами изменения флоры может вносить вклад в развитие септического состояния и синдрома полиорганной недостаточности при критических состояниях (Маршалл 1991).
1.4.3. Кишка как триггер и/или мотор полиорганной недостаточности (MOF)
Инфекция является наиболее частой причиной смертности и заболеваемости (Стехмиллер и др. 1997) в ОРИТ. Кишечник, как было предположено, оказывается вовлеченным в патогенез многих нозокомиальных инфекций и, возможно, MOF. Однако точные механизмы и корреляция между кишечной недостаточностью и MOF остаются неясными (Шмидт и др. 2001). Выдвинута гипотеза, что нарушение функций кишечника является ключевым фактором в развитии позднего (вторичного) MOF у критически больных пациентов после политравмы и шока. Кишка реагирует на несколько стресс-факторов: шок, последующие ишемия и реперфузия, хирургические процедуры, воздействие лекарств, голодание и т.д., - множественными дисфункциями. Прежде всего, потеря очень важной иммунологической и механической барьерной функции, коррелирующих с развитием соматической инфекции и воспаления. Это может привести к MOF если иммунная система находится в подавленном состоянии в это же самое время (рисунок 13).
Рис.13: Гипотетическая роль кишки в в MOF после повреждения (Мур, 2000)
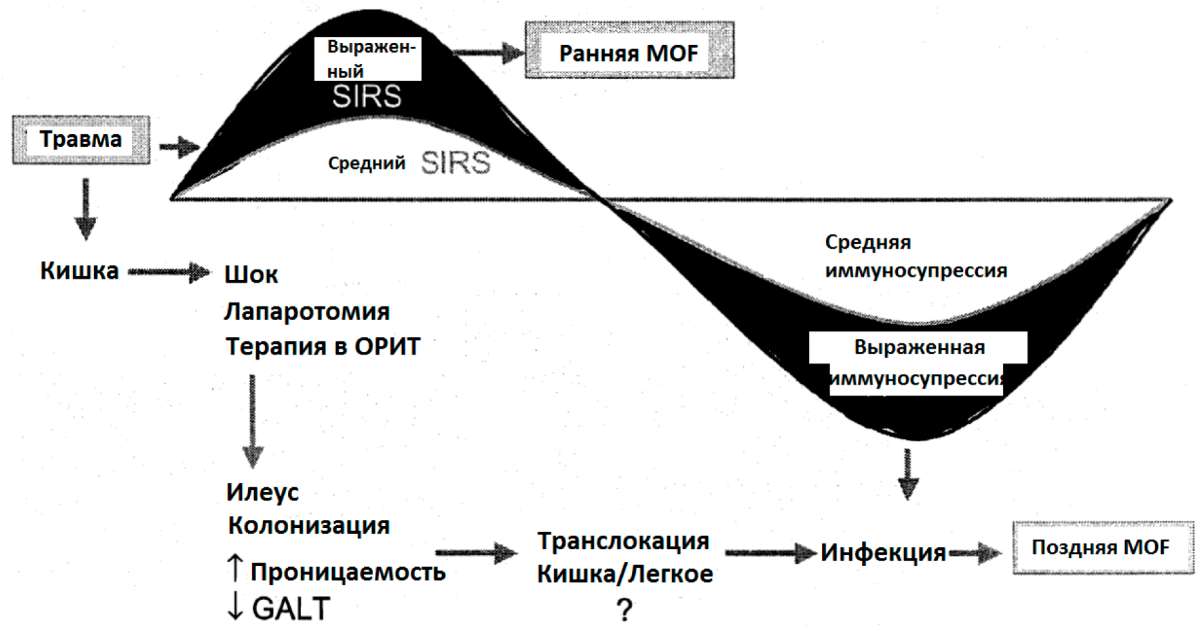
Предполагается, что кишка может быть входной точкой для патогенных бактерий и токсинов в кровь - явление, которое называется «бактериальным переносом». Бактерии и токсины, которые мигрировали через слизистую оболочку кишки, достигают другого органа, такого как печень и легкое, через кровь и лимфу. В частности, купферовские клетки печени играют, по-видимому, важную роль в опосредовании стрессовой реакции. Стрессовые гормоны, свободные радикалы и посредники, вызывающие воспаление, типа цитокинов, высвобождаются в виде реакции на внедрение патогенов. Обычный каскад воспалительных процессов может привести к гипервоспалению, серьезному нарушению функции органа вплоть до отказа органа (Хартиг и Вейманн 2000, Сухнер и др. 2000) (рисунок 14).
Рис 14: Гипотетическая роль кишки и печени в развитии MOF
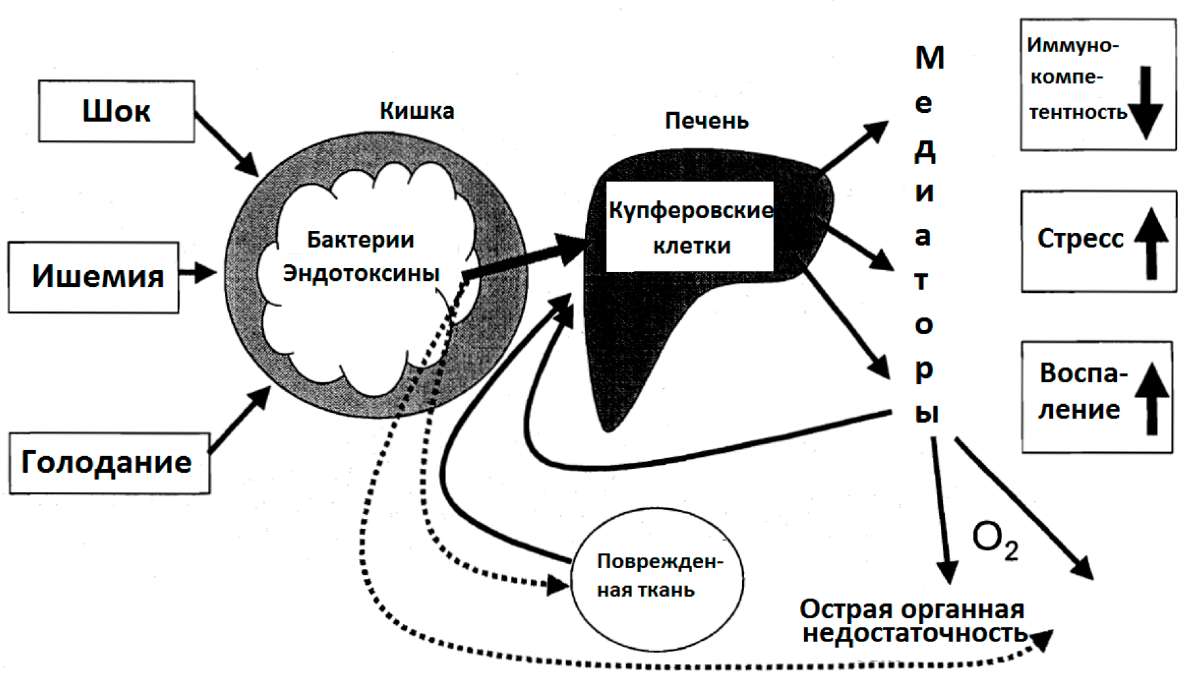
Имеется много лабораторных данных, идентифицирующих перенос бактерий или эндотоксинов как ключевой фактор в сепсисе и SIRS. Хотя клинические свидетельства ещё предстоит получить, предполагается, что бактериальный перенос также имеет место у критически больных пациентов, что было показано в исследовании на ожоговых пациентах (Ньювенхузен и Горе, 1999, Шмидт и Мартиндэйл, 2001).
«Ясно, что изменения в проницаемости стенки кишечника происходят, и что кишечные бактерии и эндоксины действительно находят себе путь в межклеточные пространства, однако роль этого явления в развитии удалённой инфекции и полиорганной недостаточности остаётся открытой для обсуждения» (Шмидт и Мартиндэйл, 2001).
Даже если перенос бактерий не вызывает начала соматической инфекции и множественной дисфункции органов, также возможно предположить, что кишка может быть «мотором MOF» другим способом. Если нарушение кишки следует из соматического нарушения вслед за травмой и шоком, потеря этого важного тракта иммунологической защиты может усугубить воспалительное состояние (Шмидт и Мартиндэйл, 2001).
Поддержание структурного и иммунологического барьера кишки, следовательно, играет ключевую роль в лечении критически больных пациентов (Ромбо и Такала, 1997, Сухнер и др. 2000, Штейн и Болдер, 2000, Гарвин и Браун, 2001). Подходы, направленные на уменьшение проницаемости кишки на ранней стадии у критически больных пациентов, могут улучшить клинические результаты и выживаемость таких пациентов (Штехмиллер, и др. 1997).
1.4.4. Уменьшение подвижности
Адекватная желудочно-кишечная моторика существенна для правильного переноса, переваривания и усвоения питательных веществ. Нарушения моторики являются ограничивающим фактором для доставки и эффективности энтерального питания (Ритц и др. 2000).
У критически больных пациентов желудочно-кишечная подвижность часто бывает нарушена в силу многих факторов (смотрите таблицу 1) (Ритц и др. 2000).
Таблица 2: Факторы, которые могут нарушать моторику ЖКТ в условиях критических состояний
|
Лежащие в основе заболевания/повреждения: травмы головы, ожоги, обширная брюшная хирургия, панкреатит, сахарный диабет, кишечная псевдонепроходимость... |
|
Метаболические нарушения: гипергликемия, гипокалиемия |
|
Лекарства: опиаты (мех. вентиляция!), эритромицин, антихолинергики |
|
Стресс: боль, сепсис ( |
|
Ишемия |
|
Избыточный NO |
Нарушения подвижности могут иметь место во всех частях желудочно-кишечного тракта (Херберт 1999). После хирургии, в особенности желудка и ободочной кишки, подвижность нарушается, что может вести к синдромам псевдо-непроходимости в тяжелых случаях (Гроневольд, 1996). Участвующая в этом патофизиология не вполне понятна из-за трудностей выполнения измерений желудочно-кишечной функции у критически больных пациентов (Ритц и др. 2000).
Медленное опорожнение желудка является наиболее обычным явлением у критически больных пациентов. Оно может составлять до 80% всех случаев в ОРИТ. Непереносимость поступающего объема пищи является наиболее важным последствием ненормального опорожнения желудка. Обычными симптомами являются боль в брюшине, вздутие живота, тошнота, рвота и, что наиболее вредно для критически больных пациентов, - аспирационная пневмония (Ритц и др. 2000). Кишечная моторная дисфункция также усиливается за счет имеющихся у критически больных пациентов желудочных спазмов и поноса при поступлении пищи в двенадцатиперстную кишку. Превалирование этих показателей дисфункции тонкого кишечника у пациентов в отделении интенсивной терапии составляет > 20% (Ритц и др. 2000). Непереносимость раннего кишечного питания составляет от 13% до 37% (обзор Герберта, 1999). Турнадре и соавт. (2001) обнаружили умеренные кишечные нарушения подвижности у 100% пациентов после серьезной брюшной хирургии. Дуоденальная и еюнальная моторная активность проявлялись в течение 2-х часов после операции, однако с большей частотой ненормальной миграции по сравнению со здоровыми субъектами. При инфузии нутриентов в двенадцатиперстную кишку не происходило восстановления нормальной картины подвижности кишечника.
Послеоперационный илеус в той или иной степени наблюдается после любой брюшной операции, а также после нескольких операций вне брюшины. Илеус определяется как торможение пропульсивных кишечных сокращений (Де Винтер и др. 1999). Могут наблюдаться два различных типа илеуса:
а) механический илеус из-за структурного торможения запрета, а также
б) паралитический илеус из-за функционального торможения пропульсивных сокращений. Послеоперационный илеус является в большинстве случаев паралитическим, который клинически характеризуется растяжением брюшины и болью, тошнотой, запором, а также недостаточностью выведения газов. Патогенез послеоперационного илеуса ещё остаётся спорным. По-видимому, в этот процесс вовлечены адренергические нейроны, кишечная нервная система и/или гормоны (Де Винтер и др. 1999). Прогноз послеоперационного илеуса обычно хороший: он разрешается за 2-4 дня. Продолжительный послеоперационный илеус случается только в 0.5-1.5% случаев брюшной хирургии (Де Винтер и др. 1999).
Адекватная терапия нарушенной моторной функции ЖКТ осуществляется редко. Задержанное опорожнение желудка может быть преодолено энтеральным зондовым питанием в тонкую кишкуи/или назначением лекарств с пропульсивным эффектом (Ритц и соавт., 2000, Герберт, 2002).
1.4.5. Нарушение всасывания
Всасывание некоторых аминокислот и Сахаров в кишечнике является, по-видимому, пониженным у пациентов с сепсисом (Салум и соавт., 1991, Проневельд, 1966). Всасывание глутамина, регулируемое гормонами, является важным фактором обеспечения энергией для слизистой оболочки ЖКТ (Лара, Якобе, 1998). Всасывание липидов серьезно понижается после травмы, кровоизлияния и реанимации (Кернер и др. 1995). Несколько факторов могут вести к нарушению всасывания энтерально вводимых в тонкий кишечник питательных веществ у критически больных пациентов (таблица 3).
Таблица 3; Причины плохого всасывания питательных веществ в тонком кишечнике у критически больных пациентов
• Гипоперфузия слизистой
• Повреждение слизистой
• Чрезмерный рост бактерий
• Нарушения подвижности
• Лекарственные препараты
• Повреждение экзокринной панкреатической функции
Пониженный кровоток через кишечную слизистую вслед за травмой и шоком ведет к функциональным нарушениям всасывания и ассимиляции питательных веществ. Извлечение кислорода, глюкозы и аминокислот понижается после «травмы слизистой». Метаболическая активность клеток слизистой понижается с результирующим уменьшением использования питательных веществ и пониженной активностью энзимов. Серьезность нарушения всасывания коррелирует с серьезностью повреждения слизистой (Сухнер и др. 2000).
Чрезмерный рост бактерий нарушает усвоение питательных веществ из-за повышенного роста поверхности слизистой. Он предотвращает контакт питательных веществ и клеток слизистой. Далее некоторые питательные вещества могут быть уже использованы бактериями и стать недоступными для макроорганизма. Изменение моторной функции тонкого кишечника оказывает критическое влияние на пищеварение и усвоение нутриентов. Нарушается сама предпосылка правильного пищеварения и усвоения нутриентов: содержимое тонкого кишечника должно быть смешано с пищеварительными ферментами и транспортировано к поверхности слизистой (Ритц и др. 2000). Трибл и соавт. (2000) показали, что панкреатические энзимы (амилаза, трипсин, химотрипсин) сильно зависимы у критически больных пациентов от наличия септического шока. Предполагается, что продолжительный отдых (отсутствие функционирования) кишечника ведёт к дальнейшей атрофии слизистой, понижению активности ферментов и снижению усвоения нутриентов (Гроневельд, 1996).
1.5 Окислительный (оксидативный) стресс
1.5.1. Развитие окислительного стресса в критических состояниях
Кислород часто называется «обоюдоострым мечом». Хотя он абсолютно необходим для жизни, многие существенные внутриклеточные реакции, для которых он требуется, приводят к образованию свободных кислородных радикалов (OFR). OFR являются молекулами, которые имеют один или два неспаренных электрона, что делает их чрезвычайно нестабильными, высоко реактивными и таким образом потенциально токсичными для клеточных мембран, протеинов и дезоксирибонуклеиновой кислоты (DNA) (Якоб и Бури, 1996). Представителями клинически важных OFR являются: супероксидный радикал, пероксид водорода, оксид азота и высоко реактивный гидроксильный радикал (рисунок 15).
Рис.15: Клинически важные свободные радикалы
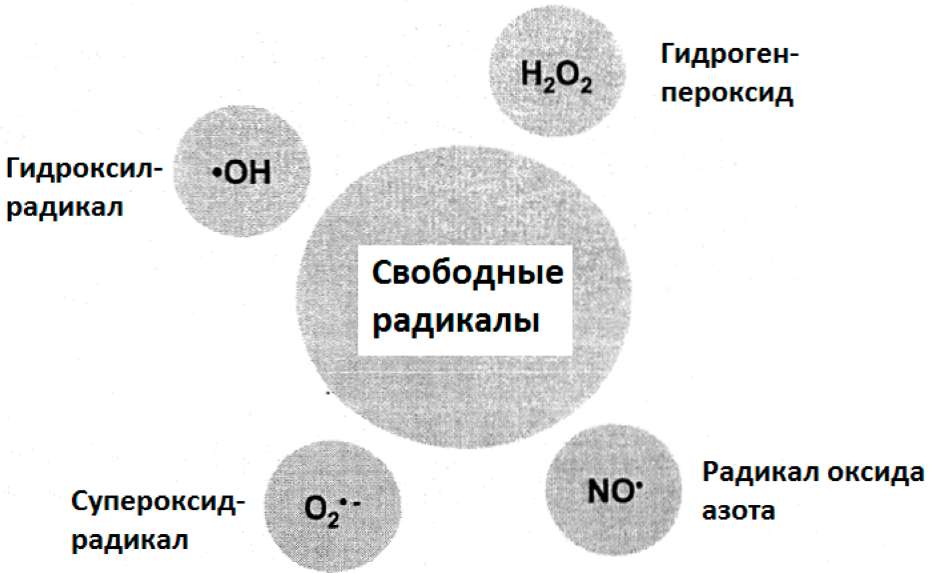
При нормальных обстоятельствах наше тело защищено от этого окислительного вызова природными защитными системами подобно утилизирующим радикалы энзимам или витаминам (Гуде и Вебстер, 1993). Тем не менее, когда баланс между защитными антиоксидантными механизмами и генерацией OFR нарушен, мы сталкиваемся с ситуацией, называемой «окислительный стресс» (Тью и Джонс, 1994).
Что нарушает баланс между производством OFR и устранением 01 R у критически больных пациентов?
- Ишемия / реперфузионное повреждение
- Воспаление
- Инфекция
- Недостаточность питания
- Токсичные агенты (химиотерапия, лекарства)
Рис. 16: Дисбаланс производства свободных кислородных радикалов и их устранения при критических заболеваний (модифицировано из Борхани и Хелтон, 2000).
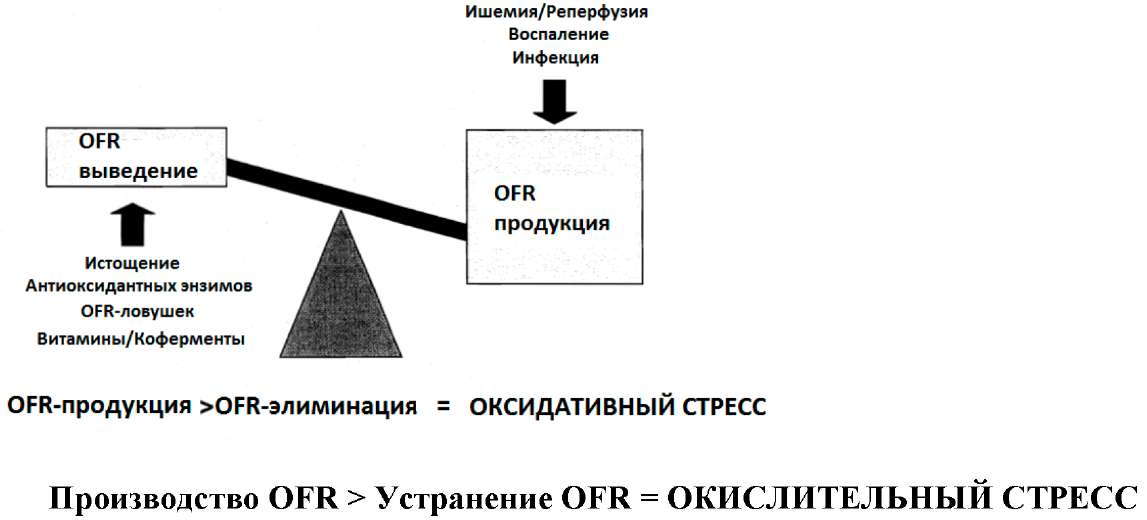
Рисунок 16 показывает дисбаланс между большим производством OFR (во время ишемии/реперфузии, воспаления и/или инфекции) и пониженным устранением OFR из-за истощения эндогенных антиоксидантов при критических состояниях. Кроме того, предшествующие факторы могут вносить свой вклад в окислительный стресс у критически больных пациентов: возраст, курение, недоедание, а также хронические заболевания, такие как атеросклероз, сахарный диабет или ревматоидный артрит -которые все связаны с повышенным производством OFR или пониженной антиокислительной способностью, или и с тем и другим.
Окислительный стресс играет главную роль в патофизиологических процессах (ишемическое /реперфузионное повреждение, воспаление, инфекция), вызванных критическими заболеваниями (Тью и Джонс, 1994). Механизмы развития окислительного стресса в критических состояниях и его последствия будут рассмотрены в следующих параграфах.
Ишемическое/реперфузиониое повреждение
Тканевая ишемия, за которой следует реперфузия, представляет собой главный механизм, с помощью которого генерируются OFR в критических состояниях. Кишечная слизистая является одной из наиболее чувствительных к ишемии тканей (смотрите раздел 1.4: Желудочно-кишечный тракт). Ишемия, определяемая как отсутствие или малый поток крови в тканях (гипоперфузия) является явно повреждающим фактором, и быстрое восстановление нормального потока крови является решающим. Если ткань выдерживает гипоксический удар, восстановление потока (реперфузия) является главным источником последующего повреждения клетки и разрушения, создавая порочный круг, т.е. нет ишемии без реперфузии и наоборот (Хаммерман и Каплан 1998).
Ишемические фазы:
Когда доступность кислорода в ткани жизненно-важного органа ограничена из-за гипоперфузии, клетки переходят от аэробного к анаэробному метаболизму. Хотя это жизненно важно, анаэробный метаболизм намного менее эффективен, давая примерно 6% энергии (запасённой как АТР) на молекулу глюкозы от той, которая была бы произведена при аэробных условиях (Хаммерман и Каплан, 1998). Когда клетки не могут поддерживать адекватное производство энергии, они компенсируют это разрушениемсуществующих АТР. Вследствие этого становится возможным приток ионов Са в клетки. Повышение содержания внутриклеточного кальция активирует различные энзимы, большинство из которых могут разрушить структурные компоненты клетки (Хаммерман и Каплан, 1998) (смотрите рис.17).
Рис. 17: Важные патофизиологические механизмы, с помощью которых ишемия и реперфузия ведёт к высвобождению OFR и клеточному повреждению
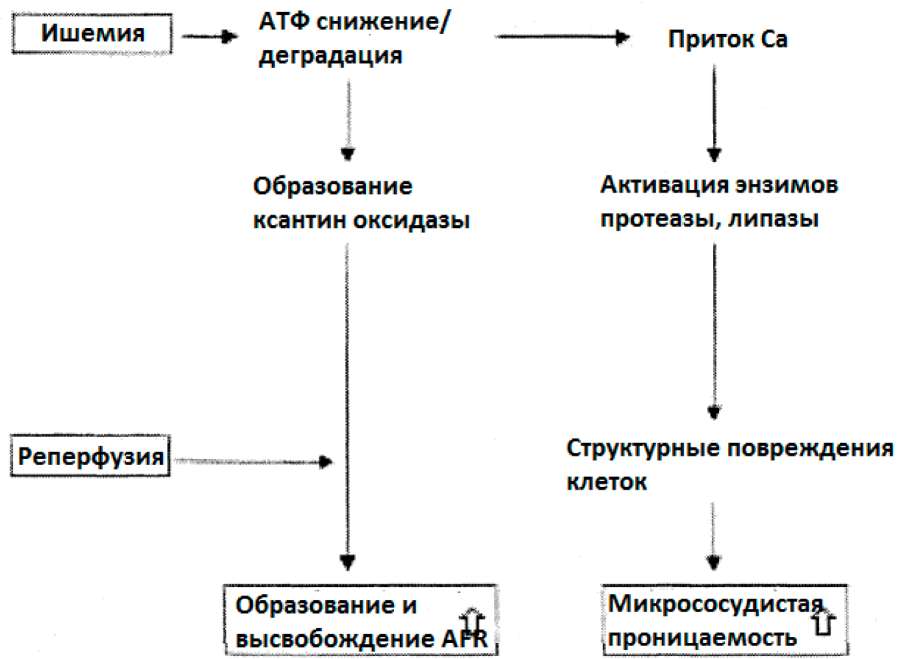
В условиях ишемии активируется энзим ксантин оксидаза. Этот энзим способен использовать молекулярный кислород как субстрат для получения высоко реактивных OFR в следующей фазе реперфузии (Лата и Бабу, 2001). Во время ишемии все эти метаболические изменения происходят в клетках, в которых активированы несколько энзимов, что может повредить клетки непосредственно и, с другой стороны, может произвести OFR во время следующей фазы реперфузии (рисунок 17). Фаза реперфузии:
Реперфузия означает восстановление нормального потока крови в ткани и органах. В начальной стадии во время реперфузии ишемической ткани генерируется всплеск OFR главным образом за счёт деятельности ксантин оксидазы в клетках. Один из этих OFR, гидроксил-радикал, особенно токсичен, так как он является наиболее реакционным OFR (Шиллер и др. 1993). Этот гидроксил-радикал настолько реакционоспособен, что он атакует все биологические вещества, такие как протеины, полисахариды, нуклеиновые кислоты (в результате разрывая цепь ДНК) и полинасыщенные жирные кислоты (Фримен иКрапо, 1982).
1.5.2. Воспалительная реакция на окислительный стресс
Произведенные ишемией/реперфузией OFR непосредственно повреждают клеточные компоненты. Еще более важно, что OFR, а также эндотоксины или перенесенные бактерии, переключают процесс высвобождения цитокинов на активацию воспалительного каскада (Гримбл, 1994). Свободные радикалы активируют резидентные макрофаги (Купферовы клетки) в печени, которые высвобождают воспалительные цитокины (TNF, IL-1, IL-6) (Вендемиал и др. 1999). Эти посредники воспалительного процесса, в свою очередь, вызывают активацию и приток воспалительных клеток (моноцитов и лейкоцитов) в ткани и органы, вызывая повреждение ткани. Далее активированные Купферовы клетки также производят большие количества OFR. И опять, создаётся порочный круг (см. рисунок ниже). Кроме того, OFR содействуют адгезии молекул, которая, в свою очередь, ведёт к аккумуляции гранулоцитов в реперфузированную ткань и к усилению повреждения клетки (Хаммерман и Каплан 1998).
Такая инфильтрация ткани гранулоцитами, например, секвестрация нейтрофила в легком у взрослого с синдромом расстройства внешнего дыхания (ARDS), является одним из признаков воспаления (Найт, 1998).
Рис.18: Порочный круг образования свободных кислородных радикалов в условиях SIRS
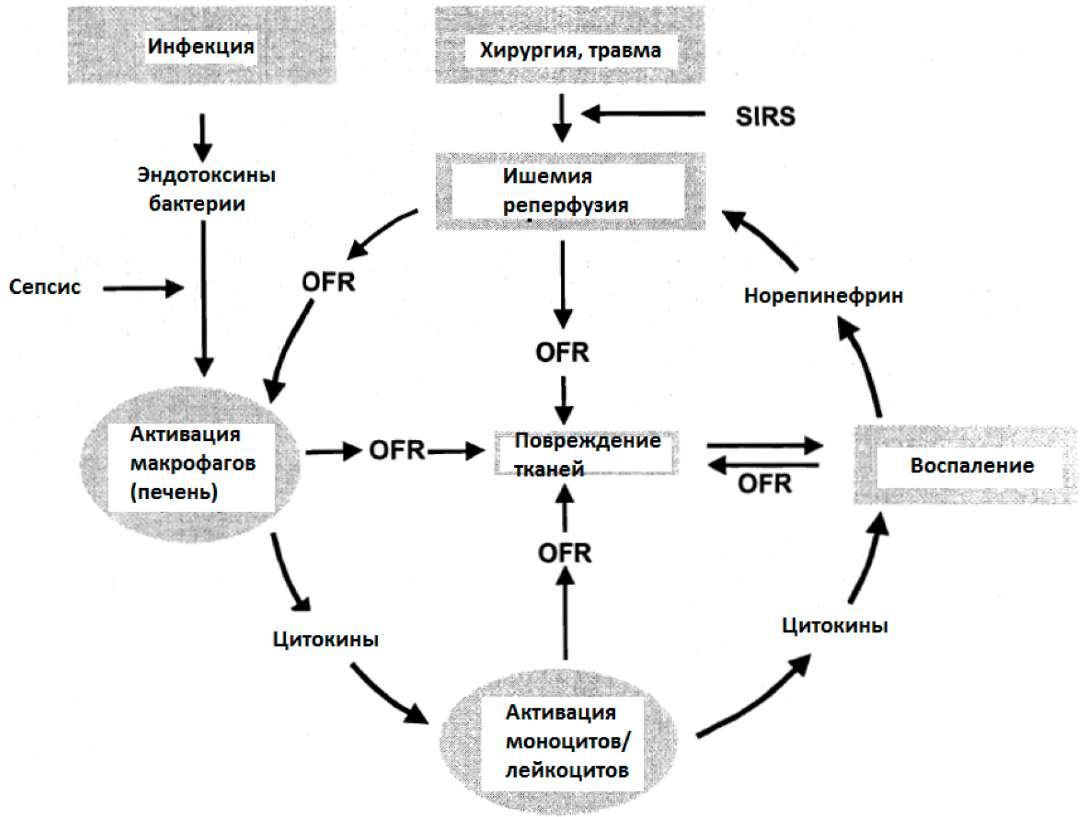
Заключение: ишемия / реперфузия после хирургии, серьезной травмы или инфекции вызывают опосредованное свободными кислородными радикалами (OFR) повреждение ткани и создают воспалительную реакцию в других, отдалённых органах и тканях. Кроме того, воспаление само стимулирует генерацию OFR и создаёт порочный круг.
1.5.3. Антиоксидантные механизмы
Наш организм поддерживает сложную эндогенную систему защиты от OFR. По
существу разнообразные вне- и внутриклеточные антиоксидантные системы защиты работают вместе, включая следующие компоненты:
- Энзимы, т.е. супероксид-дисмутаза, каталаза, глутатион-пероксидаза и глутатион-редуктаза
- Донаторы сульфгидрильных групп, в частности, глутатион
- Витамины Е, С, b-каротин.
Первая линия внутриклеточной защиты состоит из группы антиоксидантных энзимов. В условиях подавления энзиматических антиоксидантов OFR получают свободу реагировать с восприимчивыми молекулами-мишенями внутри клетки, такими как жирные кислоты в клеточной мембране. Вторая линия защиты - это поглощение OFR неэнзимными антиоксидантами, которые растворимы в воде, такими как глутатион и витамин С, или в липидах - витамины Е и b-каротин (Трансвел и Фримен, 1995).
1.5.3.1. Антиоксидантные энзимы
Энзимами, непосредственно вовлечёнными во внутриклеточную детоксикацию OFR, являются супероксид-дисмутаза, каталаза и глутатион-пероксидаза (Максвелл, 1995). Непрямые антиоксидантные функции также опосредованы энзимами, такими как глутатион-редуктаза, которая восстанавливает уровень эндогенных антиоксидантов. Супероксид-дисмутаза: Металлоэнзим - супероксид дисмутаза присутствует в цитоплазме (Cu-Zn форма) и митохондриях (Мп форма) клеток, катализирует преобразование супероксидных радикалов в перекись водорода ((V -►Н2О2).
Каталаза / глутатион-пероксидаза Каталаза и зависящая от селена глутатион-пероксидаза катализирует преобразование перекиси водорода в воду (Н2О2 -►Н2О) в присутствии восстановленного глутатиона.
Глутатион-редуктаза : Глутатион-редуктаза делает возможным рециклирование из окисленной в восстановленную форму глутатиона в присутствии НАДФ.
Рис.19: Энзимное удаление свободных кислородных радикалов (модифицировано из Барбер и Харрис, 1994).
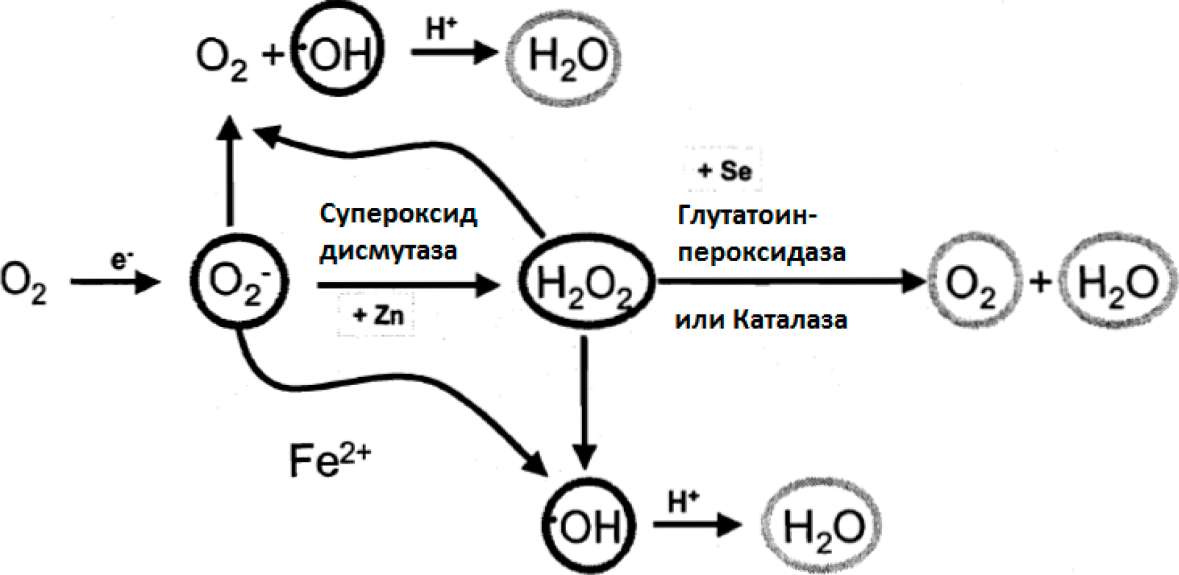
Микроминералы селен и цинк являются существенными сопутствующими факторами для некоторых из вышеупомянутых антиоксидантных энзимов. Селен : Селен является компонентом семейства примерно 3 5 селенопротеинов, некоторые из которых имеют важные энзимные функции (Рэйман 2000). Все эти зависящие от селена энзимы имеют селеноцистеин в качестве активного центра. Наиболее важные антиоксидантные функции имеет семейство глутатион-пероксидаз, которые восстанавливает перекись водорода до воды и преобразует липид и фосфолипид в безвредные спирты. Другой зависящий от селена энзим - тиоредоксин-редуктаза, которая помогает контролировать клеточный окислительно-восстановительный баланс (Циммерман и др. 2000).
Цинк: Цинк присутствует в Cu-Zn форме супероксид-дисмутазы (см.выше). 1.5.3.2. Глутатион
Глутатион - это трипептид, состоящий из трёх аминокислот: глутамина, цистеина и глицина. Глутатион преимущественно синтезируется в печени, откуда он может быть
транспортирован к другим органам. По последней информации глутатион может быть также синтезирован в ряде других тканей (Вернерман и Хаммарквист, 1999, Валенсия и др. 2001). Синтез глутатиона зависит от доступности предшественников - глутамина, цистеина и глицина (Рот и др. 2002). Внутри клетки глутатион является количественно наиболее важным эндогенным антиоксидантом и поглотителем радикалов (Вернерман и Хаммарквист, 1999). Глутатион присутствует главным образом в восстановленной, мономерной форме (GSH) и, в намного меньших концентрациях, в оксидированной димерной форме (GSSG). Отношение GSH к GSSG является наиболее важным регулятором редокс (окислительно-восстановительного) потенциала в клетках. Этот редокс-статус GSH критичен для различных биологических событий, включая активацию гена, регулировку размножения клеток, апоптоз, а также воспаление (Рот и др. 2002). Синтез некоторых цитокинов и адгезионных молекул, которые играют роль в соматическом воспалении, зависит от активации фактора считывания кода ядерного фактора-кВ (NFkB). Активация этого фактора зависит от клеточного редокс-потенциала и, отсюда, от внутриклеточного отношения GSH/GSSG (рисунок 20) (Рот и др. 2002).
Рис.20: Редокс-регулируемая активация NFkB как предшественника образования воспалительных посредников (модифицировано из Рот и др. 2002)
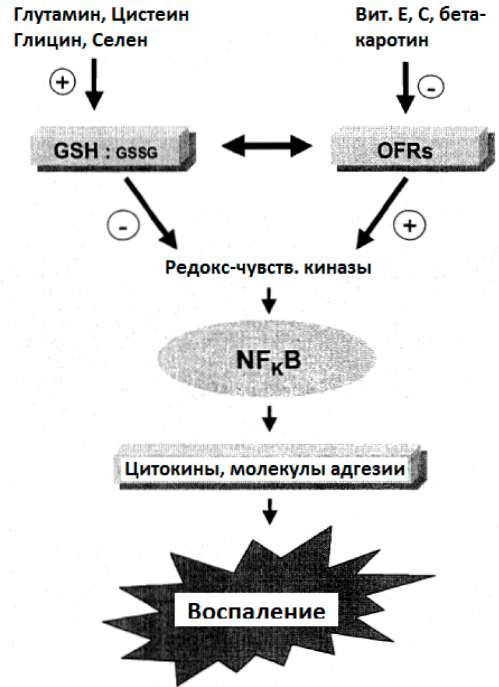
Повышение концентрации GSH за счет предшественников глутатиона или селена ведет к повышенному отношению GSH к GSSG, что предотвращает активацию NFkB. В отличие от этого, повышение производства OFR активирует NFkB и, затем, экспрессию воспалительных цитокинов и адгезионных молекул. Более того, глутатион действует как субстрат для глутатион-пероксидазы и глутатион-редуктазы (см. выше). Он также имеет антиоксидантную активность, реагируя с исключительно разрушительным гидроксил-радикалом (• ОН), который атакует все клеточные компоненты (Тансвел и Фримен, 1995).
1.5.3.3. Витамины С. Е и В-кауотин
Витамин С: Аскорбиновая кислота является превалирующим растворимым в воде антиоксидантом в теле. Витамин С имеет две первичные антиоксидантные функции. Во-первых, витамин С реагирует с OFR и инактивирует их в цитоплазме и внеклеточном пространстве. Во-вторых, С регенерирует окисленный витамин Е (Барбер и Харрис, 1994).
Витамин Е: Витамин Е является смесью близких друг к другу соединений, называемых токоферолами, а-токоферол является наиболее сильнодействующим. Витамин Е -жирорастворимый витамин и, следовательно, распределяетсяДглавным образом, в клеточных мембранах и липопротеинах, где он действует, прерывая цепные реакции свободных радикалов, таких как пероксидация липидов. После реакции со свободными радикалами образуется нереагирующий радикал витамина Е. Эта «потраченная» форма витамина Е затем реактивируется до её первоначального состояния путем взаимодействия с витамином С и глутатионом (Барбер и Харрис, 1994).
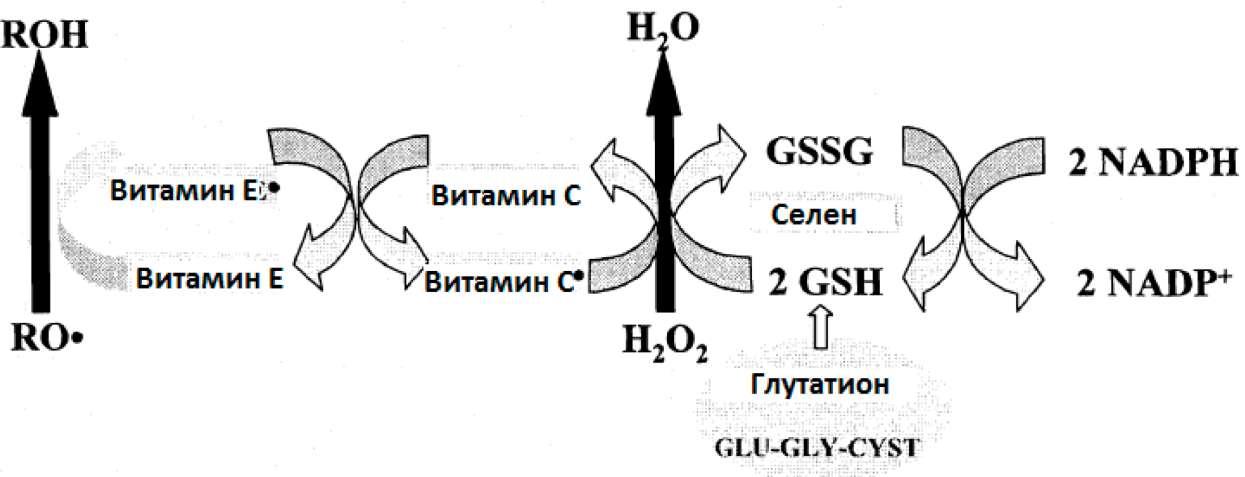
Бета-каротин: b-каротин является главным предшественником витамина А. Подобно а-токоферолу, b-каротин является растворимым в липидах веществом. b-каротин - это очень эффективный ингибитор атомарного кислорода, и он также ингибирует перекисное окисление липидов. Что интересно, он представляется особенно эффективным при низком давлении кислорода (ишемия). У людей он присутствует при концентрации, которая в 20 раз ниже, чем концентрация а-токоферола (Фрей, 1994). Взаимодействия витамина С, Е, селена и глутатиона очень важны для поддержания антиоксидантной защиты организма. Все эти антиоксиданты действуют синергически (см. рис. ниже): радикал токоферола реагирует с витамином С для регенерирования витамина Е. Радикалы витамина С затем энзимно восстанавливаются обратно в витамин С через селен-зависимую глутатион-пероксидазу. Н2О2 одновременно превращается в воду. Окисленный глутатион (GSSG) восстанавливается до GSH в присутствии НАДФ.
Рис.21: Взаимодействие витаминов Е и С, селена и глутатиона для поддержания антиоксидантной защиты организма (модифицировано из Борхани и Хелтон, 2000)
1.6. Истощение ключевых питательных веществ 1.6.1. Глутамин
В последние годы было показано, что, несмотря на большие количества глутамина в организме, запасы его могут истощиться, особенно в процессе катаболического стресса, такого как повреждение и инфекция (Неу и др. 2002).
Многие исследователи показали, что у критически больных пациентов потребление глутамина превышает эндогенный синтез глутамина, что приводит к истощению запасов глутамина (смотрите таблицу 4: Критическое состояние, связанное с низкими плазменными уровнями глутамина). Больные в критическом состоянии подвергаются сильному стрессу, что характеризуется выраженным катаболизмом. Это катаболическое
состояние характеризуется деструктивным процессом с клиническими характеристиками в виде потери веса тела, жира и тощей массы тела. Мобилизованные жир тела и протеины скелетных мышц используются как топливо из-за высоких расходов энергии во время катаболизма (Боленс и др. 2001). Глутамин главным образом формируется в скелетной мышце. В катаболическом состоянии он высвобождается в возрастающих количествах и поступает в циркуляцию, используясь как предпочтительный субстрат энергии печенью и иммунокомпетентными клетками (Боленс и др. 2001). Кроме того, в катаболических состояниях глутамин крайне важен для кишечника, потому что клетки кишечной слизистой и связанной с кишкой лимфоидной ткани используют глутамин как первичное топливо (Боленс и др. 2001). Было продемонстрировано, что истощение внутримышечного глутамина у критически больных пациентов с ожоговыми повреждениями не вызвано ухудшением синтеза этого вещества, а ускоренным выходом из мышц (Эндрюс и Гриффите, 2002). Уменьшение мышечного пула свободного глутамина (приблизительно 50% нормального уровня) оказывается признаком реакций на повреждение, инфекцию и недостаточное питание (Фюрст, 1994). Как показано в таблице 4, клинические исследования подчеркивают, что критическое состояние ассоциируется с низкими плазменными уровнями глутамина.
|
Критическое состояние |
Ссылки |
|
|
Трансплантация костного мозга |
Brown etal. 1998, Мс Burney et Ed. 1994, |
Schloerb 1999, Schloerb 1993, Ziegler 1992. |
|
Сепсис Травма Ожоги |
Griffiths et al.1997, Houdijk et al. 1998, Jensen et al. 1996, Jones etal. 1999, Scheltinga et al. 1991, |
Newsholme et al. 1987, Powell-Tuck et al. 1999, Rennie et al. 1985, Roth et al. 1990, Tremel etal. 1994. ■ |
|
Острый панкреатит |
Roth etal. 1986 |
|
|
Химиотерапия |
Decker-Baumann et al. 1999 |
|
|
Хирургические пациенты |
Hammarqvist et al. 1989, Jiang et al. 1999, Morlion et al. 1998, |
O'Riordainetal. 1994, Stehle et al. 1989. |
Таблица 4: Критическое заболевание, связанное с низкими плазменными уровнями глутамина
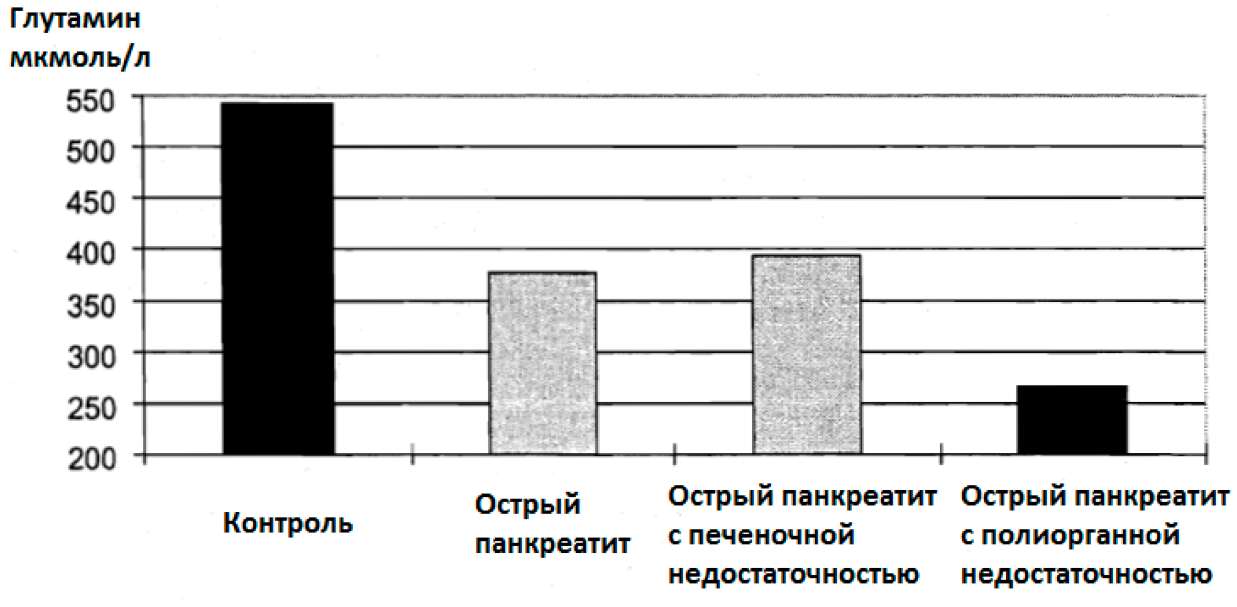
Рот и соавт. (1986) показали, что у пациентов с острым панкреатитом уровни глутамина в серозной жидкости заметно меньше. В тоже время у пациентов с острым панкреатитом в сочетании с полиорганной недостаточностью наблюдалось самое сильное понижение уровня глутамина в серозной жидкости. Следовательно, может иметься связь между остротой заболевания и пониженными уровнями глутамина (см. рис. 22: Уровни глутамина в серозной жидкости у пациентов с острым панкреатитом).
Рис.22: Уровни глутамина в серозной жидкости у пациентов с острым панкреатитом
Худик и др. показали, что критическое заболевание связано с низкими плазменными уровнями глутамина, и что глутаминовая терапия может помочь предотвратить инфекционные осложнения; это следует из впечатляющего исследования 60 пациентов с серьезными множественными травмами (Худик 1998). В этом рандомизированном контролируемом исследовании раннее энтеральное питание было начато в пределах 48 часов после травмы через назодуоденальный зонд и продолжено в течение минимум 5 дней. Пациенты в контрольной группе продемонстрировали спад плазменных концентраций глутамина уже на 3 день после события. В то время как пациенты, получающие обогащенное глутамином зондовое питание, продемонстрировали значительное возрастание плазменной концентрации глутамина на 3, 4 и 5 день после события в сравнении с контрольной группой. Пациенты, получающие обогащенное глутамином зондовое питание, имели в целом лучшие клинические показатели, чем пациенты из контрольной группы. Имелось значительное снижение (15-дневный срок наблюдения) частоты пневмонии, бактериемии и острого сепсиса (см. также раздел 3.3.1.3 Глутаминовая терапия у критически больных пациентов). Эти результаты подтверждают гипотезу о том, что обогащенное глутамином энтеральное питание может повысить плазменную концентрацию глутамина у критически больных пациентов и улучшить исход заболеваний. Гриффите и др. (1997) наблюдали пониженные уровни глутамина у критически больных пациентов в начале питательной интервенции. Показатели выживаемости в течение 6 месяцев были значительно выше при использовании глутаминовых добавок, чем в контрольной группе. Эти результаты ещё раз позволяют предположить, что эндогенная подача глутамина становится критически важной для выживания. Недостаток глутамина - это депривация кишки, печени и иммунной системы, поэтому восполнение дефицита существенно. Причины различного метаболического поведения глутамина в критических заболеваниях, приводящих к его истощению, суммированы в следующей таблице (Таблица 5).
Таблица 5: Причины истощения глутамина у критически больных пациентов
|
1. Повышенная потеря мускула / ускоренное истощение протеина |
|
• топливо для метаболизма с высоким расходом энергии |
|
П. Повышенная потребность со стороны |
|
• кишечной слизистой • печени • иммунокомпетентных клеток |
1.6 Истощение ключевых питательных веществ
1.6.2 Антиоксид анты
1.6.2.1. Почему для критически больных пациентов особенно опасен недостаток антиоксидантов?
Окислительный стресс играет главную роль в патофизиологических процессах (ишемия / реперфузионное повреждение, воспаление, инфекция), вызванных критическими заболеваниями (смотрите раздел 1.5. Окислительный стресс), ведущими к высокому потреблению антиоксидантов. Гиперметаболизм, связанный с повреждением и воспалением (инфекция), неизбежно ведет к повышенной потребности в питательных веществах, включая антиоксидантные витамины и микроэлементы. Критически больные пациенты склонны терять заметные количества антиоксидантных питательных микроэлементов. Потери могут быть значительными после ожогов (через экссудативную жидкость), у пациентов с большой потерей крови (геморрагический шок), у тех, кто требует заместительной почечной терапии, такой как гемодиализ или гемофильтрация после острой почечной недостаточности, а также у пациентов с послеоперационными осложнениями (Шенкин, 2000). Кроме того, ряд предшествующих факторов может вносить вклад в окислительный стресс и, следовательно, в истощение антиоксидантов у критически больных пациентов. Такие факторы включают пожилой возраст, курение, недостаточное питание, а также хронические заболевания, такие как атеросклероз, сахарный диабет, цирроз печени или ревматоидный артрит - все они связаны с повышенным производством свободных радикалов, пониженной способностью антиоксидантов, или с тем и другим (Борхани и Хелтон, 2000). Последнее, но не менее важное обстоятельство - адекватное поступление нутриентов - часто задерживается или прерывается у критически больных пациентов (см. раздел 2.2: Недостатки современного иммунопитания), тем самым усиливая истощение антиоксиданта. В таблице 6 суммированы факторы, которые участвуют в процессе истощения антиоксидантов у больных в критических состояниях.
Таблица 6: Причины истощения антиоксидантов у критически больных пациентов
|
1. Заранее существующий дефицит - из-за пожилого возраста, курения, недостаточного питания, хронических заболеваний |
|
2. Повышенная потребность - высокое потребление антиоксиданта в условиях интенсивного образования радикалов - высокие потребности в гиперметаболизме |
|
3. Повышенные потери - кожный экссудат в ожогах, потеря крови, диализ, желудочные выделения, кишечная фистула |
|
4. Пониженное поступление - посттравматическая, послеоперационная задержка в адекватном питании/подаче антиоксиданта - перерывы в подаче нутриентов из-за клинических / диагностических процедур |
Недостаток антиоксидантных витаминов и микроэлементов в фазе усиленного образования токсичных свободных радикалов серьезно усугубляет окислительный стресс у критически больных пациентов. Окислительное повреждение клеток и тканей и повышение производства провоспалительных цитокинов выступают как последствия. Наступающий драматический дисбаланс про- и антиоксидантов включается в патогенез множественной дисфункции органов (смотрите раздел 1.5: Окислительный стресс). Более того, дефицит витаминов и микроэлементов может снизить иммунные функции с повышенной вероятностью инфекционных осложнений у этих пациентов (Шенкин, 2000).
1.6.2.2. Развитие во времени дефицита антиоксидантов у критически больных пациентов
Многие исследования продемонстрировали низкие плазменные и внутриклеточные концентрации различных антиоксидантов у критически больных пациентов (таблица 7). Уровни антиоксидантов у больных в критических состояниях быстро падают после инсульта, травмы или операции и остаются ниже нормальных уровней в течение нескольких дней и даже недель. У пациентов с острым респираторным дистресс-синдромом (ARDS) плазменные уровни а-токоферола, Р-каротина, аскорбината натрия и селена были значительно ниже по сравнению с контрольной группой уже в день поступления. Нормальные уровни не достигались в течение 6 дней, несмотря на парентеральное введение антиоксидантных микроэлементов (средние дневные дозы: 9.1 мг витамина Е, 100-500 мг витамина С, 120 мкг селена). Эти уровни оставались значительно сниженными для Р-каротина, который не был включен в полное парентеральное питание (TPN). Плазменные уровни продуктов перекисного окисления липидов - маркера массивного окислительного стресса - в то же самое время значительно повышались (Метниц и др. 1999). Потенциал антиоксидантов плазмы крови у пациентов с тяжелым сепсисом был вначале пониженным (< 18 часов) и не смог вернуться к норме ранее 6 дней. Постоянно низкие уровни (до дня 12) а-токоферола и Р-каротина коррелировали с повышенной смертностью (Коули и др. 1996). Бертин и соавт. (2000) исследовали временное развитие окислительного стресса у ожоговых пациентов. Они обнаружили немедленное уменьшение плазменных уровней антиоксидантного витамина и микроэлементов, а также пониженную активность антиоксидантного энзима на 1-ый же день. В то же самое время отмечалось большое возрастание конечных продуктов перекисного окисления липидов. Этот окислительный стресс оказался устойчивым, он длился, по крайней мере, весь период наблюдения - 5 дней. Бергер и соавт. (1992А) выявили у ожоговых пациентов снижение уровней селена в серозной жидкости по сравнению с нормой течение 20 дней. Глутатион-пероксидаза была также снижена в течение 20 дней. Уровни селена оставались сниженными и у пациентов с SIRS в течение более чем двух недель у (Форсевиль и соавт., 1998). Концентрации селена и цинка также изменяются у пациентов с травмой. Выделение селена и цинка с мочой повышается, отмечается также большая потеря этих микроэлементов с экссудатом и через дренажи. Как уровни селена, так и цинка были пониженными после травмы при поступлении в интенсивную терапию и оставались таковыми до 7 дня (Бергер и соавт., 1996). Янг и соавт. (1998) наблюдали подобные понижения уровней плазменного цинка на 1-ый день после травмы, однако эти уровни возвращались к норме на 7-ой день.
1.6.2.3 Шкала дефицита антиоксидантов у критически больных пациентов
Уменьшение уровней антиоксидантов в плазме крови и активности ферментов, участвующих в метаболизме антиоксидантов, чрезвычайно велики и зависят от выраженности повреждения. У ожоговых пациентов хирургические операции иссечения и пересадки приводят к большим потерям селена через кожные покровы до 600 мкг в день (Бергер и др. 1992А). Кроме того, совокупные потери цинка за первые 7 дней составляют 212 мг, что означает 5-10% от нормального содержания в организме у ожоговых пациентов (Бергер и др. 1992В). У тяжело больных пациентов с SIRS (лекарственных, хирургических, травматических) наблюдалось раннее понижение на 40% плазменных концентраций селена, что критически значимо для поддержания нутритивного статуса (Форсевиль и др. 1998). Гуд и др. (1995) показали заметное снижение циркулирующих концентраций антиоксидантных витаминов у пациентов с септическим шоком и вторичной дисфункцией органа (рисунок 23). Плазменные концентрации Р-каротина не определялись у 8 из 16 пациентов.
Рис.23: Концентрации Р-каротина и витамина Е в плазме крови у пациентов с септическим шоком (Гуд и др. 1995)
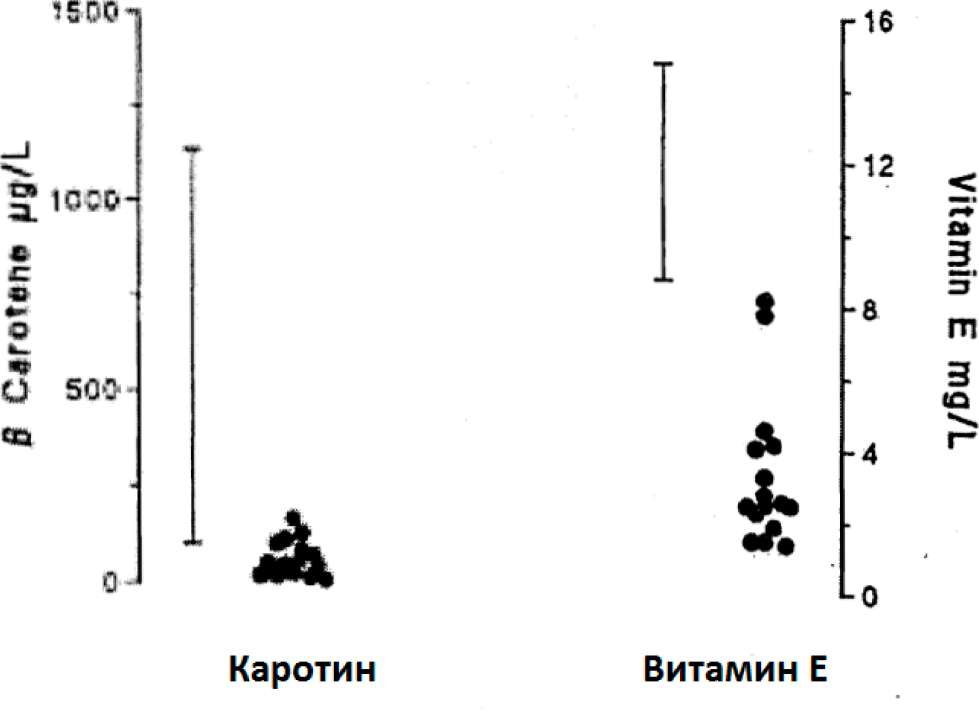
Вертикальная шкала показывает значения+2с.кв.откл. для здоровых контрольных субъектов
Величины для пациентов значительно ниже (р<0.001), чем величины для здоровых субъектов.
Имеется клиническое свидетельство того, что истощение антиоксидантов зависит от тяжести заболевания (Коули и др. 1996, Форсевиль и др. 1998).
Чем тяжелее состоояние пациента, тем больше истощение антиоксидантов!
У тяжело больных пациентов с SIRS и сепсисом была обнаружена значительная отрицательная корреляция между концентрацией плазменного селена и числом APACHE II (которое является индикатором тяжести заболевания) во время поступления. У пациентов с сепсисом средняя плазменная концентрация селена отрицательно коррелировала с тяжестью сепсиса (рис. 24) (Форсевиль и др. 1998). У пациентов с острой почечной недостаточностью и с MODS, плазменные уровни селена были ниже по сравнению с пациентами без дисфункции органов, и коррелировали с количеством органов, у которых проявлялась функциональная недостаточность (Макропулос и др. 1997).
В заключение, повреждение и воспаление вызывают значительные понижения содержания антиоксидантов в серозной жидкости и потенциала антиоксидантов противостоять окислительному стрессу у критически больных пациентов сразу после травмы или хирургической операции. Чем тяжелее состояние пациента, тем больше истощение антиоксидантов. Очень ранее обеспечение антиоксидантных микроэлементов (в течение первых 24 часов) может, таким образом, быть благоприятным для пациентов в критических состояниях (Бергер и Шенкин, 2000).
Рис.24: Плазменная концентрация селена у критически больных пациентов при поступлении относительно тяжести сепсиса (Форсевиль и др. 1998)
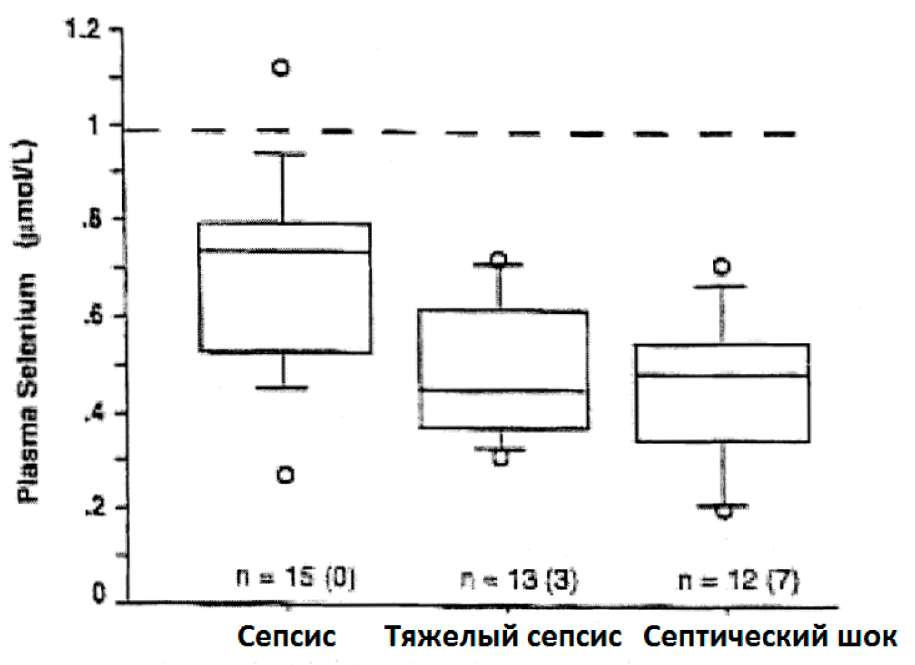
Величины показаны как медиана (средняя линия в прямоугольнике), верхняя сторона и нижняя сторона прямоугольника: 25-ый и 75-ый процентили р< 0.05 для сепсиса относ, тяжелого сепсиса и сепсиса относ, септического шока Покровные линии: 10-ый по 90-ый процентили; кружки: величины выше 90-го и ниже 10-го процентилей. Пунктирная линия: среднее + ср.кв.откл. нормальная плазменная концентрация селена (1.00+0.15мкмоль/л) п: число пациентов, в скобках: число не выживших пациентов
Табл. 8: Изменения ключевых антиоксидантных параметров в критических заболеваниях
|
Критическое состояние |
Антиоксидант |
Эффект |
Ссылки |
|
ARDS (острый респираторный дистресс-синдром) |
* витамин Е * р-каротин * витамин С * селен |
|
Cross et al. 1990, Richard etal. 1990, Nakae et al. 1995, Metnitz et al. 1999 |
|
Сепсис и септический шок |
* потенциал антиоксиданта * витамин Е * р-каротин * селен * глутатион * активность глутатион-пероксидазы |
|
Ogilvie et al. 1991, Goode et al. 1995, Cowley et al. 1996, Lyons et al. 2001 |
|
Трансплантация |
* витамин Е * В-каротин |
|
Goode et al, 1994 |
|
Ожоги |
* витамин Е * р-каротин *витамин С *селен * цинк |
|
Berger et al. 1992 A, Bergeretal. 1992 B, Gosling et al. 1995, Rock et al. 1997 |
|
SIRS (синдром системного воспалительного ответа у медицинских, хирургических и травматических пациентов) |
* витамин Е *Р-каротин *селен |
|
Hawker et al. 1990, Forceville et al. 1998, Curran et al. 2000 |
|
Травма |
* витамин Е *Р-каротин *селен * цинк |
|
Berger etal. 1996, Joung et al. 1998, Weiss et al. 1998 |
|
Острая почечная недостаточность |
* селен |
|
Makropoulos et al, 1997 |
|
Смешанная интенсивная терапия |
* витамин Е * витамин С |
|
Takeda et al. 1984 Schorah et al. 1996 Borrelli et al. 1996 Kharb et al. 1999 |
2.1. Раннее введение субстрата в кишечник (раннее энтеральное питание)
Критически больным пациентам необходимо раннее введение питательных субстратов для сохранения структуры и функции кишечника.
Дисфункция кишки и разрушение кишечного барьера играют, как предполагается, ключевую роль в развитии SIRS, сепсиса и MOF у критически больных пациентов (см. раздел 1.4). Именно поэтому необходимо приложить все усилия для того, чтобы предотвратить недостаточность кишечника и поддержать очень важные иммунные и барьерные функции желудочно-кишечного тракта у критически больных пациентов. Раннее энтеральное питание (EEN) является наиболее важным и эффективным инструментом для поддержания кишечных функций и снижения опасности инфекций, берущих начало в кишечнике. Для кишки справедливо правило «пользуйся ею или теряй её» (Драмл, 1999).
2.1.1. Почему энтеральное введение?
Слизистая оболочка кишечника не в состоянии полностью обеспечить себя питательными веществами, поступающими из крови. Питание приблизительно 50 % энтероцитов и 80% колоноцитов зависит от поступления питательных веществ из просвета кишечника. Отсутствие такого источника при голодании ведёт к атрофии и быстрому снижению размеров и функции кишечной слизистой (Экервал и Андерсон, 2001). Эти морфологические и функциональные изменения обратимы в условиях энтерального, но не парентерального питания. Благоприятный эффект энтерального питания основан на различных факторах (рис.25).
Рис.25: Энтеротрофические эффекты энтерального питания (Сухнер, 2002, не опубликовано)
Наиболее существенными преимуществами энтерального питания являются
а) подача питательных веществ и энергии к клеткам слизистой и
б) стимулирование эпителиального клеточного метаболизма прямым контактом с питательными веществами из просвета кишечника, т.е. обновление эпителиальных клеток (Драмл, 1999).
Другими эффектами энтерального питания, которые помогают поддерживать целостность барьерной функции кишечника, являются увеличение потока крови в слизистой и улучшение кишечной реперфузии, стимулирование потока желчи и панкреатической секреции, а также высвобождение энтеротрофических желудочно-кишечных гормонов, таких как гастрин и энтероглюкагон (Драмл, 1999).
Экспериментальные исследования на животных, показали что энтеральное питание поддерживает целостность слизистой и иммунологическую функцию желудочно-кишечного и респираторного тракта, уменьшает транслокацию бактерий, снижает системную воспалительную реакцию на токсическую нагрузку и повышает выживаемость в случае кровотечения и перитонитов (обзор Хейланд, 2000).
Большинство клинических исследований, сравнивающих полное энтеральное питание с полным парентеральным питанием в отношении инфекционных осложнений, продемонстрировали превосходство энтерального питания (обзоры Зингер, 1996, Хейланд, 2000, Сухнер и соавт., 2000). Рандомизированные исследования показали, что энтеральное питание обусловливает меньшую проницаемость слизистой, повышенное ранозаживление, улучшение результатов питания и меньшие госпитальные расходы. Ряд исследований показал снижение при энтеральном зондовом питании летальности в результате сепсиса у пациентов с брюшной травмой и панкреатитом (обзор Хейланд, 2000).
2.1.2 Почему, и как рано?
Существует гипотеза, что инициирование раннего энтерального питания (EEN) в первые часы после травмы будет благоприятно для поддержания барьерной функции кишечника и связанной с ней лимфатической системы (GALT), и явится первичной терапией для
больных в критических состояниях (Кудск, 1994). Целью такой терапии является поддержание кишечной иммунологической и барьерной функции, а раннее начало ЭП -наиболее важно (Кол, 1999, Любке, 2000, Сухнер и др. 2000). Однако, оптимальное время для начала такой метаболической терапии в настоящее время не определено
(Марик, Залога, 2001). Представляется, что «раннее энтеральное питание» начинается в пределах 24-72 часов после травмы или хирургического вмешательства. Немедленный посттравматический контакт кишки с питательными веществами, по-видимому, улучшает ситуацию в критических состояниях благодаря нескольким механизмам (Сухнер и соавт., 2000):
- EEN поддерживает или восстанавливает иммунную функцию и функцию кишечного барьера. Сохранение целостности кишки уменьшает транслокацию бактерий и, следовательно, уменьшает скорость распространения инфекции и полиорганной недостаточности (MOF).
- Немедленное ЭП уменьшает высвобождение стрессовых гормонов и посредников. Уменьшенная реакция на стресс понижает катаболизм.
- ЭП, включая «эффект первого прохождения» (кишка-печень-системная циркуляция), более физиологично, чем 1111, и, таким образом, оптимизирует использование субстрата, а также
- Улучшает желудочно-кишечную переносимость. Клиническими последствиями являются: лучшая кишечная способность к всасыванию, улучшенный гомеостаз субстрата и синтез висцеральных протеинов, меньшие осложнения и пониженный риск желудочно-кишечного кровотечения (см. рис. 26)
Рис.26: Потенциальные выгоды раннего энтерального питания (ЭП) у пациентов в критических состояниях (Сухнер, 2002, не опубликовано)

Накапливается все больший массив литературы, который показывает положительные эффекты раннего энтерального питания по сравнению с отсроченным. Залога (1999) сделал обзор 19 проспективных, контролируемых исследований раннего ЭП по сравнению с отсроченным ЭП у тяжелобольных или травмированных пациентов (18 исследований были также рандомизированы). В большинстве этих исследований группа раннего питания получала энтеральное питание в течение 24 часов с момента поступления в госпиталь, в то время как в группе с отсроченным ЭП нутритивная поддержкаие была дана спустя 3-5 дней. Явное большинство (16 из 19) исследований поддерживает мнение, что раннее ЭП улучшает клинические результаты.
Таким образом, клинический подход к лечению больных в критических состояниях с использованием раннего ЭП на основе имеющихся исследований, является рекомендацией Уровня I.
В проведенном мета-анализе (Марик, Залога, 2001) исследовался эффект раннего ЭП у больных в критических состояниях и пациентов с травмами. Проанализировано 15 рандомизированных, контролируемых исследований, в которых сравнивали раннее энтеральное питание (< 36 часов) с отсроченным (> 36 часов) у госпитализированных пожилых пациентов - послеоперационных, травмированных, с повреждениями головы, ожоговых пациентов, а также пациентов блоков интенсивной терапии. В целом в группе раннего ЭП была значительно меньшая доля инфекционных осложнений (19% против 41%) и более короткое время пребывания в госпитале (среднее снижение на 2,2 дня), а также наблюдалась тенденция к сниженным неинфекционным осложнениям (33% против 38%) и снижение смертности (8% против 11,5%).
Может ли эта ситуация быть улучшена дальше?
У послеоперационных или посттравматических пациентов первые часы после травмы представляют собой критический период для кишечника: даже короткие периоды кишечного голодания ведут к понижению функций слизистой и нарушению целостности кишечного барьера. Реакция острой фазы следует немедленно, пик эндотоксина в серозной жидкости имеет место в течение первых 12 часов, микробиологический перенос - сразу же после этого (Бенгмарк и соавт., 2001). Поэтому периоды энтерального голодания должны быть возможно короче, особенно при метаболическом стрессе и связанном с этим поражением слизистой (Сухнер и соавт., 2000). Можно предположить, что чем раньше начато ЭП, тем более ослаблена стрессовая реакция организма. Экспериментальные исследования ясно показывают, что только очень ранняя инициация энтерального питания после травмы способна поддерживать функцию барьера кишки и уменьшить посттравматическую гиперметаболическую стрессовую реакцию (Мочизуки и соавт., 1984, Джианотти и соавт., 1994). Клинические исследования критически больных пациентов поддерживают гипотезу, что очень раннее энтеральное питание, которое начинается в пределах 4-12 часов после травмы, значительно улучшает клинические результаты лечения пациентов. Чиарелли и соавт. (1990) были первыми, кто подтвердил экспериментальные результаты клиническими исследованиями ожоговых пациентов (п=20). Раннее ЭП начиналось через 4-5 часов после поступления в ОРИТ, в контрольной группе - спустя 55-60 часов. Пациенты с ранним зондовым ЭП имели меньшую долю положительных реакций проб крови (5 у 3 пациентов против 33 у 7 контрольных пациентов). Не было указано, коррелируют ли положительные реакции проб крови с уровнем кишечной проницаемости. Немедленная нутритивная поддержка предотвращает вызванный ожогами рост катехоламиновой и глюкагонной секреции, улучшает контроль гиперкатаболического состояния и улучшает клинические результаты. Компан и соавт. (1999) сравнили эффекты раннего ЭП, начатого в пределах 6,5 -12,1 часов после травмы у пациентов с множественными повреждениями (политравма), поступившими в состоянии шока, с эффектами ЭП, начатого между 33,9 и 53,6 часами после травмы (п=28). У пациенты с ранним ЭП отмечалась м еныпая проницаемость кишечной стенки и меньший процент полиорганной недостаточности (MOF). Чем позже начиналось ЭП, тем большее количество MOF отмечалось у пациентов (рисунок 27). ЭП, начатое сразу после политравмы, способно восстановить кишечную слизистую и, следовательно, снизить транслокацию бактерий, поступление эндотоксинов и тяжесть MOF. Частота MOF была связана с временем начала ЭП, но не с объемом получаемой пищи. В то же время, частота MOF не влияла ни на длительность пребывания в палате интенсивной терапии, ни на время механической вентиляции легких.
Рис.27: Соотношение между временем начала ЭП после множественного повреждения и MOF (Компан и соавт., 1999).
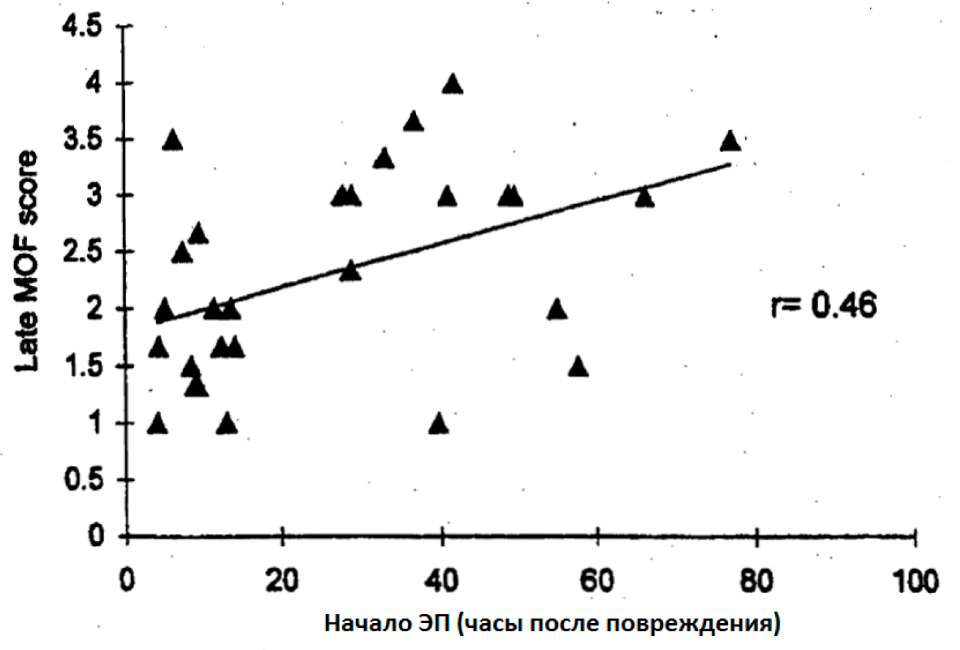
Пенг и соавт. (2001) изучали влияние очень раннего ЭП на предотвращение энтерогенных инфекций у тяжело обожжённых пациентов (п=22). Одна группа получала нутритивную поддержку энтерально или орально как можно раньше после поступления в госпиталь, другая группа получала оральную жидкую диету спустя 48 после ожога. Авторы наблюдали возросшую кишечную проницаемость в раннем периоде после ожога, которая была выше у пациентов с отсроченным питанием. Повышенная проницаемость пораженной ожогами слизистой оболочки кишечника приводила к переносу эндотоксинов из кишечного просвета в кровь. Уровни сывороточного эндотоксина значительно возрастали во время ранних стадий - с самыми высокими уровнями в 7-12 часов и 3 дня после ожога. Пациенты с ранним ЭП имели заметно более низкие уровни эндотоксина, чем пациенты с отсроченным питанием. Эти результаты предполагают, что раннее ЭП может помочь сохранить барьер кишечной слизистой, тем самым - понизить кишечную проницаемость и уменьшить кишечный перенос эндотоксинов. В результате опасная цепная реакция «эндотоксин - медиаторы воспаления - повреждение слизистой кишки» может быть прервана прежде, чем случится осложнение критического состояния. Можно сделать вывод, что энтеральное питание должно начинаться в течение первых часов во время метаболического стресса после травмы, как только макрогемодинамическая ситуация стабилизируется, до разрушения барьера кишечника и возникновения иммунной дисфункции у критически больных пациентов.
2.1.3 Возможно ли очень раннее энтеральное питание и безопасно ли оно у критически больных пациентов?
Сегодня общепринято, что энтеральное питание должно предпочитаться полному парентеральному питанию (111111, TPN) тогда, когда это возможно, по причинам, изложенным выше. Более того, требуется раннее начало ЭП. Однако у многих критически больных с травмами, а также у послеоперационных пациентов развиваются желудочно-кишечные дисфункции (ишемия, нарушения подвижности, илеус и др. - см.отрите раздел 1.4: Желудочно-кишечный тракт), которые ограничивают переносимость энтерального питания. Имеется также опасение, что раннее энтеральное питание приведёт к удалению жидкости, бактериальной колонизации и ухудшению клинических результатов лечения
(Марик, Залога, 2001). В результате, в начальных послеоперационной и посттравматической стадиях энтеральное питание часто не даётся в течение первых дней, до нормализации желудочно-кишечных функций (Коул, 1999). Однако теперь признано, что функция тонкого кишечника и способность всасывать питательные вещества остаются нетронутыми - несмотря на критическое состояние, наличие пареза и отсутствие клинических признаков движения кишечника. У пациентов, не способных переносить желудочное питание, может быть осуществлен кишечный доступ (Марик, Залога, 2001). Но имеются и другие проблемы в палате интенсивной терапии: пациенты часто поступают в очень тяжелом состоянии. Поддерживающие жизнь мероприятия, такие как гемодинамическая стабилизация, управление дыханием и волемическая терапия, имеют приоритет над питанием (Коул, 1999). Неправильная установка зонда или его несостоятельность ещё более препятствуют началу и переносимости раннего ЭП (МакКлаве и соавт., 1999, Вастиан и соавт., 1996). Отсюда Сухнер и соавт. (2000) делают вывод, что на практике инициация раннего энтерального питания у критически больных пациентов затруднена из-за часто не очень понимаемой необходимости. В то же время, уже имеются некоторые клинические данные, которые позволяют предположить, что очень раннее ЭП переносится хорошо и является безопасным даже у наиболее серьезно больных пациентов.
Брага и соавт. (2002) оценили безопасность и переносимость раннего ЭП после больших операций в абдоминальной онкохирургии у 650 пациентов. Раннее ЭП (РЭП) было начато в пределах 12 часов с помощью питания через зонд в тонком кишечнике или с помощью еюностомии. Побочные эффекты РЭП в отношении ЖКТ наблюдались у 30% пациентов. Брюшные спазмы и вздутие живота были наиболее частыми симптомами, в то время как понос и рвота имели меньшую частоту. Большинство из этих побочных эффектов были успешно устранены уменьшением или временным прерыванием питания, или с помощью лекарств. Только 59 (8.9%) пациентов должны были быть переключены на 1111 из-за устойчивой непереносимости ЭП. Связанная с РЭП смертность составляла 0.1% (1/650). Авторы заключают, что «использование кишки вскоре после операции безопасно и хорошо переносится» и оно должно быть «первым выбором для нутритивной поддержки у этого типа пациентов».
МакДональд и соавт. (1991) оценили безопасность и эффективность немедленного энтерального зондового питания (начало в пределах 6 часов) у пациентов с ожогами, составлявшими более 20% поверхности тела. Возникновение осложнений, связанных с энтеральным питанием, было редким; аспирационная пневмония не возникала. Наблюдались побочные эффекты: рвота, легкий понос и 3 эпизода наличия крови в отделяемом зонда при взятии проб. Тот факт, что ни у кого из пациентов не развился понос, достаточно серьезный для того, чтобы остановить или изменить энтеральное питание, предполагает, что немедленное начало питания может улучшить всасывание питательных веществ, ограничить или предотвратить атрофию слизистой и, тем самым, улучшить способность переносить энтерально вводимые субстраты. Пациенты, которые не переносили зондовое кормление, имели более высокий процент смертности, чем те пациенты, которые хорошо переносили зондовое питание.
Исследование Чиарелли и соавт. (1990) показало, что внутрижелудочное кормление несколько часов спустя после термического повреждения является безопасной и хорошо-переносимой техникой для питания обожженных пациентов. Кишечные осложнения наблюдались только у 2 из 10 пациентов, которых кормили спустя 4-5 часов (токсичный илеус и желудочные микроизъязвления). У двоих из 10 пациентов в контрольной группе -в которой кормление было введено спустя 55-60 часов - развились осложнения (рвота и псевдомембранный колит). Компан и соавт. (1999) показали, что РЭП было практично и полезно для тяжело больных пациентов. Желудочно-кишечная переносимость была лучше у группы с ранней нутритивной поддержкой. Авторы предположили, что проблемы переносимости у пациентов с тяжелыми повреждениями можно избежать
немедленной организацией энтерального питания - даже при небольшом объеме диеты. Эти клинические результаты обнадеживают и позволяют следовать концепции очень раннего ЭП у критически больных пациентов. Целью будет начало РЭП в пределах 6 часов после травмы или хирургии, как только макрогемодинамическая ситуация стабилизируется (Сухнер и соавт., 2000).
2.1.4. Сколько и какого энтерального питания должны получать пациенты?
Полное ЭП кажется невозможным при тяжелом стрессовом метаболизме вследствие плохого усвоения из-за структурных и функциональных нарушений, сопровождающих повреждения слизистой. Практичность и эффективность РЭП зависит от ранее существовавшего уровня травмы слизистой (ишемическое повреждение слизистой и атрофия слизистой), а также от существующей в данное время степени кишечной гиперперфузии. Поглощение и использование питательных веществ снижаются, однако пищеварительная способность может адаптироваться если питательные вещества подаются в просвет кишечника (Сухнер и соавт., 2000). Как было продемонстрировано Компаном и соавт. (1999), момент времени, а не начальные количества даваемых энтерально субстратов, критичен с точки зрения клинических результатов. Энтеральное питание оказывает своё благоприятное воздействие только в том случае, если оно даётся в объеме, который покрывает нутритивные потребности организма. У пациентов, которые должны кормиться парентерально, например, при тяжелом заболевании, дополнительная подача даже небольших количеств питательных веществ в просвет кишечника может помочь поддержать барьерную функцию кишки. Представляется достаточным обеспечить от 10% до 25% общей потребности за счет ЭП для поддержания целостности слизистой и уменьшения кишечной проницаемости (Сакс и соавт., 1996, Залога и соавт.,
1999) . Из литературных данных известны рекомендации начать «минимальное» РЭП с 510 мл элементной диеты в час. Питание должно быть свободно от волокон с калорической плотностью < 1 ккал/мл. Кроме того, потребности в энергии, протеине и других существенных питательных веществах могут быть удовлетворены парентерально (Сухнер и соавт., 2000). Ввиду того, что цель питательной поддержки должна фокусироваться на сохранении функции органа во время тяжелого стрессового метаболизма (Сухнер и соавт.,
2000) , можно предположить, что специальное энтеральное питание для кишки, которое содержит предпочтительные субстраты для слизистой кишечника - глутамин и бутират , а также высокие количества антиоксидантов для компенсации окислительного стресса -будет намного более полезно для пациента, чем обычные элементные диеты. Внимательный контроль состояния пациента очень важен, потому что и минимальное ЭП является проникающей терапевтической процедурой с потенциальной опасностью желудочной колонизации, аспирации, непроходимости, а также осложнений, связанных с зондовым кормлением. Его клиническое использование может быть ещё осложнено и нарушениями моторной и секреторной функции, а также поносом. Чтобы преодолеть большинство из этих проблем, рекомендуется применение зондового питания через тощую кишку (Сухнер и соавт., 2000).
2.2 Недостатки современного иммуно-пипшния
В течение 10 лет на рынке присутствовали специальные формулы энтерального иммуно-питания. Клинические испытания позволили предположить несколько преимуществ иммуноповышающих диет, включая снижение:
- инфекционных осложнений,
- длительности пребывания на ИВЛ,
- продолжительности интенсивной терапии и времени пребывания в госпитале.
Три мета-анализа подтвердили эти результаты (Биал и соавт., 1999, Хейс и соавт., 1999, Хейланд и соавт., 2001). Однако улучшения клинического результата при иммуно-питании наблюдались главным образом среди хирургических пациентов, что не может быть легко экстраполировано на другие группы пациентов (Нельсон, 1998, Сухнер и соавт., 2002). Имеются предположения, следующие из клинических исследований, что самые тяжелые пациенты, в особенности пациенты с тяжелым сепсисом, септическим шоком и органной недостаточностью, могут не получить пользы от повышающих иммунитет диет, существующих на рынке. Справедливым может быть прямо противоположное: что эти диеты наносят вред этим пациентам (Бауер и соавт., 1995, Саффле и соавт., 1997). В исследовании Галбана и соавт. (2000) только пациенты с самыми низкими показателями по шкале APACHE II (которые являются индикатором тяжести заболевания) имели значительно меньшую смертность после такой нутритивной поддержки. Для более тяжело больных пациентов не было значительного выигрыша от такого питания по показателям летальности. Более впечатляющий мета-анализ Хейланда и соавт. (2001) показал не полезные, а скорее вредные влияния иммунопитания на смертность у критически больных пациентов. Если оценивались только исследования с высококачественными показателями, то смертность была значительно выше среди критически больных пациентов, которых кормили по иммунопитательной формуле (относительный риск 1.46, 95% доверительный интервал 1.01-2.11).
Из этих данных со всей очевидностью следует, что имеющиеся формулы иммунопитания не могут снизить смертность среди большинства критически больных пациентов с тяжелым SIRS, септическим шоком и полиорганной недостаточностью.
Почему иммуно-питание может быть не только не полезным, но даже вредным у большинства тяжело больных пациентов?
Следующие недостатки имеющихся в настоящее время формул иммунопитания могут дать объяснение этим фактам:
1. Неадекватное поступление ключевых питательных веществ для кишечника и иммунной системы из-за
- ограниченного объема переносимого энтерального питания, а также
- недостаточного обеспечения состава ЭП
а) глутамином для тяжело больных пациентов при высоких потребностях
б) антиоксидантами для компенсации тяжелого окислительного стресса.
2. Отсутствие короткоцепочечных жирных кислот
3. Поступление высокомолекулярных питательных веществ в то время, когда пищеварение и всасывание нарушены.
4. Наличие в составе ЭП аргинина с условно провоспалительными эффектами
2.2.1. Ограниченная переносимость объема энтерального питания у больных в критических состояниях
Когда задачей является поддержание кишечных иммунологических и барьерных функций при тяжелых заболеваниях, раннее начало энтерального питания чрезвычайно важно (смотрите раздел 2.1 «Раннее поступление питания в просвет кишечника»). На практике, однако, непереносимость назначаемых формул часто препятствует началу РЭП, даже когда энтеральное питание вводится постепенно в соответствии с рекомендациями. Имеющиеся в настоящее время формулы иммунопитания обеспечивают эффективные дозы ключевых питательных веществ в суточных объемах 1500-2000 мл. Обычная схема
дозировки рекомендует начинать с 20-25 мл(ккал)/час, что соответствует примерно 500 мл в первый послеоперационный / посттравматический день. Объем кормления должен быть ступенчато повышен до примерно 750 мл на 2-ой день, 1000 мл на 3-й день и далее до полной суточной дозы 1500 мл на 4-ый и 5-ый дни.
Если пациенты адекватно переносили эти количества энтеральной пищи в течение первых послеоперационных/посттравматических дней, наблюдались положительные клинические результаты (Сенкал и соавт., 1997, Брага и соавт., 1998). Однако, имеется много критически больных пациентов, которые не переносят суточной дозы в 1500 мл энтеральной пищи на 4-ый и 5-ый послеоперационные дни. В особенности, наиболее тяжело больные пациенты часто страдают от непереносимости энтерального кормления. Некоторые из этих пациентов переносят только очень небольшие количества энтеральной пищи, другие не переносят энтеральное кормление совсем. Причинами являются многочисленные желудочно-кишечные проблемы, такие как повреждение слизистой после ишемии и реперфузии, излишний рост бактерий, проблемы с подвижностью и пониженные панкреатические функции (смотрите раздел 1.4 «Желудочно-кишечный тракт»). Переносимость энтерального питания является, вероятно, наиболее обычным используемым индикатором в клинических установках для контроля функции кишки у критически больных пациентов (Ромбо, Такала, 1997). Клиническими признаками энтеральной непереносимости являются желудочный рефлюкс, аспирация, задержанная перистальтика тонкого кишечника, растяжение брюшной полости, понос и рвота (рисунок 28).
Рис.28: Причины и следствия ограниченной переносимости энтерального объема у критически больных
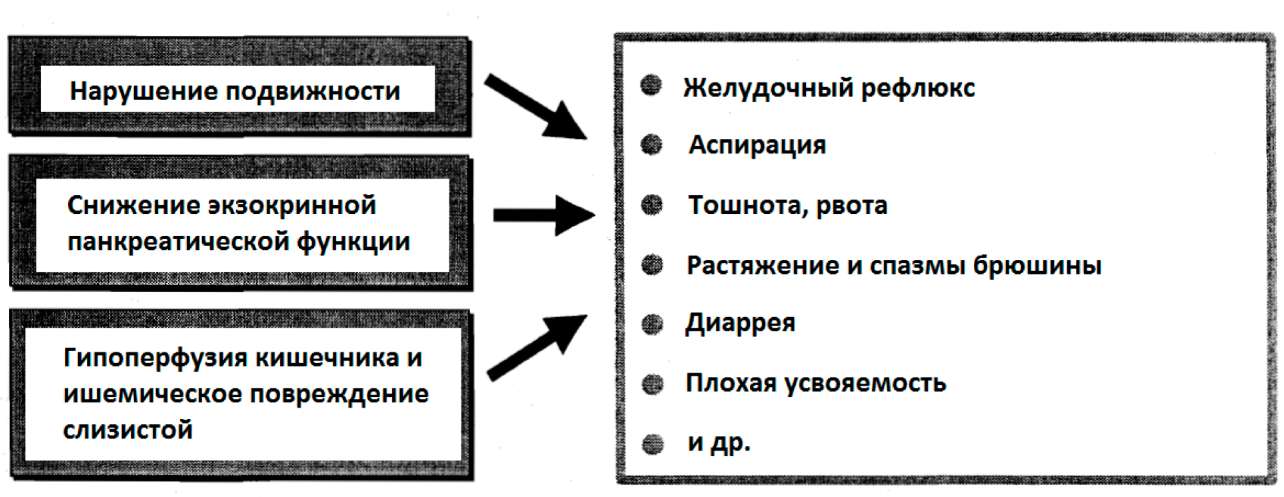
Таблица 9 отражает клиническую реальность с энтеральным питанием у пациентов интенсивной терапии. У большинства пациентов не достигается поставленная цель -адекватное питание энтеральным путем. Переносимыми являлись только 50-75 % суточных доз. Побочные эффекты со стороны ЖКТ являются обычным делом и ещё более затрудняют успешное энтеральное питание.
Таблица 9: Осуществимость энтерального питания у пациентов интенсивной терапии
|
Автор (год) |
Осуществимость энтерального питания |
Переносимые энтеральные количества* |
|
Хейланд и др. (1995) |
-74% пациентов подходящих для получения ЭП начали кормление - кормление было начато на 3- 4 день после поступлений (но иногда и очень поздно, после 18 дней пребывания в интенсивной терапии!) |
35% пациентов переносили 90% назначенного |
|
Адам и Батсон (1997) |
Брюшные осложнения: в 20% всех дней кормления |
Все пациенты: 76% от заданного; пациенты с ЖКТ осложнениями: 52% от заданного |
|
МакКлейв и др. (1999) |
|
52% заданного (интервал: 15-87%) |
|
Монтейо и др. (1999) |
- Желудочно-кишечные осложнения: у 63% пациентов + высокий уровень остатка в желудке (39%) + запор (26%) + понос (15%) + растяжение брюшины (13%) + рвота (12%) - прекращение ЭП у 15% пациентов |
пациенты с ЖКТ осложнениями: 63% от заданного |
* выражено в процентах от предписанной дозы
Ограничение переносимости питания, вводимого энтерально больным в критических состояниях, может быть только частично преодолено еюнальным кормлением, элементными смесями, начальными низкими уровнями поступления, а также лекарственными препаратами (Сухнер и соавт., 2000). Фактически, практичность и эффективность РЭП зависят от существовавшей степени травмы слизистой и текущей степени кишечной гипоперфузии (Сухнер и соавт., 2000). У пациентов с острым SIRS или опасностью его, с септическим шоком и множественными дисфункциями органов особенно вероятна очень ограниченная переносимость ЭП, что подтверждается клиническими данными (см. ниже).
Кроме того, имеются несколько практических причин в госпитале и, в особенности, в палатах интенсивной терапии, которые ведут к задержанному началу и/или частым прерываниям раннего энтерального питания у критически больных пациентов.
• Терапии, поддерживающие жизнь, такие как гемодинамическая стабилизация, управление дыханием и трансфузионная терапия, которые имеют приоритет перед питанием (Коул, 1999).
• Дисфункция зонда или неправильное его размещение ещё более затрудняют начало и переносимость РЭП (МакКлэйв и соавт., 1999, Бастиан и соаавт., 1996).
Отсутствие стандартизованного обучения сотрудников клиники в отношении питания может быть причиной неправильного назначения, позднего начала и частого прерывания энтерального питания у критически больных пациентов (Гарвин, Браун, 2000). Клинические исследования, упомянутые в таблице, показывают, что многие тяжело больные пациенты неспособны вынести более чем 300 - 800 мл энтерального питания в первые дни после травмы или операции - независимо от положения трубки в желудке или тонком кишечнике.
Таблица 10: Ограниченный переносимый энтеральный объём у «наиболее тяжело больных» пациентов интенсивной терапии

В заключение, непереносимость энтерального питания -это обычное явление у тяжело больных пациентов. Мы ясно видим ситуацию, когда подача питательного субстрата в просвет кишечника желательна по причинам, изложенным в разделе 2.1 «Ранняя подача питательного субстрата в просвет кишечника». Однако объём энтерального питания должен быть очень ограниченным, чтобы не ухудшить общую клиническую ситуацию. Таким образом, очень часто эффективные дозы существующих формул иммунопитания, предназначенные в расчете на переносимость ЭП в объеме 1500-2000 мл в день, не могут быть применены. Одновременно, дозы ключевых питательных веществ, даваемых в малых объёмах этих формул, далеки от доз, считающихся эффективными в отношении положительных клинических результатов. Следовательно, мы должны понимать возможные клинические последствия ограниченной переносимости объёма ЭП, особенно в плане иммунопитания, а также необходимость ограничения объемов ЭП и влияние всех этих факторов на исход лечения пациентов.
Установлена взаимосвязь между переносимостью энтерального объёма и клиническим исходом у критически больных пациентов (Ромбо, Такала, 1997). Пациенты с желудочно-кишечными осложнениями в исследовании Монтейо и соавт. (1999), которые получали меньшие объёмы питания, оставались примерно на 5 дней дольше в госпитале и имели значительно более высокую смертность (31% против 16%), чем пациенты без осложнений.
Таким образом, ограниченная переносимость энтерального объёма может быть прогностическим индикатором тяжести заболевания и клинического исхода. Более того, ограниченная переносимость энтерального объёма означает ограниченный прием ключевых питательных веществ для кишечника и иммунной системы, что уменьшает эффективность иммунноповышающей диеты. Ввиду этого, ограниченная переносимость энтерального объёма может непосредственно влиять на клинический исход у критически больных пациентов.
Аткинсон и др. (1998) установили что имуннообогащенные диеты могут только тогда улучшить исход критически больных пациентов, когда эти больные получают только строго определенное количество энтеральной формулы - которое составляло > 2500 мл Импакта, в течение 72 часов после поступления в интенсивную терапию. У пациентов, которым было успешно проведено ЭП, наблюдалось значительное снижение продолжительности ИВЛ и длительности пребывания в госпитале. Вейманн и соавт. (1998) не смогли продемонстрировать клиническую пользу Импакта у пациентов с SIRS и MOF после тяжелой травмы. Авторы заявили, что полученный средний энтеральный объём в 561 мл/день «может считаться слишком малым для развития клинических эффектов». Представляется обоснованным, что специальная повышающая иммунитет формула, которая обогащена ключевыми питательными веществами для кишечника и иммунной системы, - из-за более высоких потребностей в критических состояниях - не может быть эффективной, если пациент получает только 30-60% дневной дозы этих ключевых питательных веществ.
Таким образом, ограниченная переносимость энтерального объёма препятствует эффективному поступлению ключевых субстратов, которые очень нужны в критических состояниях.
2.2.2. Неадекватное снабжение глутамином тяжело больных пациентов
Часто высокие потребности в глутамине у критически больных пациентов (смотрите раздел 3.3.1 Глутамин-Дипептиды) не могут быть удовлетворены за счет имеющихся формул энтерального иммунопитания - даже тогда, когда пациенты переносят полную рекомендованную дозу в 1.5-2 л/сутки.
Недавние рекомендации для восполнения дефицита глутамина у критически и наиболее тяжело больных пациентов указывают на дозировку 30 г в день (Вилмор, Шаберт, 1998). Имеющиеся готовые к использованию формулы энтерального иммунопитания содержат, однако, только дозу в 15-22 г глутамина в день (1500-2000 мл). Кроме того, их применение вызывает серьезную обеспокоенность в ситуации критических состояний по следующим причинам:
1. Гигиенический риск. Существует повышенный риск микробиологической контаминации, если ЭП должно быть приготовлено ex tempore по сравнению со стерилизованными, готовыми к употреблению формулами.
2. Плохая растворимость. Наша собственная лаборатория показала, что порошок не растворяется полностью в рекомендованных 60 мл воды. Большая часть порошка оседает на дне вскоре после перемешивания. Пациенты могут не получить то, что запланировано.
3. Высокая кислотность приготовленной смеси.
Приготовленная смесь имеет рН 3.2, что намного меньше, чем рН готового к использованию энтерального питания (нормально примерно 7). Меньшее рН означает повышенную кислотность пищи, что может вызвать коагуляцию остатков пищи в зонде, если он не был тщательно промыт до и после приема глутамина. Частые замены зондов с остатками смеси затрудняют работу медперсонала.
2.2.3 Недостаточное поступление антиоксидантов
Больные в критических состояниях часто страдают от тяжелого окислительного стресса (см. раздел 1.5. «Окислительный стресс») и быстрого истощения эндогенных антиоксидантов (см. раздел 1.6.2.» Истощение антиоксидантов»). Вот почему эти пациенты имеют высокие потребности в поступлении экзогенных антиоксидантов, которые явно превышают нормальные потребности здоровых людей (см. раздел 3.3.2 «Антиоксидантные витамины и микроэлементы»). Имеющиеся формулы иммунопитания, однако, содержат такие количества антиоксидантных витаминов и микроэлементов в пределах суточной дозы в объеме смесей 1.5-2 л, которые лишь незначительно выше обычно рекомендуемых суточных доз для здоровых людей. Как уже отмечалось, наиболее интенсивное образование свободных кислородных радикалов происходит как раз в кишечной слизистой после ишемии и реперфузии. Вот почему поступление антиоксидантов именно в просвет кишечника является очень важным для поддержания и сохранения желудочно-кишечного барьера у больных в критических состояниях (см. раздел 3.3.2 «Антиоксидантные витамины и микроэлементы»).
2.2.4.Недостаточность коуоткоцепочечных жирных кислот(SCFA)
SCFA бутират является ключевым субстратом для кишечного питания, поддержания целостности слизистой и восстановления. Механизмы, с помощью которых SCFA могут участвовать в кишечной пролиферации и функции, включают стимуляцию локального кровотока, внешнесекреторной функции поджелудочной железы, стимуляцию автономной нервной системы, а также образование энтеротрофических гормонов (см. раздел 3.3.3 «Бутират /Трибутирин»). Поступление диетических волокон, которое является главным субстратом для образования бутирата в кишечнике, может быть связано с некоторыми нежелательными эффектами у критически больных пациентов, такими как растяжение брюшины и чрезмерный бактериальный рост. Поэтому пищевые волокна противопоказаны больным в критических состояниях (см. раздел 3.3.3 «Бутират / Трибутирин»). Альтернативой энтеральному поступлению волокон может быть дополнение SCFA. Несколько экспериментальных и клинических исследований показали благоприятный эффект орального/энтерального и парентерального введения SCFA. В
частности, SCFA усиливают пролиферацию слизистой кишечника, уменьшают атрофию тонкого кишечника в процессе полного парентерального питания (TPN) и повышают адаптацию кишечника после абдоминальной хирургии (см. раздел 3.3.3 «Бутират / Трибутирин»). Мы предполагаем, что SCFA существенны для поддержания барьерной функции кишечника при критических состояниях из-за их важности как основного источника энергии для кишечной слизистой. Имеющиеся формулы иммунопитания не содержат SCFA. Некоторые продукты (Импакт с волокнами (Impact witn Fibre), Stressor! Multifibre (мульти-волокна)) включают пищевые волокна, но в силу приведенных выше соображений эти диеты не могут быть рекомендованы тяжело больным пациентам.
2.2.5. Поступление высокомолекулярных питательных веществ при нарушенном пищеварении и всасывании
Имеющиеся формулы иммунопитания предназначены для полного энтерального питания. Они содержат высокомолекулярные питательные вещества типа протеина и жирных кислот с длинными цепями (п-6 жирные кислоты типа линолевой кислоты и п-3 жирные кислоты рыбьего жира), которые нужны для функционального пищеварения и всасывания в желудочно-кишечном тракте. Однако имеется данные, что у критических больных пищеварительные функции нарушены и способность к всасыванию уменьшена. Причинами этого могут быть упомянутая перфузия слизистой, последующее повреждение слизистой, чрезмерный рост бактерий, нарушения перистальтики и связанные с приемом лекарств расстройства. Более того, внешнесекреторная панкреатическая функция нарушена во время септического шока (см. раздел 1.4.5 «Нарушение всасывания»). Энтеральное поступление источников энергии и других высокомолекулярных питательных веществ, таких как п-3 жирные кислоты рыбьего жира, в ситуации жестко нарушенной пищеварительной и всасывательной способности, могут вызвать непереносимость и могут ухудшить общее клиническое состояние пациента.
2.2.6. Прием аргинина с условно правое п ал и тел иными эффектами
Сухнер и соавт. (2002) выдвинули гипотезу, что особые иммуноповышающие питательные вещества, в особенности аргинин, могут оказывать нежелательное действие, интенсифицируя процесс воспаления и, следовательно, ухудшить клинический исход у больных в критических состояниях. Добавление аргинина - подобно другим ключевым питательным веществам для иммунопитания - основано на том наблюдении, что у больных в критических состояниях развивается дефицит таких веществ из-за их экстенсивного потребления. Однако возможно, что уровень аргинина в критических условиях должен быть ниже нормального для того, чтобы избежать вредных эффектов при некоторых обстоятельствах. Таким образом, не всякий дефицит иммунокомпонентов должен быть восполнен, потому что адекватные уровни должны быть определены в соответствии с лежащей в основе патофизиологией (Сухнер и соавт., 2002). Более того, изменение метаболизма аргинина было недостаточно исследовано по сравнению с другими компонентами иммунопитания, такими как глутамин (Сухнер и соавт., 2002).
В заключение можно сказать, что имеющиеся в настоящее время формулы ЭП для повышения иммунитета являются «продуктами первого поколения», которые во многом не подходят для пациентов с тяжелыми проявлениями SIRS или сепсиса, как уже было отмечено в «Согласительных рекомендациях Высшего совещания США по Энтеральной терапии повышения иммунитета» в 2001 году.
3.1 Показания
Интестамин показан для очень ранней энтеральной подачи субстрата у пациентов с ограниченной переносимостью объемов ЭП и с потребностью в большом количестве глутамина и антиоксидантов, например,
^ у послеоперационных, посттравматических пациентов с высокой опасностью серьезного SIRS и сепсиса, включая следующие состояния
• недостаточное питание,
• радикальная хирургия,
• тяжелые ожоги,
• тяжелое повреждение головы,
• тяжелая тупая или проникающая травма,
• острый панкреатит.
^ у критически больных пациентов с проявлениями тяжелого SIRS или сепсиса.
Интестамин должен применяться как энтеральное дополнение в комбинации с парентеральным и/или энтеральным питанием.
(Подробности о предполагаемых режимах питания можно найти в разделе 3.5). 3.2. Оптимальный объём для эффективности субстрата
ИНТЕСТАМИН является первой готовой к использованию энтеральной добавкой, которая содержит 100% ключевых питательных веществ в малом объёме 500 мл, что соответствует тому количеству, которое может вынести кишечник у тяжело больных пациентов.
Как следует из предыдущих разделов данного Научно-информационного бюллетеня, что очень ранняя энтеральная подача субстрата чрезвычайно важна у критически больных пациентов для того, чтобы:
- сохранить целостность кишечника,
- уменьшить стрессовую реакцию,
улучшить использование питательных субстратов, а также избежать непереносимости ЭП прежде, чем она разовьётся
(см. раздел 2.1 «Раннее поступление питательных веществ в просвет кишечника»
Клинические исследования у больных в критических состояниях поддерживают гипотезу, что очень раннее энтеральное питание, которое начинается в течение 4-12 часов после травмы, значительно улучшает клинический исход. В то же время, имеются ограничения в отношении переносимого больными объема раннего ЭП (РЭП), особенно у большинства тяжело больных пациентов. Нежелательные побочные эффекты, такие как высокий уровень пищевого остатка в желудке, застой пищи, растяжение брюшины, рвота и другие расстройства случаются у почти 60% энтерально питаемых пациентов в ОРИТ (см. раздел 2.2. «Недостатки современного иммунопитания»). Эта непереносимость является одной из главных причин зачастую позднего начала и/или перерывов раннего энтерального питания у этих пациентов. Следовательно, возникает вопрос: Каков оптимальный суточный объём энтеральной формулы для очень ранней подачи энтерального субстрата, который может быть переносим большинством тяжело больных пациентов?
3.2.1. Оптимальное количество очень рано подаваемого энтерального субстрата
Количество адекватно переносимого ЭП зависит от выраженности поражения и от текущей степени гипоперфузии в слизистой оболочке кишечника. Не существует клинических параметров для оценки травмы слизистой или измерения текущей гиперперфузии - которые, следовательно, являются непредсказуемыми условиями (Ромбо, Такала, 1997; Сухнер и соавт., 2000А). Чтобы найти оптимальный объём для Интестамина, были проанализированы имеющиеся клинические данные о переносимом объёме энтерального питания у критически больных пациентов. Клинические исследования показали, что в течение первых дней после хирургии или травмы наиболее тяжело больные пациенты переносили в среднем примерно от 300 до 800 мл энтеральной формулы (см. раздел 2.2. «Недостатки современного иммунопитания»). В то время, как Аткинсон и соавт. (1998) документировали средний объём переносимости 830 мл в день в смешанной группе пациентов интенсивной терапии, объём переносимости у большинства тяжело больных пациентов в ОРИТ значительно ниже: в среднем только 400-520 мл в сутки удовлетворительно переносились у пациентов с тяжелым множественным повреждением, политравмой, длительной вентиляцией или ARDS (Вейман и соавт. 1998; Штейнбуш и соавт. 2000). Чтобы разрешить проблемы непереносимости, была предложена новая концепция минимального энтерального питания в сочетании с парентеральным поступлением энергией и протеина (Бабино, Блэкбёрн, 1994; Сухнер и соавт. 2000А). Идея этой концепции заключается в том, чтобы давать лишь небольшие количества смесей энтерально для того, чтобы извлечь пользу из положительных эффектов ранней подачи питательного субстрата в просвет кишечника - без перегрузки сниженной способности кишечника к всасыванию компонентов при критических состояниях. Реальные «питательные потребности» в энергии, протеине и существенных питательных веществах удовлетворяются парентеральным кормлением. Как только желудочно-кишечная переносимость восстанавливается, начинается ЭП с постепенным возрастанием объемов и калорийности (с учетом переносимости) и постепенной полной заменой 1111 на ЭП.
Для наиболее тяжелых пациентов в ОРИТ оптимальный переносимый объем ЭП находится в пределах 500 мл в первые послеоперационные/посттравматические дни. Целевое введение Интестамина осуществляется в объеме 500 мл/сутки.
3.2.2. Оптимальное количество очень ранней энтеральной подачи субстрата
Когда энтерально переносимый объём ограничен до примерно 500 мл/сутки у наиболее тяжелых больных, что должно быть включено в этот пониженный объём?
Такой метод - это не просто подача питательного субстрата в просвет кишечника, - но и обеспечение ключевых (существенных / условно существенных) питательных веществ, которые могут играть важную роль в поддержании кишечной структуры и функций. Вот почему качественный состав смесей для раннего энтерального питания имеет ключевое значение на фоне ограниченной переносимости (Сухнер и соавт. 2000А; Сухнер и соавт. 2000В). Глутамин и бутират являются главными источниками энергии для кишечника (смотрите разделы 3.3.1 «Глутамин-Дипептиды» и 3.3.3 «Бутират»). Антиоксидантные витамины и микроэлементы очень важны для защиты слизистой и других тканей от тяжелого окислительного стресса в критических состояниях (см. 3.3.2 «Антиоксидантные витамины и микроэлементы»).
Существенные и условно существенные питательнее вещества для кишечника, содержащиеся в Интестамине:
■ глутамин-дипептиды
■ глицин
■ бутират из трибутирина
■ антиоксиданты: Витамин Е, Витамин С, Р-каротин, селен и цинк.
Справедливо положение, что эти субстраты могут быть наиболее эффективны только в том случае, если они будут подаваться в адекватных количествах для удовлетворения зачастую высоких потребностей в случае критических заболеваний уже с начала послеоперационного/посттравматического ведения пациента. Однако выполнение этого требования невозможно на основе имеющихся формул иммунопитания, потому что они содержат недостаточные количества глутамина и антиоксидантов и не имеют добавки короткоцепочечных жирных кислот. Кроме того, целевой объем 1500-2000 мл не может переноситься многими тяжело больными пациентами, особенно в ранней послеоперационной/посттравматической фазе (см. раздел 2.2. «Недостатки существующего иммунопитания»).
Интестамин впервые позволяет осуществлять энтеральное введение 100% ключевых питательных веществ для кишечника у наиболее тяжело больных пациентов сразу после поступления в палату интенсивной терапии в готовом к использованию стерилизованном виде.
Это становится возможным потому, что Интестамин содержит ключевые питательные вещества без кормления пациента в общепринятом смысле, т.е. обеспечивая важные источники энергии и другие высокомолекулярные питательные вещества, без ненужной объемной и калорической нагрузки. Ингредиенты ограничены специальными ключевыми питательными веществами. Следовательно, небольшой объём в 500 мл достаточен, что подразумевает высокую желудочно-кишечную переносимость данной энтеральной формулы.
Эффективная доза ключевых питательных веществ, согласно существующим научным представлениям, подаётся в малом объёме, чтобы соответствовать способности кишечника переносить питательный субстрат. 500 мл ИНТЕСТАМИНА обеспечивают 100% ключевых питательных веществ для кишечника.
Таблица 11 показывает, что имеющиеся формулы иммунопитания не позволяют осуществлять оптимальную подачу ключевых питательных веществ в просвет кишечника в объёме 500 мл, который адекватно переносится в условиях очень раннего ЭП больными в ОРИТ. Некоторые антиоксиданты в составе иммунопитания содержатся в такой малой дозе, что количество 500 мл даже не отвечает потребностям здоровых людей и намного ниже высоких требований в случае критических заболеваний.
Таблица 11: Содержание ключевых питательных веществ для критически больных пациентов в 500 мл Интестамина в сравнении с имеющимися в настоящее время формулами иммунопитания
|
500 мл |
Глн |
Вит. С |
Вит.Е |
Р-кар. |
Se |
Zn |
SCFA |
|
|
г |
мг |
мг |
мг |
мкг |
мг |
г |
|
ИНТЕСТАМИН |
30 |
1500 |
500 |
10 |
300 |
20 |
1 |
|
Импакт |
7.5 |
130 |
26 |
3.9 |
35 |
10 |
- |
|
Глутамин |
|
|
|
|
|
|
|
|
Стрессон |
6.5 |
66.5 |
24.5 |
- |
21.3 |
5 |
- |
|
Алитрак |
7.5 |
100 |
10 |
- |
25 |
10 |
- |
|
Нутрикомп иммуно |
5.5 |
40 |
8 |
0.7 |
33.5 |
5 |
- |
- Глн- глутамин, Р-каротин, Se- селен, Zn -цинк, SCFA- короткоцепочечные жирные кислоты (бутират)
Обеспечение ключевых субстратов с помощью Интестамина отделено от поступления энергии и азота. Хотя ингредиентами Интестамина являются «питательные вещества», они имеют больше фармакологический, чем питательный эффект, поскольку защищают кишечный барьер и поддерживают иммунную систему. Вот почему мы называем Интестамин внешней добавкой к фармакопитанию (рисунок 29).
Рис.29: Новая концепция фармакопитания с помощью Интестамина отделяет обеспечение фармакоактивных субстратов (глутамин, антиоксиданты, бутират) от подачи энергии и азота
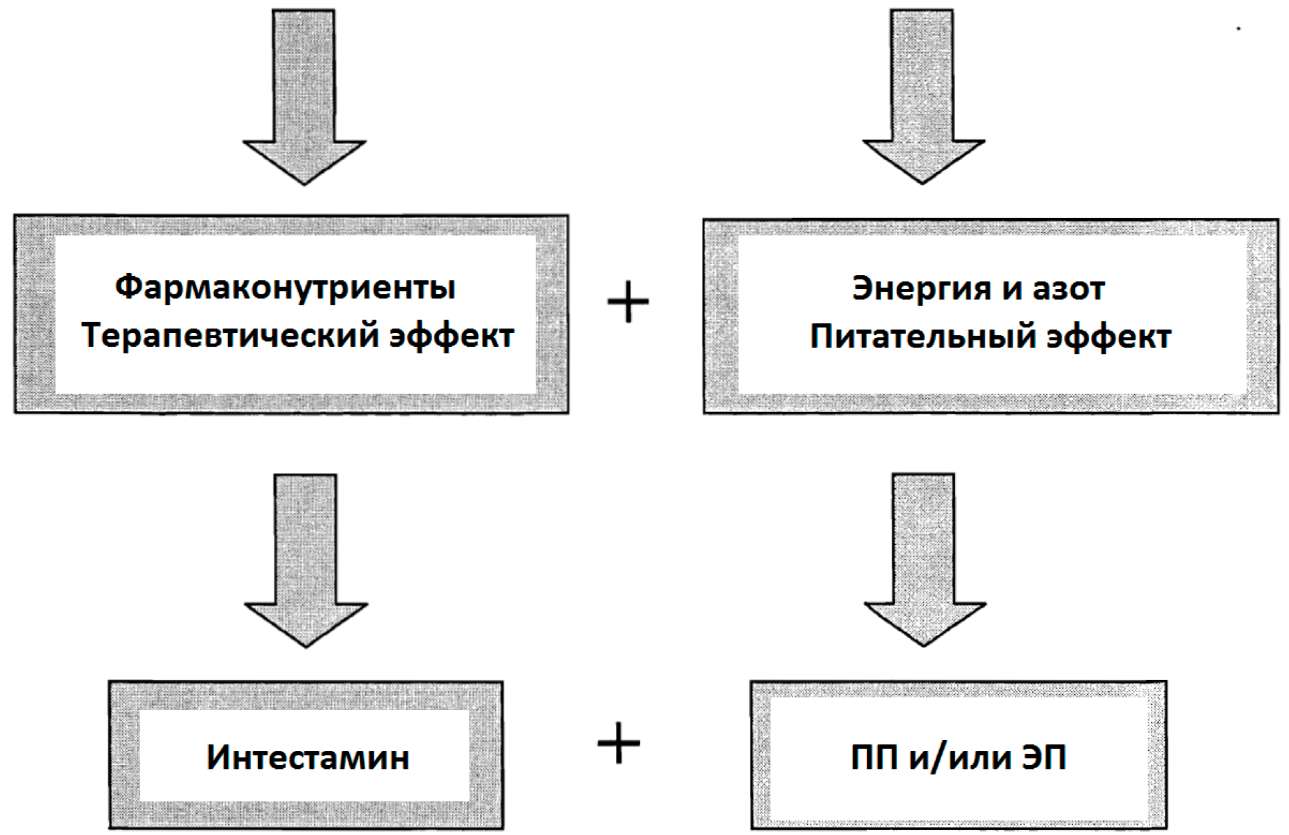
3.3. Фармакопитание с помощью Интестамина 3.3.1. Глутамин дипетиды
3.3.1.1. Глутамин в нормальном и катаболическом метаболизме
Глутамин должен быть переклассифицирован как условно незаменимая аминокислота в катаболическом состоянии, потому что расходы глутамина тела превышают синтез, а низкие уровни глутамина в плазме крови ассоциируются с ухудшением клинических исходов (Боленс и соавт. 2001).
Глутамин является наиболее доминирующей аминокислотой в человеческом теле. В скелетных мышцах глутамин составляет > 60% полного пула свободных аминокислот. Глутамин был классифицирован как заменимая аминокислота, когда было продемонстрировано, что он может быть синтезирован в организме, преимущественно в скелетных мышцах (Нё и соавт. 2002).
Рис.30: Синтез глутамина
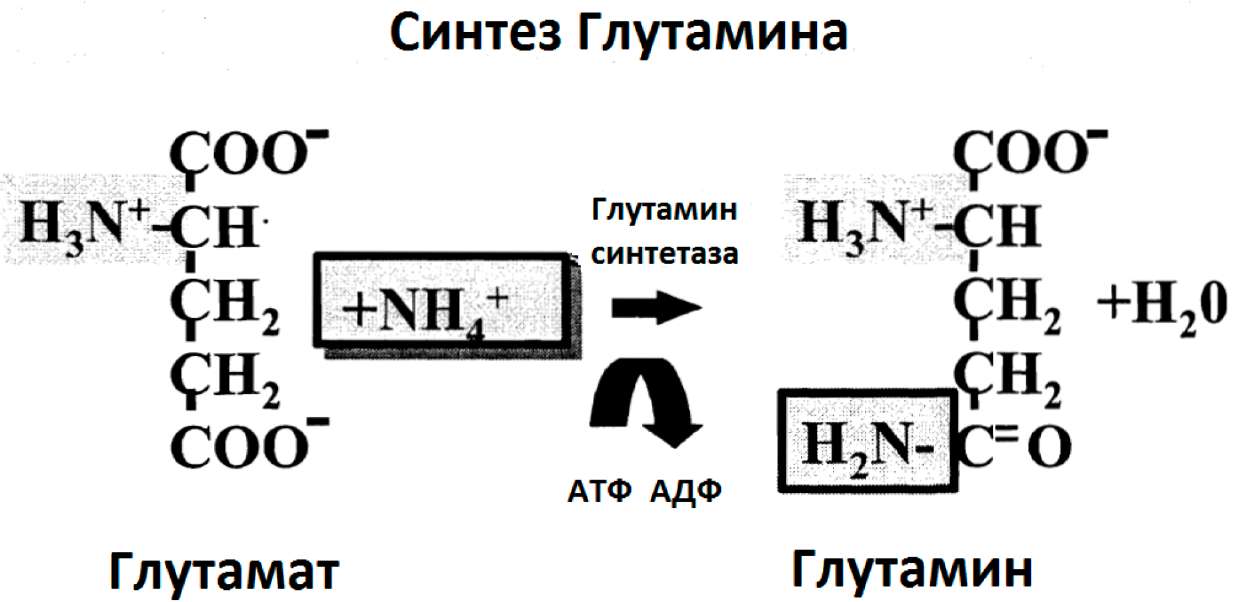
В условиях нормального метаболизма синтез глутамина и его расход хорошо сбалансированы. Следовательно, состояние дефицита не существует и аминокислота может выполнять свои важные функции в полном объеме. Основные функции глутамина проиллюстрированы рисунком 31 «Метаболические функции глутамина».
Рис.31: Метаболические функции глутамина
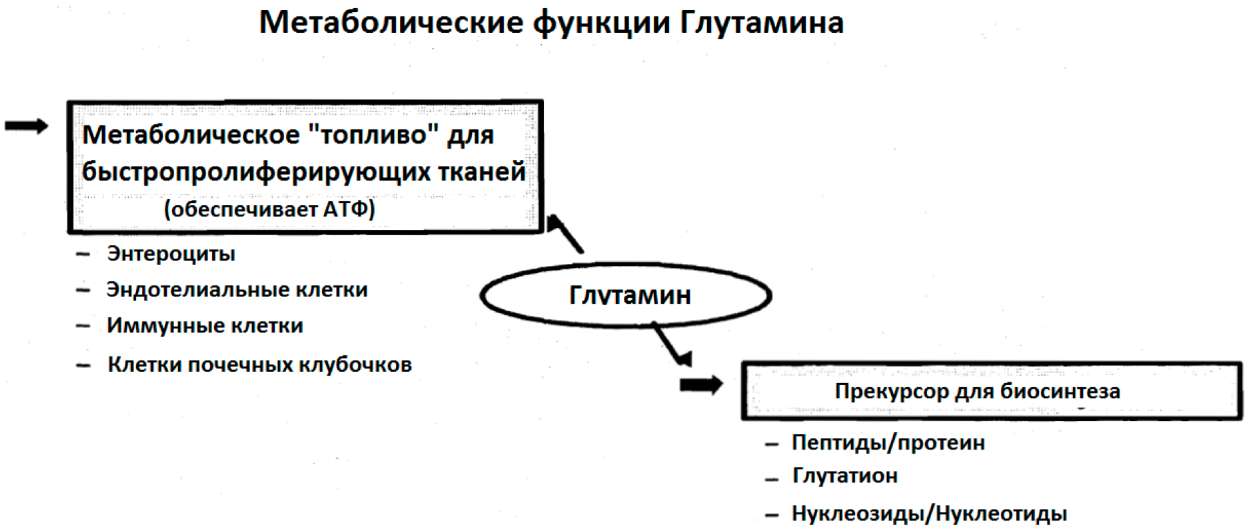
Однако одной из немедленных реакций на травму или хирургический стресс, и в особенности на кортикостероиды, является возросший экспорт глутамина из пула свободных аминокислот в мышечной ткани к кишечнику и иммунной системе (Вилмор и соавт., 1998). Глутамин становится предпочтительным субстратом энергии с помощью кишечника, иммунокомпетентных клеток и печени, и, следовательно, требуется в возрастающих количествах для того, чтобы обеспечить оптимальные реакции ткани на катаболизм, воспаление и инфекции. Поэтому при особых условиях глутамин должен считаться условно незаменимой аминокислотой, потому что эндогенный синтез не обеспечивает растущих потребностей в этих условиях (Гриффите, 1999, Вилмор и соавт., 1998). Низкие концентрации глутамина в плазме отражают уменьшение его запасов в мышечной ткани, и эта пониженная доступность глутамина в условиях катаболизма, по-видимому, коррелирует с возрастающей заболеваемостью и смертностью пациентов в ОРИТ (Боленс и соавт., 2001).
В условиях катаболизма обеспечение условно незаменимой аминокислоты -глутамина - должно считаться необходимым фактором снижения дефицита, а не добавкой (Фюрст, 2001)._
Рисунок 32 «Поток глутамина между тканями в нормальном и катаболическом метаболизме» иллюстрирует изменяющиеся метаболические условия для глутамина в катаболическом состоянии, приводящие к повышенному спросу.
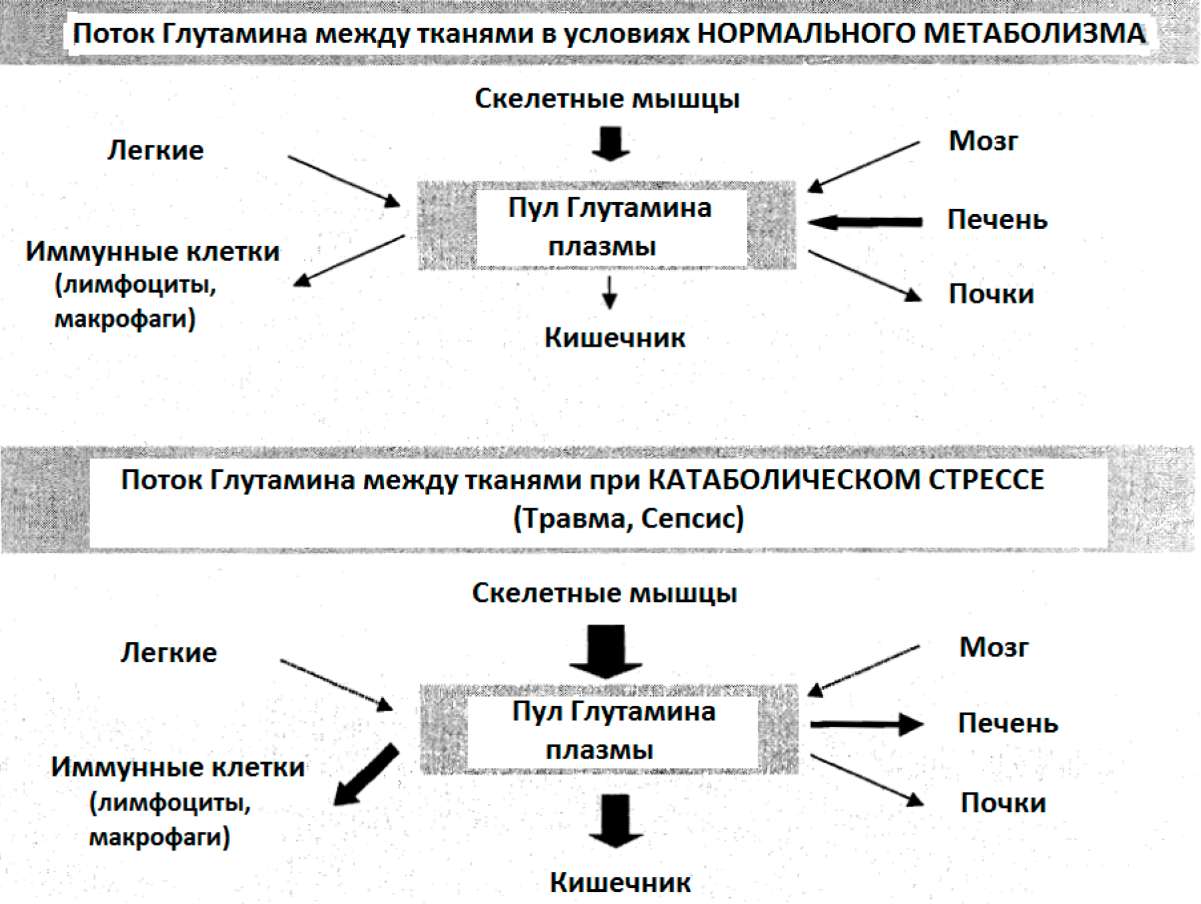
3.3.1.2 Важность глутамина для критически больных пациентов
В критических состояниях сепсис остаётся главной причиной заболеваемости и смертности. Накапливаются свидетельства того, что критически больные пациенты могут быть предрасположены к инфекционным осложнениям из-за ухудшенной функции иммунной системы. В настоящее время установлено, что специальные питательные смеси могут влиять на иммунную реакцию, а глутамин в этом плане занимает приоритетную позицию (Эндрюс, Гриффите, 2002). Уникальной особенностью клеток иммунной системы является то, что, несмотря на их отличающуюся функцию и клеточную биологию, они все зависят от глутамина одинаковым образом. Дефицит глутамина, наблюдающийся в критических состояниях, ассоциируется с ухудшением иммунной системы и повышенной восприимчивостью к инфекциям (Эндрюс, Гриффите, 2002).
В упрощенном виде, система иммунной защиты может быть условно разделена на три зоны, являющихся «мишенями» для глутамина (рис. 33 - совокупные зоны иммунной защиты: точки воздействия глутамина как питательного компонента):
1. Функция барьера слизистой.
2. Функция клеточной защиты.
3. Локальная или системная воспалительная реакция.
Глутамин может действовать во всех трёх зонах (уровнях) как иммуномодулирующее питательное вещество, и может улучшить исход критически больных пациентов, как описано в следующих разделах.
Рис.33: Совокупные площади иммунной защиты: рабочие точки глутамина как питательного вещества (Сухнер и соавт., 2000).
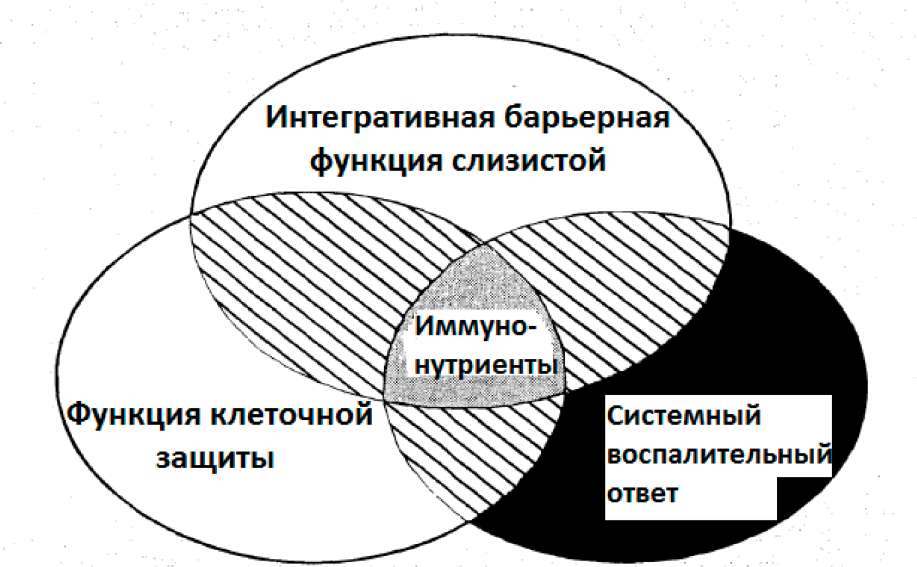
Влияние глутамина на целостность барьера слизистой кишечника
Глутамин, как главный источник энергии для быстро делящихся клеток желудочно-кишечного тракта (энтероциты, колоноциты) и связанной с кишкой лимфоидной ткани (GALT), остаётся существенным веществом для поддержания метаболизма кишечника, его структуры и функции (Боленс и соавт., 2001).
В дополнение к её роли во всасывании питательных веществ, кишечная слизистая обеспечивает важный барьер против токсинов и бактерий, находящихся в просвете кишки. Барьерная функция кишечной слизистой представляет собой первую линию защиты от перемещающихся патогенов, и уже поэтому считается важной в отношении раннего энтерального питания критически больных пациентов (Гардинер и соавт., 1995). Дисфункция кишечного барьера, как считается, позволяет перемещаться как эндотоксинам, так и всем бактериальным организмам, из просвета кишки к иммунной системе кишечника или кровотоку. Это делает возможным доступ этих патогенов к клеткам, которые вовлечены в инициацию системной воспалительной реакции, которая, в свою очередь, играет важную роль в развитии полиорганной недостаточности (Нё и соавт., 2002). Достаточная доступность ключевых субстратов, например глутамина, а также раннее энтеральное питание, считаются в настоящее время главным инструментом в поддержании структуры и функциональности барьера слизистой (Сухнер и соавт., 2000).
Глутамин является незаменимой аминокислотой для поддержания кишечной барьерной функции. Недостаток глутамина может привести к нарушению этого барьера, позволяя бактериям и/или токсинам переместиться и вызвать повреждение органа (Нё и соавт., 2002).
Рис.34: Глутамин стабилизирует кишечный барьер (Нё и соавт., 2002)
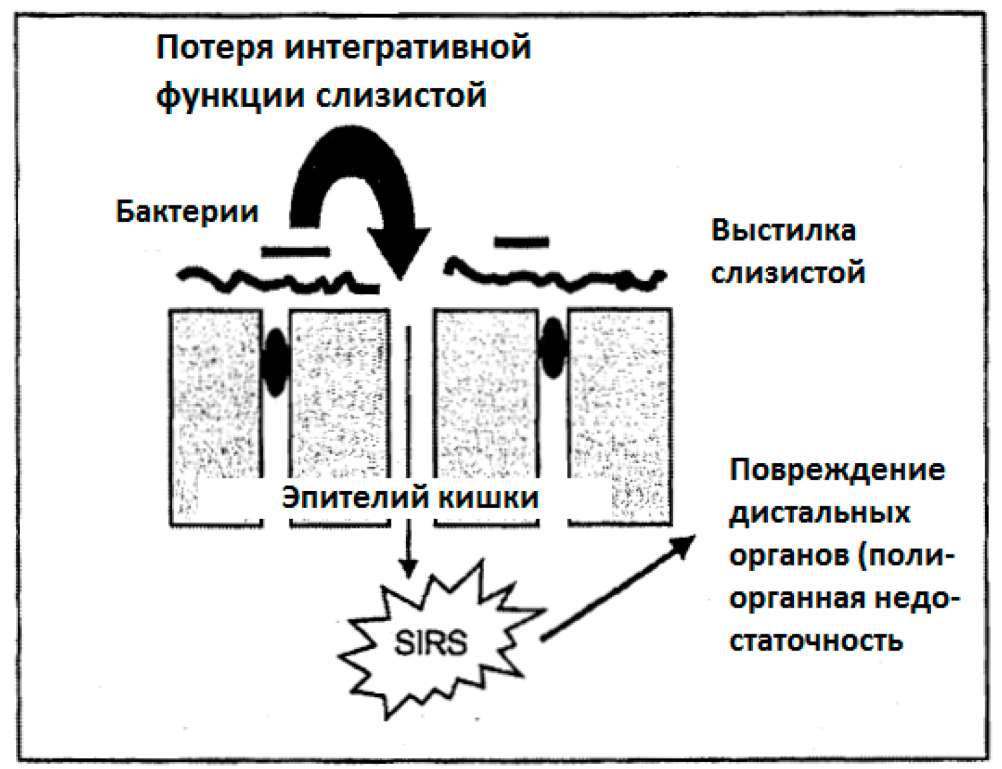
Кроме того, азот глутамина играет важную роль в поддержании структуры и функции кишечника. Это главная компонента для биосинтеза нуклеотидов (играющих ведущую роль в пролиферации) и аминосахаров (играющих ведущую роль в формировании внутреннего, подкладочного слоя ЖКТ) (Нё и соавт., 2002, см. рис. 34). Ряд исследований поддерживают точку зрения иммуномодуляторного воздействия глутамина на кишечно-слизистый барьер, как показано на рисунке 35 «Иммунно-модуляторное воздействие глутамина на целостность слизистой».
Рис.35: Иммунномодуляторные воздействия глутамина на целостность барьера слизистой (Сухнер, 2002, не опубликовано)
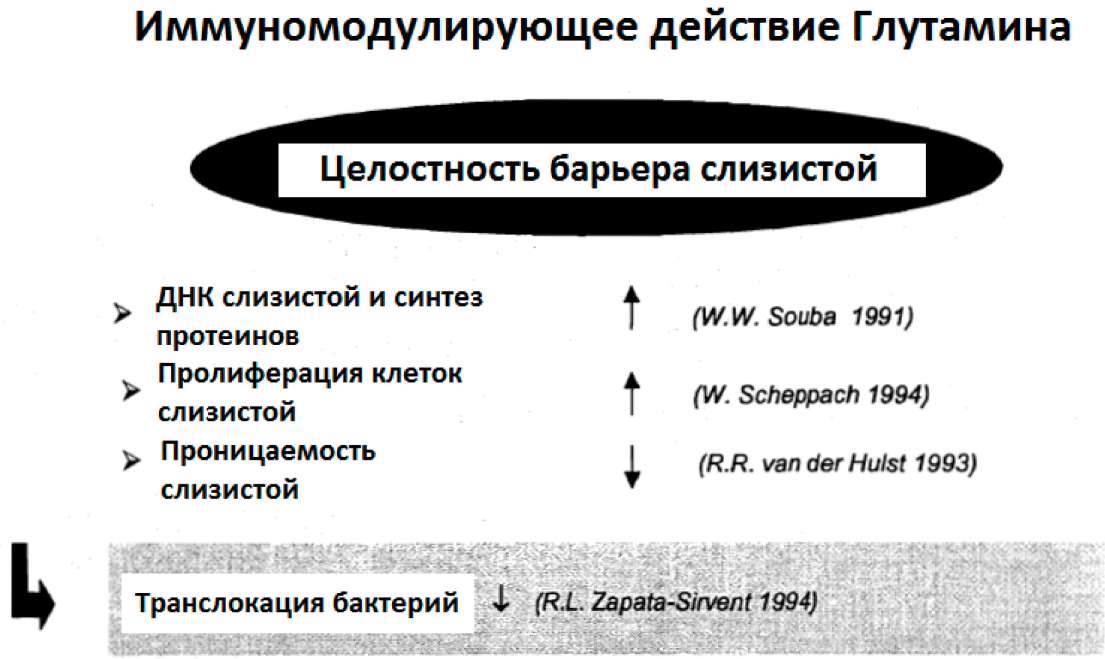
Влияние глутамина на системную воспалительную реакцию: значение для синтеза глутатиона
Синтез глутатиона при посредничестве глутамина является, вероятно, одним из наиболее важных факторов в системной воспалительной реакции. Предполагается, что синтез глутатиона является решающим фактором, вызывающим устранение клинических биохимических признаков критического состояния (Сухнер и соавт., 2000).)
Синтез глутатиона
Глутатион является трипептидом, состоящим из глутаминовой кислоты (глутамат), цистеина и глицина. Организм обладает способностью синтезировать глутатион из этих аминокислот, получаемых из пищи. Он производится внутриклеточно во всех органах, в особенности в печени (Рот и соавт., 2002, см. рис. 36 «Эндогенный синтез глутатиона»). Прямой предшественник глутатиона - глутамат - плохо транспортируется через клеточную мембрану, в то время как глутамин легко поглощается клетками. Эти биохимические особенности подчеркивают важность глутамина в синтезе глутатиона. Отмечен факт, что у критически больных пациентов низкие уровни внутримышечного глутатиона коррелируют с низкими уровнями глутамина и глутамата, но, что удивительно, уровни другого предшественника аминокислот - цистеина и глицина-сохраняются (Хаммерквист, 1997). Это указывает на существенное значение глутамина для синтеза глутатиона.
Поэтому достаточное поступление глутамина в различные органы, такие как мышцы, печень, иммунные клетки и кишечник, необходимо для того, чтобы гарантировать необходимый уровень синтеза эндогенного глутатиона (Валенсия, 2001а).
Рис.36: Эндогенный синтез глутатиона (Валенсия 2002b)
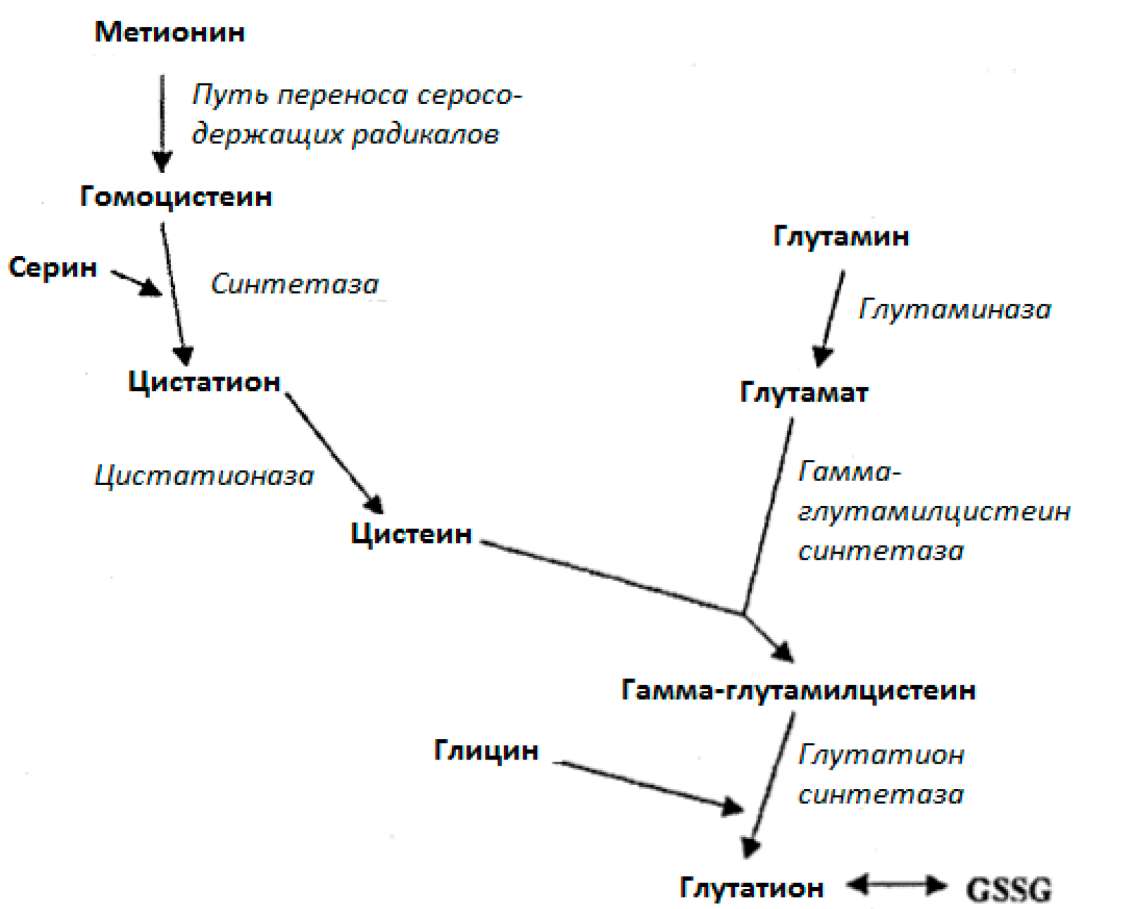
Клиническая важность глутатиона при критических заболеваниях
Физиологическая роль глутатиона многогранна, он участвует во многих клеточных функциях, таких как:
- поддержание энзимов в активной форме
(например, антиоксидантная система глутатион-оксидаза-редуктаза),
- транспорт аминокислот,
- синтез протеинов и нуклеиновых кислот,
- поддержание клеточных мембран.
Одной из удивительных характеристик в критических состояниях является системная воспалительная реакция с её возрастающим производством агрессивных свободных радикалов. Следовательно, важной функцией глутатиона в системной воспалительной реакции является его противодействие образованию и эффекту свободных кислородных радикалов. Глутатион выполняет свою функцию как компонент энзимной системы, содержащей глутатион-оксидазу и глутатион-редуктазу (Валенсия, 2001а, см. также раздел 1.5. «Окислительный стресс»).
Таким образом, глутатион играет жизненно важную роль как антиоксидативное вещество, защищая клетки от токсичного влияния повреждающих свободных радикалов, например, предотвращая окислительное повреждение в кишечнике (Вилмор и соавт., 1998).
Повышенноеобразование свободных токсичных радикалов, которое влияет на метаболизм глутатиона, также вызывается гипоперфузией, ишемией и реперфузией (Рот, 2002). В этих условиях оборот глутатиона возрастает как защитная реакция на усиленное образование свободных радикалов. Следовательно, повышенный синтез глутатиона необходим и должен быть гарантирован для противодействия вредному влиянию свободных радикалов. В экспериментальных исследованиях дополнительно вводимый глутамин способствует сохранению депо в печени и запасы глутатиона в слизистой кишечника, а также поддерживает концентрации глутатиона в плазме (Хонг и соавт., 1992, Харвард и соавт., 1994, Ю и соавт., 1996, Денно и соавт., 1996).
Рис.37: Иммунномодуляторные воздействия глутамина на системную воспалительную реакцию (Сухнер, 2002, не опубликовано)
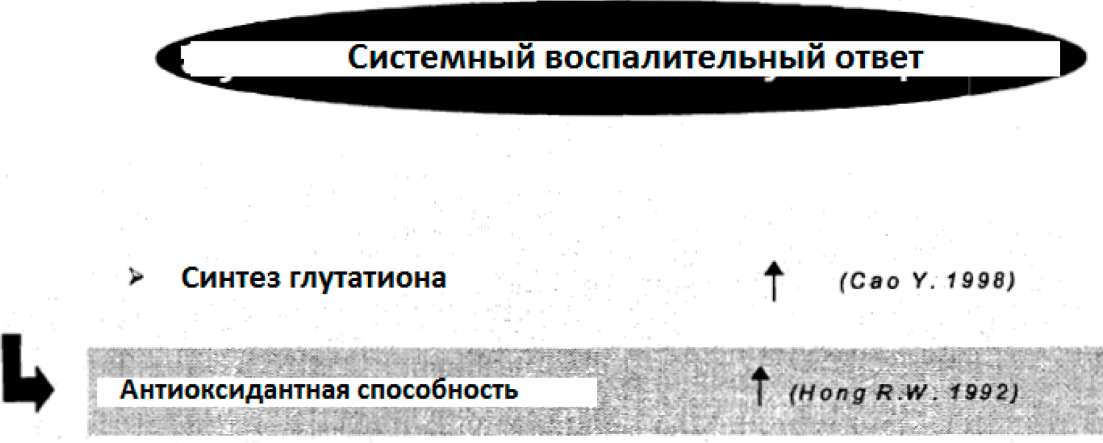
Влияние глутамина на клеточную защиту
После внедрения патогенов клеточная защита представляет собой вторую линию защиты, состоящую из гранулоцитов, макрофагов, лимфоцитов и клеток плазмы (первая линия = барьер кишечной слизистой) (Сухнер, 2000). Сложные взаимодействия между этими эффекторными клетками координируются цитокинами и другими посредниками. Питательные вещества типа глутамина могут модулировать клеточную защиту посредством образования посредника, например так, как показано на следующем рисунке (Сухнер, 2000, см. рис.38 «Иммуномодуляторные воздействия глутамина на функцию клеточной защиты).
Рис.38: Иммунномодуляторные воздействия глутамина на клеточную защитную функцию (Сухнер, 2002, не опубликовано)

3.3.1.3 Глутаминовая терапия у критически больных пациентов
В течение последних лет увеличилось понимание роли глутамина у больных в критических состояниях. Ряд клинических исследований был посвящен добавлению глутамина и получены положительные результаты, что влияет на принятие клиницистами решений об использовании глутамина в ОРИТ.
Таблица 12: Клиническое доказательства улучшения результатов лечения в ОРИТ при добавлении глутамина в парентеральное и энтеральное питание (Сухнер, 2002, не опубликовано)
|
Снижение смертности
Уменьшение частоты возникновения инфекций
Энтеральное питание, взрослые критически больные пациенты
|
Логично и важно уделять внимание вопросу: давать ли глутамин очень рано в процессе критического состояния для ликвидации дисфункции иммунной системы, а затем - предотвратить любую другую дезактивацию иммунной системы (Эндрюс, Гриффите 2001).
Общепринято, что послеоперационный пациент требует примерно 1,5 г протеина на кг веса тела в сутки. Обычная доза глутамина при этом должна быть примерно 0,3 г/кг веса тела в сутки, для 60-70 кг пациента это даёт примерно 20 г/ глутамина в сутки. Тяжелые пациенты с множественной травмой имеют более высокий уровень метаболического стресса. Такой пациент должен, следовательно, требовать больше глутамина - до 30 г/сутки (Уилмор и соавт. 1998).
Пациенты с политравмой в тяжелом состоянии требуют до 30 г глутамина в сутки (Уилмор и др. 1998).
Чтобы достигнуть такого высокого уровня поступления глутамина при существующих готовых формулах энтерального зондового питания, потребуется прием до 2,5-3 л в сутки, так как иммунопитательные диеты содержат примерно 1 г глутамина на 100 мл в качестве всего источника протеина. Однако несомненно, что такой высокий объём не будет адекватно переноситься пациентами в течение первых дней энтерального питания. Новый подход, использующий в энтеральном питании глутамин-содержащие дипептиды, облегчает первичное проведение терапии с высокой дозой глутамина на основе готовой к использованию зондовой смеси в рамках малого объёма (см. также раздел 3.3.1.4 «Обоснование использования глутамин дипептидов»). В течение определенного периода времени использовались смеси, приготавливаемые самостоятельно ex tempore с добавлением глутамина (смешивание порошка глутамина с готовым зондовым питанием). Такой метод таит потенциальную опасность в практическом плане вследствие:
- гигиенических соображений
(повышенный риск контаминации - микробактериального заражения, т.к. порошковые продукты, содержащие свободный глутамин, не могут быть стерилизованы),
- возможности ошибок в прописи и приготовлении.
Клинические исследования подтверждают эффективность ЭП с добавлением глутамина у больных в критических состояниях. Худийк и соавт. в рандомизированном контролируемом исследовании использовали ЭП с добавкой глутамина (до 30 г/сутки) через 48 часов после травмы через назодуоденальный зонд в течение минимум 5 дней Отмечено значительное снижение частоты развития осложнений у больных в ОРИТ в первые 15 дней (пневмонии, бактериемии и тяжелого сепсиса). Использование показателя TNF-рецепторов (фактор некроза опухоли) в качестве маркеров системной воспалительной реакции продемонстрировало, что пациенты на ЭП+глутамин имеют меньшую выраженность системного воспалительного ответа, чем пациенты контрольной группы (рис. 39)
Рис.39: Раннее энтеральное питание с добавлением глутамина в ОРИТ (Худийк, 1998)
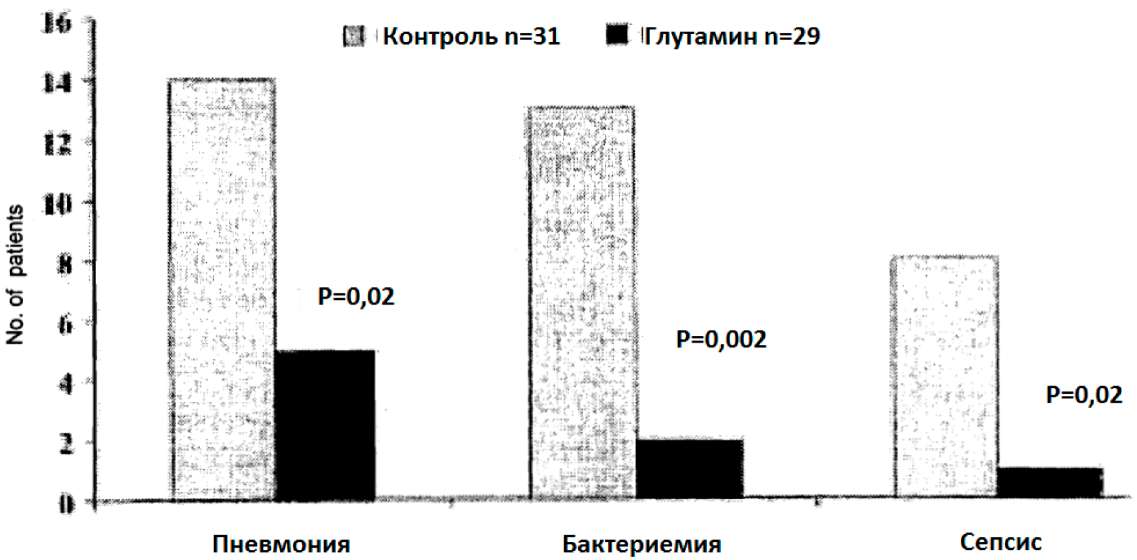
Раннее энтеральное зондовое питание с добавлением глутамина у больных в ОРИТ с политравмой проводилось с постепенным возрастанием объема ЭП. Доза глутамина на 3-4 день составила 25-30 г в сутки. При отсутствии различий в выживаемости, в первые 15 дней наблюдалось значительное уменьшение инфекционных осложнений. В обеих группах средние концентрации глутамина в плазме в первый день были меньше нижнего предела. По сравнению с контрольной группой в исследуемой группе отмечались значительно более высокие концентрации глутамина на 3, 4 и 5 день лечения. Таким образом, это исследование показывает, что обогащенное глутамином энтеральное питание может повысить концентрацию глутамина в плазме у больных в критических состояниях и улучшить клинические результаты. Джонс и соавт. (1999) провели рандомизированное двойное слепое исследование в более неоднородной группе взрослых пациентов в ОРИТ. Некоторые пациенты были уже инфицированы, но способны переносить ЭП. Дополнение 18 г/сутки глутамина давало значительное снижение госпитальных расходов. Они пришли к выводу, что у критически больных пациентов палаты интенсивной терапии энтеральное питание, содержащее глутамин, дает значительный фармако-экономический эффект Кроме того, у взрослых пациентов благоприятный эффект глутамина был подтверждён в отношении кишечной барьерной функции после того, когда его давали орально (30 г/сутки) в течение нескольких недель после высокой дозы химиотерапии/радиотерапии при раке пищевода (Йошида и соавт., 1998).
Учитывая результаты клинический исследований ЭП с добавлением глутамина, можно сделать вывод, что раннее начало энтерального питания и глутаминовая терапия эффективны у критически больных пациентов.
Глутаминовая терапия с Интестамином
Согласно современным представлениям, больные в ОРИТ требуют повышенного количества глутамина - до 30 г/сутки (Уилмор 1998). До сих пор отсутствуют готовые к использованию специальные диеты, которые бы облегчали получение такой высокой дозы глутамина. Обычное готовое к использованию зондовое питание обеспечивает поступление глутамина в дозе примерно 1 г/100 мл. В зависимости от рекомендованной суточной дозы (1,5 - 2л), это соответствует суточному поступлению глутамина 15 г -20 г. В критических состояниях необходимый высокий объём ЭП для достижения необходимого уровня поступления глутамина часто не может адекватно переноситься пациентами в первые дни после повреждения.
Интестамин представляет собой первое готовое к применению дополнительное ЭП на основе дипептида глутамина, обеспечивающее необходимую суточную дозу глутамина (30 г) в малом объеме смеси 500 мл, что является важнейшим инновационным шагом в развитии нутритивной поддержки больных в критических состояниях.
Интестамин облегчает адекватную терапию глутамином в клинических условиях. В качестве готовой к использованию дополнительной энтеральной диеты он позволяет избежать опасностей и рисков использования порошковых продуктов (заражение бактериями во время приготовления, ошибка в приготовлении) и делает ежедневное обращение с ним и проведение нутритивной поддержки в интенсивной терапии простым и безопасным.
3.3.1.4 Обоснование для использования глутамин дипептидов
Опыт использования дипептидов глутамина в клиническом питании
В начале 1980-х глутамин дипептиды не были коммерчески доступны. Начиная с 1995 года, после создания парентеральных форм дипептида глутамина, они представляют неотъемлемую часть обычной клинической практики. Базовые исследования с глутамин дипептидами (аланил-глутамин и глицил-глутамин) дают убедительные свидетельства в пользу того, что эти субстраты быстро включаются в обменные процессы после парентерального введения без накопления в тканях и с минимальными потерями с мочой. Наличие связанной с мембраной, а также не связанной с тканью внеклеточной активности гидролазы облегчает быстрый и качественный гидролиз пептида, а высвобожденные аминокислоты оказываются доступными для синтеза протеина и/или генерации энергии (Фюрст, 2001).
В многочисленных контролируемых клинических исследованиях убедительно продемонстрировано, что питание с добавлением глутамина приводит к:
- улучшению азотистого баланса,
- увеличению синтеза протеина и лимфоцитов,
- сохранению кишечной функции,
- более низкому уровню осложнений,
- снижению времени пребывания в больнице,
- уменьшению частоты возникновения сепсиса
Биодоступность дипептидов в энтеуальном питании
Основываясь на данных многочисленных исследований, можно сделать вывод, что ЭП с добавлением глутамина должно быть рекомендовано большинству пациентов в критических состояниях для обеспечения метаболизма. Биодоступность глутамин дипептидов может быть обеспечена тогда, когда они вводятся энтерально, поскольку признано, что значительное количество протеина пищи всасывается из клеток слизистой не как свободные аминокислоты, а именно как дипептиды. С этой целью необходимо гарантировать удовлетворительное всасывание глутаминсодержащих дипептидов (Лофлер, Петридес, 1997). Клетки слизистой содержат высокое количество очень активной пептидазы. Следовательно, можно предположить, что поглощённые пептиды будут разложены внутриклеточно и будут доставлены как свободные аминокислоты к системе воротной вены (Лофлер, Петридес, 1997). Преимущество в доставке глутамина энтерально, а не парентерально, может заключаться в доступности высоких концентраций глутамина в просвете желудочно-кишечного тракта, а в лабораторных исследованиях было предположено, что это способствует кишечной клеточной пролиферации (Джонс, 1999). Как подчеркнуто в разделе 3.3.2.1 «Важность глутамина у критически больных», многие исследования доказывают чрезвычайную важность глутамина для функционирования кишечного барьера.
Глутамин дипептиды в Интестамине: Новая размерность глутаминной терапии в энтеральном питании
Высокое содержание глутамина в готовой к использованию энтеральной диете (30 г/сутки) не может быть достигнуто богатыми глутамином гидролизатами белков в малых объемах, которые могут быть адекватно переносимы пациентами во время первой посттравматической фазы (см. также раздел 2.1 «Ранняя подача питательного субстрата в просвет кишечника (раннее энтеральное питание)». Неблагоприятные физические и химические свойства свободного глутамина препятствуют его использованию в больших количествах в водных препаратах, например, в готовой к использованию зондовой пище. В тепловом стерилизационном процессе, требуемом для готовой к использованию жидкой зондовой смеси, глутамин преобразуется в пироглутаминовую кислоту и аммиак. Так как Интестамин должен пройти такой стерилизационный процесс, добавление свободного глутамина нереально. Кроме того, во время длительного хранения свободного глутамина в растворе он разложится на пироглутаминовую кислоту и аммиак. Другим недостатком использования свободного глутамина является его низкая растворимость в воде (36 г/л), что ведёт к существенным производственным ограничениям.
Таблица 13: Технологические свойства свободного глутамина и дипептидов глутамина
|
Свободный глутамин: Неблагоприятные физические и химические свойства |
|
Глутамин-дипептиды: Благоприятные физические и химические свойства |
|
• Разложение до |
• Стабильность во время тепловой стерилизации и хранения |
|
|
• Ограниченная растворимость |
• Легко растворимы |
Синтетические глутамин дипептиды (L-аланил-Ь-глутамин и глицил-Ь-глутамин) высоко растворимы и стабильны во время тепловой стерилизации и хранения. При использовании этих глутамин пептидов можно избежать обычных ограничений использования глутамина в его природной форме и предложить большие количества этого условно незаменимого субстрата больных в ОРИТ.
Интестамин: Количество и качество глутамина
- 30 г глутамина /500 мл,
- получен из дипептидов L-аланил-Ь-глутамин и глицил-Ь-глутамин.
Заключение
Интестамин представляет собой новое измерение в искусственном питании. Подход, основанный на глутамин дипептидах, впервые позволяет осуществить высокодозную терапию глутамином (30 г/сутки) энтеральным путем введения вместе с готовой к использованию дополнительной диетой. Хорошо известно, что глутамин в критических состоянияхиях становится условно незаменимой аминокислотой. Введение глутамина в этих условиях должно, в первую очередь, рассматриваться как необходимая замена, а не дополнение. Раннее энтеральное введение глутамина чрезвычайно важно для поддержания состояния целостности кишечника, потому что нарушение её очень часто играет критическую роль в развитии полиорганной недостаточности. Энтеральное введение глутамина в объёме всего 500 мл/сутки обеспечивает дозу 30 г глутамина и существенное улучшение клинических результатов из-за чрезвычайно важных функций глутамина во время критических заболеваний, которые суммированы\на рис. 40.
Рис.40: Отдельные функции глутамина (Сухнер, 2002, не опубликовано)
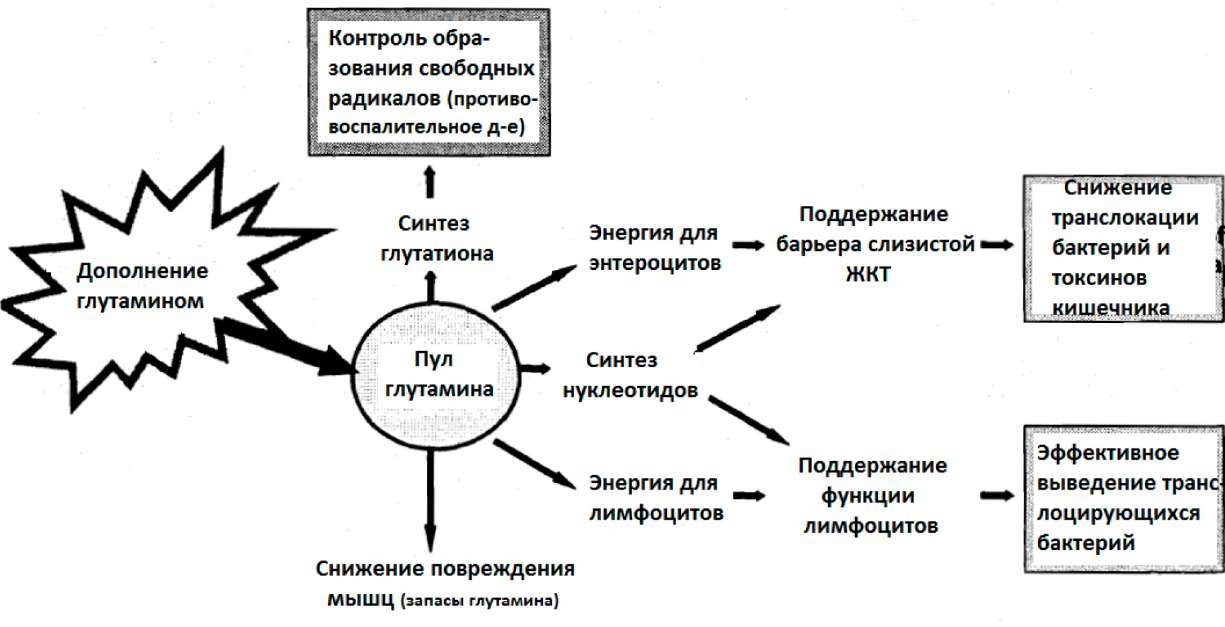
3.3.2. Антиоксидантные витамины и микроэлементы
Условием развития окислительного стресса является образование большого количества высоко реактивных свободных радикалов и их накопление в организме, которые не могут быть адекватно детоксицированы антиоксидантными защитными механизмами. Окислительный стресс играет важную роль в патогенезе SIRS и сепсиса. Ишемия и реперфузионное повреждение после хирургии, тяжелая травма или инфекция вызывают повреждения тканей за счет свободных радикалов, а также воспалительную реакцию в других удалённых органах и тканях. И наоборот, воспаление само стимулирует генерацию свободных радикалов и создаёт порочный круг (см. раздел 1.5 «Окислительный стресс»). Измеряемые признаки окислительного стресса у критически больных пациентов, - это пониженные плазменные и тканевые концентрации антиоксидантных витаминов (типа витамина Е, С и Р-каротин), а также микроэлементов (типа селена и цинка), пониженные активности антиоксидантных энзимов (например, глутатион-пероксидазы) и/или повышенные уровни липидных пероксидов в крови. Имеется много клинических свидетельств того, что все эти маркеры окислительного стресса присутствуют у посттравматических/послеоперационных пациентов сразу после начала критического состояния (см. раздел 1.6.2 «Истощение антиоксидантов»). Чем тяжелее состояние пациента, тем больше выраженность окислительного стресса. Предотвращение начала или контролирование развития окислительного стресса могут улучшать или реверсировать развитие критического заболевания, SIRS и MODS. Терапевтические подходы включают усиление антиоксидантной защиты и/или подавление производства свободных радикалов (например, путем энзимного подавления). Поступление экзогенных антиоксидантов является одним из перспективных инструментов противодействия большому производству токсичных свободных радикалов и, таким образом, восстановления баланса между оксидантами и антиоксидантами в критическом состоянии (Борхани, Хелтон, 2000). Антиоксиданты формируют важную защитную линию против повреждения свободными радикалами. Витамины Е и С и Р-каротин являются «мусорщиками» для свободных радикалов, что означает, что эти вещества детоксицируют свободные радикалы через прямое отнятие неспаренных электронов и образование менее реактивных веществ. Селен и цинк являются важными компонентами антиоксидантных энзимов. Все эти антиоксиданты функционируют вместе в сложной биохимической системе. Во время процесса устранения свободных радикалов антиоксиданты зависят друг от друга в отношении регенерации, образуя «антиоксидантную спираль». По этой причине становится очевидно, что антиоксиданты должны быть обеспечены в комбинации (см. раздел 1.5. «Окислительный стресс»). Интервенционные исследования позволяют предположить, что острые состояния могут быть модулированы путем добавления антиоксиданта до достижения более положительного исхода заболевания. В приложении к этому разделу дается обзор, посвящённый клинически доказанным выгодам добавления антиоксидантов добавки у больных в критических состояниях. Таблица разделена на 3 части:
I. Исследования с парентерально добавленными антиоксидантами.
П. Исследования с комбинированным парентерально и энтерально/орально добавлением антиоксидантов.
Ш.Исследования с энтерально/орально добавленными антиоксидантами. Добавление антиоксидантов у тяжело больных пациентов не только повышало уровни антиоксидантов в плазме, усиливая активность антиоксидантных энзимов и понижая маркеры оксидативного повреждения, но также улучшало клинические результаты лечения пациентов. Отмечалось:
- лучшее залечивание ран,
- улучшение гемодинамических параметров
- снижение неврологической симптоматики,
- снижение частоты послеоперационных осложнений,
- уменьшение потребности в ИВЛ,
- меньшая частота развития полиорганной недостаточности,
- меньшая частота развития острого панкрета,
- снижение продолжительности пребывания в ОРИТ и/или в госпитале,
- более высокая выживаемость (см. прилагаемые таблицы).
Несмотря на доказанную эффективность антиоксидантов у больных в ОРИТ, обычное добавление антиоксидантов клинически нереально. Ангштвурм и соавт. (1999) сделали вывод (см. приложение), что добавление селена «может быть важным новым терапевтическим способом улучшить выживаемость у пациентов с тяжелым сепсисом или SIRS».
Правильный выбор времени и продолжительности антиоксидантной терапии не были ещё определены. В клинических исследованиях, упомянутых в приложении, антиоксиданты давались пациентам периоперационно или немедленно после травмы или хирургии. Эта терапия была продолжена в течение от нескольких дней до нескольких месяцев, в зависимости от клинических условий. Бергер и соавт. (1994) давали Se, Zn и Си ожоговым пациентам в период ранних фаз, т.к. ожидали острых потерь этих антиоксидантов через раны немедленно после ожога. Раннее кратковременное добавление антиоксидантов может предотвратить дисфункции органов и систем и иметь положительные метаболические и клинические последствия. Вот почему очень раннее обеспечение антиоксидантов, т.е. в течение первых 24 часов - независимо от питания - было рекомендовано пациентам с сильным стрессом. Продолжительность такой терапии должна, вероятно, сопровождать весь острый период заболевания (Бергер, Шенкин, 2000).
В заключение нужно сказать, что имеются очевидные свидетельства клинических преимуществ высокого содержания антиоксидантов в нутритивной терапии критически больных пациентов. Оптимальное время и продолжительность введения антиоксидантов для различных групп пациентов в критических состояниях в настоящее время исследуются. Раннее предоставление антиоксидантов независимо от питательной поддержки рекомендуется для пациентов с сильным стрессом.
3.3.2.1. Сколько антиоксидантов должны получить критически больные пациенты?
На антиоксидантный статус пациентов влияют:
1. Поступление антиоксидантов до и во время заболевания,
2. Потери за счет экссудата, крови, мочи или из-за заместительной почечной терапии,
3. Уровень гиперметаболизма, а также
4. Выраженность оксидативного стресса.
Кроме того, уровень микрнутриентов у больных в критических состояниях часто зависит от изменений уровней протеинов в острой фазе, которые могут ухудшить поступление и транспорт антиоксидантных витаминов в организме (Гуд, Вебстер, 1993). Из-за этих факторов, которые зависят от многих индивидуальных условий (питательный статус пациента, уже имеющееся заболевание, причина и характер критического заболевания), невозможно предсказать точные потребности в антиоксидантах у пациента. Количества антиоксидантных витаминов и микроэлементов в обычных растворах для ППП и ПЭП для критически больных пациентов отвечают, вероятно, минимально рекомендованным количествам для предотвращения дефицита. Однако, для удовлетворения высоких потребностей пациентов в ОРИТ, потребуются и более высокие концентрации экзогенных антиоксидантов (Гуд и соавт., 1995, Метниц и соавт., 1999). Однако, в настоящее время
нет четко сформулированных количественных потребностей больных в ОРИТ в антиоксидантах (Борхани, Хелтон, 2000). В клинических интервенционных исследованиях, упомянутых в приложении к этому разделу, следующие количества антиоксидантов назначались больным в ОРИТ:
- Витамин Е: 1.2 -1456 мг энтерально/орально или 12-400 мг парентерально
- Витамин С: 96 -1127 мг " 1000-3000 мг "
- b-каротин: 0.5 - 30 мг "
- Селен: 500-600 мкг " 59 - 1000 мкг "
- Цинк: 13 - 30 мг
Приведенные в этих исследованиях дозы изменялись в широком диапазоне. Однако большинство доз превышают рекомендованные суточные дозы для здоровых людей, что кажется вполне разумным во время тяжелого окислительного стресса в критических состояниях. Ни официальные власти, ни Ассоциации 1111 и ЭП не выработали пока рекомендаций для введения антиоксидантов критически больным пациентам. В литературе дано несколько количественных рекомендаций (таблица 14).
Таблица 14: Рекомендации для антиоксидантной добавки у критически больных пациентов по данным литературы
|
в сутки |
Гальбан Родригес |
Бергер и Шенкин |
Борхани и Хелтон |
|
|
(2000)** |
(2000)* |
(2000)** |
|
Витамин А |
3.3 мг |
1-2 мг |
|
|
Витамин Е |
(лучше в форме Р- |
|
|
|
Витамин С |
каротина |
50-200 мг |
910 мг |
|
|
364-910 мг |
250 -> 1000 мг |
>1000 мг |
|
|
2000 мг |
|
|
|
Селен |
100 мкг |
100-500 мкг |
|
|
Цинк |
50 мг |
10-40 мг |
|
* рекомендации для парентерального введения ** нет рекомендаций
Из-за отсутствия официальных рекомендаций в отношении количеств этих антиоксидантов было решено ввести в состав Интестамина высокие - но, конечно безопасные, дозы витаминов и микроэлементов.
3.3.2.2. Какие дозы антиоксидантов безопасны у критически больных пациентов?
Совет по пищевым продуктам и питанию Института медицины США определил в 2000 и 2002 годах переносимые верхние уровни приема антиоксидантов (UL) в соответствии с их максимальными потребностями, не приносящими вреда здоровью (NOAEL) для почти всех индивидуумов в общей популяции (таблица 15). UL был основан на уровне отсутствия побочных эффектов при приеме самых высоких доз.
Таблица 15: Переносимые верхние уровни приема антиоксидантов (UL) при условии отсутствия побочных эффектов (по данным Американского Совета по пищевым продуктам и питанию, 2000, 2002)
|
Возраст (лет) |
Витамин Е (г) |
Витамин С (г) |
Se (мкг) |
Zn (мг) |
Р- каротиноиды (мг) |
|
UL9-13 |
0.6 |
1.2 |
280 |
23 |
нет |
|
14-18 |
0.8 |
1.8 |
400 |
34 |
рекомендаций |
|
>18 |
1 |
2 |
400 |
40 |
|
|
NOAEL (взрослые) |
250 мг/кг в.т. |
2 |
800 |
40 |
|
|
интестамин |
0.5 |
1.5 |
300 |
20 |
10 |
TJL для витамина Е был основан на наименьшем наблюдаемом уровне побочных эффектов (LOAEL) в экспериментах на животных, и составил 500 мг витамина Е / кг веса тела.
Научный комитет по питанию Европейской комиссии установил TJL для селена в количестве 300 мкг/сутки. Для других антиокисдантных витаминов и цинка этот Комитет ещё не установил UL (Научный комитет по питанию 2000).
Для бета-каротина в дозе 30 мг/сутки в составе пищевого рациона не выявлено сколько-нибудь значимых побочных эффектов, кроме окрашивания кожи в желтый цвет в течение длительного периода времени. Более того, не отмечено никаких побочных токсических эффектов и при очень высоких терапевтических дозах (до 180 мг/сутки) добавок |3-каротина. Только курильщики и работающие с асбестом, которые склонны к алкоголизму, имеют, вероятно, более высокий риск развития рака легких при приеме добавок |3-каротина в дозах 20 -30 мг/сутки в течение ряда лет.
Таким образом, включение антиоксидантов в состав Интестамина основано на следующих основных положениях:
1. Витамины и микроэлементы должны входить в состав в комбинации
2. Суточные дозы должны быть существенно выше тех, что рекомендуются здоровым людям
3. Не должны превышать дозы, рекомендованные Американским и Европейским Советом по питанию
Исходя из этого, Интестамин в суточной дозе 500 мл содержит (дополнительно к глутамину и трибутирину):
500 мг витамин Е 1500 мг витамин С 10 мг Р-каротин 300 мкг селен 20 мг цинк
3.3.2.3. Почему энтеральные антиоксиданты?
Из-за неопределённости адекватного (переносимого) объема энтеральных смесей у больных в ОРИТ, Бергер и Шенкин (2000) рекомендовали вводить антиоксидантные витамины и микроэлементы парентерально. Фактически на рынке не существует готовой к употреблению энтеральной смеси, которая бы обеспечивала высокую дозу антиоксидантов для критически больных пациентов (смотрите раздел 2.2.3 «Недостатки существующего иммунопитания - неадекватная подача антиоксидантов»). Однако, желудочно-кишечный тракт особенно восприимчив к окислительному стрессу по следующим причинам:
- Кишечная слизистая является границей между «внешним» и «внутренним» миром организма. Питательные вещества, лекарства, жидкости, бактерии, воздух и т.п. поступают снаружи и приносят сотни веществ в кишечник, включая потенциально токсичные вещества, антигены и т.д.
- Имеется аэробное окружение в просвете кишечника, которое благоприятствует реакциям с участием кислорода.
- Бактерии кишечной флоры могут производить свободные радикалы.
- Кишечник восприимчив к ишемическому, реперфузионному повреждению при критических состояниях из-за перераспределения крови к другим органам. Энтерально вводимые антиоксиданты прямо достигают своего целевого органа окислительного стресса и могут помочь противодействовать свободным радикалам в кишечном просвете и слизистой. Это может, вероятно, поддержать важные желудочно-кишечные барьерные функции.
Интестамин является первой готовой к употреблению энтеральной добавкой, которая обеспечивает высокие количества антиоксидантных витаминов и микроэлементов в малом суточном объёме.
3.3.3. Бутират / Трибутирин
Интестамин содержит новый важный для кишечника источник энергии - бутират жирных кислот с короткими цепями - в форме структурированного липида «Трибутирин».
3.3.3.1. Преимущества бутирата
Короткоцепочечные жирные кислоты (SCFA) в виде бутирата являются ключевым субстратом для питания кишечника, поддержания целостности слизистой и процессов ее восстановления. Обычно бутират образуется из пищевых волокон в толстом кишечнике (ободочная кишка). В ободочной кишке бутират служит главным донатором энергии и субстратом для колоноцитов. Кроме того, бутират способствует клеточной пролиферации и дифференциации (Шредер, Штейн, 1997). Этот эффект не ограничивается толстым кишечником. Экспериментальные исследования заставляют предполагать, что бутират оказывает трофический эффект также в отношении тонкого кишечника. SCFA стимулирует пролиферацию кишечной слизистой на моделях у животных, независимо от пути его поступления: орально, внутривенно, ободочно/цекально (Коруда и соавт., 1990, Франкл и соавт., 1994, Штейн и соавт., 1994, Рейли и соавт., 1995, Таппенден и соавт., 1997, Рамос и соавт., 1997). Внутривенное введение SCFA (натрий бутират, ацетат и пропионат) значительно снижают атрофию тонкого кишечника, которая была вызвана искусственным голоданием во время парентерального питания крыс (Коруда и соавт., 1990, Штейн и соавт., 1994, Таппенден и соавт., 1997). Механизмы, с помощью которых SCFA может посредничать в процессе кишечной пролиферации и функции, включают выработку энергии, стимуляцию кровотока, усиление внешнесекреторной функции поджелудочной железы и автономной нервной системы, а также образование энтеротрофических желудочно-кишечных гормонов (Вахтершау, Штейн, 2000).
Питание кишечника и поддержание кишечной функции и структуры - главные задачи Интестамина. В свете этого, бутират - важный компонент поддержания кишечника у больных в ОРИТ.
Из лабораторных результатов следует (Щепах и соавт., 1992), что стимуляция пролиферации кишечных клеток и поддержание целостности слизистой требует эффективной дозы 10-20 ммоль бутирата. Эта доза отражает минимум нормального суточного образования бутирата из непереваренных углеводов в толстом кишечнике, что составляет примерно 10-60 ммоль (Щепах и соавт., 1995, Щепах, 1995).
3.3.3.2. Как добавить бутират к Интестамину?
Поступление пищевых волокон, которые являются главным субстратом для формирования бутирата в кишечнике, может быть связано с некоторыми нежелательными эффектами у больных в критических состояниях. Ферментация пищевых волокон повышает образование кишечных газов, что может вести к растяжению брюшины. Более того, имеется риск нарушения кишечной функции и чрезмерного роста бактерий при поступлении такой пищи (рис. 41). Вот почему пищевые волокна противопоказаны больным в ОРИТ (Ромбо, Такала, 1997, Скайф и соавт., 1999).
Рис.41: Возможные нежелательные эффекты пищевых волокон у больных в ОРИТ
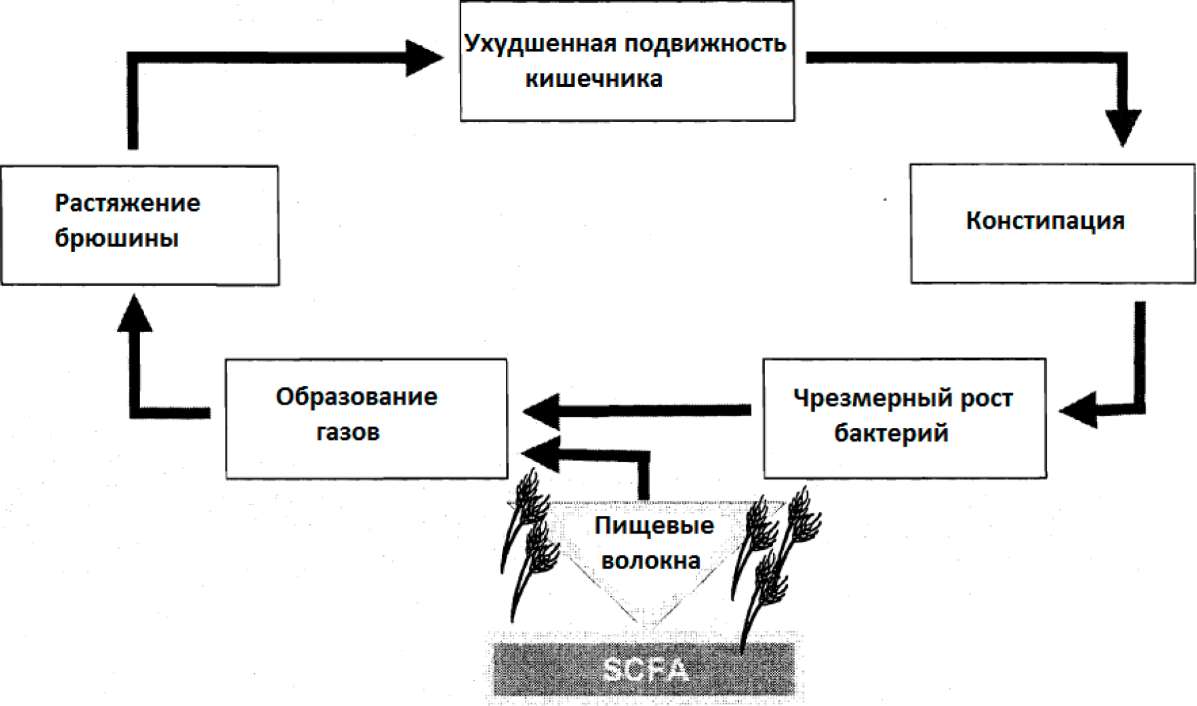
Следовательно, должны быть оценены альтернативы для энтерального введения бутирата больным в ОРИТ (Таблица 16).
Таблица 16: Альтернативы поступления бутирата
|
Источник бутирата |
ЗА |
ПРОТИВ |
|
|
-Главные источники SCFA в нормальном питании - источник различных SCFA - другие выгоды от волокна (масса, связывание токсинов и т.п.) |
- противопоказано у критически больных пациентов из-за риска вздутия живота, возникновения препятствий, чрезвычайного роста бактерий |
|
|
- природный источник бутирата |
- 1 г содержит только 0.03 г бутирата - большие количеств жира не переносимы критически больным пациентами из-за малого всасывания жира |
|
|
- поставщик бутирата в экспериментальных исследованиях |
- запах прогорклого масла -t осмолярность - т рН - t натрий |
|
|
- уже 1 г поставляет 10 ммоль бутирата - без запаха - нет влияния на рН или осмотическую концентрацию |
- новый субстрат в ЭП |
Рассмотрев все физиологические, химические и технологические аспекты вместе, можно прийти к выводу, что трибутирин является единственным подходящим источником бутирата в энтеральном питании для критически больных пациентов. Соответственно, инновационным было решение ввести в состав Интестамина трибутирин.
3.3.3.3. Характеристики и производство трибутирина
Трибутирин (1,2,3 -Трибутирилглицерин=С15Н2бОб) является структурированным липидом, состоящим из трех молекул бутирата, эстерифицированных глицеролом (рисунок 42).
Рис.42: Химическая структура трибутирина
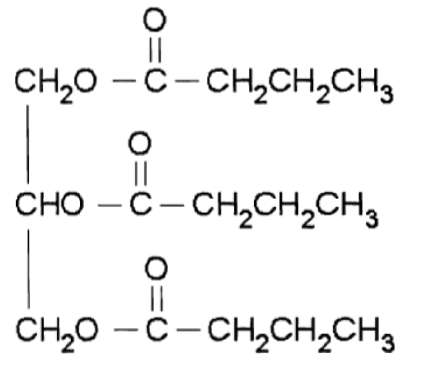
Оба компонента трибутирина - бутират и глицерол - являются нормальными промежуточными продуктами человеческого метаболизма. Помимо поступления с липидами молока, бутират производится микробной ферментацией пищевых волокон в толстом кишечнике. Глицерол является промежуточным веществом в метаболизме жира, который производится в процессе нормального пищеварения. Промышленно производимый трибутирин используется в качестве «придающей вкус специи» для выпечки, напитков, жиров и масел, десертов и другой пищи (Белл и соавт., 1997). Для этих целей трибутирин «обычно признаётся безопасным» (GRAS) Администрацией США по пищевым продуктам и лекарствам (FDA:21CFR184.1903). Трибутирин, который содержится в Интестамине, промышленно приготовлен из масляной кислоты и глицерола в простом производственном процессе с очень высокого класса чистотой > 99%..
3.3.3.4. Метаболизм трибутирина
Пищеварение, всасывание и утилизация трибутирина аналогичны тем же самым процессам для других жиров и функционируют понятным образом. Переваренный трибутирин быстро гидролизуется липазой до бутирата и глицерола в желудке и тонком кишечнике. Пищеварение и усвоение идет быстрее и более эффективно по сравнению с длинноцепочечными жирными кислотами (LCFA) (Хайес и соавт., 1994). Исследования, направленные на определение еюнального поглощения бутирата, показали, что он всасывается быстро и равномерно в тонком кишечнике, но не в ободочной кишке (Шмит и соавт., 1976). Бутират эффективно метаболизируется через [3-окисление для обеспечения энергией (Хайес и соавт., 1994). 1 г трибутирина поставляет 26,8 кдЖ (Крипке и соавт., 1991).
Любой бутират, не востребованный желудочной или кишечной слизистой, транспортируется к печени и используется там для поставки энергии или для производства LCFA или кетоновых тел (Хайес и соавт., 1994). Глицерол вступает в гликолиз. Конечные продукты метаболизма бутирата и глицерола - это ССЬ и НгО (Хайес и соавт., 1994).
3.3.3.5. Исследования с энтерально подаваемым трибутирином для процессов питания
• Экспериментальные исследования
Внутрижелудочное питание элементной формулы, которое содержало 40% небелковой энергии как 1:1 смесь трибутирина (7.2 г/кг/сутки) и триацетина, в исследованиях на крысах повышало кишечную адаптацию при экспериментальном синдроме короткой кишки. Трофические эффекты в отношении слизистой отмечались в тощей кишке, а также в ободочной кишке. Трибутирин и триацетин хорошо переносились без каких-либо изменений в составе печени и энзимах сыворотки (Крипке и соавт., 1991). Непрерывное назогастральное введение диет, содержащих 32 энергетических % трибутирина (5.5 г/кг/сутки) или смесь 16 энергетических % трибутирина (2.8 г/кг/сутки) и триацетина, в течение 12 часов хорошо переносился крысами. При этом не наблюдалось побочных эффектов. Замена углеводов трибутирином и триацетином приводила к значительно меньшим нарушениям на модели травмы головы (Робертсон и соавт., 1992).
• Исследования на людях
Имеется один отчёт из более старой литературы о переносимости и безопасности орально принимаемого трибутирина с целью нутритивной поддержки у преждевременно родившихся младенцев, которые обычно очень чувствительны к такой терапии из-за недоразвитости желудочно-кишечных функций. После кормления трибутирином как жировым компонентом в составе молока в течение 4 дней в дозах от 6,6 г/сутки до 12 г/сутки побочных эффектов не выявлено. Трибутирин полностью всасывался. У 4-х младенцев отмечено улучшение состояния и прибавка в весе. (Снайдерман и соавт., 1955).
3.3.3.6. Другие исследования с трибутирином
Имеются экспериментальные данные и клинических исследования, что бутират, вводимый в виде трибутирина, может быть эффективен в терапии рака (Щепах и соавт., 1995В, Конли и соавт., 1998, Майер и соавт., 2000). Однако, вероятно, что это не преимущество бутирата как пищевого компонента, а фармакологический эффект очень высоких доз бутирата /трибутирина.
Из-за новизны трибутирина в продуктах энтерального питания, фирма Фрезениус Каби подала заявку и получила исключительное разрешение властей Германии на включение этого компонента в состав Интестамина.
Интестамин содержит 1 г трибутирина (=10 ммоль бутирата) в суточной дозе, что представляет собой минимальное суточное количество бутирата, которое производится в кишечнике при нормальном питании.
Проф. Штейн убедительно доказал , что при энтеральном введении в ОРИТ данная доза эффективна для поддержания кишечных функций, в то время как нежелательные эффекты маловероятны.
3.3.4 Глицин
Предварительные замечания
Интестамин обеспечивает 10 г глицина в суточной дозе 500 мл, добавленный в виде глицил-глутамин-дипептида. Как показано в этом разделе, последние научные данные свидетельствуют о положительных эффектах глицина у больных в критических состояниях, хотя требуются дальнейшие исследования для окончательного решения данного вопроса Глицин может занять место одного из ключевых субстратов Интестамина, если дальнейшие клинические данные докажут явный положительный эффект этой аминокислоты.
3.3.4.1. Основы глицина
Глицин, простейший из всех аминокислот, состоит из одной молекулы углерода, прикреплённой к амино- и карбоксил группам (рисунок 43)
Рисунок 43: Химическая структура глицина
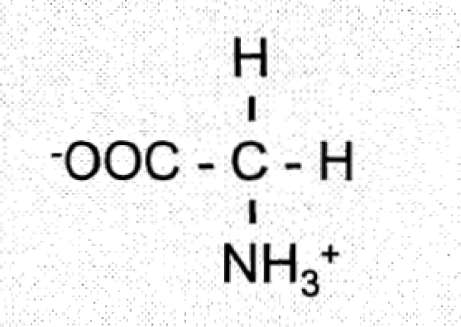
Глицин не является незаменимой аминокислотой для здоровых взрослых людей. Во многих клинических исследованиях глицин часто использовался вместе с другими аминокислотами, в частности, глутамином, для достижения изонитрогенности зондового питания. Однако в настоящее время имеются свидетельства, что сам глицин действует как мощный цитопротектор (Ли и соавт., 2002). Было показано, что глицин предотвращает гибель клеток, вызванную анорексией, окислительным стрессом и различными токсичными агентами, на уровне клетки, органа и всего организма в целом (Жонг и соавт., 1996).
Примеры экспериментально показанного цитозащитного эффекта глицина:
- Защита от окислительного повреждения в венозных эндотелиальных клетках;
- Снижение нефротоксических эффектов лекарств;
- Защита клеток печени от гипоксии и реперфузионного повреждения. (Обзор экспериментальных исследований Хадд, 1998).
Механизмы, лежащие в основе этих цитопротекторных эффектов глицина, пока не совсем понятны. Предполагаются несколько вариантов:
- Стабилизация мембранной протеиновой структуры.
- Предотвращение активации макрофагов (Купферовы клетки в печени).
- Связывание свободных радикалов.
- Модуляция производства цитокинов (подробности в обзоре Хадд, 1998).
Поскольку концентрации глицина в сыворотке уменьшаются после травмы, эндотоксемии и сепсиса (Ашкенази и соавт., 1978, Гарсиа-Мартинц и соавт., 1993, Хоффорд и соавт., 1996), можно предполагать, что глицин в условиях стресса становится условно незаменимой аминокислотой (Халл, 1998). Особый интерес для нутритивной поддержки в ОРИТ составляет предположение, что глицин может защищать печень от ранней дисфункции во время сепсиса, а также, что он может снижать эффекты ишемических/реперфузионных повреждений в кишечнике (Ли и соавт., 2002).
3.3.4.2. Благоприятные эффекты глицина на функцию печени в критических заболеваниях
Печень играет важную роль в метаболизме, гомеостазе и механизмах защиты организма. Было предположено, что печень действует как «мотор» множественной дисфункции органов в критических состояниях (Сухнер и соавт., 2000). Хотя печеночная недостаточность обычно считается более поздним осложнением по сравнению с легочной и почечной недостаточностью при критических состояниях, недавние исследования показали, что гепатоклеточная функция подавляется рано после начала сепсиса и продолжает оставаться таковой во время поздней, гиподинамической стадии сепсиса (Янг и соавт., 2001). Было предположено, что гепатоцеллюлярная дисфункция, наблюдаемая сразу после начала сепсиса, может быть последствием перепроизводства воспалительных цитокинов, таких как TNF-a (Янг и соавт., 2001). Икеджима и соавт. (1996) показали, что глицин-содержащая диета (5% глицина + 15% казеина против 20% казеина) понижала высвобождение провоспалительных цитокинов, снижая повреждение печени и легкого, а также улучшала выживаемость крыс после эндотоксического шока. Авторы сделали вывод, что глицин может быть полезен после травмы и радикальной хирургии, где эндотоксины имеют отчетливый патогненетический эффект. Янг и соавт. (2001) показали в эксперименте, что гепатоклеточная функция была уже подавлена спустя 5 часов на модели сепсиса (сшивание и пункция слепой кишки). Однако внутривенное введение глицина через 1 час после начала сепсиса понижает высвобождение TNF-a и улучшает гепатоклеточную функцию. При этом смертность животных снижается с 50% до 0% (дни 7-10). Шпиттлер и соавт. (1999) продемонстрировали в искусственных условиях, что глицин понижал уровень провоспалительных и повышал уровень противовоспалительных цитокинов в моноцитах крови человека после стимулирования эндотоксином. Модулируя воспалительную реакцию, глицин оказывает положительное действие, защищая клетки печени во время ранней стадии сепсиса и предотвращая смертность при сепсисе (Янг и соавт., 2001).
Кроме того, внутривенное введение глицина у животных защищает печень от реперфузионного повреждения после трансплантации. Подобные результаты были также получены в предварительном клиническом исследовании на человеке (Шеммер и соавт., 2001).
3.3.4.3. Благоприятные воздействия глицина на кишечную функцию в критических состояниях
Манжино и соавт. (1996) сообщили, что предварительная обработка глицином тонкого кишечника донора защищает от гипотемической ишемии перед трансплантацией на животных. Ли и соавт. (2002) продемонстрировали, что локальная перфузия 20% глицином может уменьшить повреждение от ишемии-реперфузии в тонком кишечнике крыс. Авторы постулировали полезные эффекты добавки глицина в ситуациях, где гемодинамическая нестабильность может быть ответственна за нарушение кишечного барьера. Однако глицин не оказал никакого благоприятных воздействия на целостность кишечника в нескольких экспериментальных и клинических исследованиях, оценивающих эффект глутамина и аргинина на функцию кишечного барьера (глицин использовался в качестве контрольного вещества). В недавнем большом клиническом исследовании не выявлен благоприятный эффект дополнения Импакта глицином по сравнению со стандартным Импактом у критически больных пациентов (Рот, 2002).3.4. Дозировка и применение Интестамина
3.4.1. Дозировка Интестамина
Рекомендованная суточная доза Интестамина составляет 500 мл
и содержит 30 г глутамина
1 г трибутирина
1500 мг Витамина С
500 мг Витамина Е
10 мг |3-каротина
20 мг цинка
300 мкг селена
3.4.2. Интестамин — место и время применения Место применения
Предпочтительно рекомендуется применение в просвет тощей кишки из-за часто ухудшенной желудочной подвижности у пациентов в критических состояниях.
Интестамин может быть введен в желудок при условии, что нет желудочной задержки и нет оттока выше 150-200 мл.
Время применения
В отношении времени применения Интестамина следует иметь в виду
a) обеспечить ключевые субстраты для кишечника как можно раньше (смотрите раздел 2.1.).
b) ввести полную суточную дозу ключевых субстратов (смотрите раздел 3.2), независимо от энтеральной переносимости обычных энтеральных формул.
c) поддерживать постоянный уровень ключевых субстратов в просвете кишки и в крови
Следовательно, рекомендуется
- инициировать применение Интестамина в течение 6 часов после травмы или после
хирургии - при условии, что макрогемодинамика стабилизирована.
- подавать Интестамин при постоянной скорости 20-25 мл/час с помощью насоса более 20-24 часов.
- подавать Интестамин отдельно от раствора энтерального питания, например, Реконвана.
Для практики энтерального питания ниже даются 3 предложения в отношении применения Интестамина с помощью насоса и энтерального раствора для питания.
1-ое предложение фактически представляет оптимальный путь применения с учетом целей питания, как они указаны выше. 2-ое и 3-е предложение подразумевает некоторые ограничения, как подчеркнуто ниже. Следовательно, окончательное решение о режиме приема является ответственностью доктора.
1. Одновременное применение энтерального питания с использованием двух насосов
Предпочтительным способом применения было бы использовать
один насос для подачи Интестамина с постоянной скоростью введения 21-25 мл/час - в зависимости от доступных часов для применения Интестамина в сутки; в случае 20 часов/сутки = 25 мл/час, в случае 24 часов/сутки = 21 мл/час и
второй насос для раствора энтерального питания, чтобы адаптировать объём питания к энтеральной переносимости в зависимости от клинического состояния пациента.
2. Одновременное применение энтерального питания с использованием одного насоса
В случае если двух насосов для энтерального введения нет, Интестамин может быть смешан с раствором энтерального питания в мешке для введения, который затем будет подаваться одновременно одним насосом. Это, однако, является альтернативой для одновременного применения с помощью насоса и только тогда, когда может быть ожидаема хорошая переносимость полного энтерального объёма (Интестамин + например Реконван). В случае если переносимость ухудшена и кишечные побочные эффекты требуют снижения скорости энтерального приема, это повлияет как на Интестамин, так и на раствор энтерального питания. Кроме того, по гигиеническим соображениям это не должен быть предпочтительный режим применения.
3. Последовательное применение энтерального питания с использованием одного насоса
Последовательное применение Интестамина и энтерального питательного раствора может рассматриваться как дальнейшая альтернатива доставки с помощью насоса. Например, Интестамин может быть дан в первые 12 часов суток, после чего остальную часть суток будет применяться раствор энтерального питания.
При выполнении этого варианта следует обратить внимание на следующее:
1. Последовательное применение требует более высокой скорости введения как Интестамина, так и раствора энтерального питания, что может повлиять на кишечную переносимость.
2. Последовательное применение подразумевает, что необходимо убрать раствор энтерального питания на несколько часов, а это может вызвать рост метаболических осложнений, в особенности гипоглемических реакций во время лечения инсулином.
3. Последовательное применение, ограничивающее введение Интестамина на несколько часов в сутки, может не позволить поддержать наилучшим образом постоянные уровни Интестамина в просвете кишечника и в крови.
3.5. Режимы кормления Интестамином 3.5.1. Выбор питательных растворов
Эффективное энтеральное фармакопитание с помощью Интестамина требует иного адекватного режима и состава энтерального питания, т.е.
- парентерального фармакопитания с наличием жирных кислот из рыбьего жира с противовоспалительной активностью, а также
- полноты энтерального питания в плане полного удовлетворения потребностей в протеин/аминокислотах, жирах, углеводах, витаминах, минералах и микроэлементах -парентерально и/или энтерально, адаптированного к специфическому состоянию пациента.
Потребности пациента и, соответственно, режимы питания, должны быть определены для каждого пациента отдельно и связаны со следующими факторами:
a) с кишечной переносимостью, а также
b) с метаболической переносимостью, т.е.
- степенью SIRS/стресс метаболизма и/или
- ухудшенным гомеостазом из-за дисфункции органов.
Первой смесью выбора для энтерального питания, которая должна сочетаться с Интестамином, является Реконван, при условии отсутствия медицинских противопоказаний и наличия Реконвана на фармацевтическом рынке. В противном случае могут быть использованы стандартные энтеральные смеси, например, Фрезубин оригинал.
Алгоритм решений для режимов кормления в комбинации с Интестамином (показан на рис.44), должен помочь выбрать режим питания согласно потребностям пациента.
Рис.44: Алгоритм решений для режимов питания в сочетании с Интестамином
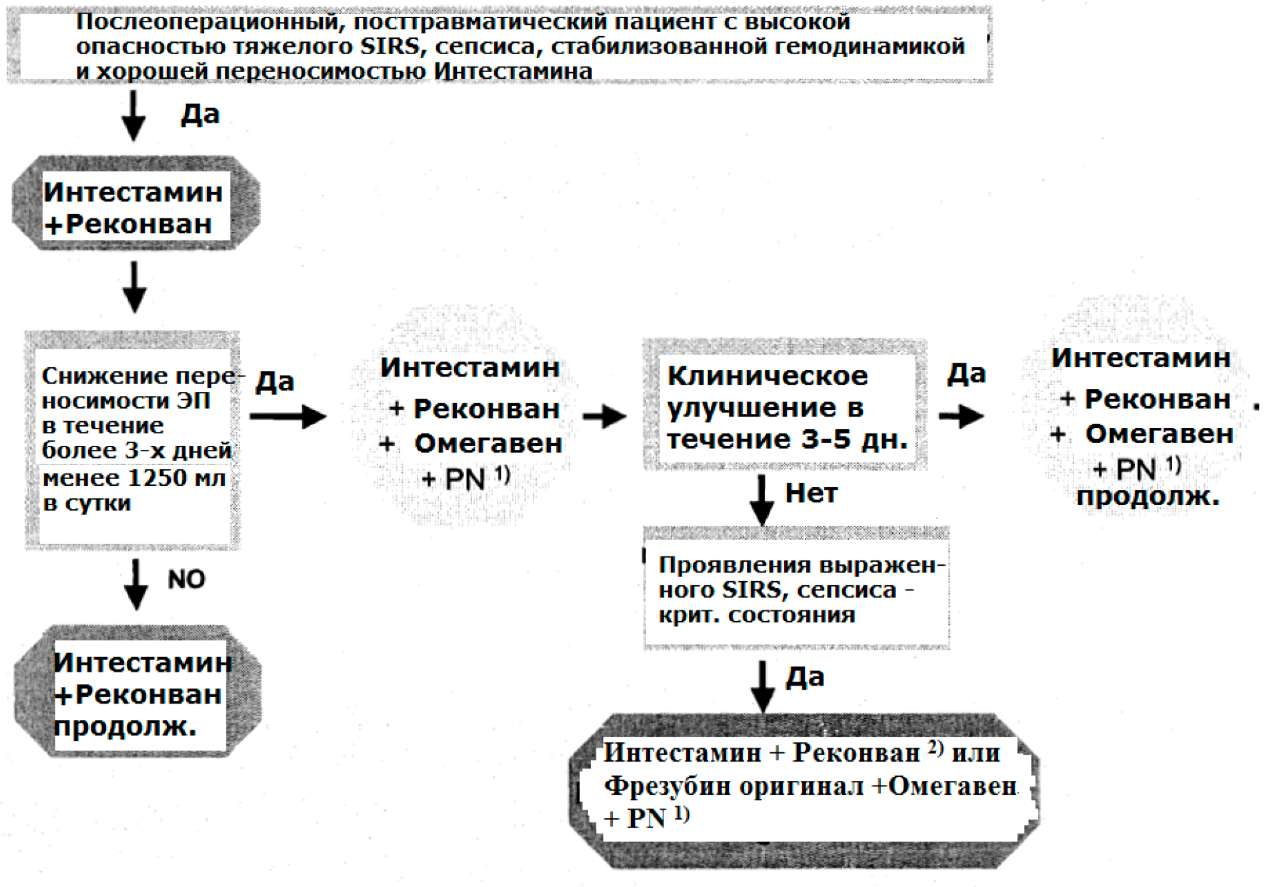
1 PN - со стандартными или адаптированными аминокислотными растворами, такими как
- при печеночной недостаточности Аминостерил N-ГЕПА
- при почечной недостаточности Нефротект
2-* Обычные повышающие иммунитет диеты не рекомендованы для пациентов с тяжелым сепсисом США-Саммит по Иммуноповышающей энтеральной терапии (2001) -следовательно, альтернативно должны быть использованы стандартные формулы.
3.5.2. Интестамин, дополняющий ЭП, ПП или оба случая — как поступать
Интестамин должен быть попеременно использован с ЭП, 1111 или обоими видами питания в зависимости от клинического состояния пациента, и, особенно, от тяжести SIRS и сепсиса. Это может быть почти 100% 1111 при тяжелом SIRS или септическом шоке, но также может означать 100% ЭП - тогда, когда клиническое улучшение становится очевидным. Продолжающиеся повторные проявления тяжелого SIRS и сепсиса могут повторно потребовать уменьшения ЭП и возрастания дозы ПП (см. рис.45).
Рис.45: Дополнение Интестамином ЭП и ПП, в зависимости от клинического состояния пациента
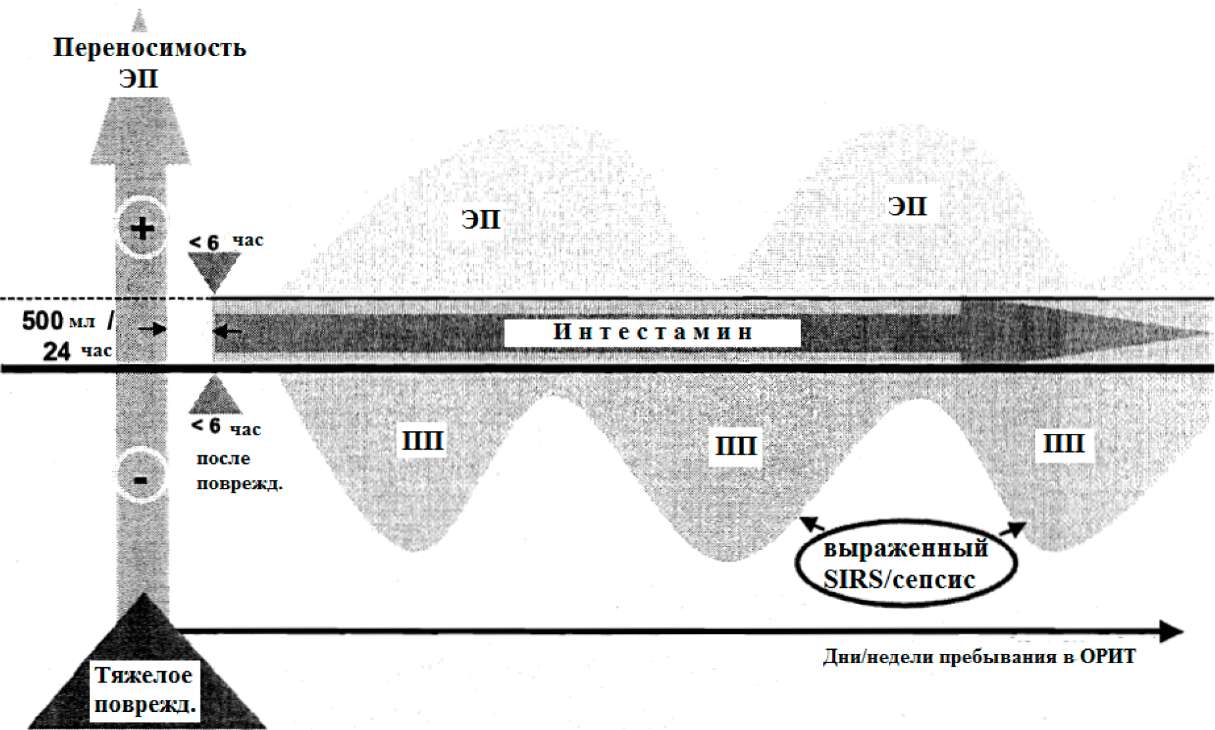
Независимо от потребности в 1111, ЭП или того и другого, Интестамин может вводиться непрерывно с постоянной скоростью из-за малого объёма и легкости всасывания ключевых субстратов, содержащихся в нем, как было показано в исследованиях безопасности и переносимости. Введение Интестамина должено конечно, быть остановлено в условиях наступающих противопоказаний (см. раздел 3.6).
Интестамин, дополняющий ЭП
У пациентов, которым планировалось вводить Интестамин в сочетании только с ЭП (см. рис. 44), его применение должно выполняться первым (см. раздел 3.4.2. «Время применения Интестамина»). Смесь для ЭП, например Реконван, должна даваться как можно раньше в дополнение к Интестамину - обычно начиная на 2-ого дня применения Интестамина. Скорость энтерального питания должна быть повышена согласно обычным рекомендациям, в зависимости от общей кишечной переносимости.
Обратите, пожалуйста, внимание: в случае кишечной непереносимости и необходимости снижения энтерально подаваемого объёма, снижен должен быть только энтеральный питательный раствор (например, Реконван), в то время как прием Интестамина продолжается. Снижение или остановка применения Интестамина обязательны только в случае наступающих противопоказаний для любого энтерального введения.
Интестамин, дополняющий комбинированное ЭП/ПП
Для пациентов, которые нуждаются в комбинированном ЭП/ПП, предлагается следующая процедура:
1. Выполните введение Интестамина в течение 6 часов после травмы или хирургии.
2. Выберите энтеральное питание: Реконван, Фрезубин оригинал (см. раздел 3.5.1 Рис.44).
3. Оцените переносимость энтерального питания: определите статус применимости 250 / 500 / 1000 / 1250 / 1500 мл энтеральной пищи.
4. Оцените метаболическую переносимость: определите полные применяемые количества протеина, жира и углеводов в г/кг веса тела.
5. Выберите растворы парентерального питания для удовлетворения общих потребностей в протеине, жирах и углеводах
6. В случае метаболической непереносимости уменьшите сначала парентеральное питание.
Комментарии
ПРАКТИКА ПЕДИАТРА












