Магний в кардиологической практике
Статьи О.Б. Талибов, В.В. Городецкий, А.Л. ВерткинМГМСУ, кафедра клинической фармакологии
Магний, впервые выделенный английским химиком Гемфри Дэви в 1808 г., является двухвалентным металлом с массой 24,301; в ионизированной форме он представляет собой положительный ион – катион – с зарядом 2+ (Mg++). Вместе с еще 11 основными структурными химическими элементами человеческого организма (углерод, водород, кислород, азот, натрий, калий, кальций, хлор, фосфор, сера и фтор) магний определяет 99% элементарного состава тела. По содержанию в организме он занимает четвертое место среди других катионов (после натрия, калия и кальция), а по содержанию в клетке – второе (после калия).
Mg++ необходим для нормального протекания множества биохимических реакций и физиологических процессов. Ионы Mg++ способны образовывать обратимые соединения с органическими веществами, обеспечивая возможность их участия в разнообразных биохимических реакциях и активируя более чем 300 ферментов. В роли кофактора он принимает участие во многих ферментативных процессах, в частности, в гликолизе, и гидролитическом расщеплении АТФ. Находясь в комплексах с АТФ, Mg++ обеспечивает высвобождение энергии через активность Mg++-зависимых АТФ-аз.
В качестве кофактора пируватдегидрогеназного комплекса Mg++ регулирует поступление продуктов гликолиза в цикл Кребса и этим препятствует накоплению лактата. Он участвует в синтезе и распаде нуклеиновых кислот, синтезе белков, жирных кислот и липидов, в частности, фосфолипидов, а также контролирует синтез ц-АМФ – универсального регулятора клеточного метаболизма и множества физиологических функций.
Mg++ является естественным физиологическим антагонистом ионов кальция (Ca++). В отличие от блокаторов медленных кальциевых каналов он конкурирует с ними не только в структуре мембранных каналов, но и на всех уровнях клеточной системы. На этой конкуренции основано подавление инициированных Ca++ реакций. При изменении внутриклеточного соотношения основных катионов и преобладании Ca++ происходит активация Ca++-чувствительных протеаз и липаз, приводящая к повреждению мембран; благодаря антагонизму с Ca++, Mg++ выступает как мембрано- и цитопротектор. Близким механизмом обусловлена и способность Mg++ уменьшать разобщение дыхания и окислительного фосфорилирования в митохондриях, вследствие чего уменьшаются непроизводительные потери энергии в виде тепла, увеличивается КПД синтеза АТФ и уменьшается потребность клетки в кислороде. Антагонизмом с Ca++ объясняют снижение под действием ионов Mg++ АДФ-индуцированной агрегации тромбоцитов и подавление других кальцийзависимых реакций в каскадах коагуляции крови.
Ионы Mg++ играют важнейшую роль в электролитном балансе и процессах мембранного транспорта, требующего больших энергозатрат. Связываясь с клеточными, митохондриальными и другими мембранами, они регулируют их проницаемость для прочих ионов. Особое значение ионы Mg++ имеют в поддержании трансмембранного потенциала. Активируя Mg++-зависимую Na+-K+-АТФ-азу, они определяют работу K+/Na+ насоса, осуществляющего накопление калия внутри клетки и выведение натрия в межклеточное пространство, обеспечивая таким образом поляризацию мембраны и способствуя ее стабильности. Регуляцией электролитного баланса в клетке объясняется способность Mg++ подавлять автоматизм, проводимость и возбудимость, увеличивать абсолютную и укорачивать относительную рефрактерность миокарда.
Принимая участие в высвобождении требующейся для функционирования мышечной клетки энергии и играя одну из главных ролей в расслаблении миоцита, Mg++ контролирует цикл систола-диастола (рис. 1).
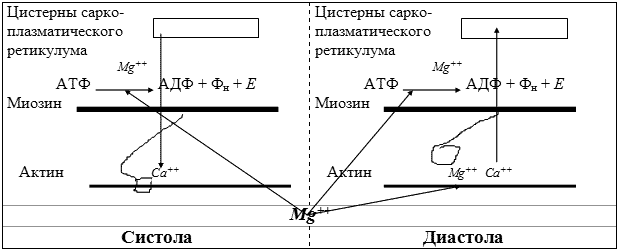
Рис. 1. Регуляция ионами Mg++ цикла “систола-дистола” (гипотетическая схема)
Взаимодействие между четырьмя белками сократительного аппарата кардиомиоцита начинается после поступления в клетку кальция, играющего роль инициатора в образовании из актина и миозина актомиозина. Последний, обладая АТФ-азной активностью, в присутствии Ca++ и Mg++ гидролизует АТФ и обеспечивает энергией сокращение мышцы, то есть систолу сердца. Высвобождаясь из комплекса с АТФ по мере потребления последней, Mg++ вытесняет Ca++ из связи с тропонином С, в результате чего прекращается взаимодействие актина и миозина, и наступает диастола. АТФ-азная активность актомиозина исчезает, а Ca++ с использованием энергии, высвобождающейся под влиянием Ca++-Mg++-зависимой АТФ-азы саркоплазматического ретикулума реабсорбируется против градиента концентрации в полость его продольных канальцев, а оттуда по градиенту концентрации – в цистерны. Таким образом, регуляция цикла “систола-диастола” осуществляется Mg++ как за счет его участия в энергетическом обмене, так и вследствие прямого антагонизма с Са++.
Описанные механизмы играют важную роль в вазодилатирующей активности Mg++, которая, возможно, опосредуется также через синтез ц-АМФ – мощного вазодилатирующего фактора, через подавляющее влияние на РААС и симпатическую иннервацию, а также через усиление натрийуреза вследствие повышения почечного кровотока посредством активации простациклина. В эксперименте было показано подавляющее влияние Mg++ на выброс эндотелина, повышение которого, сопровождая тромбоз коронарной артерии при инфаркте миокарда, приводит к выраженной локальной вазоконстрикции в зоне ишемического риска.
Так же в эксперименте продемонстрировано, что Mg++ ингибирует протромбин, тромбин, фактор Кристмаса, проконвертин и плазменный компонент тромбопластина, а также его антиагрегантное действие.
Среди метаболических функций проявляющихся на уровне целого организма, необходимо подчеркнуть его роль в поддержании нормального липидного спектра, участие в обеспечении ответа тканей на инсулин и торможение гормона паращитовидной железы.
Несмотря на то, что магний широко распространен в природе, его дефицит в человеческой популяции встречается чрезвычайно часто. Так, гипомагнезиемия определяется у 7-11% госпитализированных кардиологических больных, причем в 2 раза чаще у пациентов отделений интенсивной терапии (Weiss, 1995). Тому имеется множество причин. Однако достоверное выявление недостатка магния представляет определенные трудности, в связи с чем его диагностика на практике нередко проводится на основании клинических признаков. Так, если в одном из скрининговых исследований, проведенных в США, было показано, что гипомагнезиемия (уровень сывороточного Mg++ ниже 0,74 ммоль/л) встречалась в 47,1% случаев (Wang, 1990), то клинические признаки магниевого дефицита выявляются более чем у 72% взрослых американцев.
По причинам магниевый дефицит можно подразделить на первичный и вторичный.
I. Первичный (конституциональный, латентный) дефицит магния – в типичной, «эссенциальной», форме проявляется судорожным синдромом, называемым «спазмофилией», «конституциональной тетанией» или «нормокальциевой тетанией». У большей части больных явные клинические симптомы наблюдаются при нормальном содержании Mg++ в крови и связаны с нарушениями трансмембранного обмена Mg++, обусловленными, по-видимому, генетически.
II. Вторичный дефицит магния – явление, присущее практически всем обществам современного мира. Причин тому множество, и они с известным допущением могут быть разделены на 2 большие группы: факторы, зависящие от условий жизни и связанные с различными заболеваниями.
А. Причины магниевого дефицита, связанные с условиями жизни.
Недостаточное поступление с пищей (алиментарный дефицит). Пищевой стандарт, принятый в Росси, странах Европы и Америки, не обеспечивает достаточного поступления Mg++ в организм человека. Это не связано с недоеданием, как в слаборазвитых странах, а обусловлено качественным составом пищи. Как уже указывалось, многие основные пищевые продукты (различные виды мяса и птицы, картофель и др. овощи, молоко и молочные продукты) содержат ограниченные количества Mg++.
В большинстве продуктов с высоким содержанием Mg++ имеется либо много кальция или фосфора, либо белков или жиров, либо всех этих ингредиентов, что препятствует абсорбции Mg++. Многие богатые Mg++ продукты высоко калорийны, поэтому могут употребляться в пищу лишь в ограниченном количестве, не покрывая потребность в Mg++. Всеми этими отрицательными свойствами не обладают шпинат и морская капуста, однако для обеспечения физиологической суточной потребности в Mg++, ежедневно нужно съедать 400-450 г первого или 200 г второй. Казалось бы, как источник Mg++ идеальным продуктом оказывается арбуз, но и здесь можно возразить, что диуретическое свойство арбуза приведет к повышенным потерям электролитов и возрастанию суточной потребности Mg++.
В связи со сказанным современная популяция характеризуется пограничным количеством Mg++ в организме, поэтому, кроме непосредственно алиментарного дефицита, любая дополнительная нагрузка, способствующая затруднению всасывания Mg++, возрастанию его потерь или увеличению суточной потребности, может спровоцировать развитие магниевого дефицита. Среди таких факторов можно назвать гипокалорийные диеты при борьбе с лишним весом; стресс (как острый, так и, особенно, хронический); напряженную физическую работу и физическое перенапряжение; гиподинамию; воздействие высоких температур (жаркий климат, горячие цеха, регулярное посещение парной бани); злоупотребление алкоголем (злоупотребление алкоголем столь широко распространено в современном мире, что, являясь по сути болезнью, в данном контексте должно рассматриваться вместе с другими условиями жизни, а не с патологическими процессами); беременность и лактацию; гормональную контрацепцию.
Б. Причины магниевого дефицита, связанные с патологическими процессами – нарушение абсорбции в связи с возрастными изменениями или заболеваниями ЖКТ (от синдрома малой абсорбции при, например, болезни Крона, до относительно небольших нарушений функции кишечника при хроническом дуодените или субклиническом течении дисбактериоза); проявления сахарного диабета и его осложнения (гипергликемия, полиурия, применение сахароснижающих средств, диабетическая нефропатия с нарушением реабсорбции); гипергликемия любого происхождения (в том числе и ятрогенная); почечный ацидоз, нефротический синдром; гиперкортицизм; гипер-катехоламинемия; гиперальдостеронизм; гипертиреоз; гиперпаратиреоз; гиперкальциемия; артериальная гипертензия; инфаркт миокарда; застойная сердечная недостаточность; факторы риска ИБС, в частности ожирение; передозировка сердечных гликозидов; диуретическая, глюкокортикоидная, цитостатическая терапия.
Дефицит Mg++ проявляется разнообразными клиническими симптомами и синдромами, которые можно сгруппировать следующим образом (табл. 1). Поскольку неоднородность распределения Mg++ в тканях организма делает мало информативным определение его содержания в сыворотке или эритроцитах, заподозрить магниевый дефицит можно на основании сочетания отдельных клинических признаков магниевого дефицита, особенно, если они затрагивают различные системы и наблюдаются на фоне значимого провоцирующего фактора, например злоупотребления алкоголем.
Из множества патологических состояний, возникающих при магниевом дефиците, наиболее полно изучены сердечно-сосудистые заболевания. Инсулинорезистентность, дис- и гиперлипидемии, развивающиеся при дефиците Mg++, должны способствовать ускорению развития атеросклероза, что прогностически особенно неблагоприятно при возникающих при этом повышении активности плазменного ренина и продемонстрированного Pearson et al. (1998) снижения выделения эндотелием вазодилатирующего фактора – окиси азота. Имеются экспериментальные данные о роли дефицита Mg++ в развитии атеросклероза (Jellinek, 1995). Эти факты хорошо объясняют, почему у жителей областей с повышенным уровнем Mg++ в воде отмечается замедление развития атеросклероза и меньшая смертность от этого заболевания. Понятна и известная связь между дефицитом Mg++ в воде и летальностью от острого инфаркта миокарда (Rubenowitz et al., 1996). Необходимо подчеркнуть, что важен не только абсолютный уровень Mg++, но и уровень Ca++: величина отношения Ca++/Mg++ коррелирует со смертностью от проявлений ИБС (Tailor, at al., 1991).
Недостаток Mg++ в воде и пище служит и серьезным фактором риска развития артериальной гипертензии. Кроме самостоятельного вазодилатирущего эффекта ионов Mg++, опосредующегося многими механизмами (см. выше), в условиях магниевого дефицита отмечена повышенная чувствительность артерий к воздействию прессорных аминов.
Весьма существенна роль магния при остром инфаркте миокарда. Потеря ионов Mg++ кардиомиоцитом является его ранней реакцией на ишемию, что приводит к истощению запасов АТФ, угнетению АТФ-зависимых реакций, в том числе угнетению функционирования K+/Na+ помпы и изменению внутриклеточного соотношения основных катионов. Повышение концентрации Ca++ в цитозоле вызывает активацию Ca++-зависимых протеаз и липаз, приводящую к повреждению клетки. До 95 % больных в остром периоде инфаркта миокарда имеют сниженное содержание сывороточного магния (Святов, 1999). Одним из механизмов развития этого феномена можно считать повышенный выброс катехоламинов, который приводит к увеличению содержания свободных жирных кислот, связывающих Mg++ (что наблюдается при любом стрессе).
Дефицит Mg++ с преобладанием Са++ и неконтролируемое вхождение последнего в кардиомиоцит лежит в основе реперфузионного синдрома, развивающегося после медикаментозной, инструментальной или спонтанной реваскуляризации миокарда при остром инфаркте и проявляющегося, прежде всего, нарушениями сердечного ритма.
Как при инфаркте миокарда, так и в других ситуациях внутриклеточный дефицит Mg++ может служить причиной тахикардии и различных аритмий вплоть до фатальных. Выраженный магниевый дефицит сопровождается удлинением интервала QT (что, как известно, ассоциируется с развитием желудочковых нарушений ритма и внезапной смерти) и увеличением «дисперсии» QT (разницы между QTMAX и QTMIN), считающийся еще более надежным признаком высокой вероятности развития нарушений ритма, в том числе и фатальных. Наиболее характерным для дефицита Mg++ вариантом аритмии является желудочковая тахикардия типа «пируэт» (torsade de pointes), а также индуцированные дигиталисом нарушения ритма, пароксизмальная суправентрикулярная аритмия, мономорфная желудочковая тахикардия. У пациентов с инфарктом миокарда выявлена корреляция между дефицитом магния и разнообразными желудочковыми нарушениями ритма.
При застойной сердечной недостаточности магниевый дефицит возникает как результат нейрогуморальных сдвигов (сипато-адреналовой гиперфункции, активации ренин-ангиотензин-альдостероновой системы), застоя в ЖКТ, препятствующего абсорбции Mg++, и усугубляется вследствие диуретической и гликозидной терапии. У больных со сниженным уровнем Mg++ отмечается двукратное увеличение смертности от сердечной недостаточности.
Гипомагнезиемия ассоциируется с повышенной агрегацией тромбоцитов и возрастанием риска тромбозов и эмболий. При недостатке Mg++ ослабляется антиоксидантная защита.
Магниевый дефицит (уменьшение его содержания в мышцах и эритроцитах) обнаружен у больных с пролапсом митрального клапана (Cohen et al., 1986, Durlach, 1994), для которых также характерны нарушения ритма.
Развивающийся при злоупотреблении алкоголем дефицит Mg++ играет определенную роль в формировании многих осложнений хронической интоксикации этанолом (от поведенческих реакций до миопатии) и играет существенную роль в развитии абстинентного синдрома.
В обычных физиологических условиях кинетический цикл Mg++ склаВ обычных физиологических условиях кинетический цикл Mg++ складывается из абсорбции в ЖКТ, распределения в средах организма и элиминации, осуществляемой в основном путем экскреции с мочой.
Всасывание Mg++ может осуществляться во всем кишечнике вплоть до сигмовидной кишки. Его усвояемость из пищевых продуктов составляет 30-35% (то есть из 300-350 мг суточной потребности усваивается около 100 мг). Она может увеличиваться под влиянием витамина В6 и ряда органических кислот (молочной, аспарагиновой, оротовой). Молоко и некоторые молочные продукты, содержащие казеин, также способствуют увеличению абсорбции Mg++ (возможно, в связи с большим содержанием оротовой кислоты).
Абсорбции Mg++ в ЖКТ препятствует большое содержание в пище веществ, с которыми он образует трудно- или нерастворимые соединения – белки, жиры. Всасывание уменьшается также при избытке ионов Ca++, конкурирующих с Mg++ на слизистой кишки, и фосфатов.
Общее количество магния в организме взрослого человека составляет 24-25 г или примерно 1000 ммоль. Наибольшая его часть – 60% – содержится в костях, формируя в содружестве с кальцием их структуру; в случае необходимости отсюда может быть мобилизовано не более 20-30%. Mg++ является типичным интрацеллюлярным элементом – его внутриклеточная фракция составляет 39% всего его запаса (до 80-90% внутриклеточного магния находится в виде комплекса с АТФ, в связи с чем уровень АТФ является одним из основных факторов, лимитирующих накопление этого элемента в клетке). Оставшийся 1% распределяется во внеклеточном пространстве, включая и сыворотку крови, на которую приходится лишь 0,3%.
Наибольшие количества магния содержатся в тканях с наиболее интенсивными обменными процессами. Основная часть его внутриклеточной фракции практически поровну поделена между мозговой и мышечной тканями. При этом наивысшее относительное содержание Mg++ отмечается в миокарде.
Концентрация магния в сыворотке крови составляет в норме 0,75-0,95 ммоль/л, а в клетках может достигать 5-10 ммоль/л. Однако в связи с неоднородностью его распределения в различных тканях внутриклеточная его концентрация варьирует в широких пределах, составляя, например, в эритроцитах лишь 2-2,6 ммоль/л. Содержание магния в сыворотке крови не отражает его запасы в организме, а зависит лишь от интенсивности его движения из депо к почкам. Также мало информативно и его содержание в клеточных элементах крови из-за неоднородности распределения. Поэтому лабораторная оценка магниевого обмена наиболее достоверна, если анализируется экскреция Mg++ с мочой.
Обычно выведение Mg++ из организма осуществляется почками, через которые теряется примерно 100 мг/сут., то есть все всосавшееся из пищи количество. При его дефиците почечная экскреция снижается или прекращается вовсе; при увеличении поступления Mg++ увеличивается и экскреция. Его потери с мочой возрастают под влиянием катехоламинов и кортикоидных гормонов, чем объясняется возможность возникновения магниевого дефицита при стрессе. Существенные количества Mg++ могут теряться и в случае усиления потоотделения при напряженной физической работе или тепловой нагрузке; при этом его потери с потом могут достигать 15%, в то время как в обычных условиях они не превышают 1,5 мг/сут. (последним при анализе магниевого гомеостаза пренебрегают).
Таблица 1. Клинические проявления дефицита магния
| Эндокринно-обменные | Психические и неврологические | Сердечно-сосудистые | Висцеральные (кроме сердечно-сосудистых) | Мышечные |
|---|---|---|---|---|
Mg++ как фармакологическое средство обладает множеством разнообразных клинических эффектов, в частности гипотензивным. антиишесическим, диуретическим и др., а также обилием показаний. В большинстве случаев фармакологическое действие Mg++ проявляется и при отсутствии явных признаков его дефицита. Возможно, это объясняется тем, что при многих патологических процессах развивается вторичный (общий или местный) магниевый дефицит, выступающий одним из патогенетических механизмов, способствуя прогрессированию заболевания и усугублению клинического состояния больного. Получение фармакологических эффектов Mg++ во многих случаях с недоказанным его дефицитом можно связать и с антикальциевым действием.
Положительный эффект препаратов Mg++ наблюдается как при лечении хронических заболеваний (когда Mg++ предупреждает обострения и улучшает качество жизни), так и в ургентных ситуациях (для восстановления нормального осуществления жизненно важных функций). При разных путях введения, обеспечивающих различные концентрации Mg++, на первый план выступают его разные эффекты. Например, если седативное, спазмолитическое и некоторое гипотензивное действие при приеме внутрь проявляются довольно рано, то для заметного влияния на сердце (за исключением ЧСС) в этом случае требуется срок, измеряемый неделями.
Возможности назначения внутрь неорганических солей магния в терапевтических дозах ограничены, в связи со способностью таких доз вызывать диарею. Некоторые органические кислоты, витамины, повышая абсорбцию Mg++ в кишечнике и сокращая его потери с мочой, позволяют, использовать меньшие дозы Mg++ для получения отчетливых резорбтивных фармакологических эффектов. Среди таких факторов особое место занимает оротовая кислота (ОК), не только принимающая участие в магниевом обмене, но и обладающая самостоятельными метаболическими эффектами. К последним нужно отнести активацию синтеза нуклеиновых кислот, обновление миофибрилляреых структур и поддержание высокого содержания АТФ в клетке. Как уже указывалось выше, уровень АТФ определяет возможности клетки накапливать Mg++. Кроме того, благодаря низкой растворимости (и в воде, и в жирах), магниевой соли ОК, ее диссоциация и отщепление Mg++ происходит только интрацеллюлярно. Поэтому магниевая соль оротовой кислоты не только хорошо абсорбируется в ЖКТ, обладая весьма незначительным послабляющим эффектом, но и обеспечивает доставку Mg++ непосредственно в клетку при небольших его потерях с мочой. Таким образом, магниевая соль оротовой кислоты как лекарство должна обладать следующими достоинствами:
- обеспечивать высокую абсорбцию Mg++ в ЖКТ при минимальных гастроинтестинальных побочных эффектах;
- не допускать существенного увеличения экскреции с мочой Mg++;
- обеспечивать накопление Mg++ в клетке;
- сочетать фармакологические эффекты Mg++ и ОК;
- повышать клиническую эффективность как Mg++, так и оротовой кислоты.
Магниевая соль оротовой кислоты выпускается под названием «магнерот» в таблетках по 500 мг (32,8 мг элементарного магния). К настоящему времени накоплен значительный клинический материал об эффективности этого препарата в различных областях медицины и в первую очередь в кардиологии (табл. 2).
Таблица 2. Клинически подтвержденное действие оротата магния (Schmidt, 1998)
| Патологические состояния | Эффекты | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
| ИБС | | Артериальная гипертензия | Суправентрикулярные нарушения сердечного ритма | Левожелудочковая недостаточность | Нарушение липидного обмена | Нарушение углеводного обмена | |
Таким образом, магниевая терапия в кардиологии сегодня имеет надежную теоретическую основу и убедительное практическое подтверждение.
Комментарии
ПРАКТИКА ПЕДИАТРА
