Эффективность краниоспинальной электромагнитной и фармакологической нейромодуляции в лечении дискогенных болей в спине
СтатьиОпубликовано в журнале:
«Врач» 2008, № 7, с. 74-77
А. Воропаев
Государственная медицинская академия, Клиника новейших медицинских технологий «Маймекс», Нижний Новгород
Электромагнитные физические факторы широко применяются для лечения болевых синдромов, в том числе – вертеброгенных [3–7]. Особый интерес представляют способы сочетанной терапии, имеющие ряд преимуществ перед раздельным применением физических факторов, выбор которых осуществляется с учетом принципа синергизма, проникающей способности, индивидуальной переносимости, чувствительности церебральных систем и антисистем [2, 8].
По определению International Neuromodulation Society (INS), нейромодуляция представляет собой терапевтическую активацию различных отделов центральной, периферической или вегетативной нервной системы с помощью электрических факторов или фармпрепаратов.
Нами разработан способ краниоспинальной электромагнитотерапии (КСЭМТ), основанный на сочетанном воздействии электрическим током (транскраниально) и электромагнитным полем (дорсально) низкой частоты (до 550 Гц) с учетом индивидуальных особенностей нейродинамики пациента, и создано устройство для реализации метода (патент на изобретение № 2264234 от 11.05.2005 г.).
При дорсалгиях, сопровождающихся болезненными спазмами мышц, назначают также обезболивающие препараты, оказывающие нейропротективное и миорелаксирующее действие. Один из них – Флупиртин – является первым представителем нового класса лекарственных средств, получивших название SNEPCO (Selective Neuronal Potassium Channel Opener). Препарат имеет центральный механизм действия, но в отличие от опиоидных анальгетиков не вызывает зависимости и привыкания. Наряду с анальгетическими он обладает миорелаксирующими и нейропротективными свойствами.
Анальгетическое действие флупиртина обусловлено преимущественно его непрямым антагонизмом по отношению к N-метил-D-аспартат (NMDA)-рецепторам [10, 13].
В терапевтических дозах препарат способствует открытию потенциалнезависимых калиевых каналов, что приводит к стабилизации мембранного потенциала нервной клетки, вызывает угнетение активности NMDA-рецепторов и, как следствие, – блокаду нейрональных ионных каналов кальция, снижение внутриклеточного тока ионов кальция, угнетение возбуждения нейрона в ответ на ноцицептивные стимулы. В результате нарушается формирование ноцицептивной сенситизации (болевой чувствительности) и феномена «wind up» – повышение выраженности нейронального ответа на повторные болевые стимулы, что, в свою очередь, предотвращает усиление боли и переход ее в хроническую форму, а при уже имеющемся хроническом болевом синдроме ведет к ослаблению боли. Благодаря влиянию на нисходящую норадренергическую систему флупиртин также изменяет восприятие боли [11, 15, 17].
Миорелаксирующее действие препарата связано с блокированием передачи возбуждения на мотонейроны и промежуточные нейроны, что вызывает устранение мышечного напряжения [16, 18, 20].
Нами изучена динамика болевого синдрома у больных с дискогенными радикулопатиями на фоне монотерапии, а также при сочетанном использовании КСЭМТ и фармакотерапии флупиртином (Катадолоном).
В исследование вошел 71 пациент c дискогенной болью в спине (40 мужчин и 31 женщина) в возрасте в среднем 45 лет. Из них 47 человек – пациенты с радикулопатией, получавшие ранее только консервативную терапию со слабым эффектом; 7 – больные, перенесшие оперативное вмешательство по поводу грыжи межпозвонкового диска, у которых длительно сохраняются боли в спине; 17 – больные с радикулопатией, сопровождающейся выраженным астенодепрессивным синдромом. Все больные до исследования получали стандартное для данного заболевания лечение.
По характеру болевые ощущения подразделялись на острые, тупые, жжение, мышечный спазм. Для оценки выраженности болевого синдрома использовались визуальные аналоговые шкалы (ВАШ) боли и эмоционального состояния, методы количественно-качественной оценки боли и тревожности по Спилбергеру – Ханину.
В качестве основного терапевтического воздействия применялся один из предложенных нами способов лечения. Катадолон (фирма «АWD», Германия) назначался больным перорально в дозе 200 мг (2 капсулы) 2 раза в день до еды. Курс лечения составлял от 5 до 10 дней. КСЭМТ проводилась в течение 5–10 дней с помощью аппаратов «СЭТ-01К» и «АМнп-01» по разработанной и запатентованной методике.
Больные были подразделены на 3 группы: в 1-й (n=34) основу лечения составил Катадолон в дозе 200 мг 2 раза в сутки; во 2-й (n=19) – КСЭМТ в аналгезирующем режиме, 7–10 процедур продолжительностью 30–40 мин; в 3-й (n=18) – сочетание КСЭМТ и Катадолона по той же схеме.
В 1-й группе длительность аналгезии после приема Катадолона со ставила в среднем 5,0±0,5 ч (от 4,5 до 5,5 ч). Улучшение отметили 55,7% больных при длительности анальгетического последействия в среднем 6,8±0,5 ч (от 2 до 24 ч). При этом у 5 пациентов наблюдался стойкий регресс болевого синдрома в течение 24 ч (от 4 до 24 ч и более). Полный регресс болевого синдрома после курса лечения имел место у 69,6% больных, а частичный (умень шение болевого синдрома) – у остальных 30,4%. Среднесуточная интенсивность болей, составлявшая до лечения 6,7±0,9 балла, достоверно снизилась до 4,8±0,9–3,8±0,8 балла (рТаблица 1
Выраженность (в баллах) болевого синдрома у больных в процессе лечения по данным ВАШ (М+m)
| Группа | До лечения | После лечения |
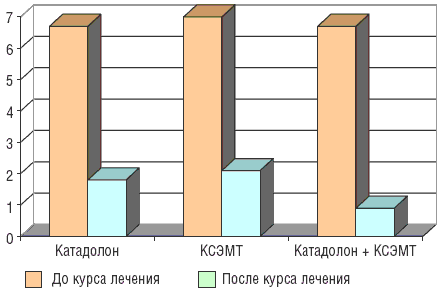
| Катадолон | 6,7±0,9 | 1,8±0,6* |
| КСЭМТ | 7,0±0,6 | 2,1±0,4* |
| Катадолон + КСЭМТ | 6,7±0,8 | 0,9±0,7* |
Примечание. * - здесь и в табл. 2, 3: различия достоверны при р
В процессе лечения изменялся и характер болевого синдрома. Регресс острых «простреливающих» болей после курса лечения наблюдался у 30,6% пациентов. При этом происходило поэтапное изменение характера болевого синдрома: от неприятных, глубинных, жгучих с симпаталгическим оттенком болей к более поверхностным, тупым, ноющим, как правило, – с меньшей зоной распространения. Впоследствии отмечался полный peгресс болевого синдрома. Так, в 42,9% случаев полностью регрессировали стягивающие, распирающие, глубинные боли в пояснице и конечностях. Регресс после курса лечения жгучих болей с неприятным оттенком наблюдался у 8,2% больных, регресс крампи – у 18,4%. Изменялось суточное распределение болей; отмечалась также смена постоянных болей в покое и при движении на периодические и эпизодические, возникавшие при двигательной нагрузке (у 38,8% больных). Ослабление парестетических явлений (ощущение покалывания, онемения, «ползания мурашек» и др.) отметили 30,6% больных, а полный их регресс после курса лечения – 36,7%. Субъективное снижение слабости в ногах после лечения зарегистрировано лишь у 28% больных с корешковыми и нейрососудистыми осложнениями. У больных заметно улучшились эмоциональное состояние (табл. 2) и показатели реактивной и личностной тревожности (табл. 3). Таким образом, эффективность устранения тупой боли составила 73%, острой – 62%, жжения – 90%, мышечных спазмов – 85%. Побочные эффекты (слабость, головокружение, тошнота) отмечались у 13% больных.
Таблица 2
Динамика эмоционального состояния больных (в баллах) с дорсалгиями в процессе лечения по данным ВАШ (М+m)
| Группа | До лечения | После лечения |
| Катадолон | 3,6±0,5 | 7,3±0,3* |
| КСЭМТ | 3,7±0,4 | 7,6±0,5* |
| Катадолон + КСЭМТ | 3,5±0,3 | 8,4±0,4* |
Таблица 3
Динамика реактивной и личностной тревожности (в баллах) у больных в процессе лечения по данным теста Спилбергера - Ханина (М+m)
| Тревожность | Катадолон (n=34) | КСЭМТ (n=19) | Катадолон+КСЭМТ (n=18) | |||
| до лечения | после лечения | до лечения | после лечения | до лечения | после лечения | |
| Реактивная | 45,8±1,1 | 26±0,9* | 48,2±2,9 | 31,4±1,8* | 48,2±3,7 | 47,1±2,1* |
| Личностная | 48,6±0,3 | 33,5±0,4* | 46,8±1,2 | 45,8±1,4* | 49,5±1,2 | 48,7±1,9* |
Во 2-й группе (n=19) длительность анальгетического периода после сеанса составила в среднем 2,0±0,5 ч (от 1 до 3,5 ч). После 5 сеансов КСЭМТ позитивное влияние лечения отметили 85,7% больных при длительности анальгетического последействия в среднем 6,8±0,5 ч (от 2 до 24 ч). При этом у 5 пациентов достигнут стойкий регресс болевого синдрома в течение 24 ч. После полного курса КСЭМТ длительность аналгезии составила в среднем 12,4±0,8 ч (от 4 до 24 ч и более). Полный регресс болевого синдрома после курса лечения наблюдался у 79,6% больных, а частичный (уменьшение болевого синдрома) – у остальных 20,4%. Отрицательных результатов лечения (без перемен или ухудшение) не установлено.
После каждого сеанса КСЭМТ период аналгезии увеличивался. При курсовом воздействии наблюдалось пролонгирование эффекта. Оптимальным оказалось назначение 10 сеансов на курс лечения – так в большинстве случаев достигался наиболее выраженный анальгетический эффект.
Среднесуточная интенсивность болей, составлявшая до лечения 7,0±0,6 балла, достоверно снизилась (рВ процессе лечения изменялся характер болевого синдрома. Регресс острых «простреливающих» болей после курса лечения наблюдался у 30,6% пациентов. При этом происходило поэтапное изменение характера болевого синдрома. Улучшение переносимости болевых ощущений отметили уже после 1-й процедуры КСЭМТ большинство пациентов (79,6%), а после полного курса лечения данный эффект наблюдался у всех больных. Улучшение переносимости болей заключалось в том, что болевой синдром становился менее значимым для больных, как бы отходил на второй план. Появлялись оптимизм, установка на выздоровление и возвращение к труду. Это явилось результатом не только аналгезии, но и влияния КСЭМТ на лимбико-ретикулярный комплекс головного мозга, корректирующий эмоциональную сферу (см. табл. 2). Под влиянием комплексного лечения изменялось суточное распределение болей. Характерным проявлением эффекта стал регресс ночных болей, наблюдавшийся после 1-й процедуры у 32,4% больных, после 5 сеансов – у 54,9%, а после курса лечения – у 73,3%. У 28,3% больных отмечалось также изменение постоянства болей: смена постоянных болей в покое и при движении на периодические и эпизодические, возникавшие при двигательной нагрузке. Уменьшение парестетических явлений (ощущение покалывания, онемения, «ползания мурашек» и др.) отметили 36,6% больных после 5 процедур, а полный регресс этих ощущений после курса лечения выявлен у 39,7%.
В 3-й группе (n=18), где больные получали КСЭМТ и Катадолон, полный регресс болевого синдрома достигнут у большинства (11) пациентов; в 2 наблюдениях динамики не отмечалось. Среднесуточная интенсивность болей, по данным ВАШ, составлявшая до лечения 6,7±0,8 балла, также достоверно уменьшилась (рДинамика болевого синдрома в процессе лечения по данным ВАШ
Катадолон – препарат, эффективный и достаточно безопасный в лечении хронических поясничных болей. Он полезен пациентам с хроническими заболеваниями нервной системы, сопровождающимися болезненными мышечными спазмами (скелетно-мышечные боли в шее и спине, артропатии, тензионные головные боли и фибромиалгии). Катадолон наиболее эффективен в случае наличия в структуре болевого синдрома выраженных мышечно-тонических проявлений. При хронической боли лечение Катадолоном позволяет «стереть» болевую память и снизить болевую чувствительность, препятствует хронизации острой боли.
Сочетание КСЭМТ и Катадолона обеспечивает максимальный эффект в лечении дискогенных болей в спине, что связано с воздействием на разные уровни болевой и противоболевой систем мозга электромагнитных физических факторов и препарата, а также с их синергизмом.
Электромагнитная и фармакологическая нейромодуляция – перспективное направление лечения болевых синдромов, в том числе – невропатических болей, поскольку дает возможность одновременно воздействовать на разные звенья патогенеза боли, активировать противоболевую систему и снизить число лекарственных препаратов, принимаемых больными.
ЛИТЕРАТУРА
1. Белоусова Т. Е. Посттравматическая регенерация нервных ганглиев и возможность ее коррекции пульсирующим магнитным полем. Дис. … канд. мед. наук. – Нижний Новгород, 1992.
2. Готовский Ю. В., Косарева Л. Б., Фролова Л. А. Краткое руководство по индукционной терапии. – М.: Имедис, 1999.
3. Гимранов Р. Ф. Транскраниальная магнитная стимуляция. – М., 2002.
4. Мальцев А. Е. Физические методы в лечении кохлеовестибулярных дисфункций. – Арзамас, 1990.
5. Мясников И. Г. Клинико-физиологическая характеристика магнитотерапии больных с начальными проявлениями сосудистых поражений мозга. Дис. ... канд. мед. наук. – Нижний Новгород, 1991.
6. Трошин О. В. Электроаурикулодиагностика в лечении кохлео-вестибулярных дисфункций. – Горький, 1990.
7. Транскраниальная электростимуляция (экспериментально-клинические исследования) / Под ред. Д. П. Дворецкого. – СПб., 1998.
8. Крыжановский Г. Н. Общая патофизиология нервной системы: Руководство. – М., 1997.
9. Ceccarelli G., Ciampini M., Frontespezi S. Flupirtine: the first Italian experience // Postgrad. Med. J. – 1987; 63 (3): 105–108.
10. Darius H., Schror K. The action of flupirtine on prostaglandin formation and platelet aggregation in vitro // Arzneimittelforschung. – 1985; 35 (1): 55–59.
11. Galasko C. S., Courtenay P. M. et al. Trial of oral flupirtine maleate in the treatment of pain after orthopaedic surgery // Curr. Med. Res. Opin. – 1985; 9 (9): 594–601.
12. Gassen M., Pergande G., Youdim M. B. Antioxidant properties of the triaminopyridine, flupirtine // Biochem Pharmacol. – 1998; 56 (10): 1323–1329.
13. Heusinger J. H. Efficacy and tolerance of flupirtine and pentazocine in two multicentre trials // Postgrad. Med J. – 1987; 63 (3): 71–79.
14. Kornhuber J., Bleich S., Wiltfang J. et al. Flupirtine shows functional NMDA receptor antagonism by enhancing Mg2+ block via activation of voltage independent potassium channels. Rapid communication // Neural Transm. – 1999; 106 (9–10): 857–867.
15. Lorenz B., Schluter T., Bohnensack R. et al. Effect of flupirtine on cell death of human umbilical vein endothelial cells induced by reactive oxygen species // Biochem Pharmacol. – 1998; 56 (12): 1615–1624.
16. Mastronardi P., D'Onofrio M., Scanni E. et al. Analgesic activity of flupirtine maleate: a controlled double-blind study with diclofenac sodium in orthopaedics // Int Med. Res. – 1988; 16 (5): 338–348.
17. McMahon F. G., Arndt W. F. Jr., Newton J. J. et al. Clinical experience with flupirtine in the U.S. // Postgrad. Med. J. – 1987; 63 (3): 81–85.
18. Osborne N. N., Cazevieille C., Pergande G. et al. Induction of apoptosis in cultured human retinal pigment epithelial cells is counteracted by flupirtine // Invest Ophthalmol Vis Sci. – 1997; 38 (7): 1390–1400.
19. Ringe J. D., Miethe D., Pittrow D. et al. Analgesic efficacy of flupirtine in primary care of patients with osteoporosis related pain. A multivariate analysis // Arzneimittelforschung. – 2003; 53 (7): 496–502.
20. Rupalla K., Cao W., Krieglstein J. Flupirtine protects neurons against excitotoxic or ischemic damage and inhibits the increase in cytosolic Ca2+ concentration // Eur. J. Pharmacol. – 1995; 294 (2–3): 469–473.
21. Szelenyi I., Nickel B. Pharmacological profile of flupirtine, a novel centrally acting, non-opioid analgesic drug // Agents Actions. – 1991; 32: 119–123.


