Азитромицин (Сумамед): основные свойства, оптимизация режимов применения на основе фармакокинетических и фармакодинамических параметров
СтатьиОпубликовано в журнале:
АНТИБИОТИКИ И ХИМИОТЕРАПИЯ »» 2003, 48; 2
Все исследования сделаны на субстанции азитромицина производства компании «Плива», Хорватия.
С. В. ЯКОВЛЕВ, С. А. УХИН
ММА им. И. М. Сеченова, Институт хирургии им. А.В.Вишневского РАМН, Москва
В начале 90-х годов прошлого столетия был получен и внедрен в клиническую практику полусинтетический антибиотик азитромицин — первый представитель новой подгруппы макролидных антибиотиков — азалидов, в структуре лактонного кольца которого содержится атом азота [1]. Такая перестройка молекулы эритромицина придала полученному соединению новые свойства, включающие расширение спектра антимикробного действия, создания высоких уровней в тканях и клетках, значительно превышающих концентрации в крови (тканевая направленность фармакокинетики), и другие свойства, существенно отличающие его от антибиотиков группы макролидов.
Антимикробный спектр. Наряду с сохранением активности в отношении грамположительных кокков, азитромицин* превышает по активности эритромицин против Haemophilus influenzae, Moraxella catarrhalis, Neisseria spp., Campylobacler jejuni, Helicobacter pylori, Borrelia burgdorferi. Он активен также в отношении некоторых энтеробактерий: значение его МПК90 в отношении Salmonella, Shigella, E.coli колеблется в пределах 4—16 мг/л. Азитромицин проявляет активность в отношении некоторых «атипичных» микроорганизмов, а также внутриклеточно расположенных возбудителей — Chlamydia spp., Mycoplasma spp. и др. (табл. 1) [1, 2].
Фармакокинетика. Азитромицин более стабилен, чем эритромицин, при различных значениях рН. После приема однократной дозы в желудке всасывается более 37% азитромицина по сравнению с 25% эритромицина. Пища или одновременное применение антацидов снижает биодоступность азитромицина, в связи с чем его следует принимать по крайней мере за 1 час до или через 2 часа после приема пищи.
Концентрация азитромицина в тканях и клетках превышает обнаруживаемую в крови в 10—100 раз; он внутриклеточно концентрируется в лизосомах. Среднее значение Т1/2 азитромицина составляет 2—4 дня. При рекомендуемых режимах лечения (3 и 5 дней) в эффективных концентрациях поддерживается в течение 7 и более дней после отмены препарата.
Азитромицин быстро включается в клетки белой крови (полинуклеары, моноциты, лимфоциты), в высоких концентрациях и длительно обнаруживается в альвеолярных макрофагах, фибробластах. При миграции в очаг инфекции полинуклеары играют транспортную роль, обеспечивая высокий и длительно сохраняющийся уровень антибиотика в тканях и клетках [3].
Азитромицин не метаболизируется в организме больного; не подавляет изоэнзимы системы цитохрома Р450. Из организма больного выводится преимущественно с калом и частично (~ 20%) с мочой. Коррекция режимов лечения азитромицином при умеренной почечной недостаточности не требуется [4].
Значение фармакокинетики (ФК) и фармакодинамики (ФД) при выборе режимов терапии
В течение многих лет антибактериальная активность антибиотика измерялась in vitro с помощью дисков, пропитанных антибиотиком (так называемый диско-диффузионный метод) или методом серийных разведений в жидкой питательной среде. В последние годы использовали Етест (полуколичественный). Значения минимальных подавляющих концентраций (МПК), получаемые методом серийных разведений, сравнивали с концентрациями антибиотиков, достигаемыми в крови, которые создаются при их введении в стандартных дозах. Эти данные использовали для прогноза эффективности лечения по клиническим и микробиологическим показателям, оценивая получаемые результаты в категориях степени чувствительности штаммов возбудителей (чувствительные, умеренно чувствительные, устойчивые). Антибактериальная активность препарата оценивалась путем сравнения его МПК в отношении выделенного патогена и степени превышения ее концентрацией антибиотика в крови[5].
Таблица 1.
Сравнительная активность in vitro азитромицина и эритромицина ([1, 2], модифицированная)
|
Микроорганизмы |
МПК9о, мг/л |
|
|
азитромицин |
эритромицин |
|
|
Грамположительные аэробы |
||
|
Staphylococcus aureus |
||
|
метициллиночувствительные (MSSA) |
1,0 |
0,25-0,5 |
|
метициллинорезистентные (MRSA) |
> 128,0 |
> 128,0 |
|
S.epidermidis метициллинорезистентные — (MRCNS) |
> 128,0 |
> 128,0 |
|
Streptococcus pyogenes труп п ы А |
0,12 |
0,03 |
|
S.pneumoniae |
0,12 |
0,03-1,0 |
|
Грамотрицательные аэробы |
||
|
Haemophilus influence |
1 ,0 |
4,0-8,0 |
|
Moraxella catairhalis |
0,5 |
0,25-2,0 |
|
Legionella pneumophila |
0,12-2,0 |
0,25-2,0 |
|
Campylobacter Jejuni |
0,12-0,5 |
1-2,0 |
|
Helicobacter pylori |
0,25 |
0,25 |
|
Neisseria spp. |
0,15 |
0,25-2 |
|
Анаэробы |
||
|
Грамположительные кокки (Peptococcus, Peptostreptococcus) |
2 |
2->32 |
|
Clostridium perfringens |
1 |
1 |
|
Bacteroidesfragilis |
8 |
4-32 |
|
Внутриклеточные возбудители |
||
|
Chlamydia pneumoniae |
0,12-0,25 |
0,06-1 |
|
C.trachomatis |
0,12-0,25 |
0,12-0,25 |
|
Mycoplasma pneumoniae |
0,001 |
0,004 |
|
Borrelia burgdorferi |
0,015-0,04"^ |
0,06-0,12 |
|
Mycobacterium avium complex (MAC) |
32 |
64 |
|
M.fortuitum |
0,5-2,0 |
8 |
В современных условиях появления и распространения антибиотикорезистентных возбудителей, особенно среди грамположительных микроорганизмов, устойчивых практически ко всем группам антибиотиков, выбор эффективных препаратов и схем антибактериальной терапии затруднен. Оптимизация терапии возможна в каждом случае на основе определения чувствительности выделенного возбудителя к отобранному препарату, бактерицидности препарата — величины разрыва между его МПК и уровнем концентрации в крови — основных показателей, определяющих эффективность, переносимость, предотвращение развития устойчивости [6, 7]. В настоящее время наиболее часто применяемыми при лечении инфекций препаратами являются беталактамы, аминогликозиды, макролиды, гликопептиды и др. Каждая их этих групп отличается особенностями антимикробного действия, фармакокинетики и путями реализации антимикробного эффекта.
Беталактамы характеризуются возможностью создания высоких уровней в крови, хорошим распределением в тканях, жидкостях организма, экстрацеллюлярном пространстве. Аминогликозиды по бактерицидности действия подобны беталактамам, но в отличие от них накапливаются в тканях, где длительно обнаруживаются после окончания лечения. Однако это свойство характеризует их специфическую ото- и нефротоксичность, но не эффективность лечения. Макролиды, и особенно азитромицин, даже при введении в максимальных дозах создают низкие концентрации в крови, но обладают высоким проникновением в полинуклеары (фагоциты), ответственные за клиренс патогенов из очага инфекции и кровяного русла.
Уникальность свойств макролидов, и прежде всего азитромицина, может быть оценена и объяснена только на основе анализа полученных фармакокинетических данных и расчетных фармакодинамических показателей, выявляющих несоответствие при определенных режимах применения между низкой концентрацией антибиотика в крови и его высокой клинической эффективностью при устойчивости возбудителя. Другим примером недооценки возможностей ФК и ФД явилось быстрое формирование устойчивости к фторхинолонам в результате их назначения в дозах без учета фармако-кинетических свойств [7—9].
В настоящее время для большинства групп антибиотиков для оптимизации эффективности антибактериальной терапии и коррекции режимов лечения используются следующие основные фармакокинетические и фармакодинамические критерии:
- величина отношения максимальной концентрации препарата в крови к минимальной подавляющей (ингибирующей) концентрации — Cmax/MIC;
- величина отношения площади под фармакокинетической кривой препарата к его МПК — AUC/MIC;
- время, в течение которого концентрация антибиотика в крови превышает значение его МПК (оптимально этот промежуток времени должен быть не менее интервала дозирования — Т>МIС).
Рис. 1.
Фармакокинетические/фармадинамические параметры, прогнозирующие эффект антибиотика .
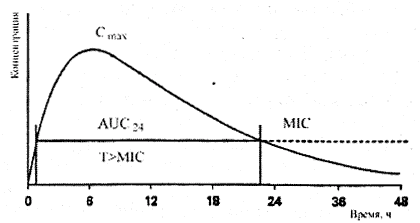
Для антибиотиков с выраженной зависимостью эффекта от максимального уровня концентраций в крови (разовой дозы препарата) Cmax/MIC и AUC(1_24/MIC являются главными параметрами, определяющими эффективность лечения. Это аминогликозиды и фторхинолоны. Величина доз для этой группы препаратов ограничена уровнем максимальных концентраций в крови, превышение которых сопровождается повышением частоты возникновения побочных реакций [6, 10]. К антибиотикам, эффект действия которых не так прочно связан с Cmax, а зависит от времени сохранения концентраций на уровне, превышающем значение МПК для выделенного возбудителя (Тэфф > 50% интервала между дозами), относятся беталактамы, природные макролиды и др. И, наконец, для антибиотиков со слабой зависимостью эффекта от уровня концентраций в крови, с пролонгированной фармакокинетикой (доксициклин, азитромицин и другие полусинтетические макролиды) предиктором клинического эффекта служат значения AUC0-24/MIC и Тэфф> MIC (рис. 1) [11, 12].
Данный подход применим ко всем антибиотикам, в том числе и новым, поскольку на его основе можно на ранних этапах доклинического и клинического изучения оптимизировать режим лечения, снизить опасность развития побочных реакций, предупредить формирование резистентности [4]. Таким образом, выбор антибиотика, максимизация режимов и схем его применения в клинике включает ряд этапов: оценку спектра действия и антимикробной активности; определение основных параметров ФК и ФД, выбор наиболее эффективного антибиотика из ряда оцениваемых; рекомендация оптимальных режимов лечения. Оценка результативности предложенной схемы на ранних этапах лечения по комплексу клинических и микробиологических данных позволяет скорректировать схемы терапии с целью повышения ее эффективности и минимизации побочных эффектов.
В последние годы для основных групп антибиотиков — аминогликозидов, беталактамов и фторхинолонов, применяемых в монотерапии или в сочетаниях установлены оптимальные значения соотношений ФК/ФД - Cmax/MIC, AUC0-24/MIC, Т>МIС, когда эффективность и бактерицидность действия четко зависят от Сmах, определяющей величину разовой дозы (ее соответствие MIC); AUC0-24/MIC — величину полной суточной дозы. Для аминогликозидов значение соотношения Cmax/MIC должно быть не более 8 из-за опасности развития токсических эффектов, характерных для этой группы антибиотиков. У фторхинолонов оптимальными соотношениями является для Cmax/MIC > 10, для AUC0-24/MIC >125.
Для беталактамов, гликопептидов и тетрациклина коррекция дозирования осуществляется путем оценки интервала дозирования, в течение которого концентрация в сыворотке крови превышает MIC. Этот промежуток времени должен составлять не менее 50% их интервала дозирования (Т>50%).. Падение концентрации антибиотика в крови ниже эффективного уровня может быть предотвращено своевременным введением повторной дозы антибиотика.
Кроме прямого антимикробного действия на микробную клетку, некоторые антибиотики отличаются наличием дополнительных эффектов, усиливающих их эффективность в условиях макроорганизма; среди них:
- постантибиотический эффект (ПАЭ), проявляющийся в отсутствие эффекта возобновления роста бактерий, несмотря на выведение антибиотика из организма. Он присущ фторхинолонам, ами-ногликозидам, макролидам и тетрациклинам [13];
- субингибирующий эффект, однако его трудно использовать в схемах терапии, поскольку применение антибиотиков в субингибирующих концентрациях может быть причиной возрастания к нему устойчивости. Его применяют как тест при оценке распределения бактериальной популяции по степени антибиотикочувствительности и доли в ней резистентных особей, высокое число которых может свидетельствовать о признаках формирования устойчивости [14];
Рис. 2.
Концентрация (в мг/л) азитромицина в гранулоцитах после его применения в дозе 500 мг в течение 3 дней [20].
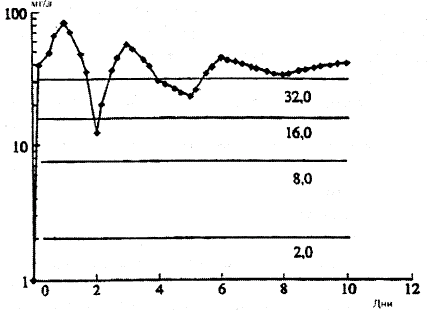
Горизонтальными линиями представлены значения МПК для потенциальных патогенов.
При ПАЭ достаточной продолжительности (1—4 часа и более) рекомендуется изменять режим лечения: уменьшать число введений таких антибиотиков в течение суток [15].
Фармакокинетика и фармакодинамика азитромицина
В отличие от беталактамов и аминогликозидов, клиническая эффективность которых прогнозируется на основе расчета параметров ФК и ФД и обусловлена ее тесной зависимостью значений МПК и уровня концентраций антибиотика в крови, такой подход в полной мере не может быть использован для прогноза эффективности азитромицина, поскольку не учитывает фармакокинетики препарата в тканях. Даже для чувствительных к азитромицину штаммов S.pneumoniae (МПК < 0,5 мг/л) его концентрация в крови превышает МПК для этого возбудителя лишь в течение короткого периода после приема антибиотика. В связи с низкой концентрацией азитромицина в крови прогнозируемый клинический эффект, основанный на расчете только данного показателя (Cmax/MIC), будет отрицательным практически при всех значениях МПК в отношении данного возбудителя. Тем более он будет отрицательным всегда при лечении азитромицином инфекций, вызванных устойчивыми штаммами S.pneumoniae (МПК > 2 мг/л), стрептококков других видов, а также H.influenzae и др., поскольку концентрация азитромицина в крови ниже значений МПК для большинства возбудителей, даже при его приеме в максимальных дозах [16].
Однако вопреки ожидаемому, положительный клинический эффект наблюдается и в отсутствие
оптимальных соотношений МПК для выделенного возбудителя и уровня концентраций азитромицина в крови. То есть критерии фармакодинамики установленные для аминогликозидов — Cmax/MIC, для фторхинолонов — AUC(0_24/MIC и Т > MIC в течение > 50% времени интервала дозирования — для беталактамов, недостаточны для прогноза эффективности азитромицина, поскольку при прогнозе его эффективности оцениваются не только клинические, но и микробиологические показатели (полнота эрадикации возбудителя из очага инфекции) [17, 18].
Внутриклеточная кинетика азитромицина
В отличие от других макролидов азитромицин характеризуется высоким внутриклеточным и тканевым проникновением. В клетках белой крови и очаге инфекции он задерживается в течение 7 и в более дней при стандартном режиме дозирования в течение 3 или 5 дней. Антибиотик концентрируется в полинуклеарах, моноцитах, лимфоцитах, альвеолярных макрофагах, фибробластах. Пик концентрации антибиотика в гранулоцитах составляет > 80 мг/л. В еще более высоких концентрациях препарат обнаруживается в моноцитах и фибробластах (100 мг/л). После прекращения лечения азитромицином на 7— 10-й день его внутриклеточная концентрация еще превышает 32 мг/л (рис. 2) [18]. В связи с особенностями химического строения азитромицин концентрируется в «кислых» органеллах фагоцитов, в лизосомах. Высокая и длительно сохраняющаяся внутриклеточная концентрация антибиотика очень важна с клинической точки зрения, позволяя максимизировать AUC0-24/ MIC в очагах локализации бактерий, в которых он ведет себя как «концентрация-независимый киллер». Благодаря слиянию лизосом (место накопления антибиотика в клетке) с фагоцитами («хранилище» захваченных фагоцитами бактерий) и образованию фаголизосом в клетках крови, в инфицированной ткани антибиотик обнаруживается длительно и в высоких концентрациях. Тем самым оптимизируется значение AUC0_ 24/MIC не только в отношении чувствительных (МПК < 0,2 мг/л), но и устойчивых микроорганизмов (МПК > 32 мг/л) — кокков, H.influenzae, атипичных внутриклеточно расположенных С.рпеиmoniae, C.trachomatis, Mycoplasma pneumonias, Mycobacterium avium complex и др. [20].
Изучение действия азитромицина на формирование устойчивости к нему у микроорганизмов при его применении в клинике в оптимальных дозах показало, что в концентрациях в крови 0,2—0,6 мг/л, т. е. характерных для данного антибиотика, он действует как пусковой механизм возрастания устойчивости возбудителя. Тем не менее присутствие его в крови, тканях, иммунокомпетентных клетках больных в течение длительного времени после отмены лечения, не способствует росту и распространению устойчивости [21]. У больных при оптимальных режимах лечения наблюдают быструю элиминацию возбудителя, благодаря высокой концентрации препарата в клетках белой крови, повторному выходу его в системный кровоток и длительной экспозиции с бактерицидными концентрациями препарата.
Таблица 2.
Фармакокинетические параметры азитромицина в сыворотке крови при его однократном введении внутрь (1,5 г) или в течение 3 дней [27]
|
Оцениваемые параметры |
Режим введения |
|
|
единственная доза (1, 5 г) |
три дозы по 500 мг в сутки |
|
|
Cmax> мг/л. |
1,46 |
0,54 |
Таблица 3.
Средние значения пиков концентраций в полинуклеарах и моноцитах /лимфоцитах при экспозиции с азитромицином, вводимым внутрь в единственной дозе (1,5 г) или по 0, 5 г в течение 3 дней [27]
Тип клеток | Оценивемый параметр | Режим введения | |
1,5 г однократно | по 0,5 г в течение 3 дней | ||
Полинуклеары | Сmах, МГ/Л AUC24o- мг-ч/л | 41,1 6447 | 31,3 5128 |
Моноциты/лимфоциты | Сmax, мг/л АUС24о, мг-ч/л | 312,7 20461 | 164,9 15706 |
Клинические данные о сохранении эффективности препарата в этих условиях совпадали с наблюдениями in vitro — в опытах по селекции резистентности у 7 свежевыделенных штаммов пневмококков после 5 пересевов на среды с возрастающими концентрациями азитромицина, ампициллина и цефаклора. Развитие устойчивости к азитромицину не наблюдали ни в одном случае, тогда как (^ампициллину и цефаклору выявлено развитие устойчивости у 6 из 7 изученных штаммов.
Следует отметить, что устойчивость нормальной микрофлоры орофарингеальной области или желудочно-кишечного тракта часто развивалась в течение курса лечения азитромицином и другими макролидами, однако она имела транзиторный характер и не сопровождалась возникновением инфекций [22, 23]. Предположения, высказываемые на протяжении 10 лет лечения инфекций новыми макролидами, о возможном риске развития бактериемии или об отсутствии клинического результата при применении азитромицина, вследствие длительного контакта возбудителя с субингибирующими концентрациями антибиотика, не были документированы бактериологически, а обнаруживаемые в редких случаях бактерии были идентифицированы как Klebsiella sp. или Proteus sp., и характеризовались природной устойчивостью к макролидам.
Несмотря на то, что макролиды являются бактериостатиками, проблема резистентное™ для них не стояла так остро до последнего времени. Ситуация резко изменилась в последние годы. Быстрый рост устойчивости к макролидам среди пневмококков и (менее выраженный) у пиогенных стрептококков явился причиной ограничения их применения как препаратов первой очереди при респираторных инфекциях. Однако исследования in vivo показали, что предиктор эффекта Т > МПК в течение принятого интервала дозирования является достаточным, чтобы обеспечить бактерицидный эффект [24]. Учитывая необходимость этого показателя для оценки эффекта можно рассчитать оптимальные дозы в случае выделения чувствительных возбудителей.
Возникновение резистентное™ к современным макролидам может впрямую не зависеть от субингибирующих концентраций в крови, прскольку важную роль в обеспечении эффекта играют внутриклеточные концентрации антибиотика. Вместе с тем недостаточное тканевое проникновение может способствовать выживанию умеренно чувствительных возбудителей и развитию реинфекции. В связи с этим рассматривается возможность достижения более полного соответствия эффективных концентраций азитромицина в крови его клиническому эффекту путем изменения режимов дозирования (увеличение однократно вводимой дозы) [25, 26].
Интерес представляют работы по изучению клинической эффективности, переносимости и фармакокинетики азитромицина, применяемого внутрь в двух режимах:
- по 500 мг один раз в сутки в течение 3 дней (всего 1,5 г);
- однократно в дозе 1,5 г (табл. 2, 3).
Из табл. 2 и 3 видно, что основные фармакокинетические параметры (Cmax, AUC0-00) при однократном введении высокой дозы (1,5 г) азитроми-
цина превышают наблюдаемые при 3-дневном режиме приема антибиотика в той же суммарной дозе (1,5 г). То же относится и к показателям клеточной кинетики: Cnm и AUC,4o полинуклеаров и, особенно, моноцитов и лимфоцитов при однократном приеме антибиотика в дозе 1,5 г существенно превышают наблюдаемые при его 3-дневном режиме введения в той же курсовой дозе. Следует подчеркнуть одинаковую эффективность (98% выздоровление) и переносимость (частота побочных реакций 5%) препарата при этих схемах. К числу важных преимуществ короткого режима применения азитромицина относятся также его высокая комплаентность, практическое отсутствие рецидивов заболевания, меньшая частота развития резистентное™, меньшие трудозатраты на обслуживание больного и др. [27, 28].
Фармакодинамические модели, используемые при оптимизации режимов терапии различными антибиотиками, не могут объяснить, почему, несмотря на нарастание в мире устойчивости пневмококков к макролидам, в том числе и современным, продолжает сохраняться их клиническая эффективность. Особенности клеточной кинетики макролидов, и особенно азитромицина, раскрывают механизм этого феномена. Азитромицин легко проникает в полиморфноядерные лейкоциты, моноциты и другие клеточные элементы крови, накапливается в них в высоких концентрациях, переносится в очаг инфекции, где возбудитель подвергается воздействию бактерицидных концентраций препарата. Защитные механизмы организма хозяина, работая в тандеме с антибиотиком, обеспечивают быструю эрадикацию возбудителя и клинический эффект — даже при значениях МП К азитромицина 32 мг/л для фагоцитированного возбудителя. То есть фармакодинамика азитромицина при приеме внутрь обеспечивает эффективность препарата при значениях его МПК до 32 мг/л. Ее основными параметрами для азитромицина и других новых макролидов является AUC0-oo/MIC и Т > MIC, учитывая чувствительность возбудителя выделенного не только из очага инфекции, но из кровотока, подвергнутого воздействию фагоцитов, нагруженных антибиотиком.
Заключение
Внедрение в клиническую практику азитромицина и других полусинтетических макролидов пролонгированного действия с высоким клеточным и тканевым проникновением, характеризующихся расширенным спектром антибактериального действия, обусловливает необходимость привлечения с целью оптимизации лечения, наряду с МПК, дополнительных параметров — фармакокинетических и фармакодинамических.
В настоящем обзоре представлены данные по оптимизации терапии лишь для азитромицина, поскольку он в наибольшей степени по особенностям фармакокинетики (тканевой и клеточной) и наиболее удобному применению (однократный, 3-, 5-дневный режим введения) превосходит кларитромицин и, особенно, эритромицин. С позиций клеточной фармакокинетики (длительное сохранение в полинуклеарах и, особенно, в моноцитах и фибробластах высоких концентраций антибиотика: Сmax — 80—100 мг/л, Cmin — 32 мг/л в течение 7— 10 дней после окончания стандартного 3-дневного применения в суммарной дозе 1,5 г) объясняется клиническая эффективность азитромицина даже при инфекциях, вызываемых устойчивыми штаммами грамположительныхвозбудителей (МПК > 2 мг/л), при МАС-инфекции с уровнем чувствительности Mycobacteriumavium-intracelulare к азитромицину 32 мг/л. Значение отношений ФК/ФД является ключом, помогающим перевести параметры, характеризующие антимикробную активность, на клиническую ситуацию и обеспечить достижение высокого клинического эффекта.
Основой эффективной антибактериальной терапии является достижение баланса концентраций антибиотика в крови и тканях, варьирующих во времени, для обеспечения максимальной эрадикации возбудителя и минимизации частоты развития побочных эффектов. Для азитромицина, характеризующегося высоким клеточным проникновением, длительной пролонгацией (тканевой и клеточной), наряду с обычными параметрами ФК и ФД, необходима информация о уровне и продолжительности сохранения его в клетках после завершения курса терапии, формализуемая параметрами AUC24/MIC и Т > MIC.
Таким образом, применительно к азитромицину необходимо учитывать показатели Сmax, AUC0-24 и Т >МIС, с точки зрения их связи с клинической эффективностью и токсичностью, возможности их использования для прогноза правильности выбора доз, режимов терапии, ее продолжительности, а также общей оценки результатов лечения, в том числе инфекций, вызываемых устойчивыми штаммами возбудителей.
ЛИТЕРАТУРА
1. Моеllering R. С. Revolution changes in the macrolide and azolide antibiotics. Am J Med 1991; 9): Suppl ЗА: 1—4.
2. Neu H. C. Clinical microbiology of azithromycin. Ibid; 12—18.
3. Schenlag J. J., Hallow C. H. Tissue directed pharmacokinetics. Ibid; 5—
Eisenberg E., Barza M. Azithromycin and clarithromycin. Curr din Top Infect Dis 1994; 14; 52-59.
Amsdem G. W., Duran J. M. Interpretation of antibacterial susceptibility reports. In viliv versus clinical break-points. Drugs 2001; 6: 12: 163— 166.
6. Craig W. A. Choosing on antibiotic of the basis of pharmacodynamics. Ear Nose Throat J 1998; 77: Suppl 6: 7-12.
7. Schenlag J. J. Antimicrobial action and pharmacokinetics/pharmacodynamics: the use of AUIC to improve efficacy: and avoid resistance. J. Chemotherapy 1999; 11: 426—439.
8. MacGowan A. P., Bowker К. Е' Pharmacodynamics of antimicrobial agents and rationale for their dosing. Ibid; 1997: 9: Suppl 1:64—73.
9. Modal J. High-dose intravenous fluoroquinolones in the treatment of severe infections. Ibid 1999; 11: 478-485.
10. Hyatt J. M., McKinnon P. S., Zimmer G. S. el al. The importance of pharmacokinetics/pharmacodymamics surrogate markers to outcome focus antibacterial agents. Clin Pharmacokinet 1995; 28: 143—160.
11. Nightingale С. Н. Pharmacokinctics and pharmacodynamics of newer macrolides. Pediatr Infect Dis J 1997; 16: 438—443.
12. Van Bambeke F., Tulkens P. M. Macrolides: pharmacokinetics and pharmacodynamics. Intern J Antimicrob Agents 2001; 18: 17—23.
13. Li R. S., Lee S. W., Kong С. Н. Correlation between bactericidal activity and postantibiotic effect for five antibiotic with different mechanisms of action. J Antimicrob Chemother 1997; 40: 39—45.
14. Cars O., Oilenholt-Torngvist Y. The postantibiotic sub-MIC effect in vitro шй in vivo. Ibid; 1992: 31: 159-166.
15. McDonald P. J., Weterhall B. L., PruulH. Postantibiotic of bacteria pretreatmed with antibiotics to activity of leucocutes. Rew Infect Dis 1981; 3: 38-44.
16. Amsden G. W. Pharmacological considerations in the emergence of resistance. Int J Antimicrob Agents 1999; 1: Suppl I: 7—14.
17. Carbon C. Clinical relevance of intracellularand extracellular concentration of macrolides. Infection 1995; 23: Suppl I: 10—14.
18. Yshiguro M., Koga H., Konno S. et al. Penetration of macrolides into human polymorphonuclear leucocytes. J Antimicrob Chemother 1989; 24:719-729.
19. Amsden G. W. Pneumococcal macrolides resistance — myth or reality. Ibid; 1999; 44: I—6.
20. Hot H. Intracellular microorganismus a particular problem chemotherapy. Infection 1996; 19: Suppl: 193-195.
21. Cauchie P., Hubloux A., Crokaerl F. Determination azithromycin concentration in plasma during a six-week period. Presented at the 4th International Conference on the Macrolides, Azalides. Streptogramins and Ketolides. 1998. Barselone. Abstr 10. 10.
22. Relsema J. A., Girard A. K., Brennan Z. A. et al. Lack of emergence of significant resistance in vitro and in vivo to the new azalide antibiotic azithromycin. Eur J Clin Microbiol Infect Dis 1991: 10: 843—846.
23. Guggenbichler J. P., Kastner U. The influence macrolide antibiotics on the normal flora. Infect Med 1998; 15: Suppl A: 15—22.
24. Wenisch C. Pharmacokinetic effects of antibiotics on the development of bacterial resistant particulary in reference to azithromycin. Wien Med Wochenschr 2000; 150: 37-41.
25. Peters D. H., Friedel H. A., Tavisch M. C. D. Azithromycin: A review of its antimicrobial activity, pharmacokinetic properties and clinical efficacy. Drugs 1992; 44: 750-799.
26. Burgges.4 D. S. Pharmacodynamic principles of antimicrobial therapy in the prevention of resistance. Chest 1999; 105: Suppl 3: 19—23.
27. Amsden G. W., Gray C. L. Serum and WBC pharmacokinetic of 1500 mg of azithromycin when given as a single close over a 3 clay period in heathy volunteers. J Antimicrob Chemother 2001; 47: 61—66.
28. Schonuald S., KuznmnJ., Oreskovic K. etal. Azithromycin: single 1.5g dose in the treatment of patients with atypical pneumonia! syndromes — randomized study. Infection 1999; 27: 198—202.
Поступила 14.11.02
Комментарии
ПРАКТИКА ПЕДИАТРА
