Биопарокс в лечении респираторных инфекций у больных аллергическим ринитом и бронхиальной астмой
СтатьиОпубликовано в журнале:
Вестник оториноларингологии, 5, 2007
Н.А. Арефьева
Bioparox in the treatment of respiratory infections in patients with allergic rhinitis and bronchial asthma
N.A. ArefyevaКафедра оториноларингологии (зав. — проф. Н.А. Арефьева) Башкирского государственного медицинского университета, Уфа
Воспалительные заболевания уха, горла и носа различного характера являются актуальной проблемой для врачей многих специальностей. Тактика лечения пациентов с респираторной патологией определяется многими факторами, в том числе возбудителем заболевания, механизмами реагирования иммунной системы и др. Необходимость комплексной оценки болезни очевидна, так как ошибки в лечении могут приводить к затяжному течению или хронизации воспаления, развитию побочных реакций, переходу заболевания в новое качество [1—3].
Особого внимания заслуживают два на первый взгляд совершенно разных состояния, такие как инфекция и аллергия. Каждое из этих заболеваний имеет свои этиологические факторы, патогенетические механизмы, соответственно которым определяется тактика лечения. Однако по существу у этих процессов теоретически велика вероятность неразрывного единства противоположностей [1, 4, 5]. Это единство противоположностей в научных исследованиях рассматривается с разных позиций, в частности, с позиции изучения роли аллергии в инфекционном процессе [6, 7]. Известно, что большинство случаев инфекционных заболеваний респираторной системы имеют вирусную этиологию. После 3—4-го дня может присоединиться бактериальная инфекция. Таким образом, аллергическое воспаление является фактором, предрасполагающим к колонизации бактериями, что объясняет возрастание числа пациентов с хроническим бактериальным риносинуситом и сопутствующей аллергией. Оперативное лечение этих больных дает слабые результаты.
С другой стороны, вирусная респираторная инфекция относится к числу факторов, усугубляющих течение респираторной аллергии. Повреждение эпителия вирусом способствует раздражению чувствительных нервных волокон, которые стимулируются, формируя гиперреактивность слизистой респираторной системы.
Иммунный ответ под влиянием респираторных вирусов характеризуется прежде всего их депрессивным влиянием на макрофаги. При этом блокируются внутриклеточные бактерицидные процессы, что предопределяет предрасположенность к бактериальной инвазии [8, 9].
Большинство осложнений респираторной вирусной инфекции связано с формированием вирусно-бактериальных ассоциаций. Установлена зависимость между гриппозной инфекцией и вторичной бактериальной флорой (пневмококк). При паратонзиллярной патологии имеется сочетание пневмококка или бета-гемолитического стрептококка с вирусом Эпштейна—Барр. При микстинфекции происходит суммация патологических проявлений и видоизменение клиники заболевания.
Определена роль респираторных вирусов в формировании синдрома гиперреактивности бронхов (ГРБ). Установлено, что риновирус является этиологическим фактором ГРБ и обострения бронхиальной астмы у детей. Эти вирусы могут быть одной из причин смерти детей-астматиков. Сочетания аллергического ринита (АР) и респираторной вирусной инфекции значительно усиливает формирование бронхиальной астмы (БА).
Доказано, что вирусные инфекции могут вызывать комплекс аллергических реакций I и II типов, первично инициируя или усиливая атопическую предрасположенность организма. Современная концепция БА трактует астму как хронический воспалительный процесс, в патогенезе которого общепризнана этиологическая роль гриппа и других респираторных инфекций. В частности, БА может инициировать РС-инфекция. Отмечен выраженный реагиновый ответ на инфекцию, вызванную вирусом Эпштейна—Барр. Обнаружены специфические IgE антитела к вирусам гриппа, парагриппа и др.
Обострение БА на фоне острой респираторной вирусной инфекции наблюдается отсроченно по отношению к инфекционному заболеванию, к концу 3—4-х суток ОРВИ или концу 1-й нед. Нарастание неспецифической гиперреактивности бронхов коррелирует с развитием вирусно-бактериальных ассоциаций, формирование которых является распространенным вариантом болезни, достигающим 100% у больных с инфекционнозависимой БА.
Учитывая сказанное, целью исследования явилось изучение микробного представительства слизистой оболочки носа и глотки под влиянием антимикробного препарата биопарокс (фузафунжин) при респираторной инфекции у больных АР и БА.
Исследование выполнено в отделениях муниципальной больницы №21 Уфы: аллергологическом, оториноларингологическом и в бактериологической лаборатории.
Материал и методы
Клинические (изучались жалобы больного, анамнез заболевания, предшествовавшее лечение, его эффективность), эндоскопические (риноскопия, фарингоскопия, ларингоскопия, по показаниям — бронхоскопия), для идентификации и определения антибактериальной резистентности использовали микробиологический анализатор АТВ Expresion (Франция) и дискодиффузный метод (ДДМ), функцию внешнего дыхания определяли прибором пикфлоуметром. Исследования проводились до и после достижения клинического результата. Данные вносились в специально разработанную анкету.
Были обследованы 35 пациентов. Из них 10 (группа контроля) и 25 больных АР и БА, из которых 10 человек имели аллергическую форму заболевания и 15 — неаллергическую. У всех больных наблюдались тяжелое течение БА и гормонозависимость.
В качестве базовой терапии использованы классические схемы лечения, включающие традиционные препараты: гормоны, бронхолитики, муколитики, дезагреганты и др. В комплекс классических методов лечения в группе наблюдения (25 человек) включали местное воздействие на слизистую носа и глотки биопарокса по 4 вдоха 4 раза в сутки в течение 5 дней.
Причиной обострения БА служила острая респираторная инфекция. Динамика субъективных ощущений больных АР и БА в процессе лечения отражена в таблице.
Как видно из таблицы, при первичном обращении у больных преобладали симптомы гиперреактивности слизистой респираторной системы в виде чиханья (80% случаев), сухого непродуктивного кашля (64%), сухости и дискомфорта в горле (48%); бронхоспазм (52%).
Динамика субъективных ощущений больных АР и БА при лечении биопароксом
| Симптом | Частота встречаемости, % | |
| До лечения | После лечения* | |
| Чиханье | 80 | 20 |
| Зуд в носу | 40 | 8 |
| Затрудненное дыхание | 52 | 16 |
| Сухость, дискомфорт в горле | 48 | 12 |
| Kашель сухой, непродуктивный | 64 | 16 |
Результаты и обсуждение
Положительный результат в группе контроля отмечен после 6-го дня лечения, в группе наблюдения — после 4-го. Сохранялись симптомы гиперреактивности и бронхоспазма: чиханье в 20% наблюдений, кашель — в 16%, затруднение дыхания — в 16%.
Динамика ринологических симптомов по данным эндоскопического исследования представлена на рис. 1. Использование биопарокса в комплексном лечении респираторной инфекции у больных АР и БА характеризовалось уменьшением отека слизистой оболочки с 52 до 16% случаев. Состояние микроциркуляции определялось цветом слизистой носа. Отек слизистой носа до лечения отмечен в 92% случаев, после лечения — в 12%. Выделения слизисто-гнойные до лечения отмечены в 56% случаев, после лечения экссудация в синусах сохранялась только в 8%.
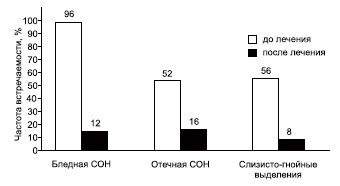
Рис. 1. Динамика ринологических симптомов в процессе лечения биопароксом
На рис. 2 представлены общие сведения о количестве бактерий, сохраняющих чувствительность к антибиотикам до и после лечения. Изучение чувствительности выделенных микроорганизмов к антибиотикам показало, что в группе контроля возросло число резистентности к антибиотикам. При этом в группе наблюдения бактерии сохраняли чувствительность к антибиотикам. Имелась тенденция к росту чувствительности с 45,2 до 54,7%.
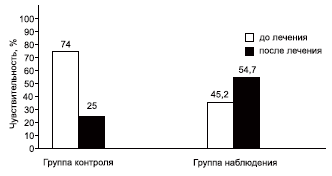
Рис. 2. Чувствительность микробов к антибиотикам
Спектр антибиотиков, к которым менялась чувствительность, представлен на рис. 3.
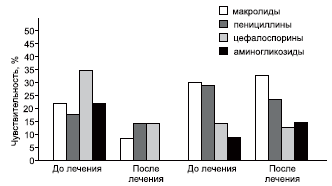
Рис. 3. Чувствительность микробов к различным антибиотикам
В группе контроля у больных АР и БА на фоне ОРВИ, получавших традиционную терапию, микроорганизмы на слизистой глотки до лечения имели чувствительность к цефалоспоринам в 35% случаев, несколько меньше к остальным антибиотикам: макролидам (22%), пенициллинам (18%), аминогликозидам (22%).
После лечения резистентность отмечена к аминогликозидам, снизилась чувствительность у макролидов до 8%, к пенициллинам и цефалоспоринам — до 13%.
В группе наблюдения после лечения статистически значимых отличий в росте числа случаев резистентности микроорганизмов к наиболее часто используемым антибиотикам не отмечено.
Представлялось важным изучить динамику микробного представительства на слизистой верхних дыхательных путей у больных АР и БА на фоне ОРИ.
Как видно из рис. 4, а до лечения у больных со слизистой оболочки носа и глотки высевалась преимущественно условно-патогенная флора — 80%. После традиционного лечения число патогенов на слизистой оболочке глотки возросло в 2 раза.
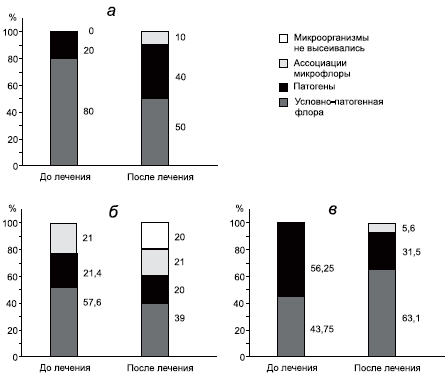
Рис 4. Микрофлора слизистой оболочки носа больных АР и БА, леченных без использования биопарокса — а; и с биопароксом (б — аллергическая форма и в — неаллергическая форма ринита)
Результаты лечения больных, которые наряду с традиционным получали биопарокс местно на слизистую оболочку верхних дыхательных путей антибиотик биопарокс, представлены на рис.4, б, в. При аллергической форме заболевания до лечения преобладала условно-патогенная флора (57,6%), патогенная — в 21,4% случаев. После лечения количество патогенов не возрастало, а в 20% случаев микроорганизмы не высевались.
У больных неаллергической (инфекционной) формой БА до лечения на слизистой оболочке глотки преобладала патогенная флора (56,25%). После лечения количество патогенов сократилось до 31,5%, а число условно- патогенной флоры возросло до 63,1% случаев.
Состояние бронхиальной обструкции оценивалось по результатам пикфлоуметрии (рис. 5).
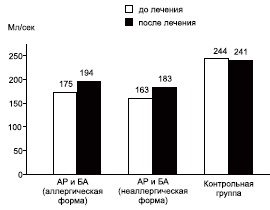
Рис. 5. Данные пикфлоуметрии больных АР и БА.
Статистически значимых отличий в зависимости от метода лечения не обнаружено. Однако в группе комбинированной терапии с включением биопарокса имелась тенденция к уменьшению бронхиальной обструкции.
Таким образом, современная классификация заболевания слизистой оболочки респираторной системы включает основные формы иммунного воспаления: инфекционную и аллергическую. При инфекционном варианте используются преимущественно препараты антибактериального действия [2], при аллергии — антимедиаторные (антигистаминные и др.) и глюкокортикоиды [10, 11]. Использование антибиотиков в лечении пациентов с атопической сенсибилизацией практически не рассматривается [12].
Результаты исследования показали, что у всех больных острой респираторной инфекцией до лечения независимо от формы заболевания (аллергическая и неаллергическая) имелись одинаковые, как субъективные, так и объективные клинические проявления, в том числе у 56% больных присутствовали слизисто-гнойные выделения из носа. Гнойное отделяемое, как симптом микробной инфицированности, подтверждался бактериологическим исследованием.
Использование классических препаратов (глюкокортикостероиды) в лечении обострений респираторной аллергии сопровождалось возрастанием числа резистентных штаммов микроорганизмов на слизистой оболочке верхних дыхательных путей. Назначение топического антибиотика биопарокс (фузафунгин) обеспечивало сохранение чувствительности флоры к антибиотикам. Уменьшилась обсемененность слизистой патогенной флорой.
Значимость полученных результатов мы видим в следующем: у больных с аллергической патологией респираторной системы на фоне острых респираторных инфекций отмечается утяжеление течения основного заболевания — АР и БА, что требует применения гормональных средств. Они снижают интенсивность аллергических проявлений болезни, но при этом возрастает риск активации инфекционного агента, даже если микроб относится к числу условно-патогенной, колонизирующей флоры.
Учитывая, что заселение слизистой оболочки бронхов в известной степени определяется микроорганизмами, присутствующими на слизистой верхних дыхательных путей, становится очевидной необходимость снижения числа патогенов в верхних отделах респираторной системы. Применение топического антибактериального препарата биопарокс на слизистую оболочку носа и трахеи позволяет уменьшить число патогенных микроорганизмов, сохранить их чувствительность к антибиотикам.
Таким образом, проблема резистентности микроорганизмов вызывает большую тревогу у специалистов [13, 14], поэтому наличие препарата, к которому не развивается резистентность микроорганизмов, к тому же обладающему противовоспалительным и иммуномодулирующим действием, привлекает особое внимание врачей и ученых-медиков [10, 13, 15]. Эффективность биопарокса при острых респираторных инфекциях подтверждена в ряде публикаций; наши исследования также показали безопасность и эффективность этого препарата в лечении острых респираторных заболеваний у больных АР и БА.
Следовательно, как показали исследования, применение биопарокса в лечении острой респираторной инфекции у больных АР и БА облегчает субъективные ощущения больных. Кроме того, после комплексного лечения с применением биопарокса на слизистой верхних отделов респираторной системы уменьшается число патогенов и ассоциированного микробного представительства, не возрастает резистентность к основным группам антибиотиков (пенициллинам, цефалоспоринам, макролидам).
Сказанное позволяет рекомендовать использование антибактериального препарата биопарокс при острой респираторной инфекции у больных АР и БА.
Литература
