Бисопролол - высокоселективный ?-адреноблокатор: клиническая фармакология и опыт при лечении сердечно-сосудистых заболеваний
Статьи Опубликовано в журнале:«CONSILIUM MEDICUM»; ТОМ 11; № 10; стр. 138-143.
Д.В.Преображенский, И.Д.Вышинская, Н.И.Некрасова
Московская медицинская академия им. И.М.Сеченова
Симпатико-адреналовая система (САС) регулирует функции внутренних органов. Ее регуляторная функция опосредуется катехоламинами, которые воздействуют на α- и β-адренорецепторы. Различают два основных катехоламина -норадреналин (норэпинефрин) и адреналин (эпинефрин). Норадреналин высвобождается в основном из окончаний постганглионарных симпатических нервов и стимулирует αи β1-адренергические рецепторы, тогда как адреналин высвобождается из мозгового слоя надпочечников и стимулирует α -, β1- и β2-адренорецепторы. Вызываемые катехоламинами разнообразные физиологические и биохимические процессы не всегда полезны, и, в частности, при таких сердечно-сосудистых заболеваниях (ССЗ), как ишемическая болезнь сердца (ИБС), артериальная гипертензия (АГ) и хроническая сердечная недостаточность (ХСН), ослабление эффектов катехоламинов может быть полезным. Это способствовало созданию блокаторов α- и β-адренорецепторов. В клинической практике наиболее широкое распространение получили блокаторы β-адренергических рецепторов, которые используются в течение почти 50 лет.
Первый β-адреноблокатор (БАБ) дихлоризопротеренол был создан в конце 1950-х годов, однако из-за выраженной внутренней симпатомиметической активности (ВСА) он оказался непригодным для клинического применения. В 1964 г. опубликованы первые сообщения о применении неселективного БАБ без ВСА пропранолола при лечении стенокардии напряжения и АГ.
В последующие годы были созданы несколько десятков лекарственных препаратов со свойствами БАБ, из которых лишь около 10 выдержали испытание временем. В клиническую практику вошли лишь такие препараты, которые имели какие-либо преимущества перед неселективным БАБ без ВСА пропранололом, например, наличие β1-селективности и сосудорасширяющих свойств.
Блокаторы β-адренергических рецепторов, обладающие β1-селективностью (атенолол, бетаксолол, метопролол и др.), получили название БАБ II поколения по контрасту с БАБ I поколения пропранололом. Блокаторы β-адренергических рецепторов II поколения значительно различаются друг от друга степенью β1-селективности, а также некоторыми другими фармакокинетическими и фармакодинамическими свойствами, многие из которых имеют клиническое значение.
Одним из наиболее β1-селективных БАБ без ВСА является бисопролол, который по степени β1-селективности значительно превосходит самые популярные в мире БАБ атенолол и метопролол.
Цель обзора - рассмотреть клиническую фармакологию бисопролола и опыт его использования при разных ССЗ.
Клиническая фармакология бисопролола и других БАБ
Для лучшего понимания клинического значения отличий бисопролола от других доступных БАБ необходимо рассмотреть основы фармакологии БАБ.
Как известно, БАБ представляют собой весьма неоднородную по своим фармакологическим эффектам группу лекарственных препаратов, единственным общим свойством которых является конкурентный антагонизм в отношении β1-адренергических рецепторов. Наряду с блокадой β1-адренергических рецепторов БАБ могут блокировать или не блокировать β2-адренорецепторы. В первом случае говорят о неселективных БАБ, во втором - о β1-селективных препаратах.
Сравнительная характеристика блокады β1- и β2-адренорецепторов
Первоначально БАБ создавались для лечения стенокардии напряжения путем уменьшения потребности миокарда в кислороде. Поскольку в миокарде преобладают β1-адренергические рецепторы (более 70%), а в бронхах и сосудах - β2-адренорецепторы, неудивительно, что при ИБС более безопасны препараты, способные блокировать β1-адренорецепторы сердца, но не блокирующие β2-адренорецепторов бронхов и сосудов, которые опосредуют полезные для организма бронхо- и вазодилатацию соответственно. Дальнейшие исследования показали, что некоторые эффекты блокады β2-адренорецепторов также могут быть полезными (см. таблицу).
| Преимущественная органная локализация двух основных типов БАБ и главные эффекты их блокады | ||
| Локализация | Тип β-рецепторов | Эффекты блокады |
| Сердце | β1 | |
| β2 | ||
| Сосуды | β1+β2 | |
| β1 | ||
| β2 | ||
| Бронхи | β1 | |
| β2 | ||
| Почки | β1 | |
| β1+β2 | ||
| Окончания симпатических нервов | β1 | ? |
| β2 | ||
| Головной мозг | β1 | |
| β2 | ||
| Поджелудочная железа | β1 | ? |
| β2 | | |
| Печень | β1+β2 | |
| β2 | | |
| Жировая ткань | β1+β2 | |
| Матка (при беременности) | β1 | ? |
| β2 | | |
| Скелетные мышцы | β1 | ? |
| β2 | | |
Тем не менее не вызывает сомнений, что подавляющее большинство фармакологических эффектов, связанных с блокадой β2-адренорецепторов, при сердечно-сосудистых заболеваниях бесполезно или даже нежелательно. Это означает, что β1-селективные препараты более перспективны при лечении ССЗ, чем неселективные БАБ без дополнительных свойств, область клинического применения которых неуклонно сужается [1-4].
Преимущества β1-селективности
Нарушения центральной гемодинамики у больных АГ и ХСН характеризуются повышенным общим периферическим сосудистым сопротивлением (ОПСС), которое объясняется рефлекторной активацией САС, а также ренин-ангиотензин-альдостероновой системы. Дальнейшее повышение ОПСС, вызываемое стимуляцией адреналином β2-адренорецепторов сосудов, которые опосредуют вазоконстрикцию, нежелательно ни при АГ, ни особенно при ХСН. По этой причине при длительном лечении этих заболеваний β1-селективные препараты, безусловно, более полезны, чем неселективные БАБ без дополнительных свойств. По некоторым наблюдениям, антигипертензивное действие β1-селективных препаратов несколько более выражено, чем действие неселективных БАБ. Кроме того, при лечении β1-селективными блокаторами вазоконстрикторная реакция на катехоламины выражена слабее, чем при лечении неселективными препаратами. Эта вазоконстрикторная реакция на катехоламины, иногда проявляющаяся резким подъемом АД, наблюдается при психоэмоциональном стрессе, курении сигарет, употреблении кофеина (с кофе или чаем), гипогликемии (у больных сахарным диабетом), а также после внезапной отмены клонидина и других агонистов центральных α2-адренорецепторов [1, 3].
В отличие от неселективного БАБ пропранолола β1-селективные адреноблокаторы (в частности, бисопролол, а также ацебутолол и метопролол) не оказывают существенного влияния на увеличение кровотока в предплечье, вызываемое изопротеренолом, и поэтому более безопасны у больных с перемежающейся хромотой. Бисопролол редко вызывает побочные эффекты, связанные с ухудшением кровообращения в конечностях (похолодание конечностей, ощущение тяжести в ногах и др.), а если такие побочные эффекты наблюдаются, то считается, что они обусловлены уменьшением сердечного выброса [1, 5].
β1-Селективные адреноблокаторы более безопасны у больных с хронической обструктивной болезнью легких (ХОБЛ), чем неселективные БАБ, причем чем выше β1-селективность препарата, тем меньшее влияние он оказывает на функцию дыхания. В частности, у больных ХОБЛ бисопролол в терапевтических дозах (5-20 мг/сут) не увеличивает сопротивления воздухоносных путей и не уменьшает объема форсированного выдоха за 1-ю секунду, даже на максимуме действия препарата. Функция легких ухудшается лишь после назначения 30 или 40 мг бисопролола, которые не рекомендуются для клинического применения. В отличие от бисопролола (20 мг) менее β1-селективный препарат атенолол (100 мг) несколько увеличивает сопротивление воздухоносных путей у больных ХОБЛ. В перекрестном исследовании показано, что у больных бронхиальной астмой сопротивление воздухоносных путей уменьшается после приема плацебо, не изменяется после приема бисопролола (10 и 20 мг), но увеличивается после приема атенолола (100 мг). У больных бронхиальной астмой бисопролол также не ослабляет бронхорасширяющий эффект β2-агониста тербуталина [1, 5, 6].
Все это доказывает, что бисопролол является высокоселективным БАБ, более β1-селективным, чем атенолол.
Неселективные БАБ, блокируя β2-адренорецепторы β-клеток поджелудочной железы, уменьшают секрецию инсулина, что сопровождается повышением базальных уровней глюкозы. Кроме того, ослабляя вазодилатацию в скелетной мускулатуре, которая опосредуется β2-адренорецепторами сосудов, они уменьшают чувствительность периферических тканей к действию инсулина. По некоторым наблюдениям, БАБ, особенно в комбинации с тиазидными диуретиками, увеличивают риск развития сахарного диабета (СД) у больных АГ [7, 8].
Учитывая, что у 20-30% больных АГ или ХСН имеется СД, неселективные БАБ не рекомендуется использовать для длительного лечения, если только они не обладают α-адреноблокирующими свойствами. Кроме того, неселективные БАБ не рекомендуется использовать в качестве антигипертензивных или антиангинальных препаратов у больных с предрасположением к развитию СД, т.е. у больных с ожирением и СД в семейном анамнезе.
В отличие от неселективных БАБ β1-селективные адреноблокаторы, в частности бисопролол, не оказывают существенного влияния ни на секрецию инсулина, ни на чувствительность тканей к инсулину [1, 5-7, 9]. По данным литературы, у больных СД типа 2 терапия бисопрололом (10 мг/сут) не оказывает существенного влияния на содержание глюкозы в крови, уровни гликозилированного гемоглобина и глюкозурию [5].
Мобилизация глюкозы из печени в ответ на гипогликемию опосредуется в основном β2-адренорецепторами. Поэтому гипогликемические реакции на инсулин или пероральные антидиабетические средства у больных СД при лечении β1-селективными блокаторами встречаются гораздо реже, чем при лечении неселективными препаратами. По некоторым наблюдениям, β1-селективные блокаторы, в частности бисопролол, не усиливают гипогликемии, вызванной инсулином [5-7, 9].
В отличие от неселективных БАБ β1-селективные блокаторы оказывают незначительное влияние на уровни общего холестерина (ХС) и ХС атерогенных липопротеинов (ЛП) низкой плотности, но увеличивают концентрации триглицеридов, а также снижают уровни ХС антиатерогенных ЛП высокой плотности (ЛПВП). Бисопролол вызывает менее значительные изменения липидного состава крови, чем другие β1-селективные препараты. В частности, в одном исследовании концентрации триглицеридов повышались на 25% при лечении бисопрололом и на 40% - при лечении атенололом. В другом исследовании концентрации триглицеридов повышались, а уровни ХС ЛПВП при лечении атенололом и пропранололом, однако не изменялись при лечении бисопрололом [5, 6].
В экспериментальных исследованиях показано, что β1-селективные блокаторы (в отличие от неселективных БАБ) не изменяют или даже увеличивают фибринолитическую активность крови. Это объясняется тем, что β1-селективные блокаторы в терапевтических дозах не оказывают существенного влияния на функцию β2-адренорецепторов, которые опосредуют высвобождение тканевого активатора плазминогена из эндотелиальных клеток. В то же время как β1-селективные, так и неселективные БАБ блокируют β1-адренорецепторы, которые опосредуют высвобождение ингибитора тканевого активатора плазминогена 1-го типа [5, 6].
При длительной терапии АГ немаловажное значение имеет лучшая переносимость β1-селективных блокаторов. В частности, частота таких побочных эффектов, как усталость, слабость, повышенная утомляемость, при лечении β1-селективными блокаторами ниже, чем при лечении неселективными БАБ. Это связано с тем, что β1-селективные препараты не влияют на кровообращение и метаболизм в скелетных мышцах.
Учитывая благоприятные гемодинамические, бронхиальные и метаболические эффекты β1-адреноблокаторов, они больше подходят для длительной терапии АГ или ХСН, чем неселективные БАБ, особенно у больных с сопутствующими ХОБЛ, СД, ожирением, атерогенной дислипидемией и облитерирующим поражением артерий нижних конечностей, а также у злостных курильщиков.
Принято считать, что БАБ вызывают эректильную дисфункцию, хотя это мнение основывается главным образом на исследованиях, в которых использовались неселективные препараты. Иное дело β1-селективные БАБ, которые в последние десятилетия в основном используются при лечении ССЗ.
По данным нескольких кратковременных исследований, бисопролол и другие β1-селективные препараты не вызывают эректильной дисфункции у мужчин АГ. В частности, в одном контролируемом плацебо исследовании двойным слепым методом показано, что у мужчин с впервые выявленной АГ сексуальная функция не изменяется при лечении бисопрололом. Более того, у больных АГ, уже получавших антигипертензивные препараты, бисопролол улучшал некоторые показатели сексуальной функции, например, усиливал эрекцию во время полового сношения и чувство удовлетворения половым актом [10]. Следовательно, высокоселективный β1-адреноблокатор не вызывает нежелательных сексуальных побочных эффектов, а у больных мужчин, получающих антигипертензивные препараты, может даже улучшать сексуальную функцию.
Фармакокинетические особенности бисопролола
Недавние исследования показали, что фармакокинетические и фармакодинамические особенности БАБ в значительной мере определяются таким их физико-химическим свойством, как растворимость в жирах и воде. На основании растворимости в жирах и воде БАБ разделяют на три группы: 1) липофильные (бетаксолол, карведилол, метопролол, пропранолол, тимолол и др.); 2) гидрофильные (атенолол, надолол, соталол и др.) и 3) амфофильные (бисопролол, пиндолол др.).
Липофильные БАБ быстро и почти полностью (>90%) всасываются в желудочно-кишечном тракте. Обычно они метаболизируются в печени (80-100%). Основной путь элиминации липофильных БАБ следует учитывать при их назначении больным с нарушенной функцией печени. Например, разовые дозы или кратность приема липофильных БАБ необходимо уменьшать у пожилых больных, больных циррозом печени или сердечной недостаточностью, а также при совместном применении с лекарственными препаратами, тормозящими активность микросомальных ферментов печени (например, с циметидином или хлорпромазином). С другой стороны, известно, что у злостных курильщиков, а также больных, получающих барбитураты, фенитоин (дифенин), рифампицин, метаболизм липофильных БАБ в печени ускорен. Соответственно во всех этих случаях требуется назначать более высокие дозы препаратов.
Гидрофильные БАБ не полностью (30-70%) и неравномерно всасываются в желудочно-кишечном тракте. Они лишь в незначительной степени (до 10%) метаболизируются в печени и экскретируются в основном почками с мочой в неизменном виде (40-70%) либо в виде метаболитов. При дозировании гидрофильных БАБ следует учитывать функцию почек. У больных с низкой скоростью клубочковой фильтрации (<30-50 мл/мин) суточную дозу гидрофильных препаратов необходимо уменьшить. С другой стороны, фармакокинетика гидрофильных БАБ (в отличие от липофильных препаратов) существенно не изменяется у больных циррозом печени, а также злостных курильщиков или при совместном применении с барбитуратами, фенитоином и рифампицином.
Бисопролол, а также ацебутолол и пиндолол растворяются как в жирах, так и в воде, поэтому их называют амфофильными БАБ. Бисопролол как амфофильный БАБ занимает промежуточное положением между липофильными и гидрофильными препаратами. После приема внутрь около 50% бисопролола подвергается биотрансформации в печени, в то время как остальные 50% в неизмененном виде выводятся почками. Несомненным преимуществом бисопролола является то, что он имеет два основных пути элиминации из организма (печеночный метаболизм и почечная экскреция). Это обстоятельство делает его более безопасным, чем липофильные и гидрофильные БАБ. В частности, он более безопасен, чем липофильные БАБ, при циррозе печени или совместном назначении с индукторами или ингибиторами микросомальных ферментов печени. С другой стороны, бисопролол более безопасен, чем гидрофильные БАБ, при почечной недостаточности [1, 3, 5, 9]. Иными словами, бисопролол как амфофильный БАБ может использоваться у более разнообразных категорий больных с ССЗ, которые нередко одновременно страдают заболеваниями печени и почек или принимают другие лекарственные препараты.
Терапевтическое применение бисопролола
Как и другие БАБ, бисопролол используется главным образом при лечении стенокардии напряжения, АГ и ХСН, обусловленной систолической дисфункцией левого желудочка.
Бисопролол в лечении стабильной стенокардии напряжения
Как и другие БАБ, бисопролол относится к одному из трех основных классов антиангинальных препаратов (наряду с антагонистами кальция и нитратами). Все БАБ используются для длительной терапии у больных ИБС со стенокардией напряжения, учитывая их способность уменьшать потребность миокарда в кислороде и даже увеличивать кровоснабжение миокарда за счет удлинения диастолы. В основе антиангинальной (антиишемической) эффективности всех БАБ лежит главным образом их способность блокировать β1-адренорецепторы сердца, которые в основном опосредуют отрицательные хроно- и инотропные эффекты.
Антиангинальная (антиишемическая) эффективность неселективных и β1-селективных блокаторов примерно одинаковая, однако β1-селективные препараты лучше переносятся и реже вызывают побочные эффекты, поскольку по определению оказывают минимальное влияние на β2-адренорецепторы сосудов, бронхов и печени.
Эффективные антиангинальные дозы бисопролола колеблются от 5 до 10 мг. Разовая доза 10 мг более эффективна, однако повышение дозы до 20 мг не увеличивает антиангинальной эффективности бисопролола. Длительность антиангинального эффекта бисопролола (5-10 мг/сут) составляет 24 ч, что позволяет принимать его 1 раз в сутки. После приема внутрь бисопролол уменьшает депрессию сегмента ST и значительно увеличивает продолжительность выполнения физической нагрузки (на 20-45%). Частота приступов стенокардии при лечении бисопрололом уменьшается в среднем на 50-98% [1, 5, 6, 11-13].
Перекрестные исследования с использованием двойного слепого метода показали, что по антиангинальной эффективности бисопролол в дозе 5-10 мг/сут сравним с атенололом 50-100 мг/сут, верапамилом 240-360 мг/сут, нифедипином ретард 40-80 мг/сут [6, 12, 13].
Антиишемические эффекты бисопролола в сравнении с нифедипином изучались в многоцентровом исследовании TIBBS у 330 больных ИБС со стабильной стенокардией напряжения [12]. Бисопролол и нифедипин в одинаковой степени достоверно уменьшали число приступов стенокардии. По данным 48-часового холтеровского мониторирования электрокардиограммы (ЭКГ), бисопролол в большей степени, чем нифедипин, уменьшал частоту преходящих эпизодов и общую длительность ишемии миокарда. Полное подавление преходящих эпизодов ишемии миокарда наблюдалось у 52,5% больных, получавших бисопролол, но лишь у 15,6% больных, получавших нифедипин. Бисопролол более эффективно подавлял эпизоды ишемии миокарда в утренние часы и около полудня, когда они регистрировались особенно часто и часто сочетались с высоким риском сердечно-сосудистых катастроф. Напротив, нифедипин в одинаковой мере подавлял эпизоды ишемии миокарда в течение суток.
Дальнейший анализ исследования TIBBS [13] показал, что у больных ИБС со стабильной стенокардией напряжения вероятность развития неблагоприятных сердечных событий напрямую зависит от числа преходящих эпизодов ишемии миокарда, регистрируемых при 48-часовом холтеровском мониторировании ЭКГ. Более того, полное подавление преходящих эпизодов ишемии миокарда с помощью бисопролола или нифедипина достоверно снижает вероятность неблагоприятных сердечных событий по сравнению с группой больных, у которых не удалось достичь полного подавления преходящих эпизодов ишемии миокарда. Попутно было обнаружено, что частота неблагоприятных сердечных событий за 8 нед наблюдения при лечении бисопрололом недостоверно меньше, чем при лечении нифедипином. Следовательно, прогноз у больных со стабильной стенокардией определяется как исходным числом преходящих эпизодов ишемии миокарда, регистрируемых при 48-часовом холтеровском мониторировании, так и степенью их подавления бисопрололом или другими антигипертензивными препаратами.
Итак, бисопролол является весьма эффективным антиангинальным средством, которое оказывает разные клинические и антиишемические эффекты на протяжении 24 ч. У больных ИБС со стабильной стенокардией напряжения вероятность развития неблагоприятных сердечных событий значительно уменьшается, если удается полностью подавить преходящие эпизоды ишемии миокарда, регистрируемых при 48-часовом холтеровском мониторировании ЭКГ.
Бисопролол в лечении АГ
Наиболее частое показание к применению бисопролола - АГ. Высокая антигипертензивная эффективность бисопролола установлена в многочисленных исследованиях. В частности, в двух контролируемых плацебо исследованиях показано, что у больных с мягкой и умеренной АГ (диастолическое АД от 95 до 120 мм рт. ст.) бисопролол при приеме в дозе 5, 10 и 20 мг 1 раз в сутки вызывает значительное снижение АД и частоты сердечных сокращений (ЧСС). Влияние бисопролола на уровень АД и ЧСС зависели от дозы препарата. Среднее снижение систолического и диастолического АД при лечении бисопрололом составило 10-20/5-15 мм рт. ст. Снижение АД нарастает в первые 2 нед лечения препаратом, а затем стабилизируется.
Антигипертензивная эффективность бисопролола не зависит от возраста и расы больных (в отличие от атенолола). Нормализация АД (диастолическое АД ниже 90 мм рт. ст.) при лечении бисопрололом достигается более чем у 80% больных с мягкой и умеренной АГ, даже через 24 ч после приема препарата. Привыкания к антигипертензивному действию бисопролола не возникает. Так, к концу 3-летнего период наблюдения 22,6% пациентов продолжали получать бисопролол в дозе 5 мг/сут, 63,7% - в дозе 10 мг/сут и 13,7% - в дозе 20 мг/сут. Из 164 больных побочные эффекты отмечены в 34 случаях, но лишь у 2 больных препарат пришлось отменить [6].
По данным мониторирования АД, бисопролол значительно снижает АД на протяжении суток, не изменяя при этом естественного ритма колебаний АД. Он предупреждает подъемы АД, связанные с физическими нагрузками, которые возникают при повседневной активности. Бисопролол не вызывает ортостатической гипотонии и синдрома отмены. Значительное уменьшение АД и ЧСС сохраняется в течение до 40 ч после отмены препарата.
При длительном назначении бисопролол вызывает обратное развитие гипертрофии левого желудочка. По способности вызывать регрессию гипертрофии левого желудочка бисопролол столь же эффективен, как и ингибитор ангиотензинпревращающего фермента (АПФ) эналаприл [14].
В нескольких многоцентровых исследованиях бисопролол сравнивали с другими антигипертензивными препаратами. Так, в исследовании BIMS двойным слепым перекрестным методом сравнивали антигипертензивные эффекты бисопролола (до 20 мг/сут) и атенолола (до 100 мг/сут) у 104 больных АГ (исходное диастолическое АД от 100 до 120 мм рт. ст.) [15]. Бисопролол оказался эффективным у 68% больных, а атенолол - у 56%. Более того, 5 больных реагировали на атенолол, но не на бисопролол; 16 больных реагировали на бисопролол, но не на атенолол (р<0,05).
По данным другого исследования, бисопролол в дозе 10 мг/сут оказывал более выраженное антигипертензивное действие, чем атенолол в дозе 100 мг/сут, однако в дозе 5 мг/сут он оказался несколько менее эффективным, чем атенолол. Бисопролол сравним по антигипертензивной эффективности с ретардной формой нифедипина (20 мг 2 раза в день), но значительно превосходил фиксированную комбинацию гидрохлоротиазида и амилорида (р<0,001).
В исследовании BISOMET бисопролол и метопролол в одинаковой степени контролировали повышение АД во время пробы с физической нагрузкой, выполненной через 3 ч после приема препаратов, но не через 24 ч [16]. Это означает, что бисопролол предупреждает подъемы АД, связанные с физическими нагрузками, которые возникают при повседневной активности, на протяжении большего времени, чем метопролол.
Таким образом, высокоселективный БАБ бисопролол является эффективным антигипертензивным препаратом, который при приеме 1 раз в сутки позволяет с успехом контролировать АД на протяжении 24 ч. Он хорошо переносится, крайне редко его приходится отменять из-за развития побочных эффектов. Кроме того, он не вызывает синдрома отмены.
Бисопролол при лечении ХСН
Сравнительно новая область клинического применения бисопролола и некоторых других БАБ - лечение ХСН, обусловленной систолической дисфункцией левого желудочка (фракция выброса <35-40%).
В 1990-е годы были выполнены два рандомизированных контролируемых плацебо исследования по изучению эффективности и безопасности бисопролола у больных ХСН, обусловленной систолической дисфункцией левого желудочка.
В первом из этих исследований CIBIS бисопролол вызвал значительное, но статистически недостоверное снижение смертности (в среднем на 20%) у больных ХСН [17]. Недостаточная эффективность бисопролола в исследовании CIBIS, возможно, была связана со сравнительно низкой целевой дозой препарата, которая составляла всего 5 мг/сут.
В крупном контролируемом плацебо исследовании CIBIS-II целевая доза бисопролола была увеличена до 10 мг/сут [18]. В результате длительная терапия препаратом сопровождалась достоверным снижением смертности у больных ХСН (в среднем на 34%; р<0,0001).
По сводным данным первого и второго исследований CIBIS, БАБ бисопролол снижает общую смертность больных с умеренной и тяжелой ХСН в среднем на 29% [19].
После публикации результатов исследования CIBIS-II бисопролол выбран экспертами Европы и США в качестве одного из БАБ первого ряда для длительного лечения ХСН, обусловленной систолической дисфункцией левого желудочка.
Бисопролол выпускается несколькими производителями под разными названиями. Большинство исследований проводили с использованием оригинального препарата. Специальные фармакокинетические исследования показали, что Кординорм, выпускаемый компанией «Актавис», в высокой степени биоэквивалентен оригинальному препарату (см. рисунок).
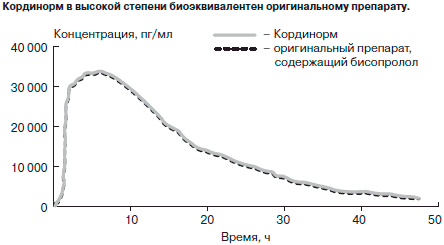
Итак, бисопролол является высокоселективным БАБ без дополнительных свойств, который с успехом используется для лечения стабильной стенокардии напряжения, АГ и ХСН. Высокая β1-селективность бисопролола делает безопасным его применение у больных ХОБЛ, СД, ожирением, атерогенной дислипидемией и перемежающейся хромотой. Благодаря амфофильности он имеет два основных пути выведения - биотрансформацию в печени (50%) и экскрецию почками в неизмененном виде, что позволяет использовать бисопролол для лечения у пациентов с сопутствующими нарушениями функции печени и почек без коррекции дозы препарата.
ЛИТЕРАТУРА 1. Cruickshank J M, Prichard BNC. Beta-blockers in clinical practice. 2nd edition. Edinburg; Churchill Livingstone, 1994
2. Сидоренко Б.A., Преображенский ДВ. Клиническое применение бета-адреноблокаторов. М., 1994.
3. Сидоренко ВА, Преображенский ДВ. бета-адреноблокаторы. М., 1996.
4. The Task Force on beta-blockers of the European Society of Cardiology. Expert consensus document on β-adrenergic receptor blockers. Eur Heart J 2004; 25: 1341-62.
5. Cruickshank JM. The place of beta-blockers in cardiovascular medicine. Cardiologia 1995; 40: 829-43.
6. Weir MR, Bolli P, Prichard BNC, Weber MA. Bisoprolol. In: Messerli FH. (ed) Cardiovascular drug therapy. 2nd ed. Philadelphia et al, 1999; p. 557-68.
7. Сидоренко Б.A., Преображенский ДВ. Диагностика и лечение артериальной гипертензии. Часть вторая. М., 2000.
8. Gress T, Nieto F, Shahar E et. al Hypertension and antihypertensive therapy as risk factors for type 2 diabetes mellitus. N Engl J Med 2000; 342:905-12.
9. Westfall TC, Westfall Adrenergic agonists and antagonists. In: Goodman & Gilman. The pharmacological basis of therapeutics. 11th ed. New York et al, 2006; p. 237-95.
10. Broekman CP, Haensel SM, van de Ven LL, Slob AK. Bisoprolol and hypertension: effects on sexual functioning in men. KSex Marital Ther 1992; 18:325-31.
11. Bethge H, Leopold G, Wagner G. Bisoprolol in angina pectoris. Cardiovasc. Drug Review 1991; 9: 110-22.
12. von Arnim T, for the TIBBS Investigators. Medical treatment to reduce total ischemic burden: Total ischemic burden bisoprolol study (TIBBS), a multicenter trial comparing bisoprolol and nifedipine.JACC 1995; 25: 231-8.
13. von Arnim T, for the TIBBS Investigators. Prognostic significance of transient ischemic episodes: response to treatment shows improved prognosis. JACC 1996; 28: 20-40.
14. Остроумова ОД Возможности применения высокоселективных β-блокаторов у больных с сопутствующими заболевания. Рус. мед. журн. 2004; 12: 721-5.
15. Buhler FR, Berglund G, Anderson OK et al Double-blind of the cardioselective β-blockers bisoprolol and atenolol in hypertension: the Bisoprolol International Multicenter Study (BIMS). J Cardiovasc Pharmacol 1986; 8 (suppl. 11): S122-30.
16. Haasis R, Bethge H. Exercise blood pressure and heart rate reduction 24 and 3 hours after administration in hypertensive patients following 4 weeks of treatment with bisoprolol and metoprolol in hypertension: A randomized multicenter double-blind study (BISOMET). Eur Heart ] 1987; 8 (97): 13S122-S130.
17. CIBIS Investigators and Committees. A randomized trial of beta-blockade in heart failure. Circulation 1994; 90:1765-73.
18. CIBIS-II Investigators and Committees. Cardiac Insufficiency Bisoprolol Study (CIBIS-II): a randomised trial. Lancet 1999; 353 (9146): 9-13.
19. McGavin JK, Keating GM. Bisoprolol. A review of its use in chronic heart failure. Drugs 2002; 62: 2677-96.
Комментарии
ПРАКТИКА ПЕДИАТРА
