Комплексная реабилитация пациентов с остеоартрозом крупных суставов
СтатьиОпубликовано в журнале: «ЛЕЧАЩИЙ ВРАЧ»; апрель; № 4; 2016; стр. 1-7.
Н. Н. Кораблева, кандидат медицинских наук
ГБОУ ДПО РМАПО МЗ РФ, Москва
Резюме. Разработан алгоритм раннего лечения суставного синдрома, принципиальной особенностью которого является цикличный подход с акцентом на «опережение». Лечение в соответствии с разработанным алгоритмом позволило снизить стандартную медикаментозную нагрузку при лечении остеоартороза, улучшить функциональные результаты, стабилизировать ремиссию, повысить качество жизни.
Ключевые слова: остеоартроз, лечение, реабилитация, алгоритм, повторяемая ремиссия, релиз-активные антитела к человеческому фактору некроза опухоли альфа.
Abstract. The algorithm of early therapy of joint syndrome was developed whose primary peculiarity is cyclic «in advance» approach. Therapy according to the algorithm allowed to reduce standard drug load in osteoarthrosis therapy, improve functional results, stabilize remission and increase quality of life.
Key words: osteoarthrosis, therapy, rehabilitation, algorithm, recurrent remission, release active antibodies to human tumor necrosis factor alpha.
Проблема лечения и реабилитации населения РФ с дегенеративными заболеваниями опорнодвигательной системы (ОДС) продолжает оставаться нерешенной задачей. Увлечение на первых стадиях заболевания медикаментозной терапией, причем в основном противовоспалительной, а затем на поздних стадиях — оперативным лечением связано с тем, что дегенеративной патологией занимаются в амбулаторной системе специалисты, далекие от понимания роли биомеханических связей в здоровье ОДС. Практически повсеместно «симптоматическое» и «базисное» лечение ОДС в рамках ОМС полноценно не восстанавливает функциональную активность, а в долговременной перспективе приводит к прогрессированию дегенеративного процесса. Формально назначенное лечение вызывает большие и бессмысленные затраты бюджетных средств, рождает уверенность пациентов в эффективности только оперативных методов лечения. Существующее мнение, что наиболее прогрессивным и эффективным методом лечения деформирующего артроза является тотальное эндопротезирование пораженного сустава, в еще большей степени мифологизирует эту уверенность населения. К настоящему времени во всем мире накоплен огромный опыт проведения операций артропластики и послеоперационного ведения таких больных. Этот метод широко распространяется и в России [1, 2].
Однако даже при успешном проведении оперативного лечения ОДС, в силу организационных причин, большинство хирургических стационаров, занимающихся эндопротезированием, не имеют возможности для проведения полноценных послеоперационных реабилитационных мероприятий. Как правило, больные вынуждены самостоятельно восстанавливать функцию проблемного сустава, руководствуясь лишь общими рекомендациями лечащего врача при выписке [3]. В связи с этим обширные научные разработки по проблеме реабилитации, посвященные ведению пациентов после операций артропластики крупных суставов, остаются недостаточно востребованными в поликлинической практике, что, безусловно, сказывается на отдаленных результатах эндопротезирования. Реабилитационные мероприятия, предлагаемые бюджетными ЛПУ, ограничиваются, как правило, занятиями лечебной физкультурой, курсом массажа и ограниченным набором физиотерапевтических процедур [4, 5].
Реабилитация имеет огромное, можно сказать ведущее, значение в дальнейшей жизни людей с дегенеративными заболеваниями ОДС. С помощью реабилитационных мероприятий возможно восстановить трудоспособность пациента и вернуть его к прежнему активному образу жизни, а также предупредить множество осложнений, особенно в геронтологической практике.
Наиболее крупная группа дегенеративных заболеваний ОДС представлена остеоартрозом (ОА) [6, 7].
При ОА в патологический процесс вовлекаются все структуры суставного органа движения: гиалиновый хрящ, связки и околосуставные мышцы, синовиальная оболочка, субхондральная кость, суставная капсула. В научной литературе, посвященной ОА, превалирует мнение о сложном воспалительном генезе гибели хряща в процессе развития дегенеративной патологии суставов, однако полностью игнорируется такая первопричина, как гипотрофия/атрофия и дисбаланс функционирования мышц сегмента с формированием нестабильности сустава и его перемежающейся макро- или микро-неконгруэнтности [6, 8].
По нашим данным, морфология гиалинового хряща при дегенеративных заболеваниях начинает страдать вторично после истощения адаптивных возможностей периартикулярных тканей [8—10].
Данное мнение подтверждается эффективностью адекватного комплексного медикаментозного и немедикаментозного лечения ОА на ранних стадиях заболевания, позволяющего предупредить необратимые изменения гиалинового хряща и увеличить продолжительность активной жизни человека.
Мнение о низкой эффективности консервативного лечения ОА связано с малой эффективностью противоболевой терапии в динамике заболевания и отсутствием рациональной реабилитации после проведенного лечения острого периода заболевания. Именно поэтому тотальное эндопротезирование крупных суставов стало наиболее эффективным методом лечения как за рубежом, так и в Российской Федерации.
Основой реабилитационных мероприятий и в процессе консервативного лечения, и в послеоперационном периоде после артропластики являются комплексные программы, включающие массаж, лечебную гимнастику, лечение термальными водами, различные варианты электротерапии, лазер, вакуумную компрессорную терапию, трудотерапию и многое другое. При этом справедливо считается, что качество реабилитации обеспечивает не менее 50% успеха артропластики, а при консервативном лечении — длительность ремиссии и замедление прогрессирования заболевания [1, 4, 11, 12].
Чрезвычайно важным аспектом лечения, а затем реабилитации хронического суставного синдрома, особенно в геронтологической практике, является обучение пациента бытовым действиям и навыкам. Для многих наших пациентов со стойкими морфологическими изменениями структуры суставов становятся малодоступными простейшие, элементарные движения. Страх и ожидание боли, контрактура или гипермобильность сустава затрудняют ходьбу, повороты в постели, присаживание или вставание со стула и кровати. Такие пациенты нуждаются в групповых и индивидуальных занятиях для восстановления повседневной двигательной активности [6]. Однако практика проведения школ для пациентов с ОА, к сожалению, не оправдала наших ожиданий: на занятия приходят, как правило, одни и те же пациенты, причем не всегда те, для которых школа по-настоящему актуальна. Главный секрет успешной реабилитации — умелое сочетание лечебных и реабилитационных мероприятий с использованием новых и классических методик, основанных на научно подтвержденных данных и истинном желании помочь пациенту. В настоящее время в крупных клиниках успешно внедряется метод ботокс-терапии — использование ботулинического токсина для купирования спастических поражений при ОА и озонотерапии путем введения в спазмированные и болезненные мышцы озона [13]. Все чаще с высоким эффектом в составе консервативного лечения и реабилитации ОА используется гирудотерапия — лечение пиявками [14].
Лечение патологии ОДС, в т. ч. дегенеративных заболеваний, подразумевает последовательное проведение в начале комплексного консервативного лечения по принципу «от простого к сложному» и в дальнейшем, по показаниям, оперативного лечения, причем в соответствии с тем же принципом: от малоинвазивного к реконструктивному. Консервативное лечение косвенно становится первой, причем паллиативной, стадией хирургического лечения суставного синдрома, целью которого в первую очередь является попытка купирования болевого синдрома и улучшение качества жизни пациента. По мере того как болевой синдром становится невыносимым, больной принимает решение обратиться к хирургическому лечению — эндопротезированию. Формальный подход к лечению суставного синдрома приводит к исключению из схем консервативного лечения реабилитационного периода в качестве самостоятельного и чрезвычайно важного элемента.
Общепринятый арсенал медикаментозных средств в остром и реабилитационном периодах состоит из анальгетиков (чаще всего ацетаминофена), селективных и неселективных пероральных нестероидных противовоспалительных средств (НПВС), локального применения НПВС и капсацина (стручковый перец), внутрисуставных инъекций глюкокортикостероидов и гиалуроновой кислоты, глюкозамина и хондроитинсульфата (ГХК) [1].
Применяемые препараты не всегда безопасны, а их побочное действие может приводить к нарушению состояния «хрупкой» компенсации и вызывать вторичные патологические изменения жизненно важных органов, особенно в пожилом и старческом возрасте. Накопление в последнюю четверть века негативных факторов окружающей среды, некачественные продукты питания, напряжение психоэмоциональной сферы, большая лекарственная нагрузка потенцируют увеличение числа лиц с заболеваниями желудочно-кишечного тракта. В связи с этим перед медицинским сообществом встает задача использования максимально безопасных, но при этом эффективных лекарственных средств, особенно для целей восстановительного лечения и профилактики обострений суставного синдрома в реабилитационном периоде. В своих разработках нами использован препарат Артрофоон. Артрофоон содержит релиз-активные антитела (РА-АТ) к фактору некроза опухоли альфа (ФНО-а) [15, 16]. Артрофоон — противовоспалительный регуляторный препарат, модифицирующий активность лиганд-рецепторного взаимодействия эндогенных регуляторов к стимулирующему воздействию провоспалительного цитокина ФНО-а. ФНО-а это универсальный, запускающий воспаление фактор, стимулирующий клетки в зоне повреждения с целью локализовать и нейтрализовать повреждающий фактор. При избыточном накоплении ФНО-а в зоне повреждения суставов отмечается чрезмерное воспаление, с разрушением компонентов сустава. Артрофоон снижает чувствительность рецепторов клеток запускающих воспаление, и снимает избыточный компонент развития воспаления. В отличие от довольно однозначного действия известных НПВС, Артрофоон при курсовом приеме обладает выраженным противовоспалительным действием и высоким уровнем безопасности, что делает его идеальным корректором воспаления не только на этапе лечения, но и реабилитации, как профилактического препарата. Многократные курсы лечения не вызывают синдрома привыкания и не искажают эффекты Артрофоона. Это подтверждается многочисленными клиническими наблюдениями [17—19].
Очевидными преимуществами и привлекательными для современной практической медицины свойствами Артрофоона с клинической точки зрения являются следующие:
1) отсутствие токсичности, формирования толерантности, привыкания и пристрастия;
2) высокая эффективность, сравнимая с фармакологическими «эталонными» препаратами (диклофенак, селективные НПВС и др.);
3) удобное сублингвальное применение;
4) оптимальное соотношение высокой терапевтической эффективности с безопасностью применения в клинической практике;
5) хорошие фармакоэкономические показатели;
6) возможность длительного применения с профилактической целью и для лечения суставного синдрома в стадии хронизации процесса;
7) высокая степень безопасности при применении у пациентов с сопутствующими заболеваниями.
Количество таблеток, назначаемое в реабилитационном периоде, зависит от продолжительности и выраженности проявлений заболевания. В тяжелых случаях (3—4 ст. процесса) при выраженном болевом синдроме и синовите назначают 4—6 таблеток в сутки сублингвально, курсом 3 месяца, при более легком течении заболевания (1—2 ст.) по 2 таблетки 2 раза в сутки.
В научной литературе мы не нашли четкой информации и рекомендаций по использованию лекарственных средств в реабилитационном периоде при дегенеративных заболеваниях суставов. В связи с чем, разрабатывая алгоритмы комплексного реабилитационного ведения пациентов с ОА, нами введено понятие фармакореабилитации как принципиально необходимой составляющей этого периода. Смысл этого термина и самого лекарственного воздействия на организм пациента в реабилитационном периоде заключается в его «опережающем» действии, направленном на профилактику возникновения патологического воспаления и, как результат, — рецидива заболевания.
На кафедре травматологии и ортопедии Российской медицинской академии последипломного образования разработана и апробирована методологическая концепция тактики ведения больных с дегенеративными заболеваниями крупных суставов. Основой разработанной методики является цикличный комплексный подход.
Цель, поставленная при разработке методики, — создание действенных и безопасных алгоритмов лечения и реабилитации больных с дегенеративными поражениями суставов:
1) минимизация использования кортикостероидов и НПВС;
2) формирование полноценного алгоритма комплексного лечения ОА;
3) обеспечение повторяемой безмедикаментозной ремиссии при ОА;
4) достижение периода постоянной этапной реабилитации.
Применение разработанного нами алгоритма позволило выделить ряд последовательных стадий восстановительного лечения суставного синдрома. Острому периоду суставного синдрома соответствует первый курс лечебных мероприятий. Статус пациента в этот период оценивается с целью подбора комплекса лечения. Учитывается выраженность болевого синдрома, клинические признаки остроты воспаления, состояние кровообращения заинтересованного сегмента, психоэмоциональное состояние, готовность пациента участвовать в лечебном процессе. Кроме того, учитывается уровень коморбидности пациента, поскольку лечение ОА не должно усугублять состояния жизненно важных органов и систем. В среднем курс лечения занимает 3 месяца. Цель данного периода лечения связана с максимальным купированием болевого синдрома и клинических проявлений ОА. Метод лечения больных с обострением ОА разработан и описан нами ранее [9], и в данной работе не предполагается его подробный разбор. Второй курс лечения проводят при появлении малейших признаков обострения суставного синдрома, но не позднее чем через 6 месяцев даже при отсутствии жалоб со стороны пораженного сустава. Поскольку после первого курса нередко остаются те или иные ощущения суставного дискомфорта, данный период определен нами как подострый период лечения. В этом периоде назначают курс, повторяющий все назначения острого периода, либо проводят корректировку в отношении целесообразности использования и дозы НПВС, вазодилататоров, инъекционных форм хондропротекторов (внутримышечно) и т. д. После завершения второго курса лечения пациент переходит в предреабилитационный период, который характеризуется безмедикаментозной ремиссией более полугода. Тем не менее, при отсутствии жалоб со стороны пациента с ОА, через 6 месяцев после завершения второго курса лечения его вновь повторяют. После чего считаем цикл лечения завершенным и отмечаем переход в реабилитационный период. В зависимости от степени поражения сустава/суставов, возраста пациента, его активности, наличия факторов риска усугубления суставного синдрома определяем продолжительность периода реабилитации: 1—2 года или пожизненно.
Более поздние стадии заболевания у пациентов, отказывающихся от оперативного лечения, имеют свои особенности, и главной особенностью является формирование индивидуальной схемы фармакореабилитации, носящей характер пожизненной. Примером может быть лечение остеопороза или в практике терапевта — гипертонической болезни и т. п. При этом схемы и лечения, и реабилитации содержат в своем составе неизменные мероприятия, которые являются существенными и отказ от которых приводит к потере эффекта лечения и реабилитации (рис. 1). Остальные мероприятия и лекарственные средства носят характер индивидуальных рекомендаций.
Рис. 1. Базисные мероприятия в лечении и реабилитации ОА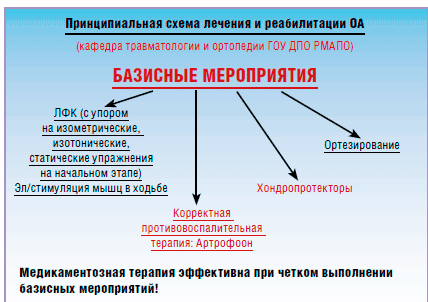
Объективные критерии достижения периода реабилитации
- Проведение цикличного комплексного лечения острого, подострого и предреабилитационного периодов по схеме кафедры.
- Обеспечение безмедикаментозной ремиссии после второго курса лечения.
- Купирование болевого синдрома при 1—2 ст. полностью, при 3—4 ст. в пределах 1—4 баллов по визуально-аналоговой шкале (ВАШ) и не требующего приема анальгетиков.
- Активное и осмысленное участие пациента в оздоровительном процессе.
- Адекватное ведение сопутствующей соматической патологии смежными специалистами.
Базовые реабилитационные мероприятия в перерыве между острым и подострым периодами ОА
Реабилитационные мероприятия в этом периоде зависят от возможностей пациента и состояния его костно-мышечной системы (КМС).
Поскольку болевой синдром в большей или меньшей степени купирован в результате первичного курса лечения, основой этого периода является корректная аккуратная лечебная физкультура с обязательным контролем инструктора. В этом периоде пациента обучают релаксирующим упражнениям, упражнениям на координацию. В этом периоде у пациента формируют критичное состояние комплаентности, причем по отношению как к лекарственной, так и симптоматической терапии.
ОА нередко в пожилом возрасте сочетается с остеопорозом, в связи с чем необходимо минимизировать или исключить длительные вертикальные и физические нагрузки, а также упражнения на гибкость и «скручивание», которые могут приводить к перестроечным переломам, особенно в зоне эпифиза.
В течение всего цикла лечения (три курса) Артрофоон должен назначаться в комплексной медикаментозной терапии. Схемы назначения препарата зависят от выраженности патологического процесса, активности болевого синдрома. Неудовлетворенность результатами часто применяемого такого метода лечения, как внутрисуставное введение кортикостероидных препаратов (Кеналог, Дипроспан), и подмеченный клинический эффект оптимизации лечения суставного синдрома при одновременном применении Артрофоона заставили исследователей провести сравнительное изучение эффективности комбинированной локальной суставной терапии (ЛСТ) и Артрофоона.
Анализ двух групп больных, которым в качестве основного лечения была выбрана ЛСТ, но второй оно было дополнено, после внутрисуставного введения Дипроспана, Артрофооном, показал безусловное усиление эффекта комплексного лечения [20].
Оценку качества терапии проводили с учетом изменений напряженности боли, окружности сустава, объема движений в пораженном суставе. Анализировали динамику индекса WOMAC, выраженность и продолжительность ремиссии, частоту повторных внутрисуставных инъекций глюкокортикостероидов. Проведенное 6-месячное исследование показало достоверно более выраженные положительные изменения в группе больных, которые помимо ЛСТ получали Артрофоон, в отличие от пациентов контрольной группы, не получавших препарата. Отличия проявлялись в том, что у пациентов основной группы, принимавших после ЛСТ Артрофоон, были отмечены: уменьшение боли, припухлости, увеличение объема движений сустава при оценке эффективности лечения по WOMAC. Выявлено снижение потребности пациентов в НПВС в группе принимавших Артрофоон. За 6-месячный период после ЛСТ приемом НПВС воспользовались только 10 пациентов из 20 основной группы больных, принимавших Артрофоон (50%), в то время как среди пациентов контрольной группы, не принимавших Артрофоон после ЛСТ, число больных, которым потребовалось назначение НПВС, составило 14 человек (70%). Чрезвычайный интерес представляют данные эффективности Артрофоона на этапе реабилитации после оперативных вмешательств на суставах. Было проведено изучение эффективности Артрофоона после эндоскопических вмешательств: менискэктомии по поводу травматических повреждений или на фоне дегенеративных изменений сустава, причем исследователям удалось изучить две группы с применением в послеоперационном периоде монотерапии Артрофооном и без него [21].
Исследование, проведенное в условиях послеоперационной монотерапии Артрофооном, неопровержимо доказало эффективность препарата в отношении образования послеоперационного синовита: на 5-й день после артроскопической менискэктомии и приема Артрофоона гиперэкссудация отмечалась в 2,4 раза реже, чем в группе пациентов, не принимавших Артрофоон. На 10-й день в группе, принимавшей препарат, синовит не отмечен ни у одного пациента, в то время как в контрольной группе гиперэкссудация выявлена в 18,1% случаев. В реабилитационном периоде действие Артрофоона проявляется быстро, в процессе приема больные отмечают исчезновение утренней скованности, уменьшение ощущения отечности сустава, улучшение качества жизни вследствие возможности увеличить дистанцию ходьбы.
В последние годы одним из популярнейших направлений в лечении больных с остеоартрозом крупных суставов стало эндопротезирование. Однако разработке методов и схем послеоперационной лекарственной терапии не придается необходимого значения (не оказывается должного внимания) (в разрезе) в аспекте оптимизации реабилитации пациентов с эндопротезом. Тем не менее следует отметить, что в литературе появились данные научно-клинических исследований по разработке безопасных методов фармакотерапии послеоперационного алгического синдрома, способствующих ускорению восстановительного периода после тотальной артропластики. Я. В. Руденко и соавт. оценили клиническую эффективность препарата Артрофоон после тотального эндопротезирования крупных суставов [22]. Было выявлено, что в группе пациентов, принимавших Артрофоон, лучших результатов было больше, чем в контрольной группе больных, не получавших Артрофоон. Более того, среди принимавших Артрофоон не отмечено ни одного случая ухудшения, в то время как в контрольной группе было двое таких больных из двадцати. Ни в одном случае среди пациентов, которые принимали Артрофоон, не было отмечено побочных эффектов.
Таким образом, использование Артрофоона в лечении ОА повышает результативность терапии, в том числе после оперативного лечения суставов. Обеспечение эффекта лечения достигается путем комбинирования Артрофоона с другими противовоспалительными средствами для усиления противовоспалительного и анальгетического эффекта, минимизации применения других препаратов и для предупреждения осложнений, вызванных этими препаратами. Наиболее часто Артрофоон сочетают с хондропротекторами, что в значительной степени повышает эффективность и безопасность лекарственной терапии суставного синдрома [23].
Основной точкой приложения хондропротекторов является структурный компонент хрящевой ткани. Путем воздействия на обмен этих веществ хондропротекторы регулируют обменные процессы в хряще, замедляя их разрушение и активируя их регенерацию. Применение хондропротекторов преследует цель — нормализовать белковый состав хряща, ускорить его восстановление после повреждений или остановить процесс его разрушения. Комплексное применение хондропротекторов и Артрофоона оказывает мягкое метаболическое и противовоспалительное действие на компоненты сустава на протяжении всего курса лечения и реабилитации с развитием снижения проявлений суставного синдрома и повышения качества жизни.
Чрезвычайно важным является аспект обучения пациента ортопедическому поведению в острый период. В этот период необходимо ограничивать все движения, повышающие нагрузку на сустав. Полностью исключают подъем и ношение тяжестей. Женщинам рекомендуют отказаться от обуви на каблуках выше 3—4 см. При гонартрозе больному рекомендуют сидеть на высоких стульях. Подниматься из сидячего положения необходимо с опорой на руки, сдвинув центр тяжести на край стула. Это облегчает процесс подъема и снижает нагрузку на сустав. Осознание пациентом наличия у него заболевания остеоартрозом и понимание правил поведения позволяет не бояться этого диагноза и жить полноценной жизнью. При ОА нижних конечностей пациентам следует избегать фиксированных поз, затрудняющих кровообращение в больных суставах. Такими позами являются, например, положение сидя на корточках, сидение на низком диване или в кресле. Необходимо чередовать периоды физической активности с периодами отдыха. В остром периоде противопоказана длительная ходьба без перерыва. Через каждые 20 минут вертикальных нагрузок целесообразен отдых в положении сидя.
Лечебная физкультура в остром периоде также имеет свои особенности. Лечебная физкультура, безусловно, должна носить индивидуальный характер, учитывающий как тренированность данного конкретного пациента, так и особенности его коморбида. Упражнения необходимо выполнять в положении сидя или лежа медленно и плавно, с постепенным увеличением амплитуды движений. Резкие движения и упражнения, вызывающие выраженные болевые ощущения, исключают. Основным принципом, которого должен придерживаться пациент, являются постепенность и регулярность занятий. Занятия в остром периоде проводят с несколькими заходами в течение дня, но непродолжительно. Интенсивность физической нагрузки и частота повторений определяются субъективными ощущениями — выраженностью болей. Занятия должны создавать ощущение легкой усталости. Если при выполнении физических упражнений возникла и продолжается длительное время боль в суставе, необходимо уменьшить число повторов. Оптимальным для острого периода суставного синдрома являются занятия лечебными упражнениями в бассейне с теплой водой, например, аквааэробикой. Поскольку в воде вес тела уменьшается более чем в 5 раз, движения в суставах будут менее травматичными. Следует отметить, что возрастных ограничений для занятий лечебной гимнастикой нет. Помимо положительного влияния на симптоматику ОА, физическая нагрузка способствует укреплению сердца, сосудов и костей.
В конце острого периода рекомендуют размеренную (не быструю) ходьбу по ровной местности в умеренном темпе, по показаниям, в бандаже или с использованием средств поддержки, что является хорошим способом укрепления и поддержания мышечного тонуса. Рекомендуют ежедневные прогулки продолжительностью 30 минут. Регулярные адекватные физические нагрузки в 3—4 раза увеличивают потребление хрящом питательных веществ, находящихся в синовиальной жидкости, оказывают положительное влияние на мышцы и кровообращение. Регулярные занятия укрепляют мышцы пораженного сегмента, что в свою очередь формирует мышечный корсет и улучшает опорную функцию конечности.
Следует отметить целесообразность у большинства пациентов в остром периоде использования ортезов. Как известно, квалифицированно подобранный ортез позволяет в значительной степени уменьшить болевой синдром при поражении суставов, разгрузить и нормализовать функцию пораженного сегмента.
В подостром периоде целесообразно включение в комплекс лечебных мероприятий — ручного массажа и/или электростимуляции гипотрофированных мышц (в ходьбе).
Эффективность массажа трудно переоценить: будучи научно обоснованным методом, он восстанавливает физическую работоспособность, улучшает функциональное состояние нервномышечного и суставно-связочного аппарата, позволяет снять рефлекторный мышечный спазм, активизировать кровообращение в тканях суставов, ликвидировать лимфовенозный стаз и нормализовать внутрикостное давление. Под влиянием массажных процедур повышается эластичность, тонус мышц, сократимость, купируется мышечная атрофия.
Успешное завершение лечения предполагает жизнь пациента на уровне приобретенных морфологических изменений сустава без признаков их прогрессирования.
Критерии достижения реабилитационного периода для пациента с ОА
1. Боль отсутствует или периодически составляет менее 4 баллов по ВАШ.
2. Средства поддержки (трость, ходунки) используются только при выраженных (рискованных) нагрузках.
3. Наличие состоятельной когнитивной деятельности пациента.
4. Признаки стремления к независимой жизни.
5. Адекватное лечение сопутствующей патологии.
При достижении стойкой реабилитации проводятся базисные мероприятия предупредительного характера (рис. 2), основу которой представляют:
Фармакореабилитация:
— Артрофоон;
— глюкозамин-хондроитиновый комплекс (ГХК) (например, Терафлекс);
— по показаниям, при запущенных формах суставного синдрома, курсами могут быть назначены: витамины группы В (Мильгамма), ферменты (Вобэмзим, Панкреатин), миорелаксанты (Сирдалуд), препараты, улучшающие сегментарное кровообращение (преимущественно: мужчинам вазодилятаторы — Трентал, женщинам венотоники — Венарус);
— адекватная медикаментозная терапия сопутствующей патологии.
Рис. 2. Базисные мероприятия в период достижения реабилитации ОА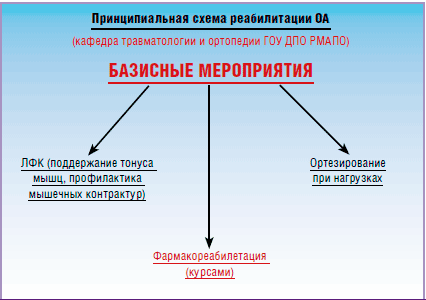
Нефармакологическая реабилитация (проводится пожизненно) включает:
1. Обучение пациента. Включает несколько правил, которые обязательно должны быть доведены до каждого пациента:
— ограничение чрезмерных специфических физических нагрузок, к которым относят подъем и ношение грузов, монотонный труд, длительное вынужденное положение, нефизиологическое состояние нагрузочных суставов;
— использование поддерживающих и разгружающих средств при передвижении (трость, костыли, ходунки, серийная ортопедическая обувь, индивидуальные супинаторы);
— формирование «правильного» стеореотипа походки [11].
2. ЛФК по индивидуально откорректированным схемам с использованием умеренных растяжек, резинового эспандера лыжника и гантелей. Затем проводят занятия на специальных тренажерах и механотерапию, помогающие усилить положительные тенденции реабилитации, эффективно стимулируя мышечную систему и суставной аппарат. По показаниям — аэробные нагрузки и акватерапия.
— Тепловые методы лечения (при отсутствии противопоказаний): чрескожная электрическая миостимуляция при малой эффективности ЛФК.
— Контроль массы тела.
— Кинезиотерапия, глубокий миофасциальный массаж.
— Физические упражнения выполняются интенсивно два-три раза в неделю по 40—60 минут и должны быть направлены, в первую очередь, на укрепление мышц и увеличение объема движений в суставах. Характер и объем нагрузок выполняемых физических упражнений чрезвычайно важны и должны контролироваться правильно обученным медицинским персоналом или непосредственно лечащим врачом. Оптимальным являются физические нагрузки по индивидуально подобранным схемам с использованием растяжек, резинового эспандера лыжника и гантелей. При отсутствии противопоказаний целесообразна аквааэробика.
— Оптимальными являются занятия в центрах типа центра Бубновского, но большинству пожилых пациентов курсовое посещение коммерческих центров — недоступно.
3. Использование ортезов при нагрузках и, по показаниям, — коррекция укорочения конечности, варусной или вальгусной деформации нижней конечности.
4. Дополнительное лечение:
— адекватное лечение сопутствующей патологии, в т. ч. региональной лимфовенозной недостаточности (гирудотерапия, пневмо- и лимфодренаж);
— психологическая реабилитация.
Каждому пациенту необходим ежегодный контрольный осмотр ортопеда.
Обязательным считаем тщательное заполнение лечащим врачом медицинской документации и даваемых рекомендаций. При обращении пациента за консультативной помощью врач-консультант как специалист «разового» посещения должен в ограниченном отрезке времени сориентироваться относительно не только профильного заболевания и получаемого лечения, но и сопутствующей патологии.
На кафедре травматологии и ортопедии ГБОУ ДПО РМАПО накоплен большой опыт применения препарата Артрофоон, который занимает ведущее место в схемах и алгоритмах комплексного лечения дегенеративных заболеваний опорнодвигательного аппарата. При этом многолетнее изучение препарата позволило на сегодняшний день дать четкие рекомендации по показаниям, временным параметрам применения, моно- или в комплексе с другими фармакопрепаратами, в зависимости от локализации, продолжительности и остроты проявления болевого синдрома и др. Было показано, что применение Артрофоона в комплексе с хондропротекторами и НПВС позволяло уменьшить дозы и сроки курсового лечения. Нами проведены по разработанным алгоритмам 92 пациента с первичным и вторичным деформирующим остеоартрозом. Контрольную группу составили 129 пациентов, получавшие стандартное лечение в поликлиниках мегаполиса. В контрольной группе больным, как правило, назначали НПВС инъекционно и перорально, интраартикулярное или параартикулярное введение кортикостероидов (Дипроспана), а также гиалуроновой кислоты. Следует отметить, что нередко одновременно назначались НПВС разных групп. В контрольной группе пациенты не достигали состояния повторяемой безмедикаментозной ремиссии, т. к. лечение проводилось от обострения к обострению и больные практиковали бесконтрольный прием НПВС и простых анальгетиков, создававших иллюзию временного благополучия и выздоровления. У всех больных этой группы наблюдалось неизменное прогрессирование суставного синдрома. Учитывались больные, которым было проведено не менее двух курсов лечения. В основной группе больных, пролеченных по алгоритму кафедры, положительный эффект лечения с достижением стойкой ремиссии и периода реабилитации отмечены у 78 пациентов, в т. ч. у 37 с 3—4 стадией патологического процесса. Остальные больные (12 человек) были оперированы: им было произведено тотальное эндопротезирование.
В соответствии со схемой кафедры больным основной группы назначались НПВС коротким курсом в начале лечения с одновременным назначением Артрофоона по 2 таблетки 2—4 раза в сутки (в зависимости от интенсивности воспаления в суставах и болевого синдрома) курсом от 3 до 6 месяцев и хондропротекторы в виде глюкозамин-хондроитинового комплекса в терапевтической дозе курсом 3 месяца. Схема лечения повторялась трижды с интервалом 5—7 мес с незначительной коррекцией: например, исключали из схемы НПВС и миорелаксанты. Результатом воспроизведения такой схемы лечения был переход в реабилитационный период.
«Правильное» адекватное цикличное лечение суставного синдрома позволяло ограничиться ежегодным назначением трехмесячного превентивного курса Артрофоона, полностью исключив использование НПВС.
Все вышеизложенное позволяет сделать следующие выводы.
1. Реабилитация при ОА возможна лишь при полноценном цикличном комплексном лечении суставного синдрома.
2. Неотъемлемой частью реабилитационных мероприятий при ОА должна быть «фармакореабилитация», проводимая ежегодно определенным курсом.
3. Только комплексный цикличный подход в лечении и реабилитации заболеваний ОДС позволяет обеспечить предупреждение или замедление морфологических изменений в суставах.
4. Профилактические курсы препарата Артрофоон в реабилитационном периоде позволяют предупредить развитие рецидива суставного синдрома, сохранить функцию суставов и улучшить качество жизни пациентов.
5. Препарат Артрофоон обладает высоким уровнем фармакологической безопасности, так как характеризуется хорошей переносимостью и отсутствием побочных действий.
6. Применение Артрофоона позволяет сократить применение НПВС в остром периоде лечения суставного синдрома и уменьшить частоту повторных внутрисуставных инъекций глюкокортикостероидов.
7. Артрофоон практически не имеет альтернативы в целях профилактики обострения суставного синдрома.
ЛИТЕРАТУРА:
1. Девятова М. В., Смирнов Г. И., Машков В. М. и др. Двигательная реабилитация при эндопротезировании тазобедренного сустава // Теория и практика физ. культуры. 1998, 1, 52—53.
2. Рыбачук О. И., Калашников А. В. Искусственный тазобедренный сустав. Пособие для врачей. К., 2000. С. 88.
3. Ласкутков А. Е. Памятка для пациентов, которым предстоит эндопротезирование тазобедренного сустава. Днепропетровская государственная медицинская академия. Кафедра травматологии и ортопедии. Научно производственное предприятие ОРТЭН ЛТД. Днепропетровск, 2004. 18 с.
4. Возницкая О. Э., Сабирьянов А. Р., Атманский И. А. Восстановительное лечение при эндопротезировании коленного сустава. Учебное пособие для системы послевузовского профобразования. Изд-во Челябинской ГМА. Челябинск, 2009
5. Woolfe F D., Pfleger B. Burden of major musculoskeletal conditions // Bull World Organ. 2003; 81: 646-564.
6. Лила А. М. Современные аспекты диагностики и лечения остеоартроза (интервью). Русский медицинский журнал // РМЖ. 2007, 15 (4), 3-6.
7. Nguyen U. D. T., Zhang Y., Niu J., Zhang B., Felson D. T. Increasing prevalence of knee pain and symptomatic knee osteoarthritis. Paper presented at: American College of Rheumatology/Association of Rheumatology Health Professionals Annual Scientific Meeting, Atlanta, GA., 2010.
8. Van den Berg W. B. Pathophisiology of osteoarthritis // Joint Bone Spine. 2000; 67: 555-556.
9. Кораблева Н. Н. Комплексная профилактика дегенеративных заболеваний суставов // Бюлл. экспериментальной биологии и медицины. 2009, 8, приложение. С. 140-143.
10. Смирнов А. Н. Суставные синдромы: дифференциальная диагностика и принципы патогенетической терапии. М., 1999.
11. Кораблева Н. Н. Комплексное лечение и реабилитация больных с дегенеративными заболеваниями суставов. Взгляд реабилитолога // Поликлиника. 2014, 2 (1), 38-41.
12. Бирюков А. А. Лечебный массаж: Учебное пособие. К.: Олимпийская литература, 1995. 200 с.
13. Орлова О. Р. Применение Ботокса (БТА) в клинической практике. Рук-во для врачей. М.: Каталог, 2000. 208 с.
14. Баскова И. П., Бородин В. Г., Селезнев К. Г., Щетинина Е.А. Гирудотерапия. Методические рекомендации для практикующих врачей. М., 1990.
15. Эпштейн О. И. Релиз-активность — от феномена до создания новых лекарственных средств // Бюлл. экспериментальной биологии и медицины. 2012, т. 154, № 7, 62-67.
16. Бадокин В. В. Артрофоон — модификатор симптоматики и клинического течения остеоартрита // Consilium medicum. 2015, 17 (9), 128-132.
17. Шостак Н.А., Клименко А. А., Бабадаева Н. М., Павленко А. Ю. Остеоартроз (остеоартрит) — новые технологии лечения // Consilium medicus. 2007; 9 (2): 24-27.
18. Алиханов Б. А. Опыт длительного применения сверхмалых доз антител к фактору некроза опухоли-a при остеоартрозе: эффективность и переносимость // Клиницист. 2007; 4: 62-67.
19. Качанова М. В., Шерстобоев Е. Ю., Бабаева А. Р. и др. Экспериментальноклиническое исследование влияния препарата «Артрофоон» на продукцию провоспалительных цитокинов // Бюл. экспер. биол. и мед. 2008. Т. 145, № 1. С. 64-67.
20. Хитров Н. А. Локальная стероидная терапия остеоартроза с использованием Артрофоона // Поликлиника. 2009, 1, 99-102.
21. Митрофанов В. А., Фроленков А. В., Воскресенский О. Ю., Горшков В. Ю. Оптимизация послеоперационного периода после артроскопических менискэктомий // Травматология и ортопедия России. 2006, 40 (2), 205-206.
22. Руденко Я. В., Окладникова Ю. В., Гондаренко Е. К., Мальцев Е. А. Применение препарата Артрофоон после тотальной артропластики крупных суставов. «Медицина завтрашнего дня» Материалы Х1 региональной межвузовской научно-практической конференции молодых ученых 25-28 апреля 2012 года. Чита, ГМА, 2012. С. 63-64.
23. Шостак Н. А., Бабадаева Н. М. Опыт применения сверхмалых доз актител к фактору некроза опухоли-а у больных остеоартрозом // Клиницист. 2008; 1: 64-69.
