Назначение дазатиниба в дозе 100 мг 1 раз в сутки снижает частоту плеврального выпота у больных с хронической фазой хронического миелоидного лейкоза
Статьи Опубликовано в:Cancer 2010;116:377–86. © 2010 American Cancer Society.
Kimmo Porkka, MD, PhD1; H. Jean Khoury, MD2; Ronald L. Paquette, MD3; Yousif Matloub, MD4; Ritwik Sinha, PhD4; Jorge E. Cortes, MD5
Адрес для переписки: Kimmo Porkka, MD, PhD, Helsinki University Central Hospital, Biomedicum Helsinki, Hematology Research Unit, P.O. Box 700, FIN-00029 HUCH, Helsinki, Finland; Fax: (011) 358-9-471-71897; kimmo.porkka@helsinki.fi
1 Hematology Research Unit, Biomedicum Helsinki, Helsinki University Central Hospital, Helsinki, Finland; 2 Winship Cancer Institute, Emory University School of Medicine, Atlanta, Georgia; 3 Department of Medicine, Division of Hematology / Oncology, Ronald Reagan UCLA Medical Center, Los Angeles, California; 4 Bristol-Myers Squibb, Wallingford, Connecticut; 5 Department of Leukemia, The University of Texas MD Anderson Cancer Center, Houston, Texas
David Dejardin (Bristol-Myers Squibb) помогал провести статистический анализ. Обоснование. Дазатиниб — высокоактивный ингибитор BCR-ABL, эффективен у пациентов с хронической фазой (ХФ) хронического миелоидного лейкоза (ХМЛ) после развития резистентности, субоптимального ответа или непереносимости предшествующего лечения иматинибом. Как показало исследование III фазы CA180-034 по оптимизации дозы дазатиниба у больных с ХФ ХМЛ, частота плеврального выпота значительно снижалась при использовании этого препарата в дозе 100 мг 1 раз в сутки по сравнению с другими режимами (70 мг 2 раза в сутки, 140 мг 1 раз в сутки или 50 мг 2 раза в сутки). Методы. Данные исследования CA180-034 проанализировали, чтобы изучить частоту и методы лечения плеврального выпота, возникшего на фоне терапии дазатинибом, а также оценить эффективность этого препарата у больных с плевральным выпотом и без этого осложнения. Результаты. При минимальном сроке наблюдения 24 мес. плевральный выпот (III степени — 2% случаев, IV степени — 0%) возник у 14% больных, получавших 100 мг дазатиниба 1 раз в сутки, по сравнению с 23% и 26% в других группах лечения. В период с 12-го по 24-й месяц число случаев плеврального выпота увеличилось минимально. Среди пациентов, получавших 100 мг дазатиниба 1 раз в сутки, медиана времени до появления плеврального выпота любой степени составила 315 дней; после возникновения выпота 52% больных потребовался временный перерыв в лечении, 33% — снижение дозы, 57% — назначение диуретиков, 26% — кортикостероидов. У 3 пациентов, получавших 100 мг дазатиниба 1 раз в сутки, после развития плеврального выпота этот препарат был отменен. Во всех группах лечения у пациентов с плевральным выпотом и без него выживаемость без прогрессирования и общая выживаемость были сходными. Частота цитогенетического ответа у больных с плевральным выпотом была более высокой. Заключение. Применение дазатиниба в дозе 100 мг 1 раз в сутки минимизирует частоту плеврального выпота. Появление выпота не влияет на эффективность препарата в ближайшие и отдаленные сроки. Cancer 2010;116:377–86. © 2010 American Cancer Society.
Ключевые слова: дазатиниб, хронический миелоидный лейкоз, плевральный выпот, результаты лечения, выживаемость без прогрессирования, лимфоцитоз.
Дазатиниб (Спрайсел; Bristol-Myers Squibb, США) представляет собой ингибитор тирозинкиназы BCRABL, который в условиях in vitro в 325 раз более активен против немутантной формы BCR-ABL, чем иматиниб.1 Дазатиниб также ингибирует фактор роста тромбоцитов (PDGFR)-β, SRC и c-KIT. У больных хроническим миелоидным лейкозом (ХМЛ) или острым лимфобластным лейкозом с Филадельфийской хромосомой (Ph+ ОЛЛ) и резистентностью, субоптимальным ответом или непереносимостью предшествующего лечения иматинибом дазатиниб вызывает высокую частоту гематологических, цитогенетических и молекулярных ответов; частота перекрестной непереносимости иматиниба и дазатиниба низка.2-6 В исследовании III фазы по оптимизации дозы дазатиниба CA180-034 с участием больных с хронической фазой (ХФ) ХМЛ назначение этого препарата в дозе 100 мг 1 раз в сутки значительно снижало частоту ключевых нежелательных явлений (НЯ), включая плевральный выпот, при сохранении эффективности.6
Целью настоящей статьи стал анализ данных CA180034 за 24 мес., при этом особое внимание уделялось таким вопросам, как динамика плеврального выпота, борьба с данным осложнением и эффективность дазатиниба у больных с плевральным выпотом и без него.
Материалы и методы
Дизайн исследования
О дизайне и методологии исследования CA180-034 уже сообщалось.6 Кратко отметим, что CA180-034 представляет собой исследование III фазы, посвященное оптимизации дозы дазатиниба у пациентов с ХФ ХМЛ после развития резистентности, субоптимального ответа или непереносимости иматиниба. Пациентов рандомизировали с использованием факториального дизайна 2 × 2 для получения дазатиниба в одном из четырех режимов: 100 мг 1 раз в сутки, 70 мг 2 раза в сутки, 140 мг 1 раз в сутки или 50 мг 2 раза в сутки. При развитии токсичности или неадекватном ответе допускалось прерывание терапии, снижение или наращивание дозы. Лечение продолжали до прогрессирования заболевания или развития чрезмерной токсичности, что определялось лечащим врачом. Для оценки выживаемости наблюдение за всеми пациентами осуществляли независимо от прерывания терапии или прогрессирования заболевания. Исследование проведено в соответствии с Хельсинкской декларацией и одобрено этическими комитетами каждого участвовавшего в нем учреждения. От всех участников получено письменное информированное согласие.
Оценка плеврального выпота
Степень выраженности плеврального выпота определяли по общим терминологическим критериям нежелательных явлений (CTCAE) версии 3.0, разработанным Национальным институтом рака США: I степень — бессимптомный выпот; II степень — с клиническими проявлениями, показано любое вмешательство, такое как назначение диуретиков, или до 2 терапевтических торакоцентезов; III степень — с клиническими проявлениями, требующими ингаляций кислорода, более 2 торакоцентезов, установки дренажа или плевродеза; IV степень — угрожающий жизни (например, вызывающий нестабильность гемодинамики или требующий ИВЛ). Всем пациентам выполняли рентгенографию грудной клетки по назначению исследователя либо через зафиксированные в протоколе промежутки времени (до начала терапии дазатинибом, через 12 нед. и 6 мес.), чтобы свое временно выявить бессимптомный плевральный выпот.
Для данного анализа любого пациента с плевральным выпотом, развившимся в любое время, включали в группу плеврального выпота независимо от того, относил ли исследователь это осложнение к связанному с терапией дазатинибом. По статистическим соображениям данные анализировали, исходя из первого зафиксированного для каждого пациента упоминания о плевральном выпоте. Поскольку, согласно протоколу, обследования и индивидуальные регистрационные формы не предусматривали сбор информации о длительности плеврального выпота, его рассасывании или рецидивировании, эти данные не подлежали анализу.
Лечение плеврального выпота
В протоколе исследования содержались следующие рекомендации по лечению негематологических НЯ II степени и выше: после возникновения НЯ II степени прием дазатиниба прерывали до тех пор, пока это НЯ не разрешалось (до I степени и ниже, что определялось отдельными исследователями), затем прием препарата возобновляли в той же дозе. При первом рецидиве НЯ II степени терапию дазатинибом прерывали, а затем назначали препарат в сниженной дозе (например, уменьшали дозу со 100 до 80 мг 1 раз в сутки). В случае повторного рецидива НЯ II степени исследователь мог отменить дазатиниб, если это было лучшим выходом для пациента (в группах 140 мг 1 раз в сутки и 70 мг 2 раза в сутки допускалось второе уменьшение дозы). При возникновении НЯ III степени терапию дазатинибом прерывали до разрешения НЯ, затем дозу препарата снижали. После рецидива НЯ III степени решался вопрос о полной отмене препарата (или дозу повторно уменьшали, если это допускалось протоколом). В случае НЯ IV степени больной, как правило, больше не получал дазатиниб, если только исследователь не считал, что в интересах пациента — продолжить терапию.
Другие мероприятия по поводу плеврального выпота проводились по усмотрению исследователя. Для оценки влияния диуретиков и кортикостероидов, которые могли бы применяться для лечения плеврального выпота, был выполнен поиск в листах назначений с использованием названий 26 различных диуретиков и 15 различных кортикостероидов. Все диуретики и кортикостероиды, которые получал больной в то время, когда у него имелся плевральный выпот, считали использованными для лечения этого осложнения.
Также изучалось применение торакоцентеза при плевральном выпоте, который проводили по решению исследователя. Отчетность по торакоцентезу и НЯ велась раздельно, при этом, как правило, не указывалось, с какой целью была выполнена процедура: диагностической, лечебной или и с той и с другой. Результаты диагностического торакоцентеза не учитывали, т. к. протокол этого не требовал.
Оценка ответа
Эффективность оценивали с помощью стандартных исследований крови и костного мозга, позволявших определить частоту полного гематологического ответа (ПГО), большого цитогенетического ответа (БЦО) и полного цитогенетического ответа (ПЦО), что было описано ранее.7
Лимфоцитоз
В настоящем анализе лимфоцитозом, возникшим во время терапии дазатинибом, считали минимум двукратное выявление абсолютного числа лимфоцитов в крови более 3,6 × 109/л в период более 4 нед. от начала приема дазатиниба. Общий анализ крови выполняли перед началом исследуемой терапии, а затем — через регулярные промежутки времени (каждые 2 нед. в первые 12 нед. и каждые 3 мес. после этого срока). В настоящем исследовании повышенное число лимфоцитов, выявленное в пределах первых 4 нед. терапии дазатинибом, не учитывали как лимфоцитоз. Среднее число лимфоцитов в группах больных рассчитывали по средним значениям всех измерений абсолютного содержания лимфоцитов после первых 4 нед. терапии дазатинибом у каждого пациента.
Статистический анализ
Длительность ответа, выживаемость без прогрессирования (ВБП), общую выживаемость (ОВ) и длительность терапии до появления плеврального выпота оценивали по методу «продукт-лимит» Каплана—Мейера с расчетом 95%-х доверительных интервалов (ДИ). Прогрессированием считали повышение числа лейкоцитов, утрату ПГО или БЦО, повышение числа метафаз Ph+ на 30% и более, подтвержденный переход заболевания в фазу акселерации или бластного криза, а также смерть. При определении длительности ответа и ВБП остававшихся в живых пациентов, у которых никогда не было прогрессирования или утраты ответа, цензурировали на момент последнего (перед выбыванием из-под наблюдения) цитогенетического или гематологического обследования. Наблюдение прекращалось в случаях отмены исследуемого препарата по причинам, обговоренным в протоколе, в т. ч. вследствие отзыва информированного согласия, любого НЯ, отклонения лабораторных показателей от нормы или сопутствующего заболевания (при котором, по мнению исследователя, продолжение приема дазатиниба не было лучшим выбором для пациента), а также беременности или трансплантации гемопоэтических стволовых клеток (ТГСК). При анализе ОВ больных, которые не умерли, и тех, которые выбыли изпод наблюдения, цензурировали по последней дате, на момент которой было известно, что они живы, независимо от того, продолжали ли они прием дазатиниба или нет. При анализе длительности терапии до появления плеврального выпота пациентов, у которых не возникло данного осложнения, цензурировали в случае отмены дазатиниба по любой причине.
Для сравнения частоты плеврального выпота в разных группах лечения применяли точный критерий Фишера. Для оценки возможной связи между плевральным выпотом и лимфоцитозом или цитогенетическим ответом использовали критерий χ2 Пирсона. Поскольку эти анализы не были предусмотрены заранее и не были контролируемыми, интерпретировать их статистическую значимость невозможно, а значения p вычислены только в целях описания.
Анализ факторов риска
В качестве потенциальных факторов риска плеврального выпота изучали исходные характеристики больных и возникновение лимфоцитоза на фоне терапии дазатинибом. Отношения шансов (ОШ) и 95% ДИ вычисляли с помощью модели логистической регрессии. Вероятность плеврального выпота подвергалась регрессии как единичная ковариата. Непрерывные переменные делили на категории (возраст) или квартили (время от первоначальной постановки диагноза). Протокол исследования не предусматривал рутинный сбор данных по сопутствующим заболеваниям и состояниям (например, патология сердца или легких в анамнезе, задержка жидкости при лечении иматинибом), поэтому эта информация не была включена в анализ факторов риска. Была создана модель многомерной логистической регрессии, в которой оценивалась вероятность достижения цитогенетического ответа (БЦО и ПЦО) в зависимости от исходных характеристик пациента и возникновения во время исследования лимфоцитоза и плеврального выпота. Больных, у которых отсутствовала информация по любой из заданных ковариант, из регрессионного анализа исключали. Вследствие большого числа полученных значений p, а также из-за отсутствия коррекции по множественным сравнениям значения p приводятся только в целях описания.
Результаты
Демографические характеристики пациентов
Демографические характеристики пациентов и особенности заболевания в исследовании CA180-034 уже были представлены ранее.6 Всего дазатиниб получало 662 больных: 165 — в дозе 100 мг 1 раз в сутки, 167 — по 70 мг 2 раза в сутки, 163 — 140 мг 1 раз в сутки, 167 — по 50 мг 2 раза в сутки. Медиана возраста была равна 55 годам (диапазон 18–84 года). Медиана предшествующей терапии иматинибом составила около 3 лет. Во всех группах медиана длительности лечения дазатинибом равнялась 22 мес. Минимальный срок наблюдения для данного анализа составил 24 мес. (первый визит последнего пациента до закрытия базы данных).
Режим приема дазатиниба и плевральный выпот
Плевральный выпот любой степени возник у 22% всех пациентов. В группе 100 мг дазатиниба 1 раз в сутки общая частота плеврального выпота после минимум 24 мес. наблюдения составила 14% (III степени — 2%, IV степени — 0%). При сроке наблюдения минимум 12 мес. плевральный выпот отмечен у 10% пациентов (III степени — 2%, IV степени — 0%), что свидетельствует о минимальном нарастании частоты этого осложнения между 12-м и 24-м месяцем. Общая 24-месячная частота плеврального выпота в остальных группах исследования составила 23%–26% (p = 0,021 для сравнения всех 4 групп) (табл. 1). При объединении всех групп лечения медиана времени до появления плеврального выпота любой степени составила 183 дня. В группе 100 мг дазатиниба 1 раз в сутки этот показатель был равен 315 дням по сравнению с 136, 148 и 289 днями в группах приема препарата по 70 мг 2 раза в сутки, 140 мг 1 раз в сутки и 50 мг 2 раза в сутки соответственно. Согласно анализу по методу Каплана— Мейера, у пациентов, получавших 100 мг дазатиниба 1 раз в сутки, 12- и 24-месячная частота плеврального выпота составили 10% и 16% соответственно (рис. 1).
Таблица 1. Характеристики пациентов и возникновение плеврального выпота
| 100 мг 1 раз в сутки, n = 165 | 70 мг 2 раза в сутки, n = 167 | 140 мг 1 раз в сутки, n = 163 | 50 мг 2 раза в сутки, n = 167 | Все пациенты, n = 662 | ||||
|---|---|---|---|---|---|---|---|---|
| Медиана (диапазон) возраста, лет | 56 (20–78) | 54 (18–83) | 54 (20–84) | 55 (21–84) | 55 (18–84) | |||
| Медиана (диапазон) длительности ХМЛ до рандомизации, мес. | 55 (2–251) | 52 (1–246) | 56 (1–227) | 52 (4–212) | 54 (1–251) | |||
| Медиана (диапазон) длительности терапии дазатинибом, мес. | 22 (1–30) | 22 (22 (22 (22 ( | Пациенты с плевральным выпотом (учитывалась наибольшая степень), n (%) | |||||
| Любой степени | 23 (14) | 42 (25) | 43 (26) | 39 (23) | 147 (22) | |||
| I | 2 (1) | 7 (4)a | 8 (5) | 6 (4) | 23 (3)a | |||
| II | 17 (10) | 25 (15) | 27 (17) | 27 (16) | 96 (15) | |||
| III | 4 (2) | 8 (5) | 6 (4) | 6 (4) | 24 (4) | |||
| IV | 0 (0) | 2 (1) | 2 (1) | 0 (0) | 4 (1) | |||
| Медиана (диапазон) времени до первого обнаружения плеврального выпота, дни | ||||||||
| Любой степени | 315 (19–805) | 135,5 (1–881) | 148 (4–785) | 289 (12–798) | 183 (1–881) | |||
| I | 282 (88–322) | 171 (1–753) | 85 (12–603) | 299,5 (36–613) | 173 (1–753) | |||
| II | 338 (19–805) | 87 (20–881) | 161 (4–785) | 289,0 (12–798) | 201 (4–881) | |||
| III | 315 (266–503) | 339,5 (39–696) | 246,5 (69–738) | 172,5 (16–370) | 289 (16–738) | |||
| IV | — | — | 53 (13–93) | — | 53 (13–93) | |||
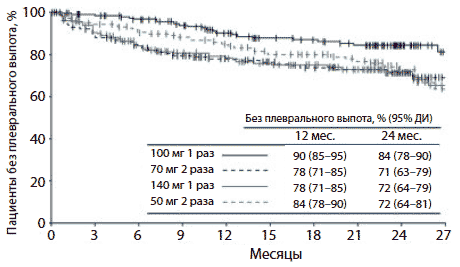
Рис. 1. Результаты анализа по методу Каплана—Мейера длительности терапии дазатинибом до появления плеврального выпота любой степени. Пациентов цензурировали на момент окончания лечения дазатинибом
Лечение плеврального выпота
После развития плеврального выпота лечение было временно приостановлено у 12 пациентов из группы 100 мг дазатиниба 1 раз в сутки (что составляет 7% от всех 165 больных этой группы и 52% от 23 пациентов с плевральным выпотом) по сравнению с 22–25 пациентами из остальных групп (13%–15% всех пациентов в каждой группе и 56%–60% больных с плевральным выпотом) (табл. 2). Доза дазатиниба после появления плеврального выпота была снижена у 8 пациентов из группы приема препарата 100 мг 1 раз в сутки (5% всех больных этой группы, 35% — с плевральным выпотом) по сравнению с 13–16 пациентами в остальных группах (8%–10% больных в группе, 30%–38% — с плевральным выпотом).
Дополнительные препараты, назначенные при появлении плеврального выпота пациентам, которые получали 100 мг дазатиниба 1 раз в сутки, в 13 случаях включали диуретики (8% от всех больных в данном исследовании, 57% — с плевральным выпотом), в 6 случаях — кортикостероиды (4% от всех больных, 26% — с плевральным выпотом). В остальных группах лечения диуретики вводили 17–20 пациентам (10%–12% больных из каждой группы, 40%–51% — с плевральным выпотом), кортикостероиды — 8–9 пациентам (5% больных из каждой группы, 19%–23% — с плевральным выпотом).
Диагностический или лечебный торакоцентез при наличии плеврального выпота проведен у 12 больных из всех групп. В одном случае торакоцентез, вероятно, с диагностической целью был выполнен пациенту с плевральным выпотом I степени. Кроме того, этой процедуре подверглось 5 больных с плевральным выпотом II степени и 6 — III степени. У 3 из 12 пациентов (1 получал дазатиниб по 50 мг 2 раза в сутки, 2 — по 70 мг 2 раза в сутки) торакоцентез выполнялся дважды. Плевральный выпот послужил основанием для отмены исследуемого лечения у 3 (2%) больных из группы 100 мг дазатиниба 1 раз в сутки и у 7 (4%–5%) из 9 пациентов из других групп.
Таблица 2. Лечение плеврального выпота в рамках исследования CA180-034
| 100 мг 1 раз в сутки | 70 мг 2 раза в сутки | 140 мг 1 раз в сутки | 50 мг 2 раза в сутки | Все пациенты | |
|---|---|---|---|---|---|
| Пациенты с плевральным выпотом, n | 23 | 42 | 43 | 39 | 147 |
| Прерывание терапии, n (%) | 12/23 (52) | 25/42 (60) | 24/43 (56) | 22/39 (56) | 83/147 (56) |
| Снижение дозы, n (%) | 8/23 (35) | 16/42 (38) | 13/43 (30) | 14/39 (36) | 51/147 (35) |
| Диуретики, n (%) | |||||
| Любая степень | 13/23 (57) | 19/42 (45) | 17/43 (40) | 20/39 (51) | 69/147 (47) |
| I | 0/3 (0) | 2/13 (15) | 2/10 (20) | 1/6 (17) | 5/32 (16) |
| II | 12/17 (71) | 16/25 (64) | 13/27 (48) | 17/27 (63) | 58/96 (60) |
| III | 1/3 (33) | 1/4 (25) | 2/4 (50) | 2/6 (33) | 6/17 (35) |
| IV | — | — | 0/2 (0) | — | 0/2 (0) |
| Кортикостероиды, n (%) | |||||
| Любая степень | 6/23 (26) | 9/42 (21) | 8/43 (19) | 9/39 (23) | 32/147 (22) |
| I | 1/3 (33) | 3/13 (23) | 4/10 (40) | 1/6 (17) | 9/32 (28) |
| II | 4/17 (24) | 5/25 (20) | 3/27 (11) | 5/27 (19) | 17/96 (18) |
| III | 1/3 (33) | 1/4 (25) | 1/4 (25) | 3/6 (50) | 6/17 (35) |
| IV | — | — | 0/2 (0) | — | 0/2 (0) |
Лимфоцитоз
Среди всех обследованных пациентов лимфоцитоз был обнаружен у 37% больных с плевральным выпотом и у 26% — без него (табл. 3). Среди оцененных больных с лимфоцитозом плевральный выпот появился у 29% по сравнению с 20% пациентов без лимфоцитоза. Критерий χ2 указывает на возможную связь между лимфоцитозом и плевральным выпотом (p = 0,0082). Среднее число лимфоцитов у оцененных больных с плевральным выпотом равнялось 2,82 × 109/л, а у пациентов без выпота — 2,05 × 109/л.
Таблица 3. Возникновение лимфоцитоза и плеврального выпота у пациентов, получавших любую дозу дазатиниба в рамках исследования CA180-034 (p = 0,0082 для сравнения 2 × 2)
| Без плеврального выпота | Плевральный выпот | Общее число пациентов | |
|---|---|---|---|
| Лимфоцитоз | 132 71% больных с лимфоцитозом 26% больных без плеврального выпота | 54 29% больных с лимфоцитозом 37% больных с плевральным выпотом | 186 |
| Без лимфоцитоза | 371 80% больных без лимфоцитоза 72% больных без плеврального выпота | 91 20% больных без лимфоцитоза 62% больных с плевральным выпотом | 462 |
| Не оценены | 12 | 2 | 14 |
| Всего | 515 | 147 | 662 |
Факторы риска плеврального выпота
В качестве потенциальных факторов риска плеврального выпота изучались следующие исходные характеристики больных: возраст, пол, длительность ХМЛ до назначения дазатиниба и ТГСК в анамнезе. Из них единственным параметром, связанным с повышенным риском плеврального выпота, оказался пожилой возраст (рис. 2, табл. 4). Развитие лимфоцитоза на фоне терапии дазатинибом повышало риск плеврального выпота в 1,7 раза (95% ДИ 1,1–2,5).
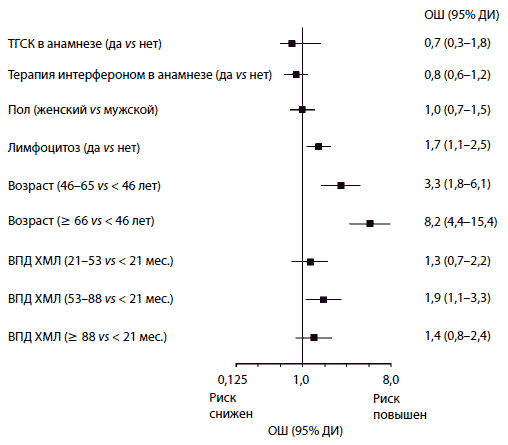
Рис. 2. Анализ исходных характеристик пациентов и возникновения лимфоцитоза на фоне лечения дазатинибом как факторов риска для плеврального выпота. ВПД — время от постановки диагноза
Таблица 4. Возникновение плеврального выпота в зависимости от возрастной группы
| Возраст, лет | Число пациентов | Пациенты с плевральным выпотом, n (%) |
|---|---|---|
| 44 | 3 (7) | |
| 30–39 | 79 | 2 (3) |
| 40–49 | 123 | 17 (14) |
| 50–59 | 160 | 32 (20) |
| 60–69 | 160 | 47 (29) |
| ≥ 70 | 96 | 46 (48) |
Гематологический и цитогенетический ответ
Плевральный выпот не влиял на достижение и сохранение ответа на дазатиниб. Частота ПГО как при наличии, так и отсутствии плеврального выпота равнялась 91% (табл. 5). В группе 100 мг дазатиниба 1 раз в сутки частота ПГО у пациентов с плевральным выпотом и без него составила 96% и 92% соответственно. Общая частота БЦО при наличии плеврального выпота была равна 70%, а при его отсутствии — 61% (p = 0,044); в группе 100 мг дазатиниба 1 раз в сутки этот показатель составил 70% и 63% соответственно (p = 0,57). Среди всех больных с БЦО из 4 групп этот ответ к 18-му месяцу сохранялся у 85% пациентов с плевральным выпотом и у 89% — без него (рис. 3). В группе 100 мг дазатиниба 1 раз в сутки БЦО к 18-му месяцу сохранялся у 93% больных как с наличием выпота, так и с его отсутствием. Общая частота ПЦО при наличии и отсутствии выпота была равна 61% и 49% соответственно (p = 0,13), те же показатели отмечены и в группе 100 мг дазатиниба 1 раз в сутки (p = 0,27). Среди всех пациентов, достигших ПЦО, из 4 групп этот ответ к 18-му месяцу сохранялся у 88% больных с плевральным выпотом и у 92% — без него. В группе 100 мг дазатиниба 1 раз в сутки ПЦО к 18-му месяцу сохранялся у 93% пациентов с плевральным выпотом и у 95% — без него. У больных с плевральным выпотом гематологический и цитогенетические ответы были достигнуты не только до появления выпота, но и после него (табл. 6).
Был выполнен многофакторный анализ отобранных исходных характеристик больных (возраст, время от первоначальной постановки диагноза ХМЛ, результат применения иматиниба [ резистентность / субоптимальный ответ, непереносимость], БЦО при терапии иматинибом, исходное число Ph+-клеток или бластов в костном мозге, исходное число лейкоцитов или базофилов в крови), а также возникновения плеврального выпота и лимфоцитоза, их связи с БЦО или ПЦО при лечении дазатинибом (табл. 7). В анализ включили всех пациентов, получивших любую дозу дазатиниба. Плевральный выпот был связан с повышенной вероятностью БЦО (p = 0,0039) и ПЦО (p = 0,0027). После корректировки по другим проанализированным переменным при сравнении пациентов с плевральным выпотом и без него ОШ достижения как БЦО, так и ПЦО составило 2,1 (95% ДИ 1,3–3,5). Таким образом, плевральный выпот может быть связан с повышенной вероятностью получения ответа на дазатиниб.
Таблица 5. Частота гематологического и цитогенетического ответов у больных с плевральным выпотом и без него
| Пациенты, n (%) | |||||
|---|---|---|---|---|---|
| 100 мг 1 раз в сутки, n = 165 | 70 мг 2 раза в сутки, n = 167 | 140 мг 1 раз в сутки, n = 163 | 50 мг 2 раза в сутки, n = 167 | Все пациенты, n = 662 | |
| ПГО | |||||
| Все пациенты | 152 (92) | 148 (89) | 145 (89) | 156 (93) | 601 (91) |
| С плевральным выпотом | 22 (96) | 38 (90) | 36 (84) | 38 (97) | 134 (91) |
| Без плеврального выпота | 130 (92) | 110 (88) | 109 (91) | 118 (92) | 467 (91) |
| БЦО | |||||
| Все пациенты | 106 (64) | 103 (62) | 105 (64) | 103 (62) | 417 (63) |
| С плевральным выпотом | 16 (70) | 27 (64) | 32 (74) | 28 (72) | 103 (70) |
| Без плеврального выпота | 90 (63) | 76 (61) | 73 (61) | 75 (59) | 314 (61) |
| ПЦО | |||||
| Все пациенты | 83 (50) | 90 (54) | 84 (52) | 84 (50) | 341 (52) |
| С плевральным выпотом | 14 (61) | 24 (57) | 26 (60) | 25 (64) | 89 (61) |
| Без плеврального выпота | 69 (49) | 66 (53) | 58 (48) | 59 (46) | 252 (49) |
Таблица 6. Ответ на дазатиниб у пациентов с плевральным выпотом любой степени: достижение начального ответа до или после возникновения выпота
| 100 мг 1 раз в сутки (n = 23) | Все группы (n = 147) | |||||
|---|---|---|---|---|---|---|
| Ответ до возникновения выпота | Ответ после возникновения выпота | Всего, n (%) | Ответ до возникновения выпота | Ответ после возникновения выпота | Всего, n (%) | |
| ПГО | 22 | 0 | 22 (96) | 122 | 12 | 134 (91) |
| БЦО | 14 | 2 | 16 (70) | 67 | 36 | 103 (70) |
| ПЦО | 12 | 2 | 14 (61) | 55 | 34 | 89 (61) |
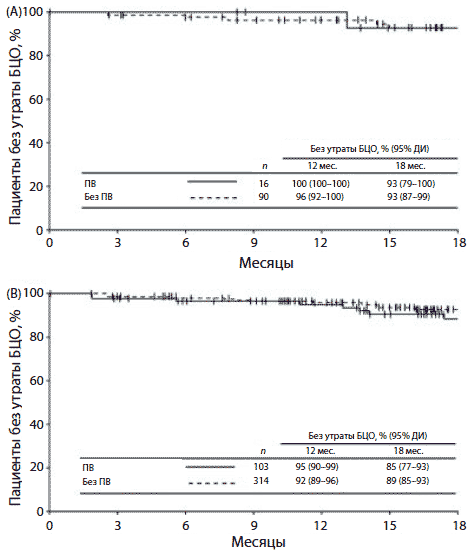
Рис. 3. Результаты анализа длительности БЦО по методу Каплана—Мейера у пациентов с плевральным выпотом и без него. (A) Дазатиниб 100 мг 1 раз в сутки. (B) Все больные, получившие лечение. ПВ — плевральный выпот
Таблица 7. Многофакторный анализ связи исходных характеристик пациентов, возникновения плеврального выпота или лимфоцитоза с достижением БЦО либо ПЦО при терапии дазатинибом (n = 621)
| Переменная | p | |||
|---|---|---|---|---|
| БЦО | ПЦО | |||
| Возраст | 0,0003 | |||
| Исходное число лейкоцитов | 0,1511 | 0,1806 | ||
| Исходное число базофилов | 0,6866 | 0,3427 | ||
| Исходное содержание бластов в костном мозге | 0,3868 | 0,3857 | ||
| Исходное содержание клеток Ph+ в костном мозге | Резистентность к иматинибу или его непереносимость | 0,0224 | 0,0003 | |
| БЦО на иматиниб в анамнезе | Время от выявления ХМЛ до первого приема дазатиниба | 0,0011 | 0,0001 | |
| Лимфоцитоз во время терапии дазатинибом | 0,0006 | 0,0995 | ||
| Плевральный выпот во время терапии дазатинибом | 0,0039 | 0,0027 | ||
ВБП и ОВ
У пациентов с наличием и отсутствием плеврального выпота ВБП и ОВ были сопоставимы. Так, 24-месячная ВБП у больных с плевральным выпотом составила 75%, а у пациентов без выпота — 76% (рис. 4). В группе 100 мг дазатиниба 1 раз в сутки ВБП была равна 78% и 80% соответственно. 24-месячная ОВ у всех больных с плевральным выпотом и без него составила 93% и 90% соответственно, а у пациентов, получавших 100 мг дазатиниба 1 раз в сутки, — 89% и 91% соответственно (рис. 5).
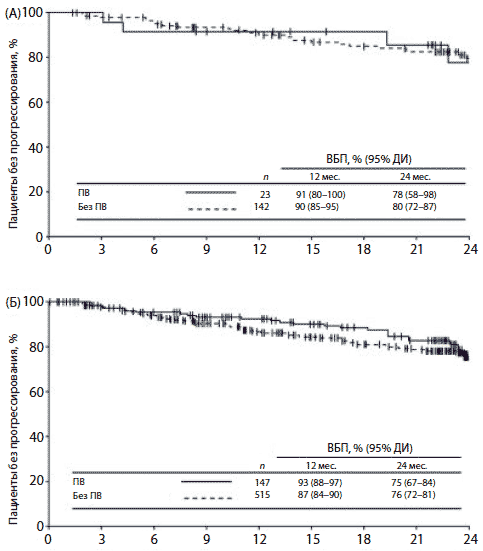
Рис. 4. Результаты анализа ВБП по методу Каплана—Мейера у пациентов с плевральным выпотом и без него. (A) Дазатиниб 100 мг 1 раз в сутки. (B) Все больные, получившие лечение. ПВ — плевральный выпот

Рис. 5. Результаты анализа ОВ по методу Каплана—Мейера у пациентов с плевральным выпотом и без него. (A) Дазатиниб 100 мг 1 раз в сутки. (B) Все больные, получившие лечение. ПВ — плевральный выпот
Обсуждение
Результаты настоящего анализа свидетельствуют, что одобренная в настоящее время для лечения ХФ ХМЛ доза дазатиниба (100 мг 1 раз в сутки) минимизирует частоту плеврального выпота. При минимальном времени наблюдения 24 мес. в группе 100 мг дазатиниба 1 раз в сутки это осложнение возникло у 14% пациентов, а в остальных группах — у 23%–26%. Кроме того, лишь у 2% больных, получавших 100 мг дазатиниба 1 раз в сутки, отмечен плевральный выпот III степени, а случаев этого осложнения IV степени не зафиксировано. В остальных группах частота выпота III–IV степени составляла 4%–6%. Наблюдение показало, что к 24-му месяцу частота плеврального выпота возрастала в минимальной степени по сравнению с таковой к 12-му месяцу. Терапия дазатинибом в дозе 100 мг 1 раз в сутки также была связана с наибольшим временем до появления плеврита (медиана 315 дней vs 136–289 дней в других группах). Более низкая частота и большее время до возникновения плеврального выпота, наблюдаемые в группе 100 мг дазатиниба 1 раз в сутки, могут быть результатом либо более редкого, либо более позднего возникновения выпота (или и того и другого), поэтому наблюдение целесообразно продолжить.
Необходимо обратить внимание на то, что частота ПГО, БЦО, ПЦО, продолжительность ответов, ВБП и ОВ у пациентов с плевральным выпотом были сопоставимыми или превосходили те же показатели у пациентов без выпота. Во всех 4 группах отмечена сходная эффективность дазатиниба. В некоторых случаях ПГО, БЦО или ПЦО на дазатиниб были получены после появления плеврального выпота. Следовательно, плевральный выпот, несмотря на то что он иногда приводит к перерывам в терапии и снижению дозы, не препятствует достижению ответа.
В исследовании CA180-034 лечение плеврального выпота во всех группах имело большое сходство. Примерно в 1/2 случаев появление выпота повлекло за собой временное прерывание терапии, а приблизительно в 1/3 случаев — снижение дозы. Пациенты с плевральным выпотом чаще получали диуретики, чем кортикостероиды (примерно 50% vs 25% случаев). В группе 100 мг дазатиниба 1 раз в сутки по сравнению с другими реже требовалось прерывание лечения и снижение дозы из-за плеврального выпота, хотя дизайн исследования и не позволил провести статистическое сравнение. Методы лечения плеврального выпота в настоящем наблюдении соответствовали описанным в других работах.8,9 Поскольку в ходе исследования CA180-034 данные по длительности и разрешению плеврального выпота не собирались, относительную эффективность различных мер по лечению этого осложнения оценить невозможно; изучение данного вопроса может стать целью для последующих работ.
Лучшая переносимость режима приема дазатиниба по 100 мг 1 раз в сутки может частично быть обусловлена прерывистым воздействием ингибирующих концентраций препарата в отличие от непрерывного влияния в случае приема 2 раза в сутки.6 Недавний фармакокинетический анализ показал, что риск плеврального выпота снижался при уменьшении минимальной концентрации дазатиниба в плазме, при этом прием 100 мг препарата 1 раз в сутки давал наименьшую устойчивую концентрацию по сравнению с другими режимами приема.10 Лабораторные исследования свидетельствуют, что вследствие высокой активности дазатиниба его прерывистого воздействия достаточно, чтобы ингибировать киназу BCR-ABL и вызвать апоптоз в клеточных линиях ХМЛ.11 Этот факт помогает объяснить одинаковую эффективность дазатиниба в 4 группах лечения в исследовании CA180-034.
Точный механизм возникновения плеврального выпота при терапии дазатинибом неизвестен. Исследования в рамках одного медицинского учреждения показали, что в большинстве случаев выпот носил экссудативный характер.8,9 Имеются сообщения о высоком содержании лимфоцитов в жидкости и плевре,8 а также о связи выпота с иммунными реакциями, например кожной сыпью или аутоиммунными нарушениями в анамнезе.12 Эти данные позволили предположить иммунный механизм возникновения плеврального выпота. Такую гипотезу поддерживает недавнее сообщение Mustjoki et al., касающееся пациентов с различными фазами ХМЛ или Ph+ ОЛЛ; показано, что у больных с лимфоцитозом, возникшим на фоне терапии дазатинибом, частота плеврального выпота повышена.13 В настоящем анализе, в который вошли больные только с ХФ ХМЛ, отмечена возможная связь между лимфоцитозом и развитием плеврального выпота, хотя частота последнего у пациентов с лимфоцитозом (29%) была ниже, чем в работе Mustjoki et al. (около 60%). С другой стороны, еще в одной статье не обнаружено никакой связи между лимфоцитозом и плевральным выпотом.14 Поскольку дазатиниб ингибирует не только BCR-ABL, для объяснения задержки жидкости и образования плеврального выпота предложены другие объяснения, в т. ч. ингибирование PDGFR-β, которое снижает давление интерстициальной жидкости, или ингибирование киназ из семейства SRC, которое повышает проницаемость сосудов.9
Помимо иммунных заболеваний в анамнезе описаны и другие факторы риска плеврального выпота, в т. ч. гипертензия, болезни сердца, сопутствующая патология легких, суточная доза дазатиниба более 100 мг, а также лечение на поздних стадиях ХМЛ.9,12,15 Протокол настоящего исследования и собранная информация не позволяли провести аналогичную оценку сопутствующей патологии, тем не менее отмечена связь пожилого возраста и повышенного риска плеврального выпота. Ранее проведенный однофакторный анализ тоже показал, что пожилой возраст (более 60 лет) служит фактором риска для плеврального выпота, однако при последующем многофакторном анализе это не подтвердилось.9
В настоящем анализе отмечена возможная связь между плевральным выпотом и лимфоцитозом, а также достижением цитогенетического ответа при терапии дазатинибом. В предшествующем исследовании плевральный выпот, возникший во время терапии дазатинибом, коррелировал с повышенной частотой молекулярного ответа, в то время как различия в частоте цитогенетического ответа были статистически незначимыми.15 В других исследованиях показан благоприятный результат лечения у пациентов с лимфоцитозом, возникшим на фоне терапии дазатинибом; было предположено, что данный факт мог быть обусловлен антилейкозными эффектами, вызванными активацией иммунитета.13,14 Чтобы подтвердить эту предполагаемую связь, нужны дополнительные проспективные исследования. Гипотетический иммунный механизм, включающий возникновение лимфоцитоза, наводит на мысль, что для лечения плеврального выпота, связанного с терапией дазатинибом, целесообразно применять кортикостероиды.
В заключение стоит отметить, что, согласно представленному анализу, у пациентов с ХФ ХМЛ и резистентностью, субоптимальным ответом или непереносимостью предшествующей терапии иматинибом дазатиниб в дозе 100 мг 1 раз в сутки минимизирует частоту плеврального выпота. Следует подчеркнуть, что появление выпота не влияет на достижение гематологического и цитогенетических ответов, а также на их длительность, ВБП и ОВ.
Конфликты интересов
Проведение клинического исследования, статистический анализ и помощь в написании данной статьи спонсировались Bristol-Myers Squibb (BMS). Kimmo Porkka выступал как консультант, получал гонорары и средства на исследования от BMS и Novartis. H. Jean Khoury получал гонорары от BMS, Novartis и Genzyme. Ronald L. Paquette выступал консультантом для BMS, Alexion и Telik, а также получал гонорары как представитель бюро докладчиков BMS и Novartis. Yousif Matloub и Ritwik Sinha владеют акциями и являются служащими BMS. Yousif Matloub владеет акциями GlaxoSmithKline. Jorge E. Cortes получал средства на исследование от BMS, Wyeth и Novartis.
Литература
