Проблемы заместительной терапии гипотиреоза: современность и перспективы
Статьи Опубликовано в журнале, Клиническая и экспериментальная тиреоидология, 2012, том 8, №3 В.В. ФадеевФГБУЭндокринологический научный центр Минздравсоцразвития России, Москва
Challenges in replacement therapy of hypothyroidism: everyday practice and perspectives
V. V. Fadeyev
Federal Endocrinological Research Center, Moscow
Проблема заместительной терапии гипотиреоза, распространенность которого в общей популяции достигает 3,7% [1], так или иначе касается любого заболевания щитовидной железы (ЩЖ), поскольку в клинической практике большинство из них гипотиреозом так или иначе заканчивается, как самопроизвольно, так и вследствие врачебных вмешательств. На первый взгляд, заместительная терапия гипотиреоза достаточно проста и в соответствии с многочисленными клиническими рекомендациями подразумевает ежедневный прием L-T4 под периодическим контролем уровня тиреотропного гормона (ТТГ). Тем не менее, даже если не считать такого важного момента, как приверженность пациента к правильному лечению, здесь есть много дискуссионных вопросов и сложностей, решение которых, по мнению автора этого обзора, и представляет перспективу в обсуждаемой области тиреоидологии.
1. "Синдром НТВ-П" - на тироксине, но все равно плохо
Современным стандартом заместительной терапии гипотиреоза является монотерапия которая исходит из того, что дейодиназы - селеноэнзимы, экспрессированные в большинстве тканей, дейодируют Т4, превращая его в биологически активный Т3 [2]. Многолетняя клиническая практика показала, что на фоне монотерапии L-T4 в большинстве случаев достигается нормализация уровня ТТГ и св. Т4, при этом уровень циркулирующего Т3 остается ниже такового у здоровых людей [3], однако большинство пациентов чувствуют себя при этом в полной мере хорошо и только 10-15% пациентов, несмотря на стойкую нормализацию уровня ТТГ, продолжают предъявлять жалобы, сходные с таковыми при гипотиреозе [4]. Эту ситуацию, когда у пациента сохраняются жалобы, несмотря на стойкую нормализацию уровня ТТГ на фоне монотерапии L-T4, мы образно назвали "синдром НТВ-П", или "на тироксине, но все равно плохо". Именно этот "синдром" на сегодняшний день и представляет одну из основных проблем заместительной терапии гипотиреоза. Такое положение дел, когда существенная часть (10%) пациентов остается недовольной проводимым лечением, с одной стороны, стимулирует поиск причин сохраняющихся жалоб и методов усовершенствования заместительной терапии, а с другой - поддерживает распространение многочисленных пищевых добавок, экстрактов ЩЖ животных и всякого рода "формул щитовидной железы", которые распространяются через интернет и, увы, находят своего потребителя.
Симптомы гипотиреоза очень неспецифичны, в связи с этим потенциальных причин плохого самочувствия пациента с компенсированным по уровню ТТГ гипотиреозу может быть достаточно много. На уровне клинической практики, о которой речь еще пойдет, объяснить, почему пациент недоволен, для самого себя врачу удается почти всегда, при этом проблема недовольства пациента в дальнейшем, как правило, остается нерешенной. Другой путь состоит в попытке понять возможный патогенез плохого самочувствия пациента с гипотиреозом, несмотря на терапию L-T4, которая поддерживает нормальный ТТГ, отбросив на время личностные особенности пациента. Попробуем посмотреть на проблему и с той и с другой стороны.
1.1. Попытки выяснения патогенеза
В норме примерно 80-90% Т3 образуется за счет дейодирования Т4 дейодиназами 1-го и 2-го типов, которые, опять же, по-разному экспрессированы в различных тканях: D1 - преимущественно в печени и почках, а D2 - в центральной нервной системе, костях, коже, гипофизе, бурой жировой ткани и в небольших количествах - в скелетной мускулатуре и миокарде [7]. Таким образом, источником Т3 может быть как сама ЩЖ, так и в большей степени периферическое дейодирование Т4. Помимо этого, существует еще третья дейодиназа - D3, которая может инактивировать как Т4, так и Т3. Этот фермент экспрессируется преимущественно на эмбриональной стадии развития и лишь в следовых количествах у взрослых в головном мозге, коже, миокарде и β-клетках поджелудочной железы [8, 9]. В критических состояниях, при тяжелых заболеваниях, экспрессия D3 может многократно увеличиваться [10].
Так выглядит обмен тиреоидных гормонов в норме. Но возникает вопрос: может ли у лиц с гипотиреозом на фоне монотерапии L-T4 поддерживаться нормальный уровень Т3 в крови и клетках-мишенях? В недавнее одномоментное исследование было включено 3900 здоровых людей и 1800 пациентов, которым в прошлом была предпринята тиреоидэктомия. Как и следовало ожидать, было показано, что у получающих монотерапию L-T4 уровень Т3 сыворотки значимо ниже, чем у здоровых людей. Кроме того, оказалось, что у 15% пациентов на фоне терапии L-T4 уровень Т3 был ниже нормы, несмотря на нормализацию уровня ТТГ (опять же, именно у 10-15% пациентов с гипотиреозом сохраняются его симптомы, несмотря на нормализацию ТТГ; но у этих цифр, видимо, разное происхождение). Более того, повышение в этой ситуации дозы L-T4 зачастую не приводило к нормализации уровня Т4, несмотря на то, что уровень ТТГ порой падал ниже нор мы [11]. Представляет интерес тот факт, что когда пациентов и контрольную группу разделили на подгруппы в зависимости от уровня ТТГ, то в этих подгруппах (как при относительно низком, так и при относительно высоком ТТГ) уровень Т3 был ниже у лиц, получающих L-T3 [11]. Другими словами, зависимость между уровнем ТТГ и Т3 у лиц, получающих терапию L-T4, весьма умеренная. Сходные данные были получены и в одном из наших исследований [3].
Тем не менее полной уверенности в том, что этот феномен можно рассматривать как недостаток монотерапии L-T4, нет, поскольку Т4 по большей части является внутриклеточным гормоном. Конечно, существует зависимость между его сывороточным уровнем и содержанием в клетке, но как образование, так и деградация Т3 - процессы внутриклеточные и регулируются они внутриклеточными механизмами [12]. Другими словами, в защиту монотерапии L-T4 можно предположить, что недостаток Т3 в плазме на ее фоне компенсируется внутриклеточными процессами. Судя по всему, это определяется экспрессией дейодиназ в различных клетках.
О том, что сывороточный уровень Т3 - достаточно плохой маркер содержания Т3 внутри клетки, свидетельствует ряд экспериментов на животных. Так, у мышей с инактивированной D2 уровень Т3 всыворотке находится в пределах нормы, в то время как в головном мозге содержание Т3 в 2 раза ниже, чем у нормальных крыс [13]. Таким образом, вряд ли у пациентов с гипотиреозом, у которых мы пытаемся объяснить наличие симптомов неким "нарушением дейодирования Т4 в тканях", будет определяться сниженный уровень Т3 в крови. И наоборот, вряд ли несколько сниженный уровень Т3 в крови предопределяет такую симптоматику по той причине, что он ниже, чем у здоровых и у тех пациентов, которые на фоне монотерапии L-T4 не предъявляют особых жалоб.
С другой стороны, саму возможность такого нарушения или, вернее, особенностей обмена тиреоидных гормонов списывать со счетов не стоит, при этом логично предположить, что уровень Т3 сыворотки в первую очередь необходим тканям и клеткам, в которых низка экспрессия дейодиназ. Более точно ответить на этот вопрос могло бы прямое измерение содержания Т3 в клетках, которое проводилось пока только у грызунов. Здесь следует заметить, что обмен тиреоидных гормонов у крыс существенно отличается от человеческого: уровень Т3 в сыворотке у крыс примерно на 40% выше [12]. Тем не менее в хорошо известном испанском исследовании было показано, что когда крысам после тиреоидэктомии назначали L-T4, то, несмотря на повышение его дозы, не удалось достичь нормализации уровня Т4 и Т3 одновременно во всех тканях, а также одновременно нормализовать уровень Т3 как в плазме, так и в тканях (за исключением головного мозга). Содержание же Т3 в ликворе, коре головного мозга и мозжечке приходило в норму и при назначении даже относительно небольших доз L-T4, которые даже не приводили к нормализации уровня ТТГ [14]. Таким образом, в клетках головного мозга у крыс (а возможно, и у людей) содержится высокоэффективная D2, которая превращает циркулирующий Т4 вТ3. С одной стороны, это объясняет то, что почти 90% пациентов с гипотиреозом на фоне монотерапии L-T4 не предъявляют особых жалоб, а также то, что их вообще не предъявляет большая часть пациентов с субклиническим гипотиреозом, при котором уровень Т4 в крови нормальный. С другой стороны, чем объективно и доказательно объяснить недовольство лечением и симптомы гипотиреоза у оставшихся 10%?
У здоровых взрослых людей уровень Т4 и Т3 в сыворотке на протяжении жизни, как правило, остается более или менее постоянным [15], в то время как внутриклеточный уровень Т3 может изменяться вследствие различных метаболических и внешних факторов [16]. То есть в зависимости от обстоятельств продукция Т3 в отдельных тканях и/или его поступление туда меняются. Теоретически можно предположить, что эти процессы на фоне терапии L-Т4 неким образом изменяются. В свою очередь эти изменения можно объяснить неким нарушением функции внутриклеточных дейодиназ, которые не проявляются в норме, но появляются в ситуации, когда функция собственной ЩЖ заменяется приемом постоянной дозы L-T4.
Мутации генов дейодиназ, приводящие к выпадению их функции, до настоящего времени не описаны. Тем не менее существует описание двух семей, в которых у 3 человек определялась задержка роста вследствие дефекта экспрессии дейодиназ на фоне выраженного нарушения синтеза селенопротеинов [17]. Это крайне редкий синдром, при котором нарушается функция всех трех дейодиназ, при этом данных о том, что у пациентов нарушено внутриклеточное содержание Т3, пока нет.
У мышей с дефектом дейодиназы 1-го типа (D1) определяется повышение уровня Т4 и rТ3, тогда как уровень ТТГ и Т3, а также ряд показателей, свидетельствующих о периферических эффектах тиреоидных гормонов, остаются в норме. Кроме того, при дефиците D1 увеличивается экскреция с калом эндогенных йодтиронинов, что позволяет предполагать участие D1 в процессах компенсации йододефицитных состояний [18].
Что касается людей, то нуклеотидный полиморфизм rs2235544 гена DIO1 ассоциирован с повыше нием уровня св. Т3 и снижением уровня св. Т4 и fT4 при нормальном уровне ТТГ [19]. Сходным образом, у носителей аллеля D1b-G/T (rs12095080) среди пожилых людей определяется более высокий уровень Т3 и соотношения Т3/rТ3, тогда как у носителей аллеля D1a-C/T (rs11206244) - более высокие уровни св.Т4 и rT3, а также более низкие уровни Т3 и соотношения Т3/rT3 [20]. Вопреки указанным находкам, пациенты не испытывали никаких симптомов нарушения функции ЩЖ и, кроме того, уровень внутриклеточного Т3 у них не изучался.
У мышей с дефектной дейодиназой 2-го типа (D2) описаны множественные изменения, связанные с изменением внутриклеточного уровня Т3 в различных тканях: бурой жировой, головном мозге, гипофизе, скелете, скелетной мускулатуре и легких [8]. Возможно, с полиморфизмом или дефектами D2 связан ряд клинических синдромов у людей, поскольку именно активностью D2 определяется содержание Т3 в клетках головного мозга. Например, у крысят более половины Т3 в головном мозге определяется активностью D2 [21].
Полиморфизм DIO2-гена Thr92AlaD2 обнаруживается примерно у 15% здоровых людей. По имеющимся данным, он ассоциирован с инсулинорезистентностью, повышенным индексом массы тела, а также с сахарным диабетом [22]. По данным исследования случай-контроль, в которое вошли 1057 пациентов с сахарным диабетом 2-го типа и 516 здоровых людей, распространенность Thr92AlaD2 при сахарном диабете 2-го типа составила 16,4%, а у здоровых - 12%, что определило отношение шансов 1,41 [23]. Кроме того, была обнаружена ассоциация указанного полиморфизма с психической ретардацией [24], гипертензией [25], остеоартритом [26], биполярными расстройствами [27] и рядом других изменений. В контексте тематики этого обзора можно высказать предположение о том, что полиморфизм Thr92AlaD2 определяет некоторое снижение активности D2, что в свою очередь приводит к снижению внутриклеточного содержания Т3 в ряде тканей, т.е. к некоему "тканевому гипотиреозу", который и может обусловить те или иные расстройства, с которыми ассоциирован этот полиморфизм.
К сожалению, исследования, напрямую изучавшие активность D2 на тканевом уровне, пока были безуспешны. Тем не менее в двух клинических исследованиях было показано, во-первых, что у пациентов - носителей полиморфизма Thr92AlaD после тиреоидэктомии потребовались большие дозы L-T4, чтобы нормализовать уровень ТТГ, по сравнению с контрольной группой [28], а во-вторых, что указанный полиморфизм ассоциирован с более медленным повышением уровня Т3 в крови в ответ на стимули рующий тест с тиреоглобулином [29]. Каких-либо других изменений обмена тиреоидных гормонов у этих пациентов не выявлено. В целом результаты исследований, посвященные обсуждаемому полиморфизму, достаточно дискуссионны, но, безусловно, могут лежать в основе разработки более индивидуализированной заместительной терапии гипотиреоза в перспективе.
Дефект дейодиназы 3-го типа (D3) у мышей является причиной развития выраженных фенотипических изменений, которые обусловлены повышением уровня Т3 в фетальном периоде и после рождения, поскольку, как сказано выше, D3 отвечает за внутриклеточную деградацию Т4 и Т3. У таких животных имеет место вторичный гипотиреоз (высокое содержание Т3 в клетках гипоталамо-гипофизарной системы подавляет продукцию ТТГ), задержка роста и развития ЦНС, включая развитие фоторецепторов, улитки и слуховых функций; кроме того, таким животным свойственно агрессивное поведение и бесплодие [30]. Каких-либо потенциально значимых мутаций или полиморфизмов гена D3 у человека до настоящего времени не выявлено.
Дефицит тиреоидных гормонов в той или иной ткани, в частности в головном мозге, теоретически может быть обусловлен не только функцией дейодиназ, но и вариабельностью или дефектом транспорта гормонов через клеточные мембраны. Прежде чем поступить в клетку, как Т4, так и Т3 должны проникнуть через гематоэцефалический барьер, а затем через него же покинуть клетку. Т4 захватывается астроцитами и таницитами, содержащими D2, после чего образовавшийся Т3 должен покинуть эти клетки и попасть в соседние нейроны, где проявить свой биологический эффект, связываясь с рецепторами [31]. Любые нарушения на этом пути потенциально могут вести к снижению внутриклеточного содержания Т3 и дефициту его эффектов. В качестве модели такого состояния можно привести пример синдрома Алла-на-Гердона-Дадли (Allan-Herndon-Dudley), который развивается в результате инактивирующей мутации Х-сцепленного гена МСТ-8, продукт которого - белок семейства МСТ - является транспортетом Т3 через клеточную мембрану и экспрессируется во многих органах, включая головной мозг. При этом синдроме наблюдается психомоторное недоразвитие, развивается неврологический дефицит и вторичный гипотиреоз [32].
Еще одним транспортером является специфичный гематоэнцефалический анионный транспортер ОАТР1С1, который преимущественно экспрессируется в капиллярах головного мозга и имеет высокую аффинность и специфичность по отношению к Т4 [5]. У крыс экспрессия ОАТР1С1 и его мРНК зависит от уровня Т4 в сыворотке, что позволяет предположить его значение в регуляции содержания тиреоидных гормонов в клетках головного мозга [33]. В этой связи представляет интерес клиническое исследование, в которое вошел 141 пациент с гипотиреозом, при этом было показано, что полиморфизм ОАТР1С1 ассоциирован с усталостью и депрессией, но не связан с нейрокогнитивной дисфункцией [34].
Таким образом, если исходить из того, что у разных людей есть индивидуальные особенности ферментных и траспортных систем, которые обеспечивают поступление и внутриклеточный метаболизм тиреоидных гормонов, можно предположить, что именно они и являются возможной патогенетической основой некоего "тканевого гипотиреоза", объясняющего "синдром НТВ-П". В таком случае нужно постулировать, что все эти особенности нивелируются или компенсируются при нормально работающей собственной ЩЖ и проявляются только при ее разрушении (удалении), когда пациент начинает получать монотерапию L-T4. С другой стороны, "синдром НТВ-П" на клиническом уровне можно объяснить значительно проще.
Другим, достаточно простым объяснением, которое сродни первому, является наличие каких-то сопутствующих заболеваний, при этом статистика их распространенности, опять же, может убедить нас в том, что ситуация с сохранением жалоб у части пациентов вполне естественна. Достаточно указать, что, по данным зарубежных исследований, депрессивные состояния являются единственной причиной 10-20% визитов к врачам общей практики [36]. Не менее очевидно, что у пациентов с аутоиммун ным тиреоидитом (АИТ) или у получавших аблативную терапию по поводу болезни Грейвса (БГ) с повышенной частотой встречаются другие аутоиммунные заболевания.
Наконец, не менее очевидно, что при той же БГ, по крайней мере на этапе ее манифестации, не малое значение имеют крупные стрессорные события [37]. Кроме того, доля пациентов с гипотиреозом, "недовольных" заместительной терапией, несмотря на нормализованный ТТГ, значимо больше среди пациентов, перенесших аутоиммунные заболевания ЩЖ, чем среди прооперированных по поводу многоузлового зоба и рака ЩЖ [38]. Эти данные позволяют считать, что причиной дисфории пациентов с гипотиреозом могут быть некие неизвестные нам аутоиммунные процессы либо, наоборот, что некие психологические особенности, проявляющиеся в дальнейшем, способствуют развитию аутоимунных тиреопатий. Последнее в большей степени соответствует старым, так называемым неврогенным, теориям патогенеза БГ.
Так или иначе, эти достаточно простые объяснения не особо продуктивны, поскольку скорее оправдывают врача, но никак не способствуют решению проблемы пациента. В этой связи был предпринят ряд клинических исследований, которые, опять же, пытались исходить из концепции, в соответствии с которой у части пациентов с гипотиреозом на фоне монотерапии L-T4 сохраняется некая недостаточность тиреоидных гормонов. Такие исследования, увы, пока безуспешные, на сегодняшний день можно разделить на две группы: первые пытались исходить из того, что как минимум часть обсуждаемых проблем можно решить, сузив целевой диапазон ТТГ до низконормального, т.е. назначив несколько большую дозу L-T4; вторая группа исследований, опубликованных на протяжении последних 10 лет, пытается противопоставить монотерапии L-T4 комбинированную терапию L-T4 + L-T3.
Наиболее значимое (двойное слепое) исследование, в котором изучались возможные преимущества достижения у пациентов с гипотиреозом низконормального уровня ТТГ (0,4-2,0 мЕд/л), было опублиовано в 2006 г. John Walsh и соавт. В него были включены 52 женщины с установленным диагнозом гипотиреоза, которые находились на заместительной терапии препаратами L-T4 в дозе 100 мкг/сут и более. Исходный уровень ТТГ у всех обследуемых находился в пределах референсного интервала. В дальнейшем было проведено разделение пациентов на 3 группы (в зависимости от уровня ТТГ), в которых путем изменения дозы L-T4 оценивали параметры когнитивных функций и липидного профиля. По результатам исследования был сделан вывод, что изменение дозы L-T4 на 25-50 мкг/сут в ту или другую сторону не приводит к значимым изменениям в состоянии пациентов [39]. Помимо этого, было опубликовано еще несколько подобных исследований, в том числе и наше [40, 41], где не было показано существенных преимуществ достижения низконормального уровня ТТГ у пациентов с гипотиреозом, за исключением некоторых тенденций, которые не позволяют сделать более или менее оформленных выводов.
Более внушительная группа работ посвящена изучению возможностей комбинированной терапии L-T4 + L-T3 при гипотиреозе. История этого вопроса движется по спирали: первым синтетическим препаратом тиреоидных гормонов, который был внедрен в клиническую практику, был как раз L-T3. В дальнейшем, примерно в 70-80-е годы, от его использования практически само собой, т.е. без проведения особых сравнительных исследований, отказались, что произошло на фоне появления L-T4 и, что не менее важно, внедрения в клинику определения ТТГ (который успешно нормализовался на фоне одного только L-T4), а также разработки концепции внутриклеточного образования Т3 из циркулирующего Т4. Вновь возродило идею комбинированной терапии достаточно небольшое исследование R. Bunevicius и соавт. [42]. Оно, с одной стороны, было одним из первых сравнительных исследований в этом плане, с другой - подверглось аргументированной критике, как в плане использованных методов, так и в плане весьма разнородной группы вошедших в него пациентов.
Дальнейшие исследования и даже их метаанализ обладали более совершенным дизайном. Если суммировать их результаты, то большинство рандомизированных исследований, посвященных сравнительной оценке комбинированной и монотерапии, за исключением 3 [42-44] (при этом 2 из них принадлежат одной и той же группе авторов), не обнаружил статистически значимых различий между ними по каким-либо клиническим показателям. Метаанализ 11 исследований, в которые было суммарно рандомизировано 1216 пациентов, не выявил различий в эффективности монотерапии и комбинированной терапии по таким показателям, как симптомы гипотиреоза, выраженность депрессии, тревожности, усталости, а также по различным показателям качества жизни, уровню холестерина и его фракций [45].
На основании этих данных только что вышедшие клинические рекомендации Американской тиреоидной ассоциации (ETA) и Американской ассоциации клинических эндокринологов (ААСЕ) [46] "не рекомендуют комбинированное назначение L-T4 и L-T3 для заместительной терапии гипотиреоза в связи с отсутствием доказательных данных о его преимуществах". Более лояльны к комбинированной терапии недавние рекомендации Европейской тиреоидной ассоциации [47], в которых указывается, что "комбинированная терапия T4 + T3 может быть рекомендована в качестве экспериментального подхода у комплаентных пациентов, получающих L-T4, при наличии сохраняющихся жалоб, несмотря на нормализацию ТТГ, при условии исключения других хронических и сопутствующих аутоиммунных заболеваний, которые могут быть их причиной". При этом подчеркивается, что при отсутствии улучшения состояния пациента в течение 3 мес терапию L-T4 + L-T3 рекомендуется отменить [47, 48].
Со сделанными в этих рекомендациях выводами следует полностью согласиться, хотя к ним есть несколько ремарок. Во-первых, исходя из клинического опыта, часть пациентов при назначении им комбинации L-T4 + L-T3 чувствуют себя определенно лучше и часть пациентов (по нашим данным 17% [49], а в норвежском исследовании почти 40% [44]) при анкетировании выбирает именно ее, предпочитая монотерапии L-T4. Во-вторых, в проведенных исследованиях использовали разные дозировки и режимы приема L-T3. Это отражает тот факт, что в настоящее время на фармацевтическом рынке отсутствуют препараты L-T3, которые содержат дозы, близкие к физиологическим (соотношения L-T4: L-T3 между 13:1 и 20 : 1 [47]), и одновременно обладают физиологической кинетикой L-T3, т.е. обеспечивают стабильную концентрацию гормона в крови, а не его пиковые подъемы сразу после приема препарата. Наконец, в-третьих, все обсуждаемые исследования включали общую группу пациентов с гипотиреозом, а не пациентов с "синдромом НТВ-П". При этом совершенно очевидно, что если 90% общей группы пациентов на фоне подобранной монотерапии L-T4 чувствуют себя прекрасно, то оставшиеся 10% "недовольных" растворятся в этой несоразмерно большей группе и различий между двумя вариантами терапии найдено не будет. Исследований же отдельно отобранной группы пациентов - тех самых 10% "недовольных" монотерапией - пока не проводилось. Последней гипотезе отчасти вторят некоторые молекулярно-генетические данные. В исследовании WATTS, в которое вошли 552 человека, было показано, что у лиц, которые предпочитают комбинированную терапию L-T4 + L-T3 чаще встречается дейодиназный полиморфизм Thr92AlaD2 [50].
В этом разделе статьи были приведены различные научные гипотезы и результаты пилотных научных исследований, которые еще весьма далеки от внедрения в практику. В этой связи, поскольку этот обзор в первую очередь адресован практическим врачам, хотелось бы еще раз подчеркнуть, что для сегодняшней клинической практики следующие три положения остаются пока незыблемыми:
- Традиционная заместительная терапия L-T4, обеспечивающая стойкую нормализацию уровня ТТГ, позволяет поддерживать приемлемое качество жизни у подавляющего большинства пациентов с гипотиреозом.
- Около 10% пациентов с гипотиреозом, несмотря на нормализацию уровня ТТГ на фоне терапии L-T4, продолжают испытывать симптомы, сходные с гипотиреоидными, но в силу их неспецифичности генез этой симптоматики редко удается объективно выяснить и связать именно с недостаточностью тиреоидных гормонов.
- Все известные на сегодняшний день модификации заместительной монотерапии L-Т4 или ее альтернативы не имеют доказанных преимуществ.
2. Референсный диапазон для уровня ТТГ и субклинический гипотиреоз
Эти вопросы имеют единую суть и подразумевают одинаковое решение, которого в настоящее время пока нет. Тем не менее проблема имеет свою почти 40-летнюю историю (субклинический гипотиреоз описан в 1973 г.), с наиболее активным ее обсуждением с позиции доказательной медицины на протяжении последних десятилетий. Исходно, после описания субклинический гипотиреоз (СГ), особенно на этапе использования недостаточно совершенных методов определения уровня ТТГ и тиреоидных гормонов, воспринимался как компенсаторная реакция, не требующая никакой коррекции. В дальнейшем было показано, что он сопровождается изменением многочисленных суррогатных показателей, которые могут быть связаны с сердечно-сосудистым риском. Кроме того, с конца 80-х годов стала активно обсуждаться проблема СГ во время беременности. Все это вывело проблему СГ на уровень наиболее актуальных в области изучения патологии ЩЖ. На протяжении последних 10-15 лет как в зарубежной, так и в отечественной литературе опубликованы сотни обзоров, а всего на октябрь 2012 г. в базе данных Medline на ключевые слова "subclinical hypothyroidism" нами было обнаружено 2168 статей.
В первые годы XXI века проблема получила "новую жизнь", поскольку были опубликованы результаты сначала американских [51], а затем европейских [52] эпидемиологических исследований, где было показано, что референсный диапазон для ТТГ, под которым подразумевается его уровень у 95% здоровой популяции, явно слишком широк, поскольку у подавляющего большинства здоровых людей без признаков патологии ЩЖ он не превышает 2-2,5 мЕд/л. Высказывались идеи о целесообразности сужения референсного диапазона для диагностики гипотиреоза, а затем о сужении целевого диапазона для уровня ТТГ на фоне заместительной терапии.
По сути же все это были и есть проблемы, связанные одним узлом, поскольку, не ответив на вопрос о целесообразности лечения СГ, сложно обсуждать необходимость сужения референсного диапазона до 2 мЕд/л, не говоря уже о потенциальных социальных последствиях такого рода изменений с многомиллионным увеличением числа пациентов с гипотиреозом, тактика в отношении которого остается непонятной.
Если обратиться к последним рекомендациям ЕТА и ААСЕ [46], то они вряд ли привносят что-то новое к тому, что было принято в отношении СГ и референсного (целевого) диапазона для ТТГ. С другой стороны, эти рекомендации дают оценку многочисленным исследованиям, которые пытаются сделать вывод о целесообразности лечения СГ и выделения так называемого низконормального диапазона ТТГ, признавая их результаты недостаточными для этого. Суммировать основные положения этих рекомендаций можно следующим образом:
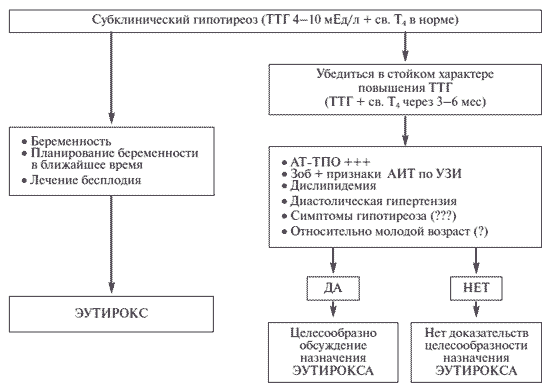
Рис. 1. Тактика при субклиническом гипотиреозе.
Нерешенность вопроса о лечении субклинического гипотиреоза, по сути, предопределяет и другую часто обсуждаемую проблему: скрининг гипотиреоза у взрослых. С одной стороны, гипотиреоз - это часто заболевание с неблагоприятными последствиями для здоровья, которое имеет хороший и доступный диагностический маркер - ТТГ и лечение которого относительно не сложно и не требует больших затрат, что в целом соответствует критериям целесообразности скрининга. С другой стороны, очевидно, что при скрининге среди нарушений функции ЩЖ чаще всего будет выявляться именно СГ, врачебная тактика в отношении которого пока четко не определена. Действительно, зачем активно искать заболевание или состояние, в отношении которого мы пока не ответили на вопрос: лечить его или нет?
Тем не менее есть у этого высокая доказательность или нет, субклинический диапазон для уровня ТТГ, равно как и его референсный диапазон, продолжает активно "анатомироваться" не только в научных работах и рассуждениях, но и на практике (рис. 2).
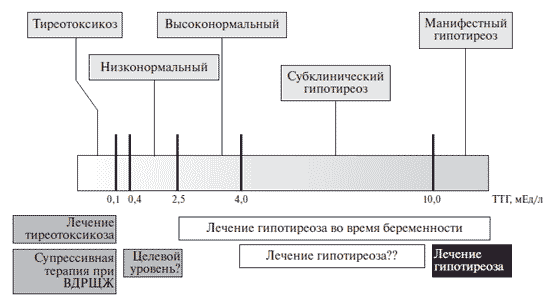
Рис. 2. Современная интерпретация уровня ТТГ. ТТГ<0,1 мЕд/л - достаточно надежно свидетельствует о наличии у пациента избытка тиреоидных гормонов (тиреотоксикоза).
Этот же уровень является целевым для большинства пациентов, получающих супрессивную терапию по поводу высокодифференцированного рака ЩЖ (ВДРЩЖ).ТТГ 0,1-0,4 мЕд/л - сниженный, но не подавленный уровень ТТГ;
четко не свидетельствует о наличии у пациента тиреотоксикоза, но говорит о высоком риске его развития;
у части тест-наборов в этом пределе еще находится нижняя референсная граница (0,2-0,3 мЕд/л).ТТГ 0,4-4 мЕд/л - общепринятый референсный диапазон для уровня ТТГ и целевой уровень ТТГ на фоне заместительной терапии первичного гипотиреоза. ТТГ 0,4-2,5 мЕд/л - так называемый низконормальный уровень ТТГ, в котором этот показатель находится у большинства здоровых людей;
по данным ряда рекомендаций рассматривается как целевой при заместительной терапии гипотиреоза;
кроме того, 2,5 мЕд/л ограничивается референсный диапазон ТТГ у женщин в I триместре беременности, т.е. гипотиреоз в этой ситуации диагностируется при ТТГ выше 2,5 мЕд/л.ТТГ 2,5-4 мЕд/л - так называемый высоконормальный уровень ТТГ;
по данным проспективных и эпидемиологических исследований, является независимым предиктором развития гипотиреоза в дальнейшем и с повышенной частотой встречается у носителей АТ-ТПО.ТТГ 4,0-10 мЕд/л - уровень ТТГ, как правило, соответствующий субклиническому гипотиреозу; имеющиеся исследования не позволяют сделать однозначный вывод о назначении заместительной терапии в этой ситуации;
общепринято, что заместительная терапия показана при беременности и ее планировании.ТТГ более 10 мЕд/л - уровень, который может соответствовать как субклиническому (нормальный Т4), так и манифестному (сниженный Т4) гипотиреозу; заместительная терапия показана практически всем пациентам.
Так, по данным опроса отечественных эндокринологов, проведенного нами в 2008 г., более половины сочли, что оптимальным целевым уровнем ТТГ на фоне терапии L-T4 является 0,4-2 мЕд/л [53]. Такое тяготение врачей к внедрению в практику еще не доказанных новшеств можно объяснить как минимум двумя психологическими моментами. Во-первых, это желание хоть как-то помочь пациенту, который не удовлетворен стандартным лечением, при том, что других осмысленных методов лечения гипотиреоза нет. Во-вторых, эндокринологи уже десятилетиями проводят заместительную терапию, принципы которой мало меняются, что само по себе многих психологически утомляет - хочется чего-то нового, новых препаратов, которые в других областях эндокринологии, например в лечении диабета, появляются достаточно часто.
Так или иначе, если мы обсуждаем какие-то части рефересного интервала для уровня ТТГ, да и субклинический диапазон от 4 до 10 мЕд/л, а также триместрспецифические диапазоны уровня ТТГ во время беременности, нужно хорошо понимать следующее:
- В этой ситуации зависимость клинициста от качества работы гормональной лаборатории возрастает максимально. Если лаборатория работает не качественно, то рассуждения о некоем низко- или высоконормальном уровне ТТГ лишены смысла. Более того, в случае столь детального рассмотрения уровня ТТГ, как это сделано на рис. 2, при гормональном исследовании начинают приобретать значение так называемые преаналитические факторы, которые в рутинной практике при определении уровня ТТГ клиницисты редко учитывали. Так, может приобретать значение даже время сдачи крови для определения уровня ТТГ. Минимальная циркадианная вариабельность уровня ТТГ и некоторое его снижение к середине дня и к вечеру могут привести к тому, что утром, на фоне относительно высокого уровня ТТГ у пациента выявляется субклинический гипотиреоз, а если повторить анализ в послеобеденное время - ТТГ зачастую сам по себе снижается до нормы. Как показано в наших исследованиях, время забора крови может приобрести значение как в случае диаг ностики и лечения субклинического и явного гипотиреоза, так и при супрессивной терапии при раке ЩЖ [54-56].
- При проведении заместительной терапии необходимо максимально точное дозирование препаратов L-T4, которые, как известно, имеют очень узкий терапевтический диапазон, при этом нежелательны бессистемный переход с одного бренда препарата на другой, а также деление целых таблеток L-T4 на части для получения нужной дозировки. С этой целью препараты L-T4 выпускаются с шагом между дозировками в целой таблетке не менее 25 мкг, а в идеале еще меньше - около 12 мкг. Так, препарат ЭУТИРОКС в настоящее время выпускается в РФ в девяти дозировках: 25, 50, 75, 88, 100, 112, 125, 137 и 150 мкг в одной таблетке, что делает подбор терапии очень удобным и точным.
3. Гипотиреоз и беременность
Эта проблема красной нитью проходит через многие клинические рекомендации по гипотиреозу, поскольку является наименее разработанной и сложной для изучения. Кроме того, было создано несколько специальных рекомендаций по диагностике и лечению заболеваний ЩЖ во время беременности, в которых теме диагностики и лечения гипотиреоза уделяется особое внимание. В чем основные причины противоречий и почему столь низок уровень доказательности имеющихся у нас рекомендаций?
Первая и базовая причина состоит в том, что во время беременности кардинально меняется функция ЩЖ и обмен ее гормонов, что делает невозможным использовать для диагностики гипотиреоза общепринятые референсные интервалы, которые разрабатываются для общей популяции. Кстати говоря, это же справедливо и для многих других гормональных показателей.
В общем и целом уже давно показано, что уровень ТТГ в первой половине беременности существенно снижается вследствие гиперстимуляции ЩЖ хорионическим гонадотропином человека и продукции дополнительных количеств Т4. Но до тех пор, пока в клинических проспективных исследованиях не будет доказано, что высоконормальный уровень ТТГ, который для ряда ситуаций уже практически признан патологией, сопровождается какими-то неблагоприятными исходами, рекомендации по назначению заместительной терапии L-T4 в этой ситуации будут по своему уровню близки к экспертному мнению. Более того, доказательностью так называемого уровня "А" фактически не обладает даже рекомендация и по назначению L-Т4 женщинам с ТТГ между 4 и 10 мЕд, хотя необходимость этого уже почти никем не оспаривается.
Проведение же исследований, которые могли бы подтвердить необходимость заместительной терапии L-Т4 при СГ и так называемом высоконормальном уровне ТТГ, сопряжено как минимум с двумя сложностями:
- Этические ограничения: в ситуации, когда есть хотя бы даже не очень строгие данные о неблагоприятном влиянии СГ на интеллект ребенка, достаточно сложно сознательно назначить части беременных женщин плацебо вместо L-T4 и не менее сложно получить на это их информированное согласие, при всем при том, что терапия L-T4 достаточно безопасна и дешева.
- Реальные доказательства неблагоприятного влияния СГ у матери на интеллект ребенка можно получить только спустя много лет после включения в исследование беременных, поскольку оценка уровня психического развития совсем маленьких детей с прогностической точки зрения имеет ограниченную ценность. То есть, даже если какие-то изменения будут выявлены, это еще не значит, что они будут стойкими и не подвергнутся обратному развитию в более старшем возрасте.
Самые последние и полные клинические рекомендации по диагностике и лечению заболеваний ЩЖ во время беременности, которые были созданы Американской тиреоидной ассоциацией (АТА), вышли в конце 2011 г. [57] и подробно обсуждались в этом журнале [58]. Еще одни рекомендации вышли в августе 2012 г. [59], при этом они тоже американские и половина их авторов одновременно являются авторами предыдущего документа. Все они требуют отдельного обсуждения, содержат по описанным выше причинам немало противоречий, и здесь мы остановимся лишь на самых практических вещах, касающихся диагностики и лечения гипотиреоза. Суммировать их можно следующим образом:
- Референсными диапазонами для уровня ТТГ во время беременности следует считать: для I триместра - 0,1-2,5 мЕд/л, для II триместра 0,2-3 мЕд/л, для III триместра - 0,3-3 мЕд/л.
- При СГ, которым следует считать повышение уровня ТТГ выше 2,5 мЕд/л, заместительная терапия L-T4 показана женщинам, у которых определяются циркулирующие АТ-ТПО, при их отсутствии данные о преимуществах и недостатках назначения L-T4 отсутствуют.
Условность и противоречивость этих рекомендаций очевидна, но увы, это с практической точки зрения максимум из того, что на уровне сегодняшних знаний может быть рекомендовано. Действительно, откуда взялась цифра 2,5? Почему не 2? Откуда 3? Откуда именно 0,1, 0,2 и 0,3? Очевидно, что чисто эмпирически! Самый главный вопрос, следующий из двух приведенных пунктов рекомендаций: если четко обозначены референсные диапазоны, то почему решение о назначении заместительной терапии зависит от того, обнаружены у женщины АТ-ТПО или нет?
С другой стороны, действительно, если мы назвали высоконормальный уровень ТТГ патологией, то где в каждом конкретном случае ее морфологический субстрат? Что именно вызвало этот минимальный гипотиреоз? В случае, если у женщины есть признаки АИТ, такие как циркулирующие АТ-ТПО, ситуация более или менее ясна, но почему и какой патологией считать высоконормальный ТТГ во время беременности, если какие-либо признаки изменения самой ЩЖ не выявляются?
Как поступить на практике? Во-первых, нужно помнить о том, что писалось о качестве лабораторной диагностики, заложником которой оказывается как пациент, так и врач. То есть повторное проведение анализа крови в экспресс-режиме снимает многие вопросы. Если высоконормальный уровень выявляется повторно, то терапию L-T4 с психологической точки зрения иногда проще назначить, чем не назначить, даже при отсутствии у женщины АТ-ТПО, но нужно помнить, что доказательная база у такой тактики очень слабая.
Особняком стоит проблема так называемого синдрома изолированной гипотироксинемии - частой ситуации, когда во второй половине беременности у женщин выявлется несколько сниженный уровень свободного Т4 при нормальном уровне ТТГ. Этот вопрос выходит за рамки нашего обсуждения, укажем лишь на то, что такая ситуация обусловлена методическими сложностями определения св. Т4 во время беременности, на фоне очень высокого уровня тироксинсвязывающего глобулина, а также на то, что в таких случаях заместительная терапия не требуется.
Алгоритм диагностики и лечения гипотиреоза во время беременности представлен на рис. 3 и в комментариях к нему.
Рис. 3. Диагностика гипотиреоза во время беременности. Если у беременной выявляется уровень ТТГ менее 0,1 мЕд/л, речь, как правило, идет о гиперфункции ЩЖ, которая в 95% случаев носит физиологический характер, обозначается как транзиторный гестационный гипертиреоз и не требует каких-либо вмешательств. В ряде случаев речь может идти о болезни Грейвса, которая чаще предшествует наступлению беременности, чем манифестирует на ее фоне. Уровень ТТГ 0,1-2,5 мЕд/л считается нормальным и не требует никаких действий. Уровень ТТГ более 4 мЕд/л соответствует гипотиреозу и требует назначения заместительной терапии L-T4. В ситуации, когда у женщины выявляется уровень ТТГ 2,5-4 мЕд/л, заместительная терапия имеет большие основания, когда у женщины выявляются циркулирующие АТ-ТПО и/или другие признаки АИТ.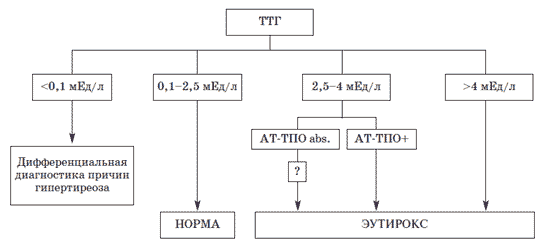
Практические врачи всегда предпочитают полную ясность и так называемые стандарты, но в таком недостаточно разработанном вопросе, как диагностика и лечение заболеваний ЩЖ во время беременности, эта ясность есть далеко не во всем.
4. Заключение
В этом обзоре мы кратко обсудили наиболее критические и не до конца изученные вопросы диагностики и лечения гипотиреоза, касаясь как базисных, так и клинических аспектов проблемы. С одной стороны, создается впечатление, что уже несколько десятков лет, с тех пор, как появились синтетические препараты L-Т4 и в клинику было внедрено определение ТТГ, подходы к этой проблеме никак не изменились. С другой стороны, не верится, что всего лишь 20 лет назад встречались пациенты, которые принимали сушеные экстракты ЩЖ животных, и на достаточно серьезных конференциях приходилось слышать выступления, которые были посвящены обсуждению преимуществ перед ними синтетического L-T4. За последние 10 лет достаточно хорошо продвинулось такое молодое направление эндокринологии, как заболевания ЩЖ во время беременности. Хотя здесь еще остается очень много противоречий, но те же 15-20 лет назад этот вопрос обсуждался лишь вскользь. Если говорить о перспективах, то, по мнению автора этой статьи, они состоят в разрешении тех многочисленных противоречий, которые здесь обсуждались. Наверняка достижений следует ждать от молекулярно-генетических исследований, которые позволят тем или иным образом индивидуализировать заместительную терапию гипотиреоза, максимально приведя ее в соответствие особенностям обмена тиреоидных гормонов у того или иного пациента.
Литература
1. Aoki Y, Belin R.M., Clickner R. et al. Serum TSH and total T4 in the United States population and their association with participant characteristics: National Health and Nutrition Examination Survey (NHANES 1999-2002). Thyroid 2007; 17: 1211-1223.
2. Larsen P.R., Silva J.E., Kaplan M.M. Relationships between circulating and intracellular thyroid hormones: physiological and clinical implications. Endocr. Rev. 1981; 2; 87-102.
3. Fadeyev V.V., Morgunova T.B., Sytsh J.P., Melnichenko G.A. TSH and thyroid hormones concentrations in patients with hypothyroidism receiving replacement therapy with L-thyroxine alone or in combination with L-triiodthyronine. HORMONES 2005; 4 (2): 101-107.
4. Saravanan P., Chau W.F., Roberts N. et al. Psychological well-being in patients on adequate doses of L-thyroxine: results of a large, controlled community-based questionnaire study. Clin. Endocrinol. (Oxf.) 2002; 57; 577-585.
5. Visser W.E., Friesema E.C., Visser T.J. Thyroid hormone transporters: the knowns and the unknowns. Mol. Endocrinol. 2011; 25: 1-14.
6. Zhang J., Lazar M.A. The mechanism of action of thyroid hormones. Ann. Rev. Physiol. 2000; 62: 439-466.
7. Ramadan W., Marsili A., Larsen P.R. et al. Type-2 iodothyronine 5-deiodinase in skeletal muscle of C57BL/6 mice. I. Identity, subcellular localization, and characterization. Endocrinology 2011; 152: 3082-3092.
8. Galton V.A. The roles of the iodothyronine deiodinases in mammalian development. Thyroid 2005; 15: 823-834.
9. Medina M.C., Molina J., Gadea Y. et al. The thyroid hormone-inactivating type III deiodinase is expressed in mouse and human P-cells and its targeted inactivation impairs insulin secretion. Endocrinology 2011; 152: 3717-3727.
10. HuangS.A., Bianco A.C. Reawakened interest in type III iodothyronine deiodinase in critical illness and injury. Nat. Clin. Pract. Endocrinol. Metab. 2008; 4: 148-155.
11. Gullo D., Latina A., Frasca F. et al. Levothyroxine monotherapy cannot guarantee euthyroidism in all athyreotic patients. PLoS One 2011; 6: e22552.
12. Bianco A.C., Salvatore D., Gereben B. et al. Biochemistry, cellular and molecular biology and physiological roles of the iodothyronine selenodeiodinases. Endocr. Rev. 2002; 23: 38-89.
13. Schneider M.J., Fiering S.N., Pallud S.E. et al. Targeted disruption of the type 2 selenodeiodinase gene (DIO2) results in a phenotype of pituitary resistance to T4. Mol. Endocrinol. 2001; 15: 2137-2148.
14. Escobar-Morreale H.F., Obregon M.J., Escobar del Rey F., Morreale de Escobar G. Replacement therapy for hypothyroidism with thyroxine alone does not ensure euthyroidism in all tissues, as studied in thyroidectomized rats. J. Clin. Invest. 1995; 96: 2828-2838.
15. Andersen S., Bruun N.H., Pedersen K.M., LaurbergP. Biologic variation is important for interpretation of thyroid function tests. Thyroid 2003; 13: 1069-1078.
16. Bianco A.C., Silva J.E. Cold exposure rapidly induces virtual saturation of brown adipose tissue nuclear T3 receptors. Am. J. Physiol. 1988; 255: 496-503.
17. Dumitrescu A.M., Liao X.H., Abdullah M.S. et al. Mutations in SECISBP2 result in abnormal thyroid hormone metabolism. Nat. Gen. 2005; 37: 1247-1252.
18. Schneider M.J., Fiering S.N., Thai B. et al. Targeted disruption of the type 1 selenodeiodinase gene (Dio1) results in marked changes in thyroid hormone economy in mice. Endocrinology 2006; 147: 580-589.
19. Dayan C.M., Panicker V. Novel insights into thyroid hormones from the study of common genetic variation. Nat. Rev. Endocrinol. 2009; 5: 211-218.
20. De Jong F.J., Peeters R.P., den Heijer T. et al. The association of polymorphisms in the type 1 and 2 deiodinase genes with circulating thyroid hormone parameters and atrophy of the medial temporal lobe. J. Clin. Endocrinol. Metab. 2007; 92: 636- 640.
21. Crantz F.R., Silva J.E., Larsen P.R. Analysis of the sources and quantity of 3,5,3-triiodothyronine specifically bound to nuclear receptors in rat cerebral cortex and cerebellum. Endocrinology 1982; 110: 367-375.
22. Canani L.H., Capp C., Dora J.M. et al. The type 2 deiodinase A/G (Thr92Ala) polymorphism is associated with decreased enzyme velocity and increased insulin resistance in patients with type 2 diabetes mellitus. J. Clin. Endocrinol. Metab. 2005; 90: 3472-3478.
23. Dora J.M., Machado W.E., Rheinheimer J. et al. Association of the type 2 deiodinase Thr92Ala polymorphism with type 2 diabetes: case-control study and meta-analysis. Eur. J. Endocrinol. 2010; 163: 427-434.
24. Guo T.W., Zhang F.C., Yang M.S. et al. Positive association of the DIO2 (deiodinase type 2) gene with mental retardation in the iodine-deficient areas of China. J. Med. Genet. 2004; 41: 585-590.
25. Gumieniak O., Perlstein T.S., Williams J.S. et al. Ala92 type 2 deiodinase allele increases risk for the development of hypertension. Hypertension 2007; 49: 461-466.
26. Meulenbelt I., Min J.L., Bos S. et al. Identification of DIO2 as new susceptibility locus for symptomatic osteoarthritis. Hum. Mol. Genet. 2008; 17: 1867-1875.
27. He B., Li J., Wang G. et al. Association of genetic polymorphisms in the type II deiodinase gene with bipolar disorder in a subset of Chinese population. Prog. Neuropsychopharmacol. Biol. Psychiatry. 2009; 33: 986-990.
28. Torlontano M., Durante C., Torrente I. et al. Type 2 deiodinase polymorphism (Thr92Ala) predicts L-thyroxine dose to achieve target TSH levels in thyroidectomized patients. J. Clin. Endocrinol. Metab. 2008; 93: 910-913.
29. Butler P.W., Smith S.M., Linderman J.D. et al. The Thr92Ala 5-type 2 de-iodinase gene polymorphism is associated with a delayed triiodothyronine secretion in response to the thyrotropin-releasing hormone-stimulation test: a pharmacogenomic study. Thyroid. 2011; 20: 1407-1412.
30. Ng L., Lyubarsky A., Nikonov S.S. et al. Type 3 deiodinase, a thyroidhormone-inactivating enzyme, controls survival and maturation of cone photoreceptors. // J. Neurosci. 2010; 30: 3347-3357.
31. Mohacsik P., Zeold A., Bianco A.C., Gereben B. Thyroid hormone and the neuroglia: both source and target. J. Thyroid. Res. 2011; 2011: 215718.
32. Dumitrescu A.M., Liao X.H., Best T.B. et al. A novel syndrome combining thyroid and neurological abnormalities is associated with mutations in a monocarboxylate transporter gene. Am. J. Hum. Genet. 2004; 74: 168-175.
33. Sugiyama D., Kusuhara H., Taniguchi H. et al. Functional characterization of rat brain-specific organic anion transporter (Oatp14) at the blood-brain barrier: high affinity transporter for thyroxine. J. Biol. Chem. 2003; 278: 43489-43495.
34. Van der Deure W., Appelhof B.C., Peeters R.P. et al. Polymorphism in the brain-specific thyroid hormone transporter OATP-C1 are associated with fatigue and depression in hypothyroid patients. Clin. Endocrinol. 2008; 69: 804-811.
35. Canaris G.J., Manowitz N.R., Mayor G., Ridgway E.C. The Colorado thyroid disease prevalence study. Arch. Intern. Med. 2000; 28: 526-534.
36. Katon W., Schulberg H. Epidemiology of depression in primary care. Gen Hosp. Psychiatry 1992; 14: 237-247.
37. Paunkovic N., Paunkovic J., Pavlovic O., Paunovic Z. The significant increase in incidence of Graves' disease in eastern Serbia during the civil war in the former Yugoslavia (1992 to 1995). Thyroid. 1998; 8: 37-41.
38. Louwerens M., Appelhof B.C., Verloop H. et al. Fatigue and fatigue-related symptoms in patients treated for different causes of hypothyroidism. Eur. J. Endocrinol. 2012; Sep (in press).
39. Walsh J. P., WardL. C., Burke V. et al. Small changes in thyroxine dosage do not produce measurable changes in hypothyroid symptoms, well-being, or quality of life: results of a double-blind, randomized clinical trial. J. Clin. Endocrinol. Metab. 2006; 91:2624-2630.
40. Подзолков А.В., Фадеев В.В. Оценка динамики показателей липидного спектра и ранних предикторов эндотелиальной дисфункции при первичным гипотиреозе в зависимости от уровня ТТГ в пределах референсного диапазона. Клин. и экспер. тиреоидол. 2010; 3: 54-59.
41. Подзолков А.В., Фадеев В.В. Высоко- и низконормальный уровень ТТГ: клиническая картина, психоэмоциональная сфера и качество жизни пациентов с гипотиреозом. Клин. и экспер. тиреоидол. 2010; 4: 58-68.
42. Bunevicius R., Kazanavicius G., Zalinkevicius R., Prange A.J. Effects of thyroxine as compared with thyroxine plus triiodothyronine in patients with hypothyroidism. Engl. J. Med. 1999; 340: 424-429.
43. Bunevicius R.., Jakubonien N, Jurkevicius R.. et al. Thyroxine vs. thyroxine plus triiodothyronine in treatment of hypothyroidism after thyroidectomy for Graves' disease. Endocrine 2002; 18: 129-133.
44. Nygaard B, Jensen E.W., Kvetny J. et al. Effect of combination therapy with thyroxine (T4) and 3,5,3-triiodothyronine versus T4 monotherapy in patients with hypothyroidism, a double-blind, randomised cross-over study. Eur. J. Endocrinol. 2009; 161: 895-902.
45. Grozinsky-Glasberg S., Fraser A., Nahshoni E. et al. Thyroxine-triiodothyronine combination therapy versus thyroxine monotherapy for clinical hypothyroidism: meta-analysis of randomized controlled trials. J. Clin. Endocrinol. Metab. 2006; 91: 2592-2599.
46. Garber J.R., Cobin R.H., Gharib H. et al. Clinical Practice Guidelines for Hypothyroidism in Adults: Co-sponsored by the American Association of Clinical Endocrinologists and the American Thyroid Association. Endocr. Pract. 2012; 11: 1-207.
47. Wiersinga W., Duntas L., Fadeyev V. et al. The Use of L-T4 + L-T3 in the Treatment of Hypothyroidism. Eur. Thyroid. J. 2012; 1: 55-71.
48. Фадеев В.В. По материалам клинических рекомендаций Европейской тиреоидной ассоциации по использованию комбинированной терапии L-T4 + L-T3 в лечении гипотиреоза. Клин. и экспер. тиреоидол. 2012; 2: 14-18.
49. Fadeyev V.V., Morgunova T.B., Melnichenko G.A., Dedov I.I. Combined therapy with L-Thyroxine and L-Triiodothyronine compared to L-Thyroxine alone in the treatment of primary hypothyroidism. Hormones (Athens) 2010; 9: 245-252.
50. Panicker V., Saravanan P., Vaidya B. et al. Common variation in the DIO2 gene predicts baseline psychological well-being and response to combination thyroxine plus triiodothyronine therapy in hypothyroid patients. J. Clin. Endocrinol. Metab. 2009; 94: 1623-1629.
51. Hollowell J.G., Staehling N.W., Flanders W.D. et al. Serum TSH, T(4), and thyroid antibodies in the United States population (1988 to 1994): National Health and Nutrition Examination Survey (NHANES III). J. Clin. Endocrinol. Metab. 2002; 87: 489-499.
52. Volzke H., Schmidt C.O., John U. et al. Reference levels for serum thyroid function tests of diagnostic and prognostic significance. Horm. Metab. Res. 2010; 42: 809-814.
53. Фадеев В.В., Берковская М.А., Мельниченко Г.А. Результаты опроса эндокринологов по проблемам нарушения функции щитовидной железы. Клин. и экспер. тиреоидол. 2008; 2: 41-47.
54. Свиридонова М.А., Фадеев В.В., Ильин А.В. Циркадианная и индивидуальная вариабельность уровня ТТГ и тиреоидных гормонов у лиц с субклиническим гипотиреозом. Клин. и экспер. тиреоидол. 2010; 3: 35-41.
55. Свиридонова М.А., Ильин А.В., Фадеев В.В. Циркадианная и индивидуальная вариабельность уровня ТТГ у лиц, получающих заместительную терапию гипотиреоза. Клин. и экспер. тиреоидол. 2010; 4: 52-57.
56. Свиридонова М.А., Ильин А.В., Фадеев В.В. Циркадианная вариабельность уровня ТТГ на фоне супрессивной терапии левотироксином. Клин. и экспер. тиреоидол. 2011; 1: 55-57.
57. Stagnaro-Green A., Abalovich M., Alexander E. et al. Guidelines of the American thyroid association for the diagnosis and management of thyroid disease during pregnancy and postpartum. Thyroid. 2011; 21 (21): 1081-1125.
58. Фадеев В.В. По материалам клинических рекомендаций по диагностике и лечению заболеваний щитовидной железы во время беременности и в послеродовом периоде Американской тиреоидной ассоциации. Клин. и экспер. тиреоидол. 2012; 1: 7-18.
59. De Groot L., Abalovich M., Alexander E.K. et al. Management of thyroid dysfunction during pregnancy and postpartum: an Endocrine Society clinical practice guideline. J. Clin. Endocrinol. Metab. 2012, 97: 2543-2565.
Комментарии
ПРАКТИКА ПЕДИАТРА
