Синдром кавасаки у детей - актуальное
СтатьиС.А. Кирилина, канд. мед. наук, педиатр, врач общей практики, врач Посольства России в США
Опубликовано в журнале:
«Практика педиатра» № 4, 2021, стр. 5-11
Ключевые слова: дети, болезнь Кавасаки, клиническая картина, диагностика, осложнения, лечение
Keywords: children, Kawasaki disease, clinical symptoms, diagnosis, complications, treatment
Резюме. В статье представлены современные данные о болезни Кавасаки у детей. Освещены особенности клинического течения, диагностики, дифференциальной диагностики, частота осложнений, а также даны рекомендации по лечению и диспансерному наблюдению пациентов с болезнью Кавасаки.
Summary. The article presents modern data on Kawasaki disease in children. The article elaborates specific characteristics of the clinical course of Kawasaki disease, its diagnosis, differential diagnostic procedure and complications caused by the disease. Aiso offers recommendations on how to treat patients suffering from Kawasaki disease and provide follow-up care for patients.
Для цитирования: Кирилина С.А. Синдром Кавасаки у детей - актуальное // Практика педиатра. 2021. № 4. С. 5-11.
For citation: Kirilina S.A. Kawasaki syndrom in children - current. Pediatrician's Practice 2021;(4):5-11. (In Russ.)
Введение
В 2020 г., когда весь мир был поставлен в условия карантина, противоэпидемических мер и социальной изоляции из-за пандемии COVID-19, стали появляться сообщения о серьезном увеличении количества случаев воспалительного синдрома, похожего по симптомам на синдром Кавасаки [1]. Болезнь протекала как синдром токсического шока и атипичный синдром Кавасаки (с признаками гастроинтестинального поражения и кардиосимптомами). Пациенты также имели высокие уровни С-реактивного белка, прокальцитонина, ферритина, тропонина, D-димера и изменения в коронарных артериях [2]. Зачастую у этих больных были проявления системного поражения: перикардиты, плевриты, асциты. Появилось множество описаний случаев мультисистемного воспалительного синдрома у детей (pediatric multisystem inflammatory syndrome). Обращало на себя внимание отсутствие РНК вируса SARS-CoV-2, а также наличие антител класса IgG, что свидетельствует о развитии заболевания в отсроченный от начала виремии период.
Цель нашего сообщения - привлечь внимание практикующей аудитории к данной клинической проблеме.
Болезнь Кавасаки (слизисто-кожный лимфонодулярный синдром) - некротизирующий системный васкулит с преимущественным поражением средних и мелких артерий, проявляющийся лихорадкой, изменениями слизистых оболочек, кожи, поражением коронарных и других висцеральных артерий с возможным образованием аневризм, тромбозов и разрывов сосудистой стенки.
Этиология болезни Кавасаки до настоящего времени окончательно не установлена. Авторы многочисленных эпидемиологических и иммунологических исследовательских работ склоняются к тому, что наиболее вероятным причинным фактором может быть инфекционный агент (предположительно, вирус) [3]. Однако присутствие в организме антигенов стрептококков и стафилококков, которое сопровождается повышением уровня Т-лимфоцитов, может способствовать развитию болезни. На это указывало увеличение числа заболевших в конце зимы и весны и волнообразное географическое распространение эпидемий. Подозреваемыми инфекционными агентами были микоплазмы, спирохеты, риккетсии, хламидии, вирусы, такие как аденовирус, герпесвирусная инфекция, парвовирус, вирус Эпштейна - Барр. Однако в носоглотке, ротоглотке, на коже или в кале больных возбудители выявлены не были [4-6]. Вскоре было выдвинуто предположение о большой роли в развитии болезни Кавасаки аутоиммунных механизмов и генетической предрасположенности [7-10]. На сегодняшний момент имеются данные о 6 генетических локусах, связанных с этим заболеванием [11]; вероятно, этим обусловлено то, что наиболее часто (95%) пациентами становятся этнические японцы и представители других народов Азии. Исследования выявили несколько генов (FCGR2A, CD40, ITPKC, FAM167A-BLK и CASP3), повышающих восприимчивость к заболеванию и ее последствиям в различных этнических популяциях. Вопрос о генетическом вкладе в болезнь Кавасаки активно изучается во всем мире.
До недавнего времени считалось, что это довольно редкий синдром: частота варьирует в районе 10 случаев на 100 тыс. детей, однако в Японии заболеваемость составляет 219 случаев на 100 тыс. детей [12]. По статистике заболевают в основном дети от 1,5 до 5 лет. При этом у мальчиков болезнь встречается в 1,5 раза чаще, чем у девочек. Более 70% заболевших - дети младше 3 лет. Болезнь Кавасаки редко встречается у детей младше 4 мес. Это позволяет предположить, что материнские антитела могут обеспечивать пассивный иммунитет [13]. Около 2% больных имеют рецидивы, обычно спустя несколько месяцев или даже лет.
Патогенез болезни кавасаки
Провоцирующий агент активирует образование иммунных комплексов, Т-лимфоцитов и выработку цитокинов, повреждающих сосудистую стенку по типу цитокинового каскада. Также активируются матриксные металлопротеиназы, повреждающие эндотелиальные сосудистые клетки, в результате происходит фрагментация внутренней эластической мембраны, повышение проницаемости сосудов и повреждение стенки капилляров. В случае болезни Кавасаки васкулит носит генерализованный, системный характер. Сосудистое воспаление наиболее выражено в коронарных артериях, но может также возникать в венах, капиллярах, мелких артериолах и крупных артериях. На ранних стадиях заболевания наблюдаются отек эндотелия и субэндотелия сосуда, но внутренняя эластическая мембрана остается интактной. При повреждении мелких кровеносных сосудов к месту повреждения устремляются тромбоциты и образуют тромбы, закрывающие место дефекта сосуда, что может приводить к облитерации сосуда. Активное воспаление в течение нескольких недель/месяцев сменяется прогрессирующим фиброзом с образованием рубцов и стенозом сосудов.
Клиническая картина
В течении болезни Кавасаки выделяют три периода: острый, или фебрильный (7-10 дней), подострый (1421 день) и период выздоровления, который может занимать от нескольких месяцев до 1-2 лет.
Наиболее характерные проявления болезни Кавасаки представлены в табл. 1.
Таблица 1.
Стадии болезни Кавасаки [14] Появление первых признаков заболевания всегда сопровождается длительным (более 5 дней) повышением температуры тела до фебрильных или гектических цифр. Оно плохо купируется стандартным приемом нестероидных противовоспалительных средств или антипиретиков. Если своевременно не выявлена причина лихорадки и не начато лечение болезни, высокая температура может наблюдаться у ребенка до 14 дней.
Появление первых признаков заболевания всегда сопровождается длительным (более 5 дней) повышением температуры тела до фебрильных или гектических цифр. Оно плохо купируется стандартным приемом нестероидных противовоспалительных средств или антипиретиков. Если своевременно не выявлена причина лихорадки и не начато лечение болезни, высокая температура может наблюдаться у ребенка до 14 дней.
Помимо гипертермии имеются другие диагностические критерии:
- инъецирование конъюнктивы обоих глаз без гнойного отделяемого;
- хейлиты, «малиновый» или «клубничный» язык, инфицирование слизистой оболочки полости ротоглотки, кровоточивость десен, гиперемия глотки;
- эритема ладоней или стоп;
- плотный отек кистей и/или стоп на 3-5-й день болезни, сопровождающийся снижением подвижности пальцев;
- шелушение кончиков пальцев на 2-3-й неделе заболевания;
- полиморфная экзантема на туловище без пузырьков или корочек (может выглядеть как макулярная, макулопапулезная, скарлатиноподобная или кореподобная);
- острая негнойная шейная лимфаденопатия (значительное увеличение одного или нескольких шейных лимфатических узлов - более 15 мм в диаметре).
При наличии 4 и более критериев заболевания можно говорить о синдроме Кавасаки. В случае появления 3 и менее критериев устанавливается диагноз болезни с неполной (атипичной) клинической картиной. Такие неполные формы болезни чаще всего наблюдаются у грудных детей, у которых наиболее высок риск поражения коронарных артерий.
Клиническая картина болезни Кавасаки характеризуется цикличностью проявлений, выраженностью лихорадки, на фоне которой развиваются симптомы поражения слизистых оболочек, кожи, лимфатических узлов и различных систем. Поражения сердечно-сосудистой системы - самые опасные проявления синдрома Кавасаки, встречаются почти у половины больных. Могут выявляться тахикардия, аритмия, ритм галопа, различные сердечные шумы, обусловленные, например, перикардиальным выпотом, изменениями миокарда или митральной регургитацией. Изменения оболочек сердца сопровождают острую фазу болезни и обычно имеют положительную динамику по мере улучшения состояния пациента. В то же время высок риск быстрого развития аневризм коронарных артерий, которые обычно возникают в сроки от 1 до 4 нед от начала лихорадки. Поражаются преимущественно проксимальные отделы сосудов. Помимо коронарных артерий, могут быть вовлечены другие сосуды, включая брюшную аорту, верхнюю брыжеечную, подмышечные, подключичные, плечевые, подвздошные и почечные артерии с дистальной ишемией и некрозом в результате активного васкулита.
Помимо специфических симптомов к проявлениям болезни относят также:
- артралгии или полиартрит голеностопных и коленных суставов, поражения мелких суставов кистей и стоп;
- гепатомегалию;
- диарею, тошноту и рвоту, также сильный дискомфорт в области желудка;
- асептический менингит;
- легочные инфильтраты и плевральный выпот;
- уретрит, цистит, интерстициальный нефрит.
Дифференциальный диагноз
Необходимо дифференцировать болезнь Кавасаки и другие формы системных васкулитов. Проявления, сходные с таковыми при болезни Кавасаки, имеются у ряда других заболеваний: ювенильного ревматоидного артрита, синдрома Стивенса - Джонсона, а также детских «сыпных» инфекций.
Корь отличает экссудативный конъюнктивит, пятна Коплика, сыпь на лице ниже ушей с этапностью высыпания, сухой, навязчивый кашель, а также лейкопения и низкая скорость оседания эритроцитов. Также при кори шелушение кожи на кистях и на стопах не наблюдается.
Труднее всего проводить дифференциальную диагностику болезни Кавасаки и скарлатины. Однако при скарлатине не встречается инъекция конъюнктив, отек стоп и ладоней, а лихорадка быстро купируется при назначении антибиотиков (пенициллинового ряда), поэтому оценка состояния больного через 24-48 ч от начала антибиотикотерапии позволяет уточнить диагноз.
Инфекционный мононуклеоз часто сопровождается полиморфной экзантемой и лимфаденопатией, но лихорадка при нем держится обычно менее недели, и выявление в крови атипичных мононуклеаров помогает отличить это состояние от синдрома Кавасаки.
Аденовирусная инфекция отличается выраженными проявлениями назофарингита, лихорадкой длительностью около 5 дней, при этом такой симптом, как «малиновый язык», не характерен.
Для токсического шока характерны падение артериального давления, поражение почек, повышение активности креатинфосфокиназы и очаги стафилококковой инфекции.
Системный ювенильный идиопатический артрит может дебютировать с длительной гектической лихорадки, генерализованной лимфаденопатии, гепато-спленомегалии, серозитов и пятнистой розовой преходящей сыпи в отсутствие артрита. Но при этом нет характерного конъюнктивита, шелушения кистей и стоп, «малинового» языка.
Как о ювенильном ревматоидном артрите, так и об узелковом полиартериите следует думать у пациентов с подозрением на синдром Кавасаки, у которых нет эффекта от введения иммуноглобулина. Также при узелковом полиартериите выявляются подкожные узелки, множественный асимметричный мононеврит, дистальная гангрена и характерна артериальная гипертензия.
Необходима дифференциальная диагностика болезни Кавасаки и синдрома Стивенса - Джонсона (возможный возбудитель - Mycoplasma pneumoniae), для которого также характерны лихорадка, поражение слизистых оболочек и сыпь. Однако сыпь отличается наличием последовательно трансформирующихся высыпаний: макулы - папулы - везикулы и буллы, уртикарные элементы или сливная эритема с изъязвлениями и некрозом. Лихорадка редко длится более 5 дней и/или реагирует на введение антибиотика.
Осложнения
Аневризмы коронарных артерий как осложнение болезни Кавасаки развиваются у 1/4 части пациентов, не проходивших лечение. Однако даже при лечении высокими дозами внутривенных иммуноглобулинов (ВВИГ) на протяжении первых 10 дней от начала заболевания у 5% детей может возникнуть временная дилатация коронарных артерий, а у 1% - крупные аневризмы. Летальный исход может произойти либо в связи с инфарктом миокарда из-за образования тромбов в аневризме коронарной артерии, либо в связи с разрывом крупной аневризмы коронарной артерии. Были описаны и другие осложнения болезни Кавасаки - аневризмы других артерий: аортальная аневризма (при этом в большом числе случаев она включает брюшную аорту), аневризма подмышечной артерии, аневризма брахицефальной артерии, аневризмы подвздошной и бедренной артерий и аневризма почечной артерии. Другие сосудистые осложнения - повышенное истончение стенки и сниженное растяжение каротидных артерий, аорты и плечелучевой артерии [15].
За последние пятьдесят лет болезнь Кавасаки стала одной из самых распространенных причин развития приобретенных пороков сердца у детей в мире. У взрослых перенесенная болезнь приводит также к раннему атеросклерозу, кальцинозу, тромбообразованию, дистрофии миокарда, ишемической болезни сердца и инфаркту [16].
В последнее время резистентные формы болезни Кавасаки (постоянная или рецидивирующая лихорадка, невосприимчивая к терапии) и рецидивирующие формы встречаются реже.
К другим системным осложнениям можно отнести анемию, гипоальбуминемию, гиперхолестеринемию и ранний атеросклероз, электролитные нарушения (особенно гипонатриемию), паралитический илеус, дисфункцию печени, холецистит, судороги [16]. Изменения глаз, связанные с заболеванием, описываются с 1980-х. Это увеит, иридоциклит, кровоизлияние в конъюнктиву, неврит зрительного нерва, амавроз и закупорка зрительной артерии [17]. Редким осложнением является нейросенсорная глухота. Образование аневризм может вести также к периферической гангрене.
Методы диагностики
Диагностика заболевания проводится на основании анамнеза и выявленных при осмотре симптомов.
В общем анализе крови выявляется высокий уровень тромбоцитов и лейкоцитов, анемия. При проведении биохимического анализа отмечаются повышенный уровень трансаминаз, иммуноглобулинов, С-реактивного белка и других белков острой фазы, а также гипоальбуминемия. В моче больного ребенка может быть небольшая протеинурия и асептическая лейкоцитурия.
Необходимо назначить диагностические процедуры:
1. Коагулограмму.
2. Эхокардиографию (эхоКГ) для выявления поражений коронарных артерий. Это исследование выполняют при диагностике и повторяют через 2-3 нед. В случае нормальных результатов исследование еще раз проводят через 6-8 нед после начала заболевания, затем - после нормализации скорости оседания эритроцитов. В ряде центров эхоКГ дополнительно проводят через год после начала заболевания.
3. Электрокардиографию для выявления дисфункции, аритмии, желудочковой тахикардии, удлиненного интервала PR, изменения волны ST-T и снижения напряжения R-волн, указывающих на миокардит. Изменения волн Q или ST-T могут указывать на инфаркт миокарда.
4. Рентгеновский снимок грудной клетки.
5. Ультразвуковое исследование брюшной полости, почек.
6. Ангиографию коронарных артерий - по показаниям.
7. Исследование на наличие антител к кори, краснухе, скарлатине и другим инфекциям.
8. Экспресс-тест на наличие гемолитического стрептококка группы А (Streptococcus pyogenes).
В отдельных случаях для диагностики болезни ребенку с клиническими признаками менингита назначается люмбальная пункция.
Пациентам с синдромом Кавасаки показаны консультации следующих специалистов: консультация ревматолога, инфекциониста, невропатолога, нефролога, отоларинголога, офтальмолога, гематолога, а также консультация кардиохирурга (ангиохирурга) при развитии стеноза коронарной артерии, а также при повторных эпизодах коронарной ишемии для решения вопроса о хирургическом лечении.
Лечение
Лечение должно начинаться сразу же после постановки диагноза во избежание повреждений коронарных артерий. Введение ВВИГ в высоких дозах (2 г/кг массы ребенка в 1 инфузии в течение 10-12 ч) представляет собой стандартное лечение болезни Кавасаки [18]. При этом значительное улучшение состояния обычно наблюдается в течение 24 ч. Если нет контроля над гипертермией, может использоваться дополнительная 2-я доза и, в редких случаях, 3-я доза. ВВИГ наиболее эффективен для предотвращения аневризм коронарных артерий в течение первых 7-10 дней от начала заболевания. Если пациент с болезнью Кавасаки в силу каких-либо причин не получил терапию ВВИГ в первые дни болезни, рекомендовано незамедлительно провести инфузию ВВИГ сразу после подтверждения диагноза [19, 20]. У некоторых пациентов может быть резистентность к действию ВВИГ, в таких случаях Американская кардиологическая ассоциация рекомендует пульс-терапию метилпреднизолоном, прием инфликсимаба, циклоспорина А, метотрексата и плазмаферез. Кортикостероидная терапия при болезни Кавасаки не проводится, так как исследования показали, что она повышает риск коронарного тромбоза.
Терапия салициловой кислотой остается важной составляющей лечения. Она начинается в высоких дозах (30-100 мг/кг в 4 приема), проводится до тех пор, пока не купируется гипертермия, и затем продолжается с использованием низких доз (по 3-5 мг/кг в сутки) обычно на протяжении 2 мес с целью предотвращения образования тромбов. При аневризмах коронарных артерий размером >8 мм и/или наличии тромбоза рекомендована комбинация с варфарином в дозе 0,05-0,12 мг/кг под контролем международного нормализованного отношения (МНО) пожизненно [13]. При крупных или многочисленных аневризмах можно дополнительно назначить нефракционированный гепарин (доза насыщения 50 ед/кг, поддерживающая доза 20 ед/кг) под контролем МНО и активированного частичного тромбопластинового времи, дипиридамол или клопидогрел.
В настоящий момент проводится ряд экспериментальных исследований методов лечения синдрома Кавасаки. Так, антагонист рецептора ИЛ-1 (анакинра) может предотвращать коронарное повреждение при моделировании заболевания у мышей даже при позднем начале терапии. Ряд исследователей для лечения ирита и других глазных симптомов предлагают применять инфликсимаб. Он действует посредством связывания с фактором некроза опухолей альфа [21]. Наиболее эффективным может оказаться применение инфликсимаба в ранние сроки болезни в качестве стартовой терапии в сочетании с ВВИГ.
Прогноз
При условии во время начатого лечения можно ожидать быстрого устранения острых симптомов, и при этом риск возникновения аневризм коронарных артерий значительно снижается. У части пациентов даже при отсутствии лечения острые симптомы болезни Кавасаки купируются самостоятельно, но риск вовлечения коронарных артерий в патологический процесс очень высок. В целом около 2% пациентов умирает от осложнений коронарного васкулита [22]. Прогностически неблагоприятным является сохранение гипертермии более 16 сут, рецидив после 2 сут нормальной температуры. Хуже прогноз у мальчиков, а также у младенцев младше 1 года [19].
Диспансерное наблюдение
Пациенты после перенесенного синдрома Кавасаки должны оставаться под наблюдением врача-кардиолога в связи с высоким риском развития сердечно-сосудистых осложнений, а также риском развития аутоиммунных болезней.
ЭхоКГ должна проводиться регулярно, каждые 6 мес, до полного исчезновения коронарных аневризм. Детям со стойкими аневризмами проводят эхоКГ каждые 6 мес и ЭКГ пожизненно. По показаниям выполняют коронарографию и кардиотесты с физической нагрузкой. Пациентам с жалобами на боль или дискомфорт в загрудинной области и/или сердцебиение, а также всем пациентам со стенозами и гигантскими аневризмами артерий рекомендуется суточное холтеровское мониторирование для исключения аритмий и ишемических нарушений.
Рекомендовано иммунизировать детей после перенесенного синдрома Кавасаки не ранее чем через 3-6 мес инактивированными вакцинами, в том числе против ветряной оспы, кори, краснухи [22].
Нужно помнить, что данной группе пациентов вследствие высокого риска развития атеросклероза необходимо соблюдение диеты (ограничение тугоплавких жиров и «быстрых углеводов» и т. д.), важен контроль за массой тела и ведение здорового образа жизни.
Клинический пример
Вашему вниманию предлагается история болезни пациента М. в возрасте 10 месяцев, который наблюдался и проходил лечение в Морозовской детской городской клинической больнице (г. Москва) при участии сотрудников кафедры педиатрии лечебного факультета Российского национального исследовательского медицинского университета им. Н.И. Пирогова (заведующий кафедрой д.м.н., проф. С.С. Паунова).
Из анамнеза жизни известно, что ребенок от второй беременности, протекавшей с острой респираторной вирусной инфекцией в I триместре и угрозой прерывания во II триместре. Роды вторые, срочные, выполнено кесарево сечение в связи с тугим обвитием шеи пуповиной. При рождении масса тела 3950 г, рост 55 см. Период ново-рожденности протекал без особенностей. Ребенок вакцинирован только в роддоме (БЦЖ и гепатит В), далее не вакцинирован. На естественном вскармливании находился до 1,5 мес. Перенесенные заболевания - баланит в 4 мес. В семье отмечались заболевания желудочно-кишечного тракта по линии матери (язвенная болезнь желудка) и гипертоническая болезнь - по линии отца.
Анамнез заболевания. Заболел остро с повышения температуры до гектических цифр. При поступлении в больницу абактериальная лейкоцитурия (6-7 кл. в поле зрения), лейкоцитоз (до 12,4 х 109/л), фебрильная лихорадка (до 39,5°С) без катаральных явлений. Отмечалась двукратная рвота при повышении температуры. Амбулаторно был осмотрен педиатром, установлен диагноз: «Инфекция мочевой системы? ОРВИ?» Проводимая терапия: нурофен (сироп), цефекон, эффералган в свечах (без эффекта), аугментин (суспензия) в возрастной дозировке. На фоне начала антибиотикотерапии появилась мелкопятнистая сыпь, что было расценено как проявление острой аллергической реакции по типу крапивницы на полусинтетический пенициллин.
Динамика клинической картины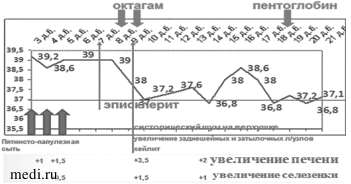
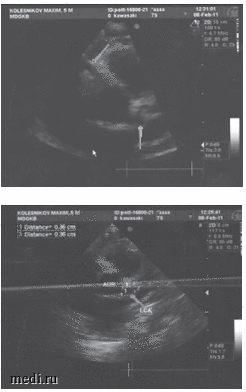
ЭхоКГ (08.02.2011)
- Дилатация обеих коронарных артерий (диаметр 4 мм, N до 2,5 мм).
- Умеренная центральная аортальная регургитация.
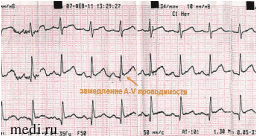
ЭКГ (04.03.2011)
- ЧСС 122-109 в мин, синусовый ритм.
- Вертикальное положение ЭОС.
- A-V блокада I ст.: интервал P-Q 0,18 с.
- ЧСС 125-109 в мин, синусовый ритм.
- Вертикальное положение ЭОС.
- A-V блокада I ст.: интервал P-Q 0,18 с.
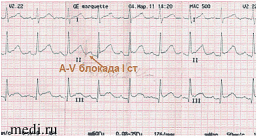
Лабораторные показатели в динамике
| ОАК | 07.02.2011 | 24.02.2011 |
| Эритроциты (х1012/л) | 5,26 | 4,79 |
| Гемоглобин (г/л) | 120 | 102 |
| Лейкоциты (х109/л) | 23 | 16,7 |
| Лимфоциты (%) | 41 | 59 |
| Тромбоциты (х1012/л) | 375 | 691 |
| СОЭ (мм/ч) | 5 | 19 |
Биохимический анализ крови
- серомукоид - 0,462 Ед ↑ (N до 0,2) ммоль/л
- СРБ - 0,061 1 (N до 0,1)
| Анализ мочи | 04.02.2011 (по Нечипоренко) |
24.02.2011 (общий) |
| Лейкоциты | 8750 | 1-2 в п/зр. |
| Эритроциты | 1000 | 0-1 в п/зр. |
Посев мочи (07.02.2011)
- стерильно
| Характерные симптомы синдрома Кавасаки | Симптомы заболевания, выявленные у пациента |
| Лихорадка не менее 5 дней | + 39,0-39,5 °С, без динамики на а/б и НПВС |
| Эритематозная сыпь | + 4 дня |
| Ладонная эритема | ? |
| Изменение слизистой оболочки, хейлит | + с 7-го дня болезни |
| Воспаленный зев | + |
| Малиновый язык с выраженными сосочками | ? |
| Конъюнктивит, другие поражения глаз | + эписклерит с 5-го дня болезни |
| Острая негнойная шейная лимфаденопатия | з/шейные л/у, затылочные с 7-го дня болезни |
| Увеличение печени | + максимально +3,5 см |
| Увеличение селезенки | + максимально +1,5 см |
| Стерильная лейкоцитурия | до 8750 по Нечипоренко |
| Поражение сердца: появление шумов в сердце | + с 7-го дня болезни |
| Изменения на ЭКГ | + замедление A-V проводимости, нарастающее в динамике |
| Изменения на эхоКГ | + дилатация обеих коронарных артерий |
| Кардит, коронарит | + |
Рентгенография грудной клетки (19.02.2011)
- Очаговых, инфильтративных теней в легких не выявлено.
- Тень сердца расширена в поперечнике.
- КТИ 0,63.
Вирусологическое обследование:
- ПЦР CMV +++
Таким образом у нашего пациента был установлен основной диагноз болезни Кавасаки.
Сопутствующий диагноз: «Цитомегаловирусная инфекция. Двусторонний острый средний катаральный отит (с 8-го дня болезни)».
Проводимая терапия.
- Патогенетическая терапия: внутривенное введение октагама в дозе 150 (2 г/кг) на 6-е, 7-е сутки заболевания и пентаглобина в дозе 150 на 17-й день болезни.
- Пульс-терапия метилпреднизолоном в дозе 80 мг однократно.
- Тромбо АСС в дозе 25 мг 4 раза в сутки с повышением дозы до 100 мг 4 раза в сутки.
- Трентал (100 мг) 1/4 таблетки 4 раза в сутки.
- Инфузионная терапия.
- Местная антибиотикотерапия отита.
- Жаропонижающая терапия ибупрофеном, парацетамолом в возрастных дозировках - по показаниям.
При выписке на 21-й день болезни у ребенка сохранялся умеренный субфебрилитет (до 37,4°С). Отмечалось небольшое увеличение селезенки (выступала на 0,5 см из-под края реберной дуги) при отсутствии гепатомегалии. Сохранились изменения на электрокардиограмме и эхоКГ.
Ребенок выписан под постоянное наблюдение участкового педиатра и кардиолога с рекомендациями проводить ежегодную углубленную диспансеризацию, включая эхоКГ, чтобы следить за состоянием изменений стенок коронарных артерий и предупредить в отдаленном будущем развитие раннего атеросклероза или кальциноза с последующей ишемией сердца, угрожающей развитием острого инфаркта миокарда.
Литература
1. Похожие на синдром Кавасаки симптомы у детей связывают с коронавирусом // BBC News Русская служба. 2020. 14 мая.
2. Hyperinflammatory shock in children during COVID-19 pandemic / S. Riphagen [et al.] // Lancet. 2020. Vol. 395 (10237). P. 1607-1608.
3. Ultrastructural, immunofluorescence, and RNA evidence support the hypothesis of a "new" virus associated with Kawasaki disease / A.H. Rowley [et al.] // Journal of Infectious Diseases. 2011. Vol. 203. P. 1021-1030.
4. Heat shock proteins and superantigenic properties of bacteria from the gastrointestinal tract of patients with Kawasaki disease / S. Nagata [et al.] // Immunology. 2009. Vol. 128, No. 4. P. 511520.
5. Ultrastructural, immunofluorescence, and RNA evidence support the hypothesis of a «new» virus associated with kawasaki disease / A.H. Rowley [et al.] // Journal of Infectious Diseases. 2011. Vol. 203, No. 7. P. 1021-1030.
6. Nagata S. Causes of Kawasaki Disease - from past to present // Frontiers in Pediatrics. 2019. Vol. 7. P. 18.
7. Marrani E., Burns J.C., Cimaz R. How should we classify Kawasaki Disease? // Frontiers in Immunology. 2018. Vol. 9. P. 297.
8. A genome-wide association study identifies novel and functionally related susceptibility Loci for Kawasaki disease / D. Burgner [et al.] // PLoS Genetics. 2009. Vol. 5, No. 1. e1000319.
9. Genome-wide linkage and association mapping identify susceptibility alleles in ABCC4 for Kawasaki disease / C.C. Khor [et al.] // Journal of Medical Genetics. 2011. Vol. 48, No. 7. P. 467-472.
10. Association of CCR2-CCR5 haplotypes and CCL3L1 copy number with Kawasaki Disease, coronary artery lesions, and IVIG responses in Japanese children / M. Mamtani [et al.] // PLoS One. 2010. Vol. 5, No. 7. P. e11458.
11. Onouchi Y. Susceptibility genes for Kawasaki disease // Nihon Rinsho. 2014. Vol. 72, No. 9. P. 1554-1560.
12. Обзор клинических рекомендаций по болезни/синдрому Кавасаки / А.А. Баранов [и др.] // Педиатрическая фармакология. 2017. Т. 14, № 2. С. 87-99.
13. Cennimo D.J. Fast Five Quiz: Kawasaki Disease // Medscape. 2020.
14. Клиника, диагностика и лечение синдрома Кавасаки. Клинические рекомендации / Г.А. Лыскина [и др.]. М.: Ассоциация детских кардиологов России, 2011. 57 с.
15. Novel and traditional cardiovascular risk factors in children after Kawasaki disease: implications for premature atherosclerosis / Y.F Cheung [et al.] // Journal of the American College of Cardiology. 2003. Vol. 43, No. 1. P. 120-124.
16. Kawasaki disease: guidelines of Italian Society of Pediatrics, part II -treatment of resistant forms and cardiovascular complications, follow-up, lifestyle and prevention of cardiovascular risks / A. Marchesi [et al.] // Italian Journal of Pediatrics. 2018. Vol. 44. P. 103.
17. Ocular manifestations of Kawasaki's disease (mucocutaneous lymph node syndrome) / S. Ohno [et al.] // American Journal of Ophthalmology. 1982. Vol. 93, No. 6. P. 713-717.
18. Pediatrics, Kawasaki Disease: Treatment & Medication - eMedicine Emergency Medicine. Emedicine.medscape.com. 201003-18. Retrieved 2010-05-19.
19. Баранов А.А., Таточенко В.К., Бакрадзе М.Д. Лихорадочные синдромы у детей. Рекомендации по диагностике и лечению. М.: Союз педиатров России, 2011. 208 с.
20. Hounsfield unitvalues retropharyngeal abscess-like lesions seen in Kawasaki disease / T. Sasaki [et al.] // Acta Otorhinolaryngologica. 2014. Vol. 134, No. 4. P. 437-440.
21. REMICADE® Becomes First Anti-TNF Biologic Therapy to Treat One Million Patients Worldwide.
22. A predictive instrument for coronary artery aneurysms in Kawasaki disease. US Multicenter Kawasaki Disease Study Group / A.S. Beiser [et al.] // American Journal of Cardiology. 1998. Vol. 81, No. 9. P. 1116-1120.
23. Calcineurin inhibitor treatment of intravenous immunoglobulin-resistant Kawasaki disease / A.H. Tremoulet [et al.] // Journal of Pediatrics. 2012. Vol. 161, No. 3. P. 506-512.

