Современная стратегия лечения хронического гепатита B: достижения и перспективы.
Статьи Опубликовано в журнале:
Экспериментальная и клиническая гастроэнтерология №2, 2007.
Исаков В.А. Отделение гастроэнтерологии и гепатологии ГУ НИИ питания РАМН, Москва
Данные, приведенные в статье, были получены в исследовании оригинального препарата энтекавира (Бараклюд®). Применение несертифицированных противовирусных средств может угрожать вашему здоровью, привести к возникновению мутантных штаммов вируса гепатита В и неэффективности дальнейшей терапии.
В последние 20 лет заболеваемость хроническим вирусным гепатитом В (ХГВ) в мире неуклонно снижалась в связи с осуществлением программ вакцинации населения против вируса гепатита В (ВГВ). Тем не менее в мире насчитывается около 350 млн инфицированных [8]. Полагают, что до 40% из этого числа умрут в ближайшие 50 лет вследствие прогрессирования ХГВ в цирроз печени, его декомпенсации и возникновения гепатоцеллюлярной карциномы (ГЦК). Опасность ХГВ в качестве предшественника цирроза печени и ГЦК всегда оценивалась специалистами как достаточно высокая. Однако, принимая во внимание значительные вариабельность и длительность течения заболевания, огромное количество кофакторов (со стороны макроорганизма и окружающей среды), влияющих на его течение, не было разработано критериев, которые помогали бы врачу определить риск неблагоприятного исхода заболевания у конкретного пациента. В последние годы были завершены крупные эпидемиологические исследования, созданы новые лекарственные препараты, эффективно подавляющие репликацию ВГВ, получены отдаленные результаты их использования, на основании которых были не только разработаны критерии прогрессирования ХГВ, но и изменилось представление о том, какие задачи должны решаться в процессе диагностики и лечения данного заболевания. Можно констатировать, что в начале XXI века была создана новая стратегия лечения ХГВ.
Если задаться вопросом, когда хронический вирусный гепатит В становится опасным и почему, то прежде всего следует вспомнить, откуда берутся больные ХГВ. Известно, что если взрослый заражается вирусом гепатита В, то в подавляющем большинстве случаев (около 90%) острая инфекция заканчивается выздоровлением, а в остальных 10% случаев течение заболевания напоминает таковое у лиц, заразившихся вирусом при рождении от инфицированной матери. Для них характерна фаза иммунной толерантности с медленной сероконверсией HBeAg и сохраняющимся умеренным уровнем ДНК ВГВ в крови (около 100 000 копий на мл). Именно такие пациенты и составляют большинство инфицированных ВГВ в мире на сегодняшний день [10]. Учитывая, что более чем у 80% из них заболевание протекает бессимптомно, а активность аланинаминотрансферазы (АЛТ) в крови флюктуирует, нередко принимая нормальные значения, такие больные выпадают из поля зрения врача, расценивающего их состояние как носительство, не предполагающее ни активного наблюдения, ни тем более проведения каких-либо лечебных мероприятий. Однако, как оказалось, у данных пациентов даже при стойко нормальном уровне АЛТ может развиваться цирроз печени [4]. Фактическое большинство случаев цирроза печени и ГЦК (> 75%) развиваются в позднюю фазу инфекции, то есть после сероконверсии HBeAg [13]. Также важно помнить, что ВГВ обладает значительным канцерогенным действием и может провоцировать возникновение ГЦК даже при отсутствии цирроза печени. Все это косвенно свидетельствует в пользу того, что пациенты с неактивным гепатитом имеют определенный и достаточно высокий риск неблагоприятного исхода заболевания при длительном течении.
Согласно опубликованным результатам нескольких эпидемиологических исследований, основным фактором, определяющим исход хронической инфекции ВГВ, является уровень вируса в крови пациентов, или вирусная нагрузка. Так, в исследовании REVEAL были проанализированы результаты наблюдения за 3653 пациентами (2925 из которых были HBeAg-негативными) в течение 11,4 лет [2]. Была выявлена прямая зависимость между уровнем вирусной нагрузки и заболеваемостью ГЦК (рис. 1). Кроме того, эта зависимость наблюдалась и среди лиц без HBeAg, нормальным уровнем АЛТ и без цирроза печени. Достоверность полученных результатов сохранялась после стандартизации по возрасту, полу, уровню потребления алкоголя и курения.
Рис. 1. Зависимость заболеваемости гепатоцеллюлярной карциномой (ГЦК) от вирусной нагрузки ВГВ. Цит. по [2]
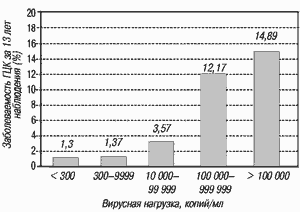
Интересно, что риск ГЦК был ниже у пациентов, у которых в процессе наблюдения вирусная нагрузка уменьшилась по сравнению с исходным уровнем, а у пациентов, вирусная нагрузка у которых увеличилась, была отмечена самая высокая заболеваемость ГЦК. Наибольший риск возникновения ГЦК был у пациентов с вирусной нагрузкой 100 000 копий/мл или выше (отношение шансов - 10,1). Даже при уменьшении в процессе наблюдения вирусной нагрузки ниже уровня в 10 000 копий/мл риск возникновения ГЦК все еще оставался достаточно высок (отношение шансов - 3,8). Иными словами ГЦК возникает у пациентов с высокой вирусной нагрузкой в 10 раз чаще, а у больных с низкой вирусной нагрузкой примерно в 4 раза чаще, чем у лиц контрольной группы, то есть не инфицированных ВГВ. Эти данные не только убедительно доказывают, что ГЦК может развиваться при отсутствии цирроза печени и активного гепатита, но что частота ее возникновения напрямую зависит от вирусной нагрузки. Все это позволяет предположить, что уменьшение вирусной нагрузки в течение заболевания (в том числе и с помощью терапии) существенно снижает риск возникновения ГЦК.
Эта же группа исследователей представила анализ наблюдения за 3582 пациентов (2923 из которых были HBeAg-негативными на момент начала наблюдения) для проведения оценки риска возникновения цирроза печени [6]. В период наблюдения (40 038 человеко-лет) было зарегистрировано 365 случаев цирроза печени. Риск возникновения цирроза печени зависел от величины вирусной нагрузки в начале наблюдения и достоверно различался в подгруппах больных (рис. 2). Многофакторный анализ показал, что риск развития цирроза печени не зависел от наличия HBeAg и от исходной активности АЛТ.
Рис. 2. Зависимость заболеваемости циррозом печени от вирусной нагрузки ВГВ. Цит. по [в]
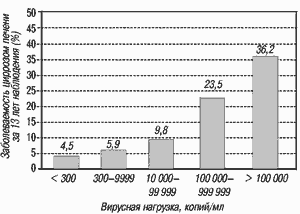
И, наконец, результаты исследования, в котором в течение 46,9 месяцев наблюдали 3233 пациента, инфицированных ВГВ, также доказали связь между содержанием ДНК ВГВ в крови и возникновением ГЦК и цирроза печени [13]. В отличие от вышеприведенных исследований в этом было продемонстрировано, что даже при практически нормальном уровне АЛТ (в 0,5-1 раз выше нормы) развивается цирроз печени. В 50% наблюдений он развился при низкой вирусной нагрузке (менее 10 000 копий/мл).
Все эти исследования ставят принципиально важный вопрос: какой уровень ДНК ВГВ считается безопасным? Иными словами, насколько необходимо подавлять репликацию вируса, чтобы кардинально снизить или совсем исключить риск возникновения цирроза печени и ГЦК? До последнего времени считалось, что риск развития осложнений ВГВ существенен, если вирусная нагрузка составляет 100 000 копий/мл или выше. Однако вышеприведенные результаты опровергают правильность данного положения. Так, в ретроспективном исследовании на 165 пациентах с гепатитом В ни уровень АЛТ, ни сероконверсия HBeAg не были достоверно связаны с вирусной нагрузкой [3]. Более чем у половины пациентов после сероконверсии HBeAg вирусная нагрузка составляла больше 100 000 копий/мл, в то же время у 45% больных HBeAg-негативным хроническим гепатитом вирусная нагрузка была меньше 100 000 копий/мл. В другом исследовании при сравнении групп больных с циррозом печени (79 человек) и носителями ВГВ (158 человек) оказалось, что цирроз печени развился у 67,1% пациентов значительно позже сероконверсии HBeAg [12]. Интересно, что у пациентов, у которых развился цирроз печени, в 37,7% наблюдений вирусная нагрузка составляла более 100 000 копий/мл, а в 24,5% наблюдений - менее 10 000 копий/мл. В целом, у пациентов с циррозом печени исходный уровень вирусной нагрузки был достоверно выше, чем у пациентов без цирроза (р = 0,02). Таким образом, хроническая виремия ВГВ даже на низком уровне может сопровождаться прогрессированием поражения печени и развитием осложнений, что совпадает с результатами эпидемиологических исследований. Таким образом, очевидно, что безопасным уровнем виремии считается наиболее низкий. На сегодняшний день это предельно определяемое количество ВГВ в крови с помощью полимеразной цепной реакции - 300-400 копий/мл.
Итак, если эти выводы справедливы, тогда в результате лечения, снижающего вирусную нагрузку, у больных должны реже развиваться осложнения и хронический гепатит не должен прогрессировать. Метаанализ результатов 26 рандомизированных клинических исследований показал, что снижение вирусной нагрузки в процессе терапии - единственно независимый прогностический фактор успешного лечения как для HBeAg-позитивных, так и для HBeAg-негативных пациентов [11]. В исследовании на 63 HBeAg-позитивных пациентах, получавших в течение 3 лет лечение ламивудином в 56% случаев индекс гистологической активности (ИГА) уменьшился на 2 балла, в 33% наблюдений не изменился и только у 11% пациентов ухудшился [5]. Важно, что индекс фиброза уменьшился на 1 пункт у 63% пациентов, в том числе и у 73% пациентов с циррозом печени. Только у 3 (9%) пациентов фиброз, по данным серийных биопсий печени, прогрессировал в мостовидный и у 1 (2%) больного развился цирроз. Главный вывод этого исследования заключается в том, что и удачное лечение, и прогрессирование заболевания зависели от вирусной нагрузки. В процессе лечения у 65% пациентов ВГВ приобрел YMDD мутацию, вследствие которой возникла резистентность к ламивудину, и препарат не подавлял репликацию вируса столь же эффективно, как в начале лечения. Дополнительно проведенный анализ показал, что у больных без YMDD мутации (и низкой вирусной нагрузкой) вышеописанное улучшение гистологической картины печени наступило в 77% случаев, а ухудшение лишь в 5%, в то же время, в подгруппе пациентов с YMDD мутацией (и, соответственно, более высокой вирусной нагрузкой) эти показатели составили 44 и 15% соответственно. У всех пациенты с прогрессированием заболевания (3 с фиброзом и 1 с циррозом печени) наблюдались YMDD мутация и более высокий уровень вирусной нагрузки по сравнению с остальными.
В плацебо-контролируемом исследовании, включавшем 185 HBeAg-негативных пациентов, было показано, что у 71% пациентов, получавших адефовир в течение 96 недель, вирусная нагрузка составила меньше 1000 копий/мл, что сопровождалось уменьшением ИГА на 4,7 балла по сравнению с исходным уровнем. У них также достоверно уменьшился индекс фиброза. Характерно, что среди получавших плацебо такой же уровень вирусной нагрузки отмечался лишь в 8% наблюдений. Эти исследования показывают, что фиброз и даже цирроз являются обратимыми при стойком уменьшении вирусной нагрузки.
В другом исследовании была изучена связь между подавлением репликации вируса и осложнениями цирроза печени. В группе из 651 пациента (58% HBeAg-положительные) с гистологически подтвержденным выраженным фиброзом или циррозом печени изучали эффективность лечения ламивудином в сравнении с плацебо в течение 5 лет [9]. Исследование было завершено через 32 месяца в виду явного преимущества ламивудина. Гораздо меньше пациентов, принимавших ламивудин, умерло от осложнений цирроза печени или ГЦК (7,8 против 17,7%, р = 0,001). Прогрессирование цирроза печени (увеличение класса по классификации Чайлд-Пью) реже наступало в группе пациентов, получавших ламивудин (3,4 против 8,8%), также в этой группе снижался риск возникновение ГЦК (3,9 против 7,4%). И вновь, как и в предыдущих исследованиях, клинические показатели эффективности были обусловлены влиянием терапии на вирусную нагрузку. Среди лиц с прогрессированием цирроза печени на фоне приема ламивудина основную массу составили пациенты с YMDD мутацией, то есть вирусная нагрузка которых не контролировалась противовирусной терапией. Так, у пациентов с YMDD мутацией цирроз прогрессировал в 7% наблюдений, если же вирус оставался чувствительным к ламивудину и вирусная нагрузка контролировалась, цирроз прогрессировал менее чем у 1% пациентов.
Из вышепредставленных данных становится понятным, что основной задачей терапии хронического ВГВ является стойкое подавление репликации вируса в течение длительного времени, так как необходимы годы для регрессии воспалительного процесса в печени и ремоделирования сформировавшейся фиброзной ткани. Эта же задача стоит и при лечении циррозов печени, сформировавшихся вследствие хронического ВГВ. Только удержание репликации на как можно более низком уровне удлиняет ремиссию и уменьшает осложнения, включая возникновение ГЦК.
Очевидно, что для достижения этой цели в большей степени подходят аналоги нуклеозидов, как пероральные препараты с высоким профилем безопасности, которые могут применяться длительно и непрерывно. Недостаток, свойственный данному классу препаратов, резистентность вируса резистентности к ним.
Следует отметить, что частота возникновения резистентности связана с противовирусной активностью, так как при лечении препаратом с более выраженной противовирусной активностью резистентность возникает реже и в гораздо более поздние сроки. Данная закономерность отражена на рис. 3 и 4. Как видно из представленных на них данных, наиболее выраженным противовирусным действием и наилучшим профилем резистентности обладает энтекавир. За 2 года у пациентов, не получавших ранее терапию нуклеозидами, не были зафиксированы штаммы вируса, резистентных к энтекавиру. 3-летнее наблюдение показало, что вирусологический рецидив, обусловленный резистентностью к энтекавиру, наблюдался менее чем у 1% пациентов, не получавших ранее нуклеозиды [14]. Эти свойства и определяют клиническую эффективность препарата.
Puc. 3. Выраженность противовирусного действия различных препаратов на момент окончания курса терапии стандартными дозами в течение 48 недель
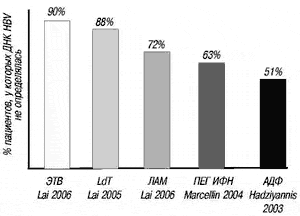
Рис. 4. Увеличение числа резистентных штаммов ВГВ на фоне терапии аналогами нуклеозидов. Цит. с изменениями по [14], а также Lai С. et at. Clin Infect Dis 2003; 36: 687-96 u Hadziyannis S. et al. Gastroenterology 2006 [in press]
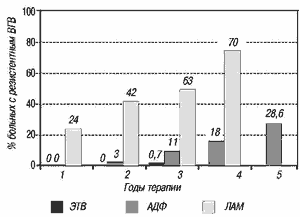
В двух мультицентровых контролируемых исследованиях, в которые были включены как HBeAg-позитивные, так и HBeAg-негативные пациенты, энтекавир по всем клиническим показателям превосходил ламивудин в течение курса терапии длительностью 48 недель (табл. 1) [1, 7]. Увеличение терапии до 96 недель улучшило эти показатели в группе энтекавира. При HBeAg-позитивном хроническом гепатите количество пациентов с содержанием ДНК ВГВ было ниже порога чувствительности метода (менее 300 копий/мл) составил 80%, в то же время в группе, получавшей ламивудин, он составил всего лишь 39% (p < 0,001) [15]. Аналогично, при HBeAg-негативном хроническом гепатите на 96-й неделе лечения этот показатель составил 94% и 77% (p < 0,001) соответственно [17].
Таблица I. Результаты применения энтекавира и ламивудина в течение 48 недель у пациентов с активным хроническим гепатитом В
| Характеристики пациентов | HBeAg-позитивный хронический активный гепатит | HBeAg-негативный хронический активный гепатит | ||
| энтекавир 0,5 мг/сут | ламивудин 100 мг/сут | энтекавир 0,5 мг/сут | ламивудин 100 мг/сут | |
| % пациентов с ДНК ВГВ < 300 копий/мл | 67* | 36 | 90* | 72 |
| % пациентов с AЛT=N | 68++ | 60 | 78+ | 71 |
| % пациентов с улучшением ИГА (> 2 балла) | 72* | 62 | 70* | 61 |
Таким образом, выраженная репликация ВГВ под действием энтекавира выразилась в более быстром уменьшении вирусной нагрузки, сопровождавшейся регрессией патологического процесса в печени у значительного числа пациентов. Результаты крупных мультицентровых исследований вновь подтвердили справедливость представлений о том, что вирусная нагрузка у больных ХГВ является не только важным критерием отдаленных исходов болезни, но и важным фактором клинической эффективности применяемой противовирусной терапии. Небольшое исследование, выполненное на группе из 47 больных с циррозом печени, также подтвердило правильность подобных выводов (рис. 5) [16]. Как видно из представленных на рис. 5 данных, энтекавир превосходил ламивудин как по числу пациентов с неопределяемой ДНК ВГВ, так и по регрессии воспалительного процесса в печени. Следует отметить, что энтекавир - первый из нового поколения аналогов нуклеозидов, созданных специально для лечения вирусного гепатита В и обладающий выраженным противовирусным эффектом. Ближайшие 5-7 лет ознаменуются появлением целого ряда аналогов нуклеозидов разнообразных по механизму действия и так же обладающих выраженной противовирусной активностью (табл. 2). Современная стратегия лечения ХГВ предполагает, что основой определения риска осложнений и отдаленных исходов заболевания является вирусная нагрузка, она же является критерием эффективности лечения. Невозможность элиминации вируса у большинства пациентов предполагает, что основным методом лечения является длительное подавление репликации вируса. Уже сейчас ясно, что такая стратегия, пусть и не идеальная, гарантирует отсутствие прогрессирования заболевания у подавляющего числа пациентов, а в случае ранней фазы таких осложнений, как цирроз печени может обеспечить его стабилизацию, уменьшение риска возникновения ГЦК, а в ряде случаев и регрессию фиброзных изменений. Существующий недостаток нуклеозидов - появление резистентных штаммов ВГВ с созданием новых, более интенсивно подавляющих репликацию вируса препаратов существенно уменьшен, а для пациентов, у которых вирус уже резистентен, в качестве терапии выбора может быть предложен переход на новый препарат или применение комбинации препаратов.
Рис. 5. Сравнительная эффективность лечения цирроза печени энтекавиром или ламивудином в течение 48 недель. Цит. по [16]
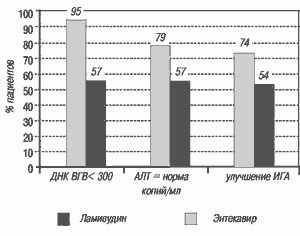
Таблица 2. Аналоги нуклеозидов и нуклеотидов, зарегистрированные в США/странах ЕС или на стадии клинических исследований
| Препарат | Фаза исследования |
| Ламивудин Адефовир дипивоксил Энтекавир Телбивудин |
Зарегистрированы |
| Эмтрицитабин Тенофовир Клевудин |
Фаза 3 |
| Амдоксовир Эльвуцитабин Рацивир Прадефовир Валторцитабин |
Фаза 2 |
| Аламовир (аналог пиримидина) MIV 210 (пролекарство FLG) Гепавир В (пролекарство РМЕА) |
Фаза 1 |
Статья подготовлена при поддержке компании Bristol-Myers Squibb
Литература
1. Chang, T. T. A comparison of entecavir and lamivudine for HBeAg-positive chronic hepatitis B. /T.T. Chang, R.G. Gish, R. de Man et al. //New Engl. J. Med. 2006. Vol. 354. № 10. P. 1001-1010.
2. Chen, C.J. Risk of hepatocellular carcinoma across a biological gradient of serum hepatitis B virus DNA level. /C.J. Chen, H.I. Yang, J. Su et al. //JAMA. 2006. Vol. 295. №1. P. 65-73.
3. Chu, C.J. Quantitative serum HBV DNA levels during different stages of chronic hepatitis B infection. / C.J. Chu, M. Hussain, A.S. Lok //Hepatology. 2002. Vol. 36. № 6. P. 1408-1415.
4. Chu, C.M. Natural history of hepatitis B e antigen to antibody seroconversion in patients with normal serum aminotransferase levels./C.M. Chu, S.J. Hung, J. Lin et al //Am J. Med. 2004. Vol. 116 №12. P. 829-834.
5. Dienstag, J.L. Histological outcome during long-term lamivudine therapy. / J.L. Dienstag, R.D. Goldin, E.J. Heathcote et al // Gastroenterology. 2003. Vol. 124. №1. P. 105-117.
6. Iloeje, U.H. Predicting cirrhosis risk based on the level of circulating hepatitis B viral load. /U.H. Iloeje, . Yang, J. Su et al.//Gastroenterology. 2006. Vol. 130. № 3. P. 678-686.
7. Lai, C.L. Entecavir versus lamivudine for patients with HBeAg-negative chronic hepatitis B. /C.L. Lai, D. Shouval, A.S. Lok et al.//New. Engl. J. Med. 2006. Vol. 354. №10. P. 1011-1020.
8. Lee, W.M. Hepatitis B virus infection. /W.M. Lee // New Engl. J. Med. 1997. Vol. 337. №24. P. 1733-1745.
9. Liaw, Y.F. Lamivudine for patients with chronic hepatitis B and advanced liver disease. /Y.F. Liaw, J.J. Sung, W.C. Chow et al. // New Engl. J. Med. 2004. Vol. 351. №15. P. 1521-1531.
10. McMahon, B.J. Epidemiology and natural history of hepatitis B. / B.J. McMahon // Semin Liver Dis. 2005. Vol. 25. P. 3-8.
11. Mommeja-Marin, H. Serum HBV DNA as a marker of efficacy during therapy for chronic HBV infection: analysis and review of the literature. / H. Mommeja-Marin, E. Mondou, M.R. Blum, F. Rousseau // Hepatology. 2003. Vol. 37. №6. P. 1309-1319.
12. Yuan, H.J. The relationship between HBV-DNA levels and cirrhosis-related complications in Chinese with chronic hepatitis B. / H.J. Yuan, M.F. Yuen, D. Ka-Ho Wong et al.//J. Viral Hepat. 2005. Vol. 12. № 4. P. 373-379.
13. Yuen, M.F. Prognostic determinants for chronic hepatitis B in Asians: therapeutic implications. / M.F. Yuen, H.J. Yuan, D.K. Wong et al.//Gut 2005. Vol. 54. №11. P. 1610-1614.
14. Colonno, R.J. Assessment at three years shows high barrier to resistance is maintained in Entecavir у treated nucleoside naive patients while resistance emergence increases over time in Lamivudine refractory patients. /R.J. Colonno, R.E. Rose, K. Pokornowski et al.//Hepatology. 2006. Vol. 44 (Suppl. 1). P. 229Aс230A.
15. Gish, R.G. Entecavir Results in Substantial Virologic and Biochemical Improvement and HBeAg Seroconversion Through 96 Weeks of Treatment in HBeAg(+) Chronic Hepatitis B Patients (Study ETV-022). /R.G. Gish, T.T. Chang, R.A. de Man et al.// Hepatology. 2005. Vol. 42 (S1). Abstract 67146.
16. Schiff, E. Efficacy and safety of entecavir (ETV) and lamivudine (LAM) in compensated, cirrhotic patients with chronic hepatitis B. /E. Schiff, W.M. Lee, Y.C. Chao et al.//Hepatology. 2005. Vol. 42 (S1). Abstract 65864.
17. Shouval, D. Continued virologic and biochemical improvement through 96 weeks of entecavir treatment in HBeAg(-) chronic hepatitis B patients (STUDY ETV-027)./D. Shouval, U.S. Akarca, G. Hatzis et al.// Hepatol. 2006. Vol. 44 (Suppl. 2). S 21.
