Детекция молекулярных нарушений, характерных для рака легкого. Возможности использования в клинической практике.
Статьи ОнкологияОпубликовано в сборнике Новое в терапии рака легкого (Москва, 2003) Зборовская И. Б., Чижиков В. В.
Введение.
Развитие злокачественной опухоли многофакторный и многостадийный процесс, в основе которого лежит накопление клетками различных генетических изменений, приводящих к злокачественной трансформации. Малигнизация нормальных клеток является следствием каскадного накопления в их геноме различных нарушений. Предполагается, что для развития рака у человека необходимы изменения не менее 6-10 генетических факторов.
Известно, что основной причиной возникновения и прогрессии злокачественных новообразований является нарушение функционирования относительно небольшого числа генов, в частности протоонкогенов и генов-супрессоров опухолевого роста (антионкогенов). Кроме того, существует большая группа генов-модуляторов, не отвечающих за злокачественную трансформацию клеток, но способствующих распространению опухоли в организме [1, 2].
В настоящее время накоплен достаточно большой объем данных, касающихся отдельных молекулярно-генетических характеристик различных типов рака легкого. И хотя спектр генетических изменений в случае каждой конкретной опухоли носит индивидуальный характер, тем не менее наблюдаются определенные закономерности генных альтераций, которые дают основания связывать их с развитием или характером прогрессии той или иной патологии.
Наследуемые особенности генома как факторы риска развития рака легкого.
В настоящее время накоплен достаточный объем данных, позволяющих связать те или иные детерминированные в геноме параметры с риском развития целого ряда неоплазий включая рак легкого (РЛ). Особая роль отводится исследованиям аллельного полиморфизма онкогенов или генов, связанных с метаболизмом канцерогенов, в частности, обнаруживаемых в продуктах сгорания табака.
Аллельный полиморфизм в локусе протоонкогена Hras1.
Аллельный полиморфизм в локусе гена Hras1 обусловлен вариабельным минисателлитным участком (в английской транскрипции - variable number of tandem repeats, VNTR), расположенным примерно на 1 т. п. н. "ниже" канонического сигнала полиаденилирования протоонкогена Hras1. Единицей повтора является мотив в 28 п. н. [З].
В 1985 году при исследовании геномной ДНК из нормальных и опухолевых клеток онкобольных с использованием рестрикционного анализа Кронтирис с соавторами [4] идентифицировали 20 аллелей Hras1, из которых 4 определили как "общие" (составляли 94% всех аллелей в исследованной популяции). Все остальные аллели, отличающиеся по размеру от любого из "общих", были отнесены к классу "редких". Этими же исследователями была выявлена статистически достоверная ассоциация между наличием у индивида "редкого" аллеля Hras1 и повышенным риском развития рака молочной железы, толстой кишки, мочевого пузыря и острой лейкемии [5]. В дальнейшем подобная связь была показана и в отношении РЛ, хотя информация по данному вопросу противоречива (Табл. 1).
Таблица 1 Ассоциация между наличием "редких" аллелей Hras 1 и риском возникновения РЛ.
|
Источник информации |
Рак легкого |
Контрольная группа |
Достоверность, P |
||
|
"Общие" аллели |
"Редкие" аллели (%) |
"Общие" аллели |
"Редкие" аллели (%) |
||
|
Чижиков с соавт., 2001 [6] |
420 |
32 (7.1%) |
405 |
9 (2.2%) |
0.0002 |
|
Rosell et al, 1999 [7] |
316 |
150 (32.7%) |
695 |
196 (21.9%) |
0.0001 |
|
Lindstedt et al, 1999 [8] Мужчины Женщины |
434 122 |
24 (5.2%) 10 (7.6) |
982 |
18 (1.8%) |
0.0003 0.0001 |
|
Гаспарьян с соавт, 1998 [9] АК (Курят) АК (Не курят) |
46 61 |
0 (0%) 13 (18%) |
109 |
3 (2.7%) |
0.0005 НД |
|
Гаспарьян с соавт, 1997 [10] ПКРЛ АК |
108 40 |
4 (3.6%) 2 (4.8%) |
103 |
3 (2.8%) |
НД НД |
|
Ryberg et al, 1995 [11] |
231 |
43 (16.7%) |
386 |
40 (9.4%) |
0.01 |
|
Krontiris et al 1993 [5] |
34 |
2 (5.8%) |
829 |
53 (6.0) |
НД |
|
Ryberg et al, 1992 [12] |
385 |
43 (10%) |
589 |
29 (4.7%) |
0.002 |
|
Sugimura et al, 1990 [13] Европеоиды Афро-американцы |
65 27 |
17 (21%) 39 (59%) |
61 41 |
13 (17%) 19 (32%) |
НД 0.07 |
|
White et all 990 [14] |
194 |
7 (3%) |
193 |
9 (4.4%) |
НД |
|
Heighway et al 1986 [15] |
248 |
16 (6. 4%) |
193 |
9 (4.4%) |
НД |
НД-статистически недостоверно (Р>>0.05)
Использование высокочувствительных методов аллелотипирования минисателлита Hras1 выявило проблему определения самого понятия "редкого" и "общего" аллеля Hras1. В ряде работ было показано, что частота некоторых из "редких" аллелей сравнима или даже выше частоты встречаемости "общего" аллеля а4 [7], что свидетельствует о некой произвольности определений, предложенных Кронтирисом с соавторами [4]. Тем не менее, данный подход был использован в подавляющем большинстве работ по настоящей тематике, хотя в последнее время ряд исследователей выделяет также "промежуточные " аллели (частота встречаемости в популяции здоровых доноров более 0.5%), а "редкими" принято называть только те аллели, частота которых была ниже 0.5% в популяции здоровых доноров [6, 8].
Существует проблема генетической адекватности сравниваемых групп в различных популяциях. В настоящее время четко показано, что частота встречаемости различных аллелей Hras1 у здоровых индивидов варьирует в отдельных популяциях и этнических группах [7, 8]. Кроме того, не всегда анализировалось морфологическое разнообразие онкологических поражений легких и влияние факторов внешней среды, которые могут маскировать участие наследственных факторов в процессе канцерогенеза.
До настоящего момента "редкие" аллели Hras1 ассоциировались только с онкологическими заболеваниями человека. Однако статистически достоверное повышение частоты "редких" аллелей Hras1 было обнаружено в группе больных хроническими неспецифическими заболеваниями легких, имеющих фиброз [16]. Важно отметить тот факт, что такие больные имеют особенно высокий риск возникновения РЛ и каждый десятый из них умирает в результате прогрессии данного заболевания [17]. Таким образом, повышенная частота "редких" аллелей Hras1 может являться фактором, обусловливающим повышенный риск возникновения РЛ в данной группе.
Помимо сравнения частот "редких" аллелей в группах больных различными формами РЛ и здоровых доноров были проведены попытки изучения различных "общих" аллелей Hras1 как наследственных факторов риска развития различных типов РЛ. Так, в двух работах было выявлено статистически достоверное повышение частоты аллеля а4 у больных НМРЛ по сравнению с группой индивидов без онкопатологии [10, 15], хотя данная тенденция не была подтверждена другими исследователями [7, 8].
На сегодняшний день неизвестно, каким образом определенные аллели Hras1 обусловливают повышенный риск возникновения ряда онкозаболеваний человека. Предполагается, что "редкие" аллели минисателлита Hras1 активируют транскрипцию расположенного в непосредственной близости от него протоонкогена Hras1 или еще неидентифицированных близлежащих протоонкогенов. В пользу этой гипотезы свидетельствует то, что "редкие" аллели минисателлита Hras1 в модельных системах обладают большим сродством к ряду транскрипционных факторов, относящихся к семейству rel/NFb kB [18, 19]. Вторая гипотеза заключается в том, что наличие "редких" аллелей данного минисателлита может быть признаком повышенной генетической нестабильности. Подтверждением этого предположения являются данные о повышенной частоте микросателлитной нестабильности в опухолях легких пациентов, имеющих "редкие" аллели Hras1 [20, 21].
Полиморфизм генов, продукты которых участвуют в метаболизме канцерогенов.
Цитохром Р4501А1 (CYP1A1), принимает участие в первом этапе метаболизма полициклических ароматических углеводородов. Данный ген содержит четыре полиморфных сайта, два из которых приводят к аминокислотным заменам (изолейцин/валин) в кодируемом белке.
Было показано, что определенные варианты двух сцепленных полиморфизмов в гене CYP1A1 (полиморфизм в 3' фланкирующем районе, выражающийся в возникновении сайта узнавания эндонуклеазы рестрикции Mspl и A4889G lle-Val полиморфизм) являются маркерами предрасположенности к заболеванию РЛ жителей Японии. Кроме того, курящие больные РЛ, гомозиготные по "редким" аллелям любого из двух вышеупомянутых полиморфных сайтов, имели повышенную частоту мутаций в гене р53, по сравнению с индивидами имеющими только "общие" аллели [22]. Обнаружена ассоциация между наличием определенного полиморфного варианта гена CYP1A1 и риском возникновения аденокарцином легкого даже при минимальной экспозиции канцерогенами табачного дыма [23]. Полученные результаты позволяют объяснить высокий риск возникновения аденокарцином у чернокожего населения Америки повышенной частотой данного полиморфного варианта в этой популяции. Однако исследования, проведенные в Европе, не выявили ассоциации между наличием каких-либо аллельных вариантов гена CYP1A1 и риском возникновения РЛ. Одной из причин, объясняющей эти противоречивые результаты, может быть очень низкая частота полиморфизма данного гена в исследованных европейских популяциях [24].
Одно из объяснений механизма ассоциации некоторых полиморфных вариантов гена CYP1A1 с повышенным риском возникновения РЛ может основываться на данных о том, что наличие по крайней мере одного из полиморфных вариантов CYP1A1 (A4889G (lle/Val) коррелирует с повышенной экспрессией этого гена и увеличением ферментативной активности в лимфоцитах, стимулированных митогеном, хотя информация по данному вопросу противоречива [25-27].
CYP2D6. также являющийся представителем семейства цитохромов Р450, обеспечивает метаболическую активацию нитрозаминов. Изучение возможной ассоциации между риском возникновения РЛ и наличием в геноме определенных полиморфных вариантов данного гена было объектом многочисленных исследований, проведенных в последнее десятилетие [28, 29]. Несмотря на то, что рядом авторов обнаружена связь между пониженной активностью этого фермента и уменьшением риска возникновения РЛ [30], другие работы не подтвердили подобной ассоциации [29, 31].
Глутатион S-трансфераза. В настоящее время ген глутатион S-трансферазы, продукт которого принимает участие в детоксикации активированных цитохромом Р450 полициклических углеводородов, является объектом пристального внимания как потенциальный маркер предрасположенности к заболеванию РЛ. Важно отметить, что около 50% европеоидов несут гомозиготные микроделеции в данном гене, которые выражаются в отсутствии функционально активного продукта в клетках таких индивидов [24]. Имеется несколько работ, связывающих указанный генотип с повышенным риском возникновения РЛ [32, 33], хотя опубликованы и противоположные данные [24]. Был выявлен синергизм между наличием определенных аллельных вариантов гена CYP1A1 и нарушением функции глутатион S-трансферазы. Так, японские исследователи показали, что у курящих больных НМРЛ, гомозиготных по A4889G (lle/Val) аллелю гена CYP1A1 и имеющих неактивную глутатион S-трансферазу, наблюдается повышение частоты возникновения мутаций антионкогена р53 и онкогена Kras в 9 и 11 раз соответственно (р<0.05), по сравнению с пациентами, которые имеют сходный ферментативный дефект глутатион S-трансферазы и lle/lle генотип CYP1A1 [22]. Подобные результаты были также получены при исследовании НМРЛ в бразильской [34] и немецкой популяциях [35], хотя не были подтверждены для некоторых других европейских популяций [36, 37].
Интересные данные получены группой из Калифорнийского университета, руководимой известным исследователем молекулярной патологии РЛ д-ром Белински. Было показано, что полиморфизм глутатион S-трансферазы Р1 ассоциирован с абберантным метилированием гена-супрессора р16, ингибитора киназ клеточного цикла и гена MGMT (0 (6) -метилгуанин-ДНКметилтрансферазы), участвующего в репарации ДНК (см. ниже) [38]. Анализ многочисленных данных о связи наследуемого функционального дефицита глутатион -S-трансферазы с генетическими нарушениями, характерными для РЛ, подтверждает непосредственное участии данного фермента в метаболических путях, обеспечивающих защиту клеток от канцерогенов табачного дыма и радона, индуцирующих повреждения ДНК.
Молекулярно-генетические маркеры в ранней диагностике рака легкого.
Существующие на сегодняшний день рутинные методы диагностики РЛ практически не позволяют обнаружить опухоль на ранней стадии, когда условия для ее лечения наиболее благоприятны. Между тем, при диагностике РЛ на I стадии выживаемость больных достигает 70% [39, 40]. Именно этим объясняется возрастающий интерес онкологов к различным молекулярным маркерам, многие из которых по чувствительности превосходят все используемые в клинической практике методы выявления опухолей легкого и часто позволяют обнаружить трансформированные клетки задолго до появления клинических симптомов опухолевого роста. Наиболее эффективными маркерами ранней диагностики являются нарушения микросателлитных маркеров (в частности, микроделеции на коротком плече хромосомы 3) и гиперметилирование промоторов некоторых генов супрессоров опухолевого роста.
Нарушения микросателлитных маркеров.
Микросателлитные маркеры представляют собой многократно повторяющиеся последовательности, диспергированные по всему геному. Единицей повтора является мотив в 2-5 п. н. Для микросателлитных маркеров характерно два типа нарушений: микросателлитная нестабильность (Ml, microsatellite instability или RER+, replication error repair) и потеря гетерозиготности (LOH, loss of heterozygosity).
Микросателлитная нестабильность проявляется в виде возникновения абберантого аллеля микросателлитного маркера в результате делеции или амплификации одного или нескольких составляющих его повторов. Впервые феномен микросателлитной нестабильности был обнаружен в клетках наследственного неполипозного рака толстой кишки. Было показано, что микросателлитная нестабильность является следствием инактивации генов системы репарации неспаренных нуклеотидов (mismatch repair genes, преимущественно hMLH1 или hMSH2 в результате герминальных мутаций [41, 42]. Таким образом, на сегодняшний день считается, что появление микросателлитной нестабильности отражает дефицит системы репарации ДНК в клетке и свидетельствует о высокой вероятности возникновения трансформирующих мутаций по всему геному. В отличии от наследственного неполипозного рака толстой кишки, точечные мутации в генах системы репарации ДНК при РЛ не были обнаружены [43]. Однако была выявлена взаимосвязь между RER+ фенотипом и аллельными делециями в локусе гена hMLH1 Показано, что до 70% случаев НМРЛ могут иметь данное нарушение, хотя экспериментальные данные по этому вопросу противоречивы [44]. Кроме того, было показано, что в значительном проценте случаев РЛ (87%) наблюдается потеря экспрессии хотя бы одного из генов системы репарации ДНК [43].
Микросателлитная нестабильность регистрируется также в пренеопластическом и гистологически нормальном бронхиальном эпителии, полученном от пациентов с онкопато-логией легких и онкологически здоровых индивидуумов [45-48], и в ряде случаев может служить дополнительным маркером риска развития злокачественной опухоли.
Потеря гетерозиготности чаще всего является результатом аллельных делеций (потери одной из копий данного локуса). Данные нарушения являются, вероятно, наиболее частыми генетическими событиями, наблюдаемыми при многих видах онкопатологий, в том числе и при РЛ. Механизмы, вызывающие аллельные делеций, так же как и биологический смысл данного явления, на сегодняшний день изучены недостаточно. Предполагается, что потеря гетерозиготности приводит к инактивации антионкогенов в опухолевых клетках в результате того, что утрата одного аллеля дает возможность проявления фатальных рецессивных мутаций в оставшемся (теория Кнадсена). С целью идентификации специфических для данного заболевания генов-супрессоров проводится анализ большого числа опухолей. Чем выше процент делеций в данном локусе при данной патологии, тем вероятней нахождение в нем гена-супрессора. Частота LOH, превышающая 60% свидетельствует о присутствии в данном районе генов супрессоров, специфичных для данного заболевания. Действительно, в ряде подобных локусов были обнаружены такие классические гены-супрессоры как p16INK4A (9р21), Rb (13q) и р53 (17р13) [49-52].
Наиболее частым и ранним событием при НМРЛ являются делеции различных локусов хромосом Зр, 5q21, 9р21 и 17р13, каждый из которых теряется в 30-80% случаев данной онкопатологии [53, 54]. Кроме того, LOH в этих локусах обнаружена и в пренеопластических поражениях легких, хотя и с меньшей частотой, чем в инвазивных карциномах. Некоторые из них были выявлены в бронхиальном эпителии онкологически здоровых индивидуумов. Вистуба с соавторами, использовав 15 микросателлитных маркеров, обнаружили микросателлитную нестабильность в образцах бронхиального эпителия, полученных от 86% здоровых курильщиков, причем у 24% из них LOH была обнаружена во всех исследованных образцах [47]. Мао с соавторами выявили LOH трех микросателлитных маркеров, локализованных на Зр14, 9р21 и 17р13 в бронхиальном эпителии, полученном от 75%, 57% и 18% курильщиков, не имеющих онкопатологии легких, соответственно [46]. Предполагается, что индукторами потери гетерозиготности в специфических хромосомных локусах являются мутагенные компоненты табачного дыма. В пользу этого предположения свидетельствует тот факт, что подобные нарушения наблюдаются крайне редко в биопсийных образцах эпителия бронхов, полученных от некурящих индивидуумов без онкопатологии легких [46, 47]. Молекулярные нарушения, характерные для немелкоклеточного рака легкого, обнаружены в бронхиальном эпителии 72.2% курящих и 57.1% некурящих ликвидаторов последствий аварии на ЧАЭС без онкопатологии, а также 57.1% курильщиков, не имевших контакта с радиацией, но ни у одного из 23 индивидуумов, не подвергавшихся канцерогенной экспозиции. Экспозиция канцерогенами табачного дыма и длительное присутствие радиоактивной пыли в легких коррелируют с появлением аллельных делеции локусов Зр12, Зр14.2, Зр21, Зр22-24, Зр25, 9р21 и 17р13, а также мутациями гена K-ras и гиперметилирова-нием промотора гена p16INK4A[55].
Наиболее частым и показательным признаком наличия трансформированных клеток эпителия бронхов являются делеции короткого плеча хромосомы 3.
Делеции на Зр наблюдаются в 100% случаев МРЛ и 60-65% случаев НМРЛ [56]. О значении делеции в этой области генома на ранних стадиях канцерогенеза свидетельствуют данные об аномалиях Зр, выявленных в клетках из зон пренеопластических поражений легких, таких как гиперплазия и дисплазия, а также в карциномах in situ [57-59]. Другими словами, потеря генетического материала на коротком плече хромосомы 3 может быть фиксирована до проявления клинически диагносцируемого рака легкого [56](рис1).
Таблица 2
Гены короткого плеча хромосомы 3.
|
Локус |
Ген |
Функция |
Нарушения при РЛ |
|
Зр12 |
hMLH1 |
Система репарации генома |
Частые аллельные делеции [41, 44]. |
|
Зр14 |
HRCAI |
|
[63] |
|
Зр14.2 |
PTPRG |
Рецептор протеинтирозин фосфатазы (гамма) |
[54] |
|
Зр14.2 |
FHIT |
Динуклеозидфосфат гидролаза |
Снижение экспрессии, гл. обр. за счет метилирования промотора [52, 53]. |
|
Зр21-р25 |
erbA Beta |
Рецептор тиреоидных гормонов |
[64] |
|
Зр21 |
PTPG |
Протеин тирозин фосфатаза (гамма) |
[65] |
|
Зр21 |
D8 |
Неизвестна, экспрессия низкая |
[см. 66] |
|
Зр21 |
Alpha ric |
Субъединица интегрина |
Снижение клеточной адгезии [63] |
|
Зр21 |
TACA |
Участие в транслокации |
[56] |
|
Зр21.1 |
ACYI |
Аминоацилаза |
[67] |
|
Зр21.3 |
Unph |
Убиквитиновая протеаза |
[67, 68] |
|
Зр21.3 |
BAP1 |
Убиквитиновая карбоксильная гидролаза, регуляция BRCA1 |
Снижение экспрессии [69] |
|
Зр21.3 |
Beta-catenin (CTNNB1) |
Участие в клеточной адгезии |
Делеции, мутации редки. [70] |
|
Зр21.3 |
RASSF1A |
Член семейства газ, потенциальный ген-супрессор |
Метилирование промотора, аллельные делеции [71, 72]. |
|
Зр21.3 |
FUS1 |
Потенциальный ген-супрессор опухолевого роста |
Делеции и потеря экспрессии отменяют арест клеток в фазе G1 [73] |
|
Зр21.3 |
SEMA3B |
|
Делеции и/или гиперметилирование промотора [74, 75] |
|
Зр22 |
HVRI |
Вазоактивный рецептор |
[63] |
|
Зр24 |
RARB |
Рецептор ретиноевой кислоты |
Метилирование промотора [76-78] |
|
Зр25 |
VHL |
Ген-супрессор опухолевого роста von Hippel-Lindau |
Делеции [53] |
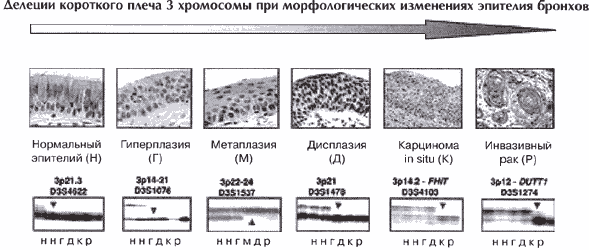
Эти результаты весьма убедительно свидетельствуют о локализации на коротком плече 3 хромосомы генов, вовлеченных в индукцию рака легкого на ранних стадиях. Активные поиски специфичного гена, утрата (либо повреждение) которого приводит к возникновению рака легкого позволили с большой достоверностью идентифицировать участки, специфично утрачиваемые при раке легкого - Зр14, Зр21 и Зр24-25 [52, 60-62]. Делеции именно этих участков наиболее часто регистрируются и при различных пренеопластических поражениях легочной ткани. Какой либо из этих фрагментов поврежден в 57% гиперплазий, в 53% дисплазий и в 100% карцином in situ [56, 58].
В настоящее время на коротком плече хромосомы 3 идентифицировано более 45 генов, 25 из которых локализовано в области Зр21.3. Данная область размером 630-kb является одним из самых генонасыщенных участков генома и интенсивно исследуется [63]. Существует даже Международный Консорциум по исследованию генов-супрессоров опухолевого роста короткого плеча хромосомы 3, возглавляемый одним из самых известных специалистов по изучению молекулярно-генетических нарушений при раке легкого профессором Минной (The International Lung Cancer Chromosome Зр21.3 Tumor Suppressor Gene Consortium). В таблице 2 представлен далеко не полный перечень потенциальных кандидатов в гены-супрессоры, для которых показаны структурные и/или функциональные нарушения при РЛ. Супрессивное антиопухолевое действие некоторых известных генов, локализованных на хромосоме 3 еще ждет подтверждения.
Метилирование промоторов генов-супрессоров.
Метилирование цитозина в составе Ср островков генных промоторов является механизмом эпигенетической регуляции, приводящей к прекращению экспрессии модифицированного гена. В настоящее вpeмя существует несколько гипотез, объясняющих каким образом Метилирование может влиять на уровень экспрессии того или иного гена:
1) Метилирование цитозина, входящего состав участка промотора может уменьшать сродство к нему специфических транскрипционных факторов (например, таких, как MYC, E2F или NFkB, сайты связывания которых содержат CpG островки).
2) Возможно непосредственное связывание репрессоров с метилированными CpG островками (в настоящее время известно о существовании как минимум двух таких белков: МеСР1 и МеСР2).
3) Метилирование ДНК может изменять структуру хроматина, переводя его в неактивную конформацию [24].
Недавние исследования показали, что метилирование CpG островков промоторов ряда классических и потенциальных генов-супрессоров (p16INK4A), MGMT, RAR DAPK, p19ARF, FHIT и глутатион трансфераза P1(GSTP1), а также генов-модуляторов опухолевого роста (TIMP3 или кадхерин является ранним и частым событием при НМРЛ [52, 67, 77-81].
Ген p16INK4A. Белок p16INK4A (9p21) является ключевым членом семейства ингибиторов циклинзависимых киназ lnk4, являющихся негативными регуляторами сигнального пути, отвечающего за реализацию программы клеточного цикла, p16INK4A обладает достаточно узкой специфичностью: связывая циклинзависимые киназы Cdk4 и Cdk6 (но не другие Cdk), он препятствует образованию их комплексов с циклинами D, регулируя таким образом прохождение фазы G1 и вхождение в S фазу клеточного цикла [82, 83].
Метилирование промотора гена p16INK4Aнаблюдается в 25-60% случаев НМРЛ [81, 82, 85, 86], а также в 17% гиперплазий, 24% метаплазий и в 50% дисплазий эпителия бронхов, выявленных у больных НМРЛ [84]. Кроме того, данное нарушение было обнаружено в 83% образцов бронхеоальвеолярного лаважа [85], 50-100% образцов мокроты [86] и 33% образцов сыворотки крови [87], полученных от больных НМРЛ в опухолевой ткани которых было выявлено данное нарушение.
Данные группы исследователей из университета Джона Хопкинса, руководимой Sidransky и Ahrendt, свидетельствуют о разных механизмах инактивации гена p16INK4A у больных НМРЛ с различным статусом курения. Аллельные делеции и мутации данного гена обнаруживаются только у курильщиков, в то время как у некурящих пациентов ген инактивируется только посредством гиперметилирования промотора [88].
Ген MGMT. MGMT ((O6 метилгуанин-ДНК-метилтрансфераза) является ферментом, принимающим участие в репарации ДНК, защищая клетки от канцерогенного действия алкилирующих агентов. Метилирование промотора гена MGMT наблюдается в 21-27% случаев НМРЛ [81, 86]. Данное нарушение было также выявлено в 66% образцов мокроты и в таком же проценте образцов сыворотки крови, полученных от больных НМРЛ в опухолевой ткани которых было идентифицированы метилированные аллели данного гена [86, 87].
Одновременный анализ статуса метилирования промоторов трех разных генов (p16INK4A, MGMT и DAPK) позволил обнаружить абберантное Метилирование промоторов хотя бы одного из этих генов в 68% случаев НМРЛ и в плазме
крови 73% больных, опухоли которых несли данное нарушение [87]. Однако Метилирование промоторов вышеупомянутых генов не является атрибутом опухолевой трансформации и обнаруживается также в образцах мокроты, БАЛ биопсийных образцах курильщиков без онкопатологии легких, хотя и с меньшей частотой. Кроме того, Палмисано с соавторами анализируя статус метилирования промоторов p16INK4A и MGMT обнаружили метилированные аллели по крайней мере одного из этих генов в 100% случаев (11/11) больных НМРЛ задолго до постановки клинического диагноза (от 5 до 35 месяцев) [86].
Эти данные свидетельствуют о том, что обнаружение метилированных аллелей данных генов, возможно, является индикатором начальных этапов возникновения онкопатологии легких у соответствующего индивидуума. Кроме того, в настоящее время разработаны простые и высокочувствительные методы детекции абберантного метилирования промоторов ряда генов, что делает возможность детекции данных нарушений особенно перспективной для использования в клинической практике.
Мутации онкогенов и генов-супрессоров.
Мутации генов семейства Ras. В геноме человека выявлены 3 представителя этого генного семейства: Kras (локализация в геноме 12p12-pter), Hras (11p15.5), Nras (1cen-p11). Все они кодируют высокогомологичные белки с молекулярной массой 21 кДа (p21ras), которые функционально относятся к G-белкам. Связывая ГТФ p21ras переходит в активную конформацию, которая позволяет осуществлять передача сигнала от ростовых факторов к генам, ответственным за клеточную пролиферацию. [2, 89, 90].
При РЛ 90% мутаций детектируемых в данном семействе генов приходится на долю Kras. 85% из них затрагивают кодон 12, в то время как остальные происходят в 13 и 61 кодонах данного гена [91]. Замещение глицина 12 или глутамина 61 различными вариантами аминокислотных остатков ослабляют ГТФазную активность p21ras, в результате чего создается эффект постоянного проведения внутриклеточного сигнала. Замена глицина 13 приводит к увеличению скорости обмена нуклеотидов в комплексе р21-ГТФ/ГДФ. Поскольку в клетке концентрация ГТФ выше, чем ГДФ, подобная мутация также придает белку трансформирующие свойства [90]. Кроме того, активированный Kras снижает экспрессию рецепторов а1b1 коллагена/ламинина и а5b1 фибронектина, участвующих в поддержании нетрансформированного фенотипа клеток. Одновременно, активированный Kras усиливает продукцию a3b1 ламинин/коллаген/фибронектинового и а5b1 витронектинового рецепторов клеточной поверхности, определяющих метастазирование опухоли [92].
Мутации в генах семейства ras наблюдаются преимущественно в аденокарциномах легких (в 20-57% случаев), возникая, по-видимому, уже на ранних стадиях опухолевого процесса [93-98]. Клетки плоскоклеточного и крупноклеточного рака легкого обнаруживают существенно меньшую частоту мутаций (в 21% и 14% случаев соответственно) [99]. Мутации в гене Kras были выявлены и в атипичной аденоматозной гиперплазии, которая рассматривается некоторыми авторами как пренеопластическое поражение, предшествующее аденокарциноме легких [100].
Наиболее вероятными индукторами мутаций генов семейства ras, по видимому, являются мутагенные компоненты табачного дыма. Так, большинство (70%) мутаций обнаруживаемых в гене Kras при РЛ, представляют собой G-T трансверсии, приводящие к замене глицина (GGT) на цистеин (TGT) или валин (GTT). Было показано, что подобные мутации, часто встречающиеся в гене р53 (обсуждается ниже), являются результатом повреждения ДНК полициклическими углеводородами и нитрозаминами, содержащимися в табачном дыме [101]. В пользу данного предположения свидетельствует и взаимосвязь между наличием мутаций в гене Kras и привычкой к курению табака [102].
Показано, что мутации в 12 кодоне гена Kras часто выявляются также и в образцах гистологически нормальной легочной ткани и мокроты, полученных от пациентов с онкологическими заболеваниями легких [103, 104].
С точки зрения ранней диагностики особенно интересно, что такие изменения в ДНК из мокроты могут обнаруживаться до проявления клинических симптомов заболевания [105].
Создание современных методик детекции мутаций в гене Kras было в значительной степени облегчено тем фактом, что подавляющее большинство их локализуется в 12 кодоне данного гена. Использование этих методов позволяет выявлять 1 мутантный аллель данного гена в присутствии 10000 аллелей дикого типа (чувствительность метода 10-4). Это делает возможным выявление мутаций в гене Kras в образцах бронхо-альвеолярного лаважа (БАЛ), мокроты и браш-биопсиях, полученных от подавляющего большинства больных [88-100%], в опухолевой ткани которых было выявлено данное нарушение [106-108].
р53 представляет собой полифункциональный белок, основная роль которого заключается в обеспечении экстренного удаления поврежденных и потенциально опасных для организма клеток (подробнее см. обзоры 1,109). Ген р53 транскрибируется и транслируется в клетке на постоянном уровне, однако сам белок быстро подвергается убиквитин-зависимой деградации в протеосомах [110, 111]. Воздействие на клетки генотоксических факторов (таких как ионизирующее излучение, УФ или некоторые химические агенты), гипоксии, теплового шока, уменьшение пула нуклеозидтрифосфатов, а также экспрессия некоторых клеточных и вирусных онкогенов вызывает активацию р53. Активация осуществляется, главным образом, на пострансляционном уровне, за счет замедления деградации и конформационной перестройки молекулы белка, приводящей к повышению ее функциональной активности [112-114], Индукция р53 приводит к задержке клеточного цикла или апоптозу. р53 способен активировать транскрипцию ряда генов, продукты которых способствуют подавлению клеточного цикла (p21WAF1, GADD45, 14-3-3-sigman В99) [115-117], или участвуют в апоптозе (ВАХ, АР01, KILLER/DR5, IGF-BP3, группа PIG и р85) [118-122], а также генов, кодирующих ингибиторы ангиогенеза и другие секретируемые факторы (Tsp1, BAI1, CD-AiF, Betta-ингибин и некоторые другие) [123-125]. Кроме того, p53 способен репрессировать транскрипцию большого числа генов, среди которых BCL2 и RELA, продукты которых играют роль ингибиторов апоптоза [126, 127].
Повреждения гена р53 имеют важное значение при развитии целого ряда опухолей, в том числе РЛ. Так, 50-80% больных РЛ несут мутации данного гена [101]. Изменения в структуре р53 обнаружены на разных стадиях РЛ, а также в пренеопластических поражениях легких [128]. Мутации в гене р53, обнаруживаемые при РЛ, включают точковые замены (нонсенс и миссенс мутации), делеции и нарушения сплайсинга. Наиболее частым типом нуклеотидных замен, наблюдаемых при РЛ, являются G-T транзиции, в отличие от других опухолей человека, где чаще встречаются G-A замены [129]. Такой тип замен ассоциирован со специфическим мутагеном - бенз(А)пиреном, содержащимся в табачном дыме, тогда как другие агенты вызывают другие варианты точечных мутаций [101]. Кроме того, была обнаружена достоверная корреляция между частотой мутаций и сроками и интенсивностью курения у исследованных пациентов [22, 99]. О значении взаимосвязи факторов окружающей среды с генетическими нарушениями в гене р53 свидетельствуют и исследования, проводимые в определенных этнических группах [130].
Мутации в гене р53 были также обнаружены в 39% образцов БАЛ [85], в 50% образцов мокроты [86] и в 33% образцов сыворотки крови [87] больных НМРЛ, в опухолевой ткани которых было выявлено данное нарушение.
Экспрессия генов.
Ген hnRNP. В 1988 году Токман с соавторами показали, что для ранней диагностики РЛ могут быть использованы опухолеспецифические моноклональные антитела 703D4 [131]. Анализ архивных образцов мокроты с помощью данных антител позволил авторам выявить специфический сигнал в препаратах, полученных в среднем за 2 года до постановки клинического диагноза. В дальнейшем было показано, что антитела 703D4 специфически узнают белок hnRNP (heterogeneous nuclear ribonuclear protein), который принимает участие в регуляции генной экспрессии на постранскрипционном уровне, регулируя кэпирование, сплайсинг, полиаденилирование и цитоплазматический транспорт мРНК [132, 133]. Показано, что повышенный уровень экспрессии данного белка наблюдается на определенном этапе развития легких млекопитающих [134]. Позднее ряд других авторов, исследовав образцы мокроты, полученные от индивидуумов, у которых впоследствии был диагносцирован РЛ, подтвердил возможность использования антител к hnRNP для ранней диагностики данного заболевания [135, 136]. Fielding с соавторами показали, что анализ образцов БАЛ с помощью антител к hnRNP обеспечивает высокую чувствительность и специфичность детекции РЛ (96% и 82% соответственно) [137].
Некоторые кератины. Кератины представляют собой фибриллярные белки, относящиеся к группе промежуточных филаментов [138]. Было показано, что кератины 5, 8, 18 и 19 экспрессируются на высоком уровне как в клетках нормального эпителия легких, так и при РЛ. Моноклональные антитела, специфически узнающие определенные кератины или амплификация фрагментов мРНК данных генов с помощью "обратной" ПЦР (RT-PCR) могут быть использованы для детекции опухолевых клеток в лимфатических узлах, клеткам которых не свойственна экспрессия этих генов [139]. Пек с соавторами постулировали возможность использования оценки уровня экспрессии гена кератина 19 для успешной детекции опухолевых клеток, циркулирующих в периферической крови больных РЛ [140]. В то же время некоторыми другими авторами экспрессия данного кератина (а также кератинов 8 и 18) была обнаружена и в 100% образцов крови, полученных от здоровых доноров [141-143], что делает дискуссионным возможность использования оценки уровня экспрессии кератинов для ранней диагностики РЛ.
Трудности и перспективы ранней клинической диагностики молекулярных нарушений.
Таким образом, не вызывает сомнений, что детекция микросателлитных нарушений может быть использована для ранней диагностики РЛ. Однако для этого должны быть решены две принципиальные проблемы.
Необходимо: 1) совершенствование методик обогащения клинических образцов клетками, которые могут содержать генетические нарушения (путем, например, элиминации неэпителиальных клеток); 2) повышение специфичности используемого спектра маркеров. Существенным недостатком методов детекции микросателлитных нарушений, ограничивающим возможность их использования для ранней диагностики РЛ, является их низкая чувствительность. Данные нарушения могут быть обнаружены только в том случае, если значительная часть клеток в анализируемом образце (не менее 50% для выявления специфических делеций и не менее 5% для выявления микросателлитной нестабильности) имеет соответствующую абберацию. Таким образом, наиболее подходящим материалом для анализа микросателлитных нарушений является ДНК, выделенная из биопсийного или операционного материала с применением микродиссекции, которая делает возможным получение образца опухолевых клеток, свободных от клеток стромы, лимфоцитов или прилегающего нормального эпителия.
Недавно было показано, что в ряде случаев микросателлитные нарушения также могут быть обнаружены в браш-биопсиях, образцах БАЛ лаважа, мокроты и в сыворотке крови. Так, микросателлитная нестабильность была обнаружена в образцах мокроты, полученных от трех из пяти больных в опухолях которых был выявлен RER+ фенотип [45]. Пауэлл с соавторами проанализировав браш-биопсии, полученных от 38 больных РЛ с использованием 22 микросателлитных маркеров, выявили специфические делеции в 79% исследованных случаев, в то время как цитологическое исследование выявило положительный результат только в 37% случаев. Теми же исследователями подобные абберации были обнаружены в биопсийных образцах, полученных от 59% индивидуумов не имеющих онкопатологии легких. Авторам удалось существенно повысить специфичность метода путем введения индекса специфических делеций (LOH score), позволяющего учитывать как количество микросателлитных маркеров, демонстрирующих потерю гетерозиготности, так и процент клеток в анализируемом образце, в которых выявляется данное нарушение. Данный индекс был выше 10 в биопсийных образцах, полученных от 58% больных РЛ, но не достиг данного значения ни в одном из биоптатов, полученных от здоровых доноров [144], Исследование нарушений микросателлитных маркеров в образцах БАЛ принесло противоречивые результаты. Так Ахрендт с соавторами [85] использовав 15 микросателлитных маркеров, обнаружили микросателлитную нестабильность только в 14% образцов БАЛ, полученного от больных РЛ, в опухолях которых было выявлено сходное нарушение. С другой стороны, Лилоглоу с соавторами обнаружили нарушения микросателлитных маркеров в образцах лаважа, полученных от 87% больных РЛ и 76.5% пациентов без онкопатологии [145]. Проанализировав частоту нарушений каждого из маркеров в различных группах образцов, авторы предложили набор маркеров (D3S1289, D3S1300, D13S171 и D17S2179E), использование которых позволяет достигнуть высокой чувствительности и специфичности детекции РЛ (73.9% и 76.5%, соответственно) [146]. Микросателлитные альтерации были обнаружены в сыворотке крови 61% больных НМРЛ, в опухолевой ткани которых было выявлено данное нарушение, но ни в одном случае у 14 контрольных пациентов [147].
Для ранней диагностики важным является наблюдение, что молекулярные нарушения в клетках бронхиального эпителия индивидуумов, подвергнувшихся канцерогенной экспозиции, обнаруживаются раньше гистологических изменений. Повышенное количество молекулярных изменений (преимущественно гиперметилирование промотора гена p16INK4A делеции локусов Зр14.2, Зр25 и 17р13а также мутации гена K-ras} было зарегистрировано в дисплазиях и фокусах нормального эпителия или гиперплазиях/метаплазиях, впоследствии превратившихся в дисплазии [55].
Перспективы определения мутаций гена p53 в целях ранней диагностики не столь очевидны. Низкий процент выявления данных нарушений в образцах биологического материала объясняется тем, что детекция мутаций в гене р53 сопряжена со значительными трудностями, Проблема заключается в том, что мутации могут затрагивать почти любой кодон (хотя и с разной вероятностью) в пределах 4-го-10-го экзонов этого гена и не концентрируются в одном или нескольких определенных точках, как в случае, например, генов семейства ras. Метод прямого сиквенирования, примененный в работах, упомянутых выше, малопригоден для использования в клинической практике в силу высокой стоимости, технологических трудностей и низкой чувствительности. Другим, широко используемым способом детекции мутаций гена р53, является метод оценки подвижности амплифицированного фрагмента ДНК в неденатурирующем ПААГ (метод PCR-SSCP) [148]. Однако, данный метод дает возможность обнаруживать только 70-90% нуклеотидных замен. Кроме того, этот метод имеет низкую чувствительность (5х10-2 [139]. Тем не менее, используя упомянутые выше методы, Мао с соавторами удалось идентифицировали специфические мутации в гене р53 в образцах мокроты у 8 индивидов за 1-13 месяцев до постановки у них клинического диагноза РЛ [106].
В настоящее время также разработан метод детекции мутаций в нескольких "горячих" точках гена р53 (кодоны 157, 175, 245, 248, 249 и 273), основанный на "обогащающей" ПЦР (EPCR). Данный метод обладает высокой чувствительностью (10-4) и позволяет выявлять мутации р53 в 80% образцов мокроты и браш-биопсий от больных НМРЛ, в опухолевой ткани которых было выявлено данное нарушение [108]. Однако, существенным ограничением методов детекции мутаций р53, основанных на EPCR, является то, что они выявляют лишь незначительный процент возможных нуклеотидных замен в пределах данного гена, т. к. мутации в кодонах 175, 245, 248, 249 и 273 составляют менее 25% от общего количества нуклеотидных замен, наблюдаемых при РЛ [149]. Кроме того, использование высокочувствительных методов показало, что мутации в гене р53 не являются исключительным атрибутом опухолевой ткани и могут быть обнаружены не только в образцах гистологически нормальной легочной ткани, полученных от пациентов с онкологическими заболеваниями легких, но также в браш-биопсиях и образцах мокроты, от индивидуумов, не имеющих видимых признаков онкопатологии легких [149, 150].
Помимо генетических методов анализа мутаций р53, широко используется иммуногистохимический анализ состояния данного белка в клетке. В большинстве случаев наличие специфического окрашивания свидетельствует о присутствии мутаций в данном гене. Этот факт объясняется тем, что точечные мутации в гене р53 обычно изменяют конформацию данного белка, увеличивая время его полужизни, что делает возможным его детекцию с помощью специфических антител. Важным преимуществом иммуногистохимических методов детекции мутаций р53 является их техническая простота. К недостаткам же можно отнести значительный процент "ложноотрицательных" (не все мутации р53 увеличивают время полужизни данного белка в клетке) [151] и "ложноположительных" (в ряде случаев возможность иммуногистохимической детекции р53 не обусловлена мутацией) [152] результатов. Возможно, именно этими причинами объясняется частичное несовпадение результатов детекции мутаций р53, полученных генетическими и иммуногистохимическими методами. Тем не менее, имеются доказательства того, что иммуногистохимический анализ р53 может быть полезен для выявления нарушений данного гена на ранних стадиях РЛ, а также в пренеопластических поражениях легких [153, 154].
Таким образом, анализ современных данных о ряде генетических нарушений, определяемых на ранних этапах малигнизации клеток, неоспоримо свидетельствует в пользу необходимости их определения в группах риска развития онкопатологии легких и, следовательно, совершенствования методов детекции таких нарушений.
Молекулярно-генетические изменения, используемые для прогнозирования течения рака легкого.
В настоящее время не подлежит сомнению тот факт, что гистологическая форма опухоли и стадия заболевания являются основными прогностическими критериями течения РЛ. Однако знание клинико-патологических параметров не всегда позволяет сделать точный прогноз. Так например, 15-20% больных с I стадией НМРЛ, имеющих в целом благоприятный прогноз, умирают в результате прогрессии заболевания, несмотря на использование современных методов лечения. Выявление пациентов, имеющих плохой прогноз течения данного заболевания представляется крайне важным, так как своевременная регистрация признаков рецидивирования и метастазирования и применение более агрессивных методов лечения способны улучшить выживаемость таких пациентов [39]. В настоящее время показано, что использование ряда биологических маркеров может существенно повысить точность индивидуального прогнозирования течения РЛ.
Аллельный полиморфизм протоонкогенов.
Аллельный полиморфизм в локусе протоонкогена Hras1. Полиморфизм онкогена Hras1 уже упоминался выше, в связи с ассоциацией между наличием "редких" аллелей и риском возникновения РЛ. При исследовании частоты распределения "общих" аллелей Hras1 у онкологических больных были получены данные, свидетельствующие о связи между наличием в геноме аллеля а4 с повышенным риском быстрого прогрессирования НМРЛ [15, 155, 156].
Было показано, что в группах больных с метастазами в регионарные лимфоузлы наблюдается достоверное увеличение частоты встречаемости аллеля а4 гена Hras1 (15.6% в группе плоскоклеточных раков и 21.9% в группе аденокарцином против 6.6% и 8.3% у аналогичных больных без метастазов). В группе больных низкодифференцированным НМРЛ также зарегистрировано 2-кратное увеличение содержания аллеля а4 по сравнению с пациентами, имеющими высоко или умеренно дифференцированные опухоли легких [156].
Аллельный полиморфизм в локусе протоонкогена L-myc. Другим онкогеном, наследственный полиморфизм которого имеет значение при прогрессии рака легкого является ген L-myc, представитель семейства ядерных генов - факторов транскрипции. Существование двух аллелей гена (L-long и S-short) обусловлено точечной герминальной мутацией, и все индивидуумы имеют три вида генотипа по гену L-myc -LL, LS и SS. Было обнаружено, что при НМРЛ у японцев, англичан и русских наличие S аллели в генотипе коррелирует с быстрой прогрессией и процессами диссеминации опухоли [156-158]. Если данный показатель сочетается хотя бы еще с одним фактором неблагоприятного прогноза, например, наличием а4 аллели Hras1 или полиморфного варианта Pro/Pro гена р53, двухлетняя послеоперационная выживаемость больных в этих группах падает до нулевых значений, вне зависимости от стадии заболевания на момент хирургического вмешательства [156, 159].
Сходные работы, проведенные на американской и норвежской популяциях пациентов не дали очевидных результатов, однако в этих исследованиях не проводилось ни анализа гистологических типов РЛ, ни определения сочетанного влияния различных неблагоприятных признаков [160-162].
Мутации онкогенов и генов-супрессоров.
K-ras. В настоящее время имеются многочисленные исследования, указывающие на более низкую выживаемость больных РЛ, имеющих мутации в гене K-ras по сравнению с пациентами, опухоли которых не имеют данного нарушения [163, 164]. В то же время имеются работы, в которых подобная ассоциация не была установлена [165, 166]. Эти противоречивые результаты, видимо, могут быть объяснены различными клинико-патологическими и демографическими характеристиками выборок индивидуумов, исследованных различными авторами. Так, например, было показано, что частота мутаций в гене K-ras зависит от гистологического типа РЛ, пола пациентов, а так же наличия и характера канцерогенной экспозиции [164, 167]. Для уточнения прогностического значения мутаций в гене K-ras необходимы дополнительные исследования, учитывающие все эти параметры.
р53. Данные об влиянии мутаций в гене р53 на характер течения НМРЛ противоречивы. Используя генетические методы определения мутаций р53, две группы авторов выявили взаимосвязь между наличием нарушений в данном гене и низкой выживаемостью пациентов [168, 169]. В то же время другие исследования, в которых использовались сходные методы, не показали подобной закономерности [129, 170]. В пяти работах ассоциация мутаций в гене р53 с пониженной выживаемостью больных НМРЛ была выявлена иммуногистохимически [170-174]. Однако наличие иммунологического сигнала не коррелировало с выживаемостью в двух других работах [152, 175]. Существуют указания на ассоциацию между наличием мутаций в гене р53 и более длительной постоперационной выживаемостью больных НМРЛ [176-177]. Кроме того, в одном из вышеупомянутых исследований [170], мутации р53 оценивались с помощью как генетических, так и иммуногистохимических методов. Было показано, что наличие иммуно-гистохимического сигнала р53, коррелируют с низкой выживаемостью больных НМРЛ, в то время как наличие мутаций в данном гене не влияло на постоперационную выживаемость пациентов. Все те факторы, которые приводились в предыдущем разделе для объяснения противоречивых данных о влиянии мутаций в гене K-ras на выживаемость пациентов больных РЛ, по-видимому, справедливы и в случае гена р53. Кроме того, противоречивые результаты, полученные с помощью иммунохимических методов, могут объясняться использованием различных типов антител для детекции данного белка. Ряд исследователей использовали антитела, специфичные только к мутантному белку, в то время как другие - антитела, узнающие как мутантный белок, так и р53 дикого типа.
Нарушения микросателлитных маркеров.
В настоящее время все большее число исследователей указывают на ассоциацию специфических делеций в тех или иных хромосомных локусах с определенным прогнозом течения НМРЛ. Показано, что потеря гетерозиготности в хромосомных локусах 5q (зона локализации генов АРС/МСС) [178], 9р21 (ген p16INK4A) [179], 17q [180] коррелирует с низкой выживаемостью больных РЛ. Кроме того, было
обнаружено, что наличие делеций в локусах Зр14.2 (FHIT) и Зр21.3 (hMLH1) является неблагоприятным прогностическим фактором в случае аденокарциномы легкого, но не коррелирует с течением плоскоклеточного РЛ [181]. Существуют и противоположные данные, свидетельствующие о том, что делеции в вышеупомянутых районах не являются прогностическим фактором [182-184].
Кроме того, имеются немногочисленные экспериментальные работы, посвященные изучению микросателлитной нестабильности как фактора прогноза течения НМРЛ. Было показано, что больные, в опухолях которых выявлена микрокросателлитная нестабильность маркеров, локализованных в хромосомных локусах 1р36, 2р, Зр и 10q24 имеют более низкую выживаемость чем пациенты не имеющие данных нарушений [184-186].
Экспрессия генов.
Представители семейства myc. Ядерные белки семейства myc (основные представители C-MYC, L- MYC и N- MYC) играют важную роль в дифференцировке, росте и апоптозе клеток. Повышенная экспрессия генов myc в клетках РЛ обнаружена во многих исследованиях [187, 188]. В ряде случаев увеличение продукции белка С-MYC обусловлено амплификацией данного гена в опухолевых клетках. Например в 50% случаев различных типов НМРЛ наблюдается суперэкспрессия белка а в 10% - амплификация протоонкогена c-myc [188]. Было установлено, что повышение экспрессии c-myc и амплификация L-myc ассоциируются с агрессивным поведением и быстрой диссеминацией опухоли [189] а также низкими показателями трехлетней выживаемости больных РЛ.
Антиген Ki-67. Подобно генам семейства myc, антиген Ki-67 специфически экспрессируется в ядрах делящихся клеток и является маркером пролиферации. Несколько исследований выявили взаимосвязь между высоким уровнем экспрессии данного белка и низкой выживаемостью больных НМРЛ [171, 190-192]. Однако в одном из вышеупомянутых исследований данная ассоциация была выявлена при анализе двухлетней, но не пятилетней выживаемости пациентов [190], а в другом, прогностическое значение экспрессии Ki-67 обнаруживалось только при использовании однофакторного, но не мультифакторного статистического анализа [171].
Ядерный антиген пролиферирующих клеток (PCNA, Proliferating Cell Nuclear Antigen) представляет собой фактор процессивности ДНК-полимеразы а. Экспрессия данного белка возрастает в конце фазы G1, достигает максимума в S-фазе, уменьшается в фазе G2 и полностью отсутствует в течение митоза [193]. Существуют данные об ассоциации высокой экспрессии данного гена с низкой пятилетней выживаемостью пациентов [194-196] или с ранним метастазированием [197]. В то же время в одной из работ прогностическое значение экспрессии PCNA обнаруживалось только при использовании однофакторного, но не мультифакторного статистического анализа [174]. Видимо, прогностическое значение уровня экспрессии данного белка, а также белков семейства МУС и Ki-67 определяется тем, что указывает на активно пролиферирующие опухоли, которые имеют тенденцию к быстрому росту и прогрессии.
Гены семейства Bcl-2. Способность избегать программированной смерти в ответ на апоптотические стимулы (например повреждение клеточной ДНК) является важной чертой опухолевых клеток. Ключевыми участниками апоптотического пути являются белки, относящиеся к семейству Bcl. Проведенные исследования показывают, что нарушение уровня экспрессии белков данного семейства могут играть важную роль в патогенезе РЛ. В этом отношении лучше всего изучен протоонкоген bcl-2, продукт которого обладает антиапоптотической активностью [24]. Использование иммуногистохимических методов позволило выявить экспрессию данного белка в 75-95% случаев мелкоклеточного РЛ [198-200] и в 10-35% НМРЛ [198, 201]. Было показано, что повышенный уровень экспрессии Bcl-2 коррелирует с высокой выживаемостью больных как МРЛ, так и НМРЛ [200-204].
HER-2/neu/c-erbB-2. Продукт протоонкогена HER-2/neu/c-erbB-2 обладает тирозинкиназной активностью и структурно гомологичен другому представителю семейства - рецептору эпидермального фактора роста (EGFR) или с-erbB [205, 206], Высокий уровень экспрессии данного белка был обнаружен во многих клеточных культурах НМРЛ, особенно аденокарцином [207, 208]. В опухолях легких, как и в случае аденокарцином молочной железы и яичников, повышенная экспрессия с-егЬВ-2 является фактором плохого прогноза течения болезни [207, 209-211].
Кроме того, в настоящее время имеются многочисленные данные о том, что одновременная оценка уровня экспрессии семейства МУС, Ki-67, PCNA, Bcl-2, HER-2 а также ряда других белков (включая p21ras, циклины Е и G1, р53, С-raf-1) может существенно повысить точность прогнозирования течения НМРЛ [212-215].
VEGF. Важным условием формирования первичной опухоли и метастазов является неоангиогенез - формирование дополнительной капиллярной сети, обеспечивающей рост опухолевого узла. Одним из наиболее важных индукторов неоангиогенеза являются фактор роста эпителия сосудов -белок VEGF. Транскрипция VEGF находится под негативным контролем р53 и существенно повышена в опухолях, имеющих мутации данного гена [216]. В ряде исследований было показано, что повышенный уровень экспрессии VEGF коррелирует с высокой плотностью капиллярной сети опухолевого узла, поздними стадиями заболевания, поражением регионарных лимфатических узлов и, как следствие этого, с низкой постоперационной выживаемостью больных НМРЛ [217-221]. В то же время существуют противоположные данные, свидетельствующие об отсутствии взаимосвязи между уровнем экспрессии VEGF и выживаемостью пациентов с НМРЛ [222].
Некоторые кератины. Использование антител, специфичных к определенному спектру кератинов, может существенно повысить точность определения степени распространения опухоли в организме. Чен с соавторами, проанализировав с помощью иммуногистохимических методов 588 лимфатических узлов, полученных от 60 больных НМРЛ, установили, что 102 из них содержали микрометастазы, которые не могли быть выявлены с помощью стандартного окрашивания гематоксилином и эозином. При этом средняя выживаемость у больных НМРЛ с микрометастазами была ниже, чем у пациентов без таковых (5,4 и 6,7 лет, соответственно) [223]. Позднее Паслик с соавторами показали, что использование иммуногистохимических методов позволяет выявить микрометастазы у 15.7% больных РЛ, первоначально диагносцированных как имеющие стадию No. Так же, как и в предыдущей работе, наличие микрометастазов в лимфоузлах коррелировало с пониженной выживаемостью пациентов [224]. Наличие микрометастазов в костном мозге онкологических больных также является фактором неблагоприятного прогноза течения заболевания, а использование антител, специфичных к определенному спектру кератинов, может способствовать выявлению опухолевых клеток в костном мозге больных РЛ [225, 226].
Заключение.
Несмотря на постоянную модернизацию методов диагностики, большинство пациентов на момент постановки диагноза имеют неоперабельную форму заболевания. В настоящее время предпринимаются постоянные попытки, направленные на улучшение выживаемости больных РЛ. Помимо совершенствования непосредственно хирургических и терапевтических методов лечения они также сосредоточены на формировании групп канцерогенного риска, разработке новых методов ранней диагностики и прогнозирования течения данного заболевания. В недалеком будущем широкое использование молекулярно-генетических тестов в клинической практике может расширить возможности диагностики онкопатологии легких, а также способствовать разработке более точных прогностических критериев, что позволяет надеяться на существенное улучшение результатов лечения этого грозного заболевания. Это может значительно повысить эффективность медицинской помощи и снизить затраты на обследование и лечение онкологических больных. Таким образом, работы, направленные на изучение молекулярно генетических нарушений в клетках РЛ представляются очень актуальными. Эти исследования необходимы для разработки более специфичных молекулярных маркеров, а также более чувствительных методов их детекции.
Список литературы к данной статье предоставляется по запросу.
Пожалуйста, представьтесь.
Новое в терапии рака легкого - Содержание
