Применение никорандила при сосудистых хирургических вмешательствах у пациентов с ишемической болезнью сердца
Статьи
Опубликовано в журнале:
Кардиология и сердечно-сосудистая хирургия 2021, Т. 14, №5, с. 420-427
doi.org/10.17116/kardio202114051420
Ю.А. Кудаев, Э.В. Кулешова, Н.Л. Лоховинина, И.Т. Абесадзе, М.З. Алугишвили, М.А. Чернявский, А.В. Панов
ФГБУ «Национальный медицинский исследовательский центр им. В.А. Алмазова» Минздрава России, Санкт-Петербург, Россия
Резюме
Цель исследования. Оценить влияние никорандила на исходы сосудистых операций и динамику уровня высокочувствительного сердечного тропонина (вч-сТн) в раннем послеоперационном периоде у больных со стабильной ишемической болезнью сердца (ИБС).
Материал и методы. В исследование включено 50 пациентов со стенокардией напряжения II-III класса, направленных на плановое аутовенозное бедренно-подколенное шунтирование (БПШ). Все больные после компьютерной рандомизации были разделены на две равные группы: группа контроля – 25 больных и основная группа – 25 больных, которым дополнительно к базовой терапии за 2 ч до хирургического вмешательства назначали никорандил (Кординик, компания ПИК-ФАРМА) в максимальной разовой дозе 20 мг. В послеоперационном периоде оценивали частоту и структуру сердечно-сосудистых осложнений (CCO), включая повреждение миокарда по динамике повышения вч-сТн. Полученные первичные данные подвергались математической обработке с использованием прикладных программ Statistica version 10,0 и пакета программ SAS 9.3.
Результаты. Исходно пациенты группы никорандила и группы контроля были сопоставимы по основным клиническим характеристикам, базовой медикаментозной терапии и продолжительности хирургического вмешательства. В группе никорандила отсутствовала динамика повышения вч-сТн, а в группе стандартной терапии в 4 случаях уровень вч-сТн через 24 ч после операции превысил пороговые значения, что свидетельствовало об интраоперационном повреждении миокарда (0 против 16%, р=0,110). Статистическая достоверность межгрупповых различий была получена при оценке общей частоты ССО (повреждение и инфаркт миокарда, развитие сердечной недостаточности и нарушений ритма) в основной группе с применением никорандила и контрольной группе (8 против 36% соответственно, p=0,037).
Выводы. Использование никорандила (Кординик, компания ПИК-ФАРМА) перед открытой артериальной реконструкцией приводит в раннем послеоперационном периоде к снижению частоты госпитальных неблагоприятных кардиальных осложнений и повреждения миокарда, определяемого по динамике вч-сТн.
Ключевые слова: никорандил, ишемическая болезнь сердца, бедренно-подколенное шунтирование.
Информация об авторах:
Кудаев Ю.А. – orcid.org/0000-0002-2111-0765;
Кулешова Э.В. – orcid.org/0000-0001-8808-5720;
Лоховинина Н.Л. – orcid.org/0000-0002-9579-061X;
Алугишвили М.З. – orcid.org/0000-0002-9397-655X;
Абесадзе И.Т. – orcid.org/0000-0002-2322-327X;
Чернявский М.А. – orcid.org/0000-0003-1214-0150;
Панов А.В. – orcid.org/0000-0003-3356-3873;
Автор, ответственный за переписку: Кудаев Ю.А.
Как цитировать:
Кудаев Ю.А., Кулешова Э.В., Лоховинина Н.Л., Абесадзе И.Т., Алугишвили М.З., Чернявский М.А., Панов А.В. Применение никорандила при сосудистых хирургических вмешательствах у пациентов с ишемической болезнью сердца. Кардиология и сердечнососудистая хирургия. 2021;14(5):420-427. doi.org/10.17116/kardio202114051420
The application of nicorandil in patients with coronary heart disease undergoing vascular surgery
Yu.A. Kudaev, E.V. Kuleshova, N.L. Lokhovinina, I.T. Abesadze, M.Z. Alugishvili, M.A. Chernyavsky, A.V. Panov
Almazov National Medical Research Center, St Petersburg, Russia
Abstract
Objective. To assess the effect of nicorandil on the the outcomes of vascular surgeries and the high-sensitivity cardiac troponin (hs-cTn) level in the early postoperative period in patients with stable coronary heart disease (CHD).
Material and methods. The study included 50 patients with class II-III stable angina pectoris who would undergo femoral-popliteal bypass (FPB). All patients were randomized into two equal groups: a control group – 25 patients, and a study group – 25 patients, who were prescribed nicorandil (Cordinic, PIQ-Pharma company) 2 hours before the surgery in addition to the basic therapy with the maximum single dose 20 mg. In the postoperative period we assessed the frequency and the structure of cardiovascular complications (CVC) including myocardial damage by the dynamics of the hs-cTn rising. The obtained primary data were mathematically processed using Statistica 10.0 software and SAS 9.3 software package.
Results. At baseline, the study nicorandil group and the control group were comparable in terms of clinical characteristics, basic medical therapy and duration of surgery. In the nicorandil group there was no increase of hs-cTn. At the same time in the standard therapy group there were 4 cases with the level of hs-cTn above certain threshold values in 24 hours after surgery, which indicated intraoperative myocardial damage (0% vs. 16%, p=0.110). The statistical significance of intergroup differences was obtained by assessing the overall frequency of CVC (myocardial infarction and damage, the development of heart failure and rhythm disturbances) in the study nicorandil group and the control group (8% vs. 36%, respectively, p=0.037).
Conclusion. The use of nicorandil (Cordinic, PIQ-Pharma company) before open arterial reconstruction leads to a decrease in the level of hospital adverse cardiac events and myocardial damage in the early postoperative period, that is determined by the dynamics of hs-cTn.
Keywords: nicorandil, coronary heart disease, femoral-popliteal bypass.
Information about the authors:
Kudaev Yu.A. – orcid.org/0000-0002-2111-0765;
Kuleshova E.V. – orcid.org/0000-0001-8808-5720;
Lokhovinina N.L. – orcid.org/0000-0002-9579-061X;
Alugishvili M.Z. – orcid.org/0000-0002-9397-655X;
Abesadze I.T. – orcid.org/0000-0002-2322-327X;
Chernyavsky M.A. – orcid.org/0000-0003-1214-0150;
Panov A.V. – orcid.org/0000-0003-3356-3873;
Corresponding author: Kudaev Yu.A.
To cite this article:
Kudaev YuA, Kuleshova EV, Lokhovinina NL, Abesadze IT, Alugishvili MZ, Chernyavsky MA, Panov AV. The application of nicorandil in patients with coronary heart disease undergoing vascular surgery. Russ. Jour. of Card. and Cardiovasc. Surg. = Kard. i serd.-sosud. khir. 2021;14(5):420-427. (In Russ.). doi.org/10.17116/kardio202114051420
Введение
Ежегодно в мире проводится более 300 млн внесердечных операций [1]. Вместе с тем хирургические вмешательства являются триггерами больших сердечно-сосудистых событий (ССС). В ретроспективном исследовании, включавшем анализ более 10 млн госпитализаций по поводу некардиальной хирургии у взрослых пациентов в США, общая частота периоперационных фатальных осложнений, инфаркта миокарда (ИМ) и острого нарушения мозгового кровообращения (ОНМК) составила 3% [2]. Диагностически значимое повышение уровня тропонина, свидетельствующее о повреждении миокарда, достигает 20% [3]. Наиболее частым периоперационным осложнением, сопровождающимся высокой летальностью – 15-25%, является ИМ [4]. Помимо непосредственной угрозы пациенты с интраоперационным повреждением миокарда и ИМ имеют повышенный риск смерти в течение первого года после выписки из стационара, вследствие развития сердечной недостаточности (СН), жизнеугрожающих аритмий и повторного ИМ [5]. По данным проспективного когортного одноцентрового исследования (BASEL-PMI), включавшего 2265 больных высокого сердечно-сосудистого риска, у каждого пятого, перенесшего внесердечную операцию, в течение 365 дней развиваются неблагоприятные ССС и наиболее высокий риск наблюдается в первые 5 мес после хирургического лечения [6]. Следует подчеркнуть, что диагностика интраоперационного повреждения миокарда и ИМ на фоне применения анальгетиков затруднительна, поскольку чаще всего наблюдается отсутствие типичных симптомов ишемии, таких как боль в грудной клетке и одышка [7]. Кроме того, повреждение миокарда зачастую остается неверифицированным ввиду отсутствия систематического скрининга маркеров повреждения миокарда в повседневной клинической практике, что приводит к недооценке частоты периоперационных осложнений и их отдаленных последствий [8].
Сосудистые хирургические вмешательства представляют особый интерес, поскольку сопровождаются наиболее высоким риском возникновения ССО. У пациентов с атеросклерозом периферических артерий после реваскуляризации пораженного бассейна 30-дневное развитие неблагоприятных кардиальных событий достигает 21% [6]. Открытые операции на аорте и бедренно-подколенном сегменте согласно рекомендациям Европейского общества кардиологов (ESC) относят к категории высокого сердечно-сосудистого риска [9]. Пациенты с заболеваниями артерий нижних конечностей (ЗАНК) обычно имеют проявления мультифокального атеросклероза с поражением нескольких артериальных бассейнов в различной степени и менее благоприятный прогноз, чем пациенты без ЗАНК [10]. Даже у больных без доказанной ИБС хирургические вмешательства на периферических артериях сопровождаются повышенной частотой периоперационного ИМ [11].
С учетом высокого риска осложнений, подготовки пациентов с ИБС перед сосудистыми операциями придается особое значение. Согласно Европейским рекомендациям по сердечно-сосудистой профилактике необходим тщательный контроль артериального давления, проведение мероприятий по коррекции образа жизни и факторов риска [10]. Перед вмешательством все пациенты с ЗАНК должны получать статины, бета-адреноблокаторы (ББ) при наличии признаков высокого риска, при необходимости контролируемую антитромботическую терапию [9]. Особый интерес представляет разработка новых способов предупреждения кардиальных осложнений при сосудистых хирургических вмешательствах у больных ИБС. С этих позиций, привлекают внимание лекарственные средства с непосредственным влиянием на метаболические процессы в кардиомиоцитах и гладкомышечных клетках (ГМК) сосудов. Одним из таких препаратов является никорандил. Препарат обладает уникальным двойным механизмом действия. Активируя открытие АТФ-зависимых калиевых каналов, никорандил вызывает гиперполяризацию мембран ГМК сосудистой стенки и уменьшение поступления Са2+ внутрь клетки, что приводит к вазодилатации и снижению постнагрузки. Активация АТФ-зависимых калиевых каналов митохондрий определяет кардиопротективные эффекты, моделируя феномен ишемического прекондиционирования. С другой стороны, наличие в составе препарата нитратной группы обусловливает нитратоподобный эффект посредством повышения уровня внутриклеточного циклического гуанозинмонофосфата и расслабления ГМК, особенно венозной системы, что приводит к увеличению объема емкостных кровеносных сосудов и уменьшению преднагрузки [12].
В рандомизированном исследовании IONA (The Impact of Nicorandil in Angina) установлено снижение частоты ССО у пациентов со стабильной стенокардией, которые на протяжении в среднем 1,6 года принимали никорандил [13]. На сегодняшний день получены новые данные о кардио-протективном эффекте никорандила при стабильной ИБС [14], чрескожном коронарном вмешательстве (ЧКВ) [15] и коронарном шунтировании (КШ) [16]. В 2015 г. J. Yang и соавт. провели специальное исследование для выявления оптимальной дозы и времени приема никорандила с целью снижения риска повреждения миокарда при проведении ЧКВ у больных с острым коронарным синдромом (ОКС). Установлено, что максимальная эффективность достигается при пероральном приеме препарата в дозе 20 мг за 2 ч до проведения хирургического вмешательства [17].
Цель настоящего исследования – оценка влияния никорандила в дозе 20 мг за 2 ч до проведения планового аутовенозного бедренно-подколенного шунтирования (БПШ) у больных со стабильной ИБС на исходы сосудистых операций и уровень высокочувствительного сердечного тропонина (вч-сТн).
Материал и методы
В исследование включались пациенты со стабильной стенокардией напряжения II-III функционального класса (ФК), направленных в клинику сосудистой хирургии ФГБУ «НМИЦ им. В.А. Алмазова» для хирургического лечения ЗАНК. В конечном результате были отобраны 50 больных с показаниями к аутовенозному БПШ. Средний возраст пациентов на момент исследования составил 67±8 лет, всего включено 38 мужчин и 12 женщин. Критериями исключения являлись острый ИМ в течение предшествующих 3 месяцев, хроническая сердечная недостаточность (ХСН) III и IV функционального класса по классификации NYHA, брадикардия с частотой сердечных сокращений менее 50 ударов в минуту в состоянии покоя, систолическое АД ниже 100 мм рт.ст., атриовентрикулярная блокада II и III степени, тяжелая анемия, прием ингибиторов фосфодиэстеразы-5 и повышенная чувствительность к никорандилу.
Все больные после компьютерной рандомизации были разделены на две группы: 1-я группа (основная) – с назначением никорандила и 2-я группа (контроля) – стандартной терапии. В 1-й группе (n=25) к базовой медикаментозной терапии, получаемой больными на госпитальном этапе, назначался никорандил (Кординик, компания ПИК-ФАРМА) в разовой дозе 20 мг за 2 ч до операции. В контрольной группе больных (n=25) никорандил в предоперационном периоде не использовался.
В период госпитализации перед вмешательством проводилось лабораторное и клинико-инструментальное обследование, включающее общий и биохимический анализы крови, оценку липидного спектра, общий анализ мочи, электрокардиографию (ЭКГ) и эхокардиографию (ЭхоКГ). Дополнительно контролировали уровень вч-сТн до и через 24 после операции. Определение вч-сТн I выполнялось на анализаторе Architect i2000 с использованием тест-системы Abbott ARCHITECT STAT High Sensitive Troponin-I (Abbott Laboratories, США). Верхняя граница нормы (ВГН) вч-сТн составляла 0,034 нг/мл. Периоперационным повреждением миокарда, согласно четвертому универсальному определению ИМ, считалось повышение уровня вч-сТн в динамике, превышающее 99-й перцентиль ВГН, при отсутствии болевого синдрома в грудной клетке, ишемических изменений на ЭКГ и новых зон нарушения локальной сократимости по данным ЭхоКГ. Оценка ФК стенокардии осуществлялась на основании классификации Канадского сердечно-сосудистого общества.
Всем больным выполнено аутовенозное БПШ. Под общей анестезией разрезами в нижней и верхней третях бедра выделяли подколенную (ПКА) и общую бедренную артерию (ОБА) соответственно. Из отдельных кожных разрезов выделяли ствол большой подкожной вены. Формировали дистальный анастомоз между аутовеной и ПКА, проксимальный анастомоз между аутовеной и ОБА. После пуска кровотока и определения отчетливой пульсации зоны реконструкции выполняли послойный шов ран с оставлением дренажей в местах артериального доступа и наложением асептической повязки. В послеоперационном периоде оценивали частоту ССО и уровень вч-сТн. Учитывали наиболее неблагоприятные ССО, такие как повреждение миокарда, ИМ, декомпенсацию или развитие СН, появление или усугубление нарушений ритма и проводимости, ОНМК. Период наблюдения в раннем послеоперационном периоде составил 9,1±2,8 дней.
При статистической обработке данных использовали программу Statistica 10.0 (Statsoft, США) и пакета программ SAS 9.3. Количественные показатели оценивались на предмет соответствия нормальному распределению. При отсутствии нормального распределения данные описывались с помощью медианы (Ме), верхнего и нижнего квартилей (Q1-Q3). Категориальные данные описывались с указанием абсолютных значений и процентных долей. Сравнение частот бинарного признака в несвязанных группах проводился с помощью таблиц сопряженности с оценкой двустороннего точного критерия Фишера. Для сравнения двух независимых групп по количественному признаку использовался U-критерий Манна-Уитни. Сравнение процентных долей при анализе многопольных таблиц сопряженности выполнялось с помощью критерия χ² Пирсона. Уровень значимости (p) при проверке статистических гипотез в исследовании принимался <0,05.
Результаты
Среди направленных для хирургического лечения ЗАНК мужчины составили 76%, женщины – 24%. Возраст больных варьировал от 43 до 89 лет. Большинство пациентов страдали артериальной гипертензией (АГ) (88%), имели избыточный вес или ожирение (70%). Частота сахарного диабета (СД) составила 28%. ОНМК в анамнезе зарегистрировано у 13 (26%) больных. У 10 (20%) пациентов выполнялись хирургические вмешательства на каротидных артериях: у 6 (24%) в основной группе и у 4 (16%) в контрольной (р=0,725). Мультифокальное атеросклеротическое поражение с вовлечением трех основных сосудистых бассейнов (коронарные, каротидные и артерии нижних конечностей) имелось у 8 (32%) пациентов основной группы и у 10 (40%) группы контроля (р=0,554). Несмотря на то что все больные относились к категории очень высокого риска, целевой уровень холестерина липопротеинов низкой плотности (ХС ЛНП) (менее 1,4 ммоль/л) на догоспитальном этапе был достигнут лишь у 5 (10%) из них.
Пациенты основной и контрольной группы были сопоставимы по основным клиническим характеристикам, объему и продолжительности хирургического вмешательства (табл. 1).
Таблица 1. Клиническая характеристика и периоперационные параметры пациентов основной и контрольной групп
Table 1. Clinical characteristics and perioperative features of patients in the study and control group
| Показатель | Группа никорандила, n=25 (%) | Группа контроля, n=25 (%) | p-критерий |
| Возраст, лет | 64 [60-67] | 67 [63-70] | 0,275 |
| Мужской пол, n | 21 (84,0) | 17 (68,0) | 0,321 |
| ИМТ, кг/м² | 26,91 [25,02-28,81] | 28,48 [25,92 – 31,04] | 0,315 |
| Курение, n | 21 (84,0) | 17 (68,0) | 0,321 |
| АГ, n | 23 (92,0) | 21 (84,0) | 0,667 |
| Длительность ИБС, годы ФК стенокардии, n: | 8 [7-9] | 8 [7-10] | 0,961 |
| II | 22 (88,0) | 23 (92,0) | 0,451 |
| III | 3 (12,0) | 2 (8,0) |
|
| ФП, n | 3 (12,0) | 8 (32,0) | 0,171 |
| ИМ в анамнезе, n | 7 (28,0) | 10 (40,0) | 0,551 |
| ЧКВ анамнезе, n | 5 (20,0) | 8 (32,0) | 0,520 |
| КШ анамнезе, n | 4 (16,0) | 9 (36,0) | 0,196 |
| СД, n | 6 (24,0) | 8 (32,0) | 0,754 |
| ОНМК, n | 5 (20,0) | 8 (32,0) | 0,520 |
| ФВ ЛЖ, % | 59 [56-62] | 57 [54-59] | 0,193 |
| Гемоглобин, г/л | 132 [125-138] | 131 [123-139] | 0,915 |
| Креатинин, мкмоль/л | 85,00 [76,00-97,00] | 80,00 [73,00-98,00] | 0,515 |
| ОХС, ммоль/л | 4 [4-5] | 4 [4-5] | 0,894 |
| ХС ЛНП, ммоль/л | 2 [2-3] | 2 [2-3] | 0,728 |
| Глюкоза, ммоль/л | 6 [5-7] | 6 [5-8] | 0,930 |
| Время операции, мин | 190 [190-200] | 185 [180-205] | 0,550 |
| Количество койко-дней, сут | 8 [7-10] | 10 [7-11] | 0,845 |
Примечание. ИМТ – индекс массы тела, ФВ ЛЖ – фракция выброса левого желудочка, ОХС – общий холестерин, ХС ЛНП – холестерин липопротеинов низкой плотности.
При поступлении в группе никорандила у 88% пациентов присутствовала клиника стенокардии II ФК и у 12% – III ФК. В контрольной группе 92 и 8% соответственно. Фибрилляцией предсердий (ФП) страдали 3 (12%) пациента группы никорандила и 8 (32%) – группы контроля (р=0,171). ИМ перенесли 7 (28%) больных основной группы и 10 (40%) – контрольной (р=0,551). Реваскуляризация миокарда, не связанная с предстоящей сосудистой реконструкцией, выполнена 9 (36%) пациентам основной группы и 17 (68%) – группы контроля. В группе никорандила в 5 (20%) случаях проведено ЧКВ и в 4 (16%) – КШ, в контрольной группе в 8 (32%) и 9 (36%) случаях соответственно.
По базовой медикаментозной терапии в предоперационном периоде обе группы пациентов также были сопоставимы (табл. 2).
Таблица 2. Медикаментозная терапия пациентов основной и контрольной группы в предоперационном периоде
Table 2. Drug therapy for patients of the study and control groups in the preoperative period
| Показатель | Группа никорандила, n=25 (%) | Группа контроля, n=25 (%) | р-критерий |
| ББ | 24 (96,0) | 22 (88,0) | 0,609 |
| иАПФ | 15 (60,0) | 16 (64,0) | 1,000 |
| БРА | 8 (32,0) | 7 (28,0) | 1,000 |
| БМКК | 10 (40,0) | 12 (48,0) | 0,569 |
| Статины | 25 (100,0) | 22 (91,7) | 0,235 |
| АСК | 24 (96,0) | 21 (84,0) | 0,349 |
Примечание. АСК – ацетилсалициловая кислота, ББ – бета-адреноблокаторы, БМКК – блокаторы медленных кальциевых каналов, БРА – блокаторы рецепторов ангиотензина, иАПФ – ингибиторы ангиотензинпревращающего фермента.
Всем больным выполнили открытую реваскуляризацию бедренно-подколенного сегмента. Длительность вмешательства в среднем составила 190 мин в группе никорандила и 185 мин в контрольной группе (р=0,550). Осложнения в раннем послеоперационном периоде были выявлены у 11 (22%) пациентов. В целом применение никорандила в основной группе в дозе 20 мг за 2 ч до операции хорошо переносилось, не зафиксировано ни одного случая выраженной гипотонии (<100 мм рт.ст.). В контрольной группе в 4 случаях уровень вч-сТн через 24 ч после операции превысил пороговые значения, что свидетельствовало об интраоперационном повреждении миокарда, в группе никорандила динамика повышения отсутствовала (16 против 0%, р=0,110). Статистически значимого различия средних значений вч-сТн после операции (табл. 3, рис. 1) в обеих группах получено не было.
Таблица 3. Уровень вч-сТн у больных основной и контрольной группы через 24 ч после операции
Table 3. The level of hs-cTn in patients of the study and control groups 24 hours after surgery
| Показатель | вч-сТн | p |
| Me | Q1-Q3 | n |
| Группа никорандила, n=25 | 0,0030 | 0,0020-0,0040 | 25 | 0,143 |
| Группа контроля, n=25 | 0,0030 | 0,0030-0,0070 | 25 | |
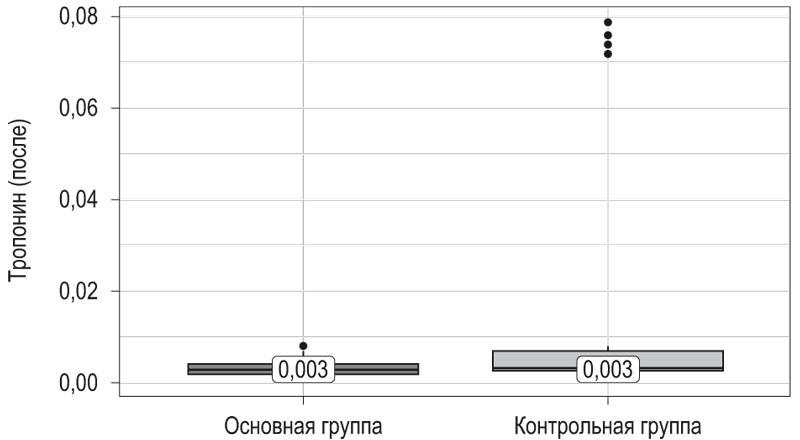 Рис. 1. Уровень вч-сТн через 24 часа после операции.
Рис. 1. Уровень вч-сТн через 24 часа после операции.
Fig. 1. The level of hs-cTn in 24 hours after surgery.
Летальных исходов, ОНМК и ИМ в обеих группах наблюдения не отмечено. Не установлено статистических межгрупповых различий при раздельном анализе выявления случаев повреждения миокарда по уровню вч-сТн, нарушений ритма и СН. Нарушения ритма зарегистрированы у 2 пациентов основной группы (пароксизмы ФП) и у 3 в контрольной (в двух случаях пароксизмы ФП и в одном – неустойчивая желудочковая тахикардия) (8 против 12%, р=1,000). Явления декомпенсации СН в раннем послеоперационном периоде выявлены у 2 больных контрольной группы при отсутствии таковой в группе никорандила (8 против 0%, р=0,490). Вместе с тем при оценке общей частоты ССО (повреждение миокарда, ИМ, нарушения ритма, СН, ОНМК) в раннем послеоперационном периоде выявлено статистически значимое их снижение в основной группе пациентов, получающих никорандил (8 против 36%, р=0,037) (табл. 4).
Таблица 4. Госпитальные послеоперационные осложнения
Table 4. Hospital postoperative complications
| Показатель | Группа никорандила, n=25 (%) | Группа контроля, n=25 (%) | р-критерий |
| Повреждение миокарда, n | 0 (0,0) | 4 (16,0) | 0,110 |
| Инфаркт миокарда, n | 0 | 0 | – |
| Нарушения ритма, n | 2 (8,0) | 3 (12,0) | 1,000 |
| Сердечная недостаточность, n | 0 (0,0) | 2 (8,0) | 0,490 |
| ОНМК, n | 0 | 0 | – |
| Комбинированная конечная точка, n | 2 (8,0) | 9 (36,0) | 0,037* |
Примечание. * – различия показателей статистически значимы (р<0,05).
Обсуждение
В 2018 г. в Российской Федерации (РФ) было выполнено 9 320 462 внесердечных хирургических вмешательства, из которых 130 109 составили сосудистые реконструкции [18]. Как уже отмечалось выше, диагностически значимое периоперационное повышение уровня тропонина при некардиальных операциях выявляется более, чем у 20% больных [3]. Таким образом, расчетный показатель случаев повреждения миокарда в РФ составляет ежегодно около 1,9 млн. С этих позиций проблема профилактики кардиальных осложнений при внесердечной хирургии, особенно при сосудистых вмешательствах высокого риска, среди пациентов нашей страны чрезвычайно актуальна. Ситуация усугубляется высокой распространенностью ИБС в РФ.
На сегодняшний день рутинное выполнение предоперационной коронарной ангиографии не рекомендуется и может рассматриваться только у пациентов с признаками высокого кардиального риска [19]. Реваскуляризация миокарда перед плановой внесердечной операцией существенно не улучшает периоперационные исходы и не должна выполняться только с превентивной целью [20]. По результатам рандомизированного исследования Coronary Artery Revascularization Prophylaxis, включавшего 510 больных с ИБС перед сосудистыми реконструкциями, смертность и частота развития послеоперационного ИМ в течение 30 дней не отличались в случае проведения предварительной реваскуляризации миокарда и без нее (22 против 23%; p=0,92) [21]. Согласно рекомендациям ESC реваскуляризация миокарда перед некардиальными хирургическими вмешательствами должна проводиться на основании стандартов лечения стабильной ИБС и ОКС либо перед операциями высокого риска после объективизации ишемии миокарда [9]. Поэтому коронарные вмешательства оправданы только у больных при наличии показаний к их проведению вне зависимости от факта планируемой некардиальной операции.
Становится очевидным, что оптимальная медикаментозная терапия остается основным инструментом кардиопротекции перед внесердечными операциями. В качестве препаратов, снижающих риск периоперационного ИМ, частоту ССО и госпитальную летальность, рассматривают ББ, статины, иАПФ, БРА и АСК.
Положительное влияние ББ заключается в снижении миокардиального стресса и пролонгации времени диастолического наполнения коронарных артерий. В исследовании POISE 8351 пациент рандомизирован в группы применения пролонгированного метопролола и плацебо перед внесердечной операцией, при этом отмечено снижение риска периоперационных кардиальных событий (ИМ, остановка сердца и сердечно-сосудистая смерть; 5,8 против 6,9%; p=0,04) при приеме ББ [22]. В настоящий момент, согласно рекомендациям ESC пациентам, принимающим ББ, целесообразно продолжить лечение в периоперационном периоде, а инициация их приема перед операцией оправдана лишь у больных с ИБС или высоким риском ССО и должна назначаться не позднее чем за 1 неделю до вмешательства для оценки переносимости и безопасности [9].
Гиполипидемическая терапия в связи с плейотропными механизмами способствует снижению периоперационных кардиальных осложнений. Ретроспективный анализ более 200 тыс. больных, перенесших некардиальные хирургические вмешательства, показал, что терапия холестеринснижающими препаратами в госпитальный период ассоциирована с более низкой летальностью (2,1 против 3,1%; ОР=0,62; ДИ 0,58-0,67) [23]. Однако результаты последних исследований эффективности статинов в профилактике ССО остаются достаточно противоречивыми [24]. В свою очередь, эксперты Американской Ассоциации Кардиологов (AHA) считают, что пациенты, получавшие статины на амбулаторном этапе, должны продолжить их прием, а предоперационное назначение статинов целесообразно при внесердечных операциях сосудистого профиля или у пациентов высокого риска, имеющих сердечно-сосудистое заболевание атеросклеротического генеза или СД [20].
В настоящее время нет единого мнения о назначении иАПФ или БРА при внесердечных операциях. Согласно мнению экспертов ESC целесообразно продолжать прием иАПФ или БРА до операции у гемодинамически стабильных пациентов с СН или систолической дисфункцией миокарда левого желудочка и временно отменять у лиц, которым они назначались по поводу АГ [9]. В свою очередь, эксперты AHA рекомендуют не прекращать терапию иАПФ или БРА в предоперационном периоде, а в случае показаний к их отмене возобновлять прием как можно раньше [20].
Вопрос о применении АСК при внесердечных вмешательствах остается спорным, ключевая проблема заключается в соотношении рисков тромботических осложнений и кровотечений. Метаанализ крупных рандомизированных исследований с участием 28 302 больных показал, что частота ИМ и сердечно-сосудистая летальность не отличаются в группах с аспирином и без него, но при этом крупные кровотечения чаще возникают у пациентов, принимающих аспирин [25]. В связи с этим целесообразность антиагрегантной терапии в периоперационном периоде должна обсуждаться индивидуально на основании оценки тромботических и геморрагических рисков.
Таким образом, арсенал медикаментозных средств для предупреждения ССО ограничен, что определяет необходимость поиска новых подходов для улучшения исходов внесердечных операций, в том числе открытых артериальных реконструкций, относящихся к категории высокого кардиального риска. Полученные в ходе проведенного нами исследования данные продемонстрировали возможность улучшения исходов сосудистых операций у пациентов со стабильной ИБС при использовании никорандила (Кординик, компания ПИК-ФАРМА) в дозе 20 мг за 2 ч до вмешательства. Препарат хорошо переносился и приводил к суммарному уменьшению количества госпитальных кардиальных осложнений и повреждений миокарда (рис. 2).
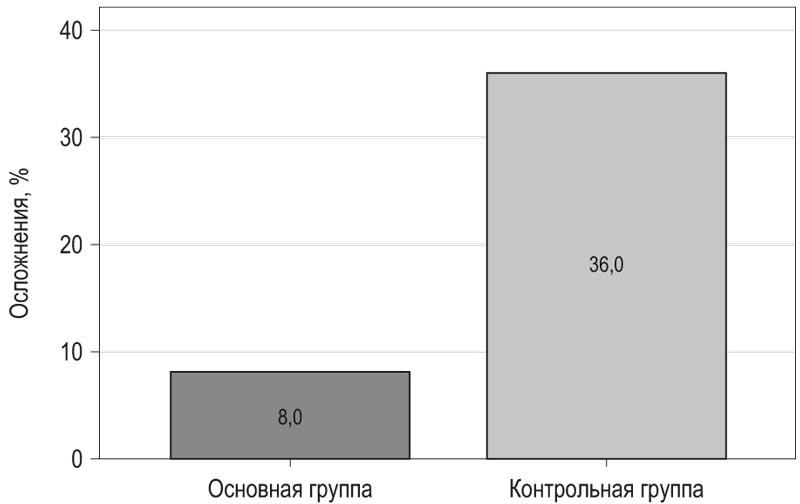 Рис. 2. Частота возникновения сердечно-сосудистых осложнений при бедренно-подколенном шунтировании на фоне применения никорандила 20 мг за 2 ч до операции (основная группа).
Рис. 2. Частота возникновения сердечно-сосудистых осложнений при бедренно-подколенном шунтировании на фоне применения никорандила 20 мг за 2 ч до операции (основная группа).
Fig. 2. The frequency of cardiovascular complications in femoral-popliteal bypass surgery with against the background of the reception nicorandil 20 mg 2 hours before surgery (study group).
Снижение уровня неблагоприятных ССО на фоне терапии никорандилом, помимо сосудистого эффекта, объясняют его уникальной фармакодинамической способностью повышать устойчивость кардиомиоцитов к повторным эпизодам гипоксии за счет воспроизведения феномена ишемического прекондиционирования [26].
На сегодняшний день получены новые данные по использованию никорандила в пероральной и парентеральной формах у пациентов с ИБС при плановых и экстренных коронарных вмешательствах. Так, по данным метаанализа 14 рандомизированных клинических исследований с участием 1864 пациентов показано, что назначение препарата после планового ЧКВ приводило к улучшению сократительной функции миокарда и снижению ССС [27]. Использование никорандила (Кординик, компания ПИК-ФАРМА) в пероральной форме за 2 суток до и в течение месяца после ЧКВ снижало частоту ИМ 4а типа и риск развития ССО в течение года после вмешательства [28]. У больных с ИМ, перенесших первичное ЧКВ, применение никорандила в течение 6 мес после реваскуляризации в суточной дозе 15 мг способствовало уменьшению зоны инфаркта и улучшению систолической функции ЛЖ [15]. Внутривенное периоперационное введение никорандила при экстренном ЧКВ уменьшало площадь повреждения миокарда [29]. В проведенном в 2020 г. метаанализе, включавшем 2965 пациентов, J. Zhou и соавт., показали, что назначение никорандила при ЧКВ у больных с ИМ улучшало реперфузию миокарда и систолическую функцию ЛЖ, снижало частоту ССО и летальность [30]. В недавно опубликованном российском исследовании терапия никорандилом у пациентов со стабильной стенокардией в предоперационном периоде КШ способствовала улучшению показателей качества жизни и течения раннего послеоперационного периода [16].
Таким образом, наши данные соответствуют последним результатам позитивного применения никорандила при реваскуляризации миокарда и открывают новые возможности использования препарата в клинической практике.
Вывод
Назначение никорандила (Кординик, компания ПИК-ФАРМА) у пациентов со стабильной ИБС в дозе 20 мг за 2 ч до операции БПШ безопасно и улучшает клинические исходы вмешательства. Использование препарата перед артериальной реконструкцией приводит к снижению частоты госпитальных неблагоприятных кардиальных осложнений и повреждения миокарда по динамике уровня вч-сТн. Результаты исследования определяют перспективы применения такого подхода с целью оптимизации хирургического лечения ЗАНК у больных с ИБС.
Конфликт интересов. Публикация статьи поддержана компанией ПИК-ФАРМА, что никоим образом не повлияло на собственное мнение авторов.
Disclosures. The publication of the article is supported by the PIQ-Pharma company, but it did not affect own opinion of the authors.
Участие авторов:
Концепция и дизайн исследования – М.А. Чернявский, А.В. Панов
Сбор и обработка материала – Ю.А. Кудаев, Н.Л. Лоховинина
Статистическая обработка – М.З. Алугишвили, И.Т. Абесадзе
Написание текста – Ю.А. Кудаев
Редактирование – Э.В. Кулешова, А.В. Панов
Литература/References
- Weiser TG, Haynes AB, Molina G, et al. Estimate of the global volume of surgery in 2012: an assessment supporting improved health outcomes. Lancet. 2015;385:S11.
doi.org/10.1016/S0140-6736(15)60806-6 - Smilowitz NR, Gupta N, Ramakrishna H, Guo Y, Berger JS, Bangalore S. Perioperative major adverse cardiovascular and cerebrovascular events associated with noncardiac surgery. JAMA Cardiol. 2017;2(2):181-187.
doi.org/10.1001/jamacardio.2016.4792 - Devereaux PJ, Biccard BM, Sigamani A, et al. Writing Committee for the VISION Study Investigators. Association of postoperative high-sensitivity troponin levels with myocardial injury and 30-day mortality among patients undergoing noncardiac surgery. J Am Med Assoc. 2017;317(16):1642-1651.
doi.org/10.1001/jama.2017.4360 - Devereaux PJ, Goldman L, Cook DJ, et al. Perioperative cardiac events in patients undergoing noncardiac surgery: a review of the magnitude of the problem, the pathophysiology of the events and methods to estimate and communicate risk. CMAJ. 2005;173(6):627-634.
doi.org/10.1503/cmaj.050011 - Thomas S, Borges F, Bhandari M, et al. Association between myocardial injuryand cardiovascular outcomes of orthopaedic surgery: a Vascular Events in Noncardiac Surgery Patients Cohort Evaluation (VISION) substudy. J Bone Joint Surg Am. 2020;102:880-888.
doi.org/10.2106/JBJS.18.01305 - Sazgary L, Puelacher C, Lurati Buse G, et al. Incidence of major adverse cardiac events following non-cardiac surgery. Eur Heart J Acute Cardiovasc Care. 2020;10(5):550-558.
doi.org/10.1093/ehjacc/zuaa008 - Hidvegi R, Puelacher C, Gualandro DM, et al. Obesity paradox and perioperative myocardial infarction/injury in non-cardiac surgery. Clin Res Cardiol. 2020;109(9):1140-1147.
doi.org/10.1007/s00392-020-01605-0 - Puelacher C, Lurati Buse G, Seeberger D, et al. Perioperative myocardial injury after noncardiac surgery. Circulation. 2018;137(12):1221-1232.
doi.org/10.1161/CIRCULATIONAHA.117.030114 - Kristensen SD, Knuuti J, Saraste A, et al. The Joint Task Force on non-cardiac surgery: cardiovascular assessment and management of the European Society of Cardiology(ESC) and the European Society ofAnaesthesiology (ESA). Eur Heart J. 2014;35(35):2383-2431.
doi.org/10.1093/eurheartj/ehu282 - Piepoli MF, Hoes AW, Agewall S, et al. 2016 European Guidelines on cardiovascular disease prevention in clinical practice: The Sixth Joint Task Force of the European Society of Cardiology and Other Societies on Cardiovascular Disease Prevention in Clinical Practice (constituted by representatives of 10 societies and by invited experts) Developed with the special contribution of the European Association for Cardiovascular Prevention & Rehabilitation (EACPR). Eur Heart J. 2016;37(29):2315-2381.
doi.org/10.1093/eurheartj/ehw106 - Ashton CM, Petersen NJ, Wray NP et al. The incidence of perioperative myocardial infarction in men undergoing noncardiac surgery. Ann Intern Med. 1993;118:504-510.
doi.org/10.7326/0003-4819-118-7-199304010-00004 - Goldschmidt M, Landzberg BR, Frishman WH. Nicorandil: a potassium channel opening drug for treatment of ischemic heart disease. Clin J Pharmacol. 1996;36:559-572.
doi.org/10.1002/j.1552-4604.1996.tb04219.x - IONA Study Group. Effect of nicorandil on coronary events in patients with stable angina: the Impact Of Nicorandil in Angina (IONA) randomised trial. Lancet. 2002;359:1269-1275.
doi.org/10.1016/S0140-6736(02)08265-X - Марцевич С.Ю., Лукина Ю.В., Кутишенко Н.П. и др. Первые результаты оценки влияния длительного применения никорандила на вероятность возникновения сердечно-сосудистых осложнений у больных стабильной ишемической болезнью сердца (данные наблюдательного исследования НИКЕЯ). Рациональная Фармакотерапия в Кардиологии. 2019;15(3):335-342. Martsevich SYu, Lukina YuV, Kutishenko NP, et al. Initial Results of Long-Term Nicorandil Treatment Effect on the Probability of Cardiovascular Complications in Patients with Stable Coronary Artery Disease (Data of Observational NIKEA Study). Rational Pharmacotherapy in Cardiology. 2019;15(3):335-342. (In Russ.).
doi.org/10.20996/1819-6446-2019-15-3-335-342 - Wang S, Duan Y, Feng X, et al. Sustained nicorandil administration reduces the infarct size in ST-segment elevation myocardial infarction patients with primary percutaneous coronary intervention. Anatol J Cardiol. 2019;21(3):163-171.
doi.org/10.14744/AnatolJCardiol.2018.57383 - Аргунова Ю.А., Шалева В.А., Федорова Н.В., Барбараш О.Л. Подготовка пациента к коронарному шунтированию. Роль эффективной медикаментозной терапии. Кардиология и сердечно-сосудистая хирургия. 2021;14(3):139-145.
Argunova YuA, Shaleva VA, Fedorova NV, Barbarash OL. Preoperative management in coronary artery bypass surgery. The role of effective therapy. Russ Jour of Card and Cardiovasc Surg. 2021;14(3):139-145. (In Russ.).
doi.org/10.17116/kardio202114031139 - Yang J, Zhang J, Cui W, et al. Cardioprotective effects of single oral dose of nicorandil before selective percutaneous coronary intervention. Anatolian J Cardiol. 2015;15:125-131.
doi.org/10.5152/akd.2014.5207 - Российский статистический ежегодник. М. 2019;708. Russian statistical yearbook. M. 2019;708. (In Russ.).
rosstat.gov.ru folder/210/document/12994 - Schulman-Marcus J, Feldman DN, Rao SV, et al. Characteristics of patients undergoing cardiac catheterization before noncardiac surgery: a report from the national cardiovascular data registry Cath PCI Registry. JAMA Intern Med. 2016;176(5):611-618.
doi.org/10.1001/jamainternmed.2016.0259 - Fleisher LA, Fleischmann KE, Auerbach AD, et al. 2014 ACC/ AHA guideline on perioperative cardiovascular evaluation and management of patients undergoing noncardiac surgery: a report of the American College of Cardiology. American Heart Association Task Force on practice guidelines. J Am Coll Cardiol. 2014;64(22):77-137.
doi.org/10.1016/joacc.2014.07.944 - Santilli SM. The Coronary Artery Revascularization Prophylaxis (CARP) Trial: results and remaining controversies. Perspect Vasc SurgEndovasc Ther. 2006;18(4):282-285.
doi.org/10.1177 1531003506295144 - Devereaux PJ, Yang H, Yusuf S, et al.; POISE Study Group. Effects of extended-release metoprolol succinate in patients undergoing non-cardiac surgery (POISE trial): a randomised controlled trial. Lancet. 2008;371(9627):1839-1847.
doi.org/10.1016/S 0140-6736(08)60601-7 - Lindenauer PK, Pekow P, Wang K, Gutierrez B, Benjamin EM. Lipid-lowering therapy and in-hospital mortality following major noncardiac surgery. J Am Med Assoc. 2004;291(17):2092-2099.
doi.org/10.1001/jama.291.17.2092 - Putzu A, de Carvalho E Silva CMPD, Pinheiro de Almeida J, Belletti A, Cassina T, Landoni G, Abrahao Hajjar L. Perioperative statin therapy in cardiac and non-cardiac surgery: a systematic review and meta-analysis of randomized controlled trials. Ann Intensive Care. 2018;8(1):95.
doi.org/10.1186/s13613-018-0441-3 - Wolf G, Navarese EP, Brockmeyer M, et al. Perioperative aspirin therapy in non-cardiac surgery: A systematic review and meta-analysis of randomized controlled trials. Int J Cardiol. 2018;258:59-67.
doi.org/10.1016/j.ijcard.2017.12.088 - Lenz M, Kaun C, Krychtiuk KA, et al. Effects of Nicorandil on Inflammation, Apoptosis and Atherosclerotic Plaque Progression. Biomedicines. 2021;9(2):120.
doi.org/10.3390/biomedicines9020120 - Zhao XT, Zhang CF, Liu QJ. Meta-analysis of Nicorandil effectiveness on myocardial protection after percutaneous coronary intervention. BMC Cardiovascular Disorders. 2019;19:144.
doi.org/10.1186/s12872-019-1071-x - Соболева Г.Н., Гостищев Р.В., Рогоза А.Н., Коткина Т.И., Самко А.И., Карпов Ю.А. Влияние фармакологического прекондиционирования никорандилом перед плановым чрескожным коронарным вмешательством на отдаленный прогноз больных стабильной ишемической болезнью сердца. Рациональная Фармакотерапия в Кардиологии. 2020;16(2):191-198.
Soboleva GN, Gostishchev RV, Rogoza AN, Kotkina TI, Samko AN, Karpov YA. The Effect of Pharmacological Preconditioning with Nicorandil before Elective Coronary Stenting on the LongTerm Prognosis of Patients with Stable Coronary Artery Disease. Rational Pharmacotherapy in Cardiology. 2020;16(2):191-198. (In Russ.).
doi.org/10.20996/1819-6446-2020-04-05 - Wang ZD, Li H, Liu M, Li P, Chen J, Liang XW, Zhu XZ, Liao W. Effect of intravenous application of nicorandil on area of myocardial infarction in patients with STEMI during the perioperative stage of PCI. Clin Hemorheol Microcirc. 2021;77(4):411-423.
doi.org/10.3233/CH-200998 - Zhou J, Xu J, Cheng A, Li P, Chen B, Sun S. Effect of nicorandil treatment adjunctive to percutaneous coronary intervention in patients with acute myocardial infarction: a systematic review and meta-analysis. J Int Med Res. 2020;48(11):300060520967856.
doi.org/10.1177/0300060520967856
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)