Сравнительная эффективность препаратов ламотриджинового ряда
Статьи Опубликовано в журнале:«ВРАЧ»; Фармакология; 12; 2007; стр. 34-36.
Г. Авакян, доктор медицинских наук, профессор, О. Бадалян, доктор медицинских наук, Р. Биктимеров, О. Варашкевич, Е. Крикова, Ф. Ридер, кандидат медицинских наук, Ю. Тихонов, кандидат медицинских наук, С. Бурд, доктор медицинских наук
РГМУ
С ростом в последние годы затрат в сфере практического здравоохранения все чаще встает вопрос об оптимальном выборе лекарственного препарата, у которого клиническая эффективность и безопасность сочетались бы с низкой стоимостью. В связи с этим в клинической практике все большее распространение получают генерики; изучение их сравнительной клинической эффективности и безопасности — одна из наиболее актуальных задач в области клиники, фармацевтики и фармакоэкономики [4, 6, 8, 9].
При эпилепсии вопрос о биоэквивалентности генериков и оригинальных препаратов стоит особенно остро [1], поскольку даже небольшие различия в биодоступности медикаментов могут привести к серьезным последствиям, например возобновлению приступов у пациентов с многолетней медикаментозной ремиссией [6, 9]. Поэтому существуют достаточно жесткие требования соответствия оригинальному лекарственному средству (ЛС), которые включают 3 важнейших компонента, обозначаемые как фармацевтическая, фармакокинетическая и терапевтическая эквивалентность [2, 5, 7]. Фармацевтическая эквивалентность предполагает, что оригинальное и воспроизведенное ЛС содержат одну и ту же активную субстанцию в одинаковых количестве и форме; допустимы лишь отличия по использованным вспомогательным средствам (наполнители, красители, особенности покрытия). Фармакокинетическая эквивалентность (или биоэквивалентность) означает, что биодоступность (скорость и степень всасывания) и метаболизм оригинального и воспроизведенного ЛС после введения в одной и той же молярной дозе сходны в такой степени, что их эффективность и безопасность не могут не быть одинаковыми, а терапевтическая эквивалентность — что оригинальный препарат и генерик по результатам клинических исследований обладают равными эффективностью и безопасностью [5, 12].
Из средств, имеющих генерические аналоги, врачи-эпилептологи используют не только противоэпилептические препараты (ПЭП) первого поколения, но и новые ПЭП. К последним относится ламиктал (действующее вещество — ламотриджин), который показан дополнительно [3, 6, 8] или в качестве монотерапии при парциальных и генерализованных приступах, включая тонико-клонические судороги и приступы, ассоциированные с синдромом Леннокса — Гасто, для взрослых и детей старше 12 лет; в режиме комбинированной терапии эпилепсии может применяться у детей до 12 лет.
Сегодня на российском рынке существует несколько генерических препаратов, активным компонентом которых является ламотриджин; в частности, к ним относится конвульсан производства «Актавис АО», Исландия [5, 6, 8, 11, 14]. Нами в сравнительном аспекте изучены переносимость и клиническая эффективность в режиме монотерапии (таблетки по 25 мг) конвульсана и ламиктала (оригинальный препарат производства «ГлаксоСмитКляйн Фармасьютикалз С. А.», Польша) у 15 пациентов с эпилепсией.
Больные были в возрасте от 20 до 69 лет. Криптогенная фокальная эпилепсия (КФЭ) была у 7 (47%), симптоматическая фокальная эпилепсия (СФЭ) — у 8 (53%) пациентов; длительность заболевания составляла от 6 мес до 42 лет. Диагноз был установлен на основе клинических и инструментальных данных в соответствии с международной классификацией эпилепсии (1989); тип эпилептических приступов также определялся согласно существующей международной классификации (1981). Всем пациентам проводили клиническое неврологическое обследование, электроэнцефалографическое (ЭЭГ) исследование (энцефалограф «МБН-Нейрокартограф», Россия), магнитно-резонансную томографию (МРТ) для верификации структурных изменений головного мозга. Концентрацию ламотриджина в плазме крови для каждого из изучаемых препаратов измеряли методом высокоэффективной жидкостной хроматографии («Altex, Ultrasphere ODS»). Клиническую эффективность препаратов определяли по изменению частоты и тяжести эпилептических приступов, а также косвенно — по оказавшейся эффективной дозе препарата.
В ходе исследования у 15 пациентов, изначально принимавших оригинальный ламотриджин в соответствии со схемой в инструкции по применению, при достижении клинического эффекта (урежение частоты приступов не менее чем на 50%) брали кровь для биохимического анализа (исследовали концентрацию препарата в крови). Параллельно анализировали частоту и тяжесть эпилептических приступов до и после приема оригинального препарата. Оценивали также изменения на ЭЭГ у пациентов до приема препарата и после достижения клинического эффекта. Затем с шагом по 25 мг в 3 дня осуществляли переход на конвульсан в соответствии с инструкцией по медицинскому применению при параллельном снижении дозы оригинального ламотриджина и проводили наблюдения в течение 3 нед: оценивали динамику клинической картины, регистрировали изменения на ЭЭГ на фоне приема конвульсана, брали кровь (из локтевой вены через 3 ч после приема конвульсана, т.е. на пике его концентрации) для определения концентрации препарата в плазме, оценивали переносимость и безопасность препарата на основании жалоб пациентов.
Доза препаратов ламотриджинового ряда, принимаемых пациентами, составила от 50 до 250 мг/сут. Эффективность действия препарата оценивали по урежению частоты эпилептических приступов (табл. 1).
Таблица 1
Изменение у больных частоты эпилептических приступов на фоне приема препаратов ламотриджина
| Урежение частоты приступов | ||||
| Форма эпилепсии | на 50% | на 75% | на 100% |
Всего больных |
| КФЭ | 3 (20) | 2 (13,5) | 2 (13,5) | 7 (47) |
| СФЭ | 3 (20) | 4 (26,5) | 1 (6,5) | 8 (53) |
У пациентов с КФЭ не выявлено структурных изменений на МРТ при наличии фокальных приступов с вторичной генерализацией или без нее. ЭЭГ до лечения оригинальным ламотриджином характеризовалась умеренно выраженными общемозговыми изменениями с нарушением регулярности α-ритма и усилением представленности диффузной медленной активности в диапазоне υ- и δ-волн, наличием (в некоторых случаях) региональной эпилептиформной активности в виде вспышек острых волн, комплексов пик — волна, спайков со вторично-билатеральной синхронизацией или без таковой. Изменения ЭЭГ на фоне приема оригинального ламотриджина характеризовались снижением количества вспышек пароксизмальной и эпилептиформной активности с тенденцией к нормализации основных ритмов и зональных распределений.
Для пациентов с СФЭ были характерны структурные изменения на МРТ и фокальные приступы с вторичной генерализацией или без нее. Регистрировались умеренные изменения биоэлектрической активности головного мозга — дезорганизованный тип ЭЭГ с замедлением основной активности в области структурного дефекта с периодическими вспышками эпилептиформной активности в виде острых волн, спайков с тенденцией к вторично-билатеральной синхронизации. Под влиянием оригинального препарата на ЭЭГ больных СФЭ уменьшились частота регистрации эпилептиформной и пароксизмальной активности и возникновения вторично-билатеральной синхронизации с модуляцией основных ритмов.
При замене оригинального ламотриджина конвульсаном эффективность лечения оценивали, помимо клинических проявлений заболевания (изменение частоты и тяжести приступов), по изменениям на ЭЭГ (уменьшение эпилептиформной активности и снижение ее спектра мощности). Нарастание при приеме оригинального препарата нормальной организации корковой ритмики регистрировалось и при переходе на конвульсан. Значимых различий изучаемых показателей (ухудшение ЭЭГ-картины, нарастание эпилептиформной активности и(или) ухудшение организации корковой ритмики) не выявлено.
До лечения препаратами ламотриджина у пациентов регистрировались следующие типы эпилептических приступов, характерные для фокальных форм эпилепсии: простые парциальные (у 12), сложнопарциальные (у 1) и вторично-генерализованные судорожные (у 2). Как отмечалось выше, на фоне приема оригинального ламотриджина отмечалась положительная тенденция, заключавшаяся в снижении количества и тяжести приступов (табл. 2).
Таблица 2
Клинический эффект при приеме оригинального ламотриджина у пациентов с различными формами фокальной эпилепсии
| Изменение частоты приступов | Формы фокальной эпилепсии | ||
| простые парциальные | сложно-парциальные | вторично-генерализованные судорожные | |
| 12 (80) | 1 (6,7) | 2 (13,3) | |
| Урежение на 50% | 4 (26,4) | 0 | 2(13,3) |
| Урежение на 75% | 5 (33,5) | 1 (6,7) | 0 |
| Медикаментозная ремиссия | 3 (20,1) | 0 | 0 |
Замена оригинального ламотриджина на конвульсан у всех пациентов с 50% урежением приступов и у 5 из 6 пациентов с урежением приступов на 75% не привела к ухудшению состояния (усилению или утяжелению эпилептических приступов), не было также необходимости в увеличении принимаемых доз. Однако у 1 пациента было зарегистрировано увеличение количества приступов в 1,8 раза и усиление их тяжести на фоне приема препарата в дозе 100 мг/сут, что потребовало возвращения больного на оригинальный ламотриджин и выведения его из исследования. В группе пациентов с 100% купированием приступов при переведении с оригинального препарата на конвульсан ухудшения состояния не наблюдалось, т.е. сохранялась медикаментозная ремиссия.
Анализ данных о концентрации препаратов ламотриджинового ряда в крови показал, что независимо от степени урежения приступов различии в концентрации оригинального ламотриджина и конвульсана не было. Полученные результаты позволили разделить пациентов на 3 группы в зависимости от средней эффективной дозы и концентрации препаратов в крови (табл. 3).
Таблица 3
Концентрация препаратов ламотриджинового ряда в плазме крови в зависимости от дозы
| Доза препарата, мг | Концентрация в плазме крови, мг/л | |
| оригинальный ламотриджин | конвульсан | |
| 50-75 | 0,535 | 0,835 |
| 100-125 | 0,731 | 0,745 |
| 200-250 | 1,463 | 1,50 |
Стандартная поддерживающая доза оригинального ламотриджина и конвульсана, согласно инструкции по медицинскому применению, составляет 100—200 мг/сут. Терапевтически значимая концентрация ламотриджина (1—3 мг/л, или 4—12 ммоль/л) наблюдалась только в группе с диапазоном доз 200—250 мг, в 2 других группах она оказалась значительно ниже, что объясняется низкой эффективной дозой препаратов и может быть связано с индивидуальными особенностями фармакокинетики у конкретного пациента.
Полученные нами данные свидетельствуют о линейной зависимости между концентрацией препарата в крови и терапевтически эффективной дозой (см. рисунок). Результаты проведенного исследования подтверждаются данными, полученными при сравнительном изучении биоэквивалентности генерических препаратов ламотриджинового ряда и их взаимозаменяемости [6]. Авторами изучалась вариабельность концентрации препарата в плазме крови при замене оригинальной формы ламотриджина на генерик. Было показано, что применение генерического препарата ламотриджина (конвульсана) не привело к изменению концентрации в плазме крови и большему разбросу в значениях показателя. Это свидетельствовало об отсутствии различий в эффекте при назначении оригинального препарата или его генерического аналога.
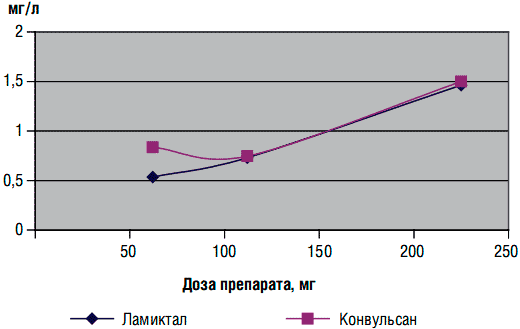
Рисунок. Зависимость концентрации препаратов ламотриджина в крови от дозы
На протяжении всего исследования мы не наблюдали у пациентов развития тяжелых побочных реакций на фоне приема конвульсана и оригинального ламотриджина. Однако при замене оригинального ламотриджина конвульсаном у 2 пациентов отмечалось ухудшение самочувствия, были зафиксированы тошнота, головокружение, диплопия. Такие побочные эффекты не являются редкостью и не относятся к жизнеугрожающим; они довольно подробно описаны в литературе [13]. Тем не менее проведенное исследование подтвердило данные о возможности появления у части пациентов нежелательных реакций [10] при замене оригинального препарата на генерический.
Таким образом, эффективная концентрация конвульсана (таблетки 25 мг производства «Актавис АО», Исландия) эквивалентна таковой ламиктала (таблетки 25 мг производства «ГлаксоСмитКляйн Фармасьютикалз С. А.», Польша), что подтверждалось отсутствием необходимости корректировать дозу при замене одного препарата на другой у включенных в исследование пациентов. Выявленная линейная зависимость концентрации препарата от принимаемой дозы может стать хорошим прогностическим критерием эффективности лечения при синонимической замене оригинального препарата на генерический. Это особенно важно для больных эпилепсией, у которых подобная замена в условиях меняющегося льготного обеспечения проводится часто. Проведенное исследование, не решая проблему замены оригинальных противоэпилептических ламотриджиновых препаратов на их генерические варианты, демонстрирует возможности исследования уровня препарата в крови при оценке эффективности данной замены.
Литература 1. Белоусов Ю. Б. Дженерики — мифы и реалии // Ремедиум. — 2003. — № 7-8: 4-9.
2. Дробижев М. Ю. // Психиатрия и психофармакотерпия. — 2007; 9 (3). Т: 43-49.
3. Andermann F., Duh M. S., Gosselin A. et al. // Epilepsia. — 2007; 48 (3): 464-469.
4. Bialer M. // Epilepsia. — 2007; 48 (10): 1825-1832.
5. Borgherini G. // Clin. Ther. — 2003; 25: 1578-1592.
6. Buck T. C., Schmedes A., Brandslund I. // Ugeskr Laeger. — 2007; 21; 169 (21): 2013-2015.
7. Chow S. C., Liu J. // J. Biopharm Stat. — 1997; 7 (1): 97-111.
8. Duh M. S., Andermann F., Paradis P. E. et al. // Dis Manag. — 2007; 10 (4): 216-225.
9. Heaney D. C., Sander J. W. // Lancet Neurol. — 2007; 6 (5): 465-468.
10. Makus K. G. // Epilepsia. — 2005; 46 (6): 279.
11. Makus K. G., McCormick // J. Clin. Ther. — 2007; 29 (2): 334-341.
12. Therapeutics and Technology Assessment Subcommittee of the American Academy of Neurology. Assessment: Generic substitution for antiepileptic medication. — Neurology. — 1990; 40: 1641-1643.
13. Wong I., Lhatoo S. // Drug. Saf. — 2000; 23 (1): 35-56.
14. Wong I., Mawer G. E., Sander J. W. // Epilepsia. — 2001; 42 (2): 237-244.
