Сравнительный мета–анализ эффективности сартанов при лечении артериальной гипертензии
СтатьиОпубликовано в журнале:
РМЖ КАРДИОЛОГИЯ ТОМ 18, No 22, 2010
Д.м.н. Г.А. Барышникова
ФГУ Учебно–научный медицинский центр управления делами Президента РФ, Москва
В настоящее время в мире артериальной гипертензией (АГ) страдает один миллиард человек. АГ является важным фактором риска развития сердечно–сосудистых осложнений (ССО), а из–за широкого распространения вносит существенный вклад (от 35 до 45%) в сердечно–сосудистую заболеваемость и смертность [1]. По мере старения населения и увеличения роли таких способствующих факторов, как ожирение, малоподвижный образ жизни и курение, к 2025 г. ожидается увеличение доли сердечно–сосудистых заболеваний в структуре смертности населения до 60% (до 1,56 млрд человек) [1,2]. Заболеваемость и смертность, связанные с неконтролируемой АГ, являются причиной существенного экономического бремени в виде расходов на лекарства, госпитализацию, хирургическое вмешательство и прочие ресурсы здравоохранения. Несмотря на широкую осведомленность о последствиях АГ и доступность эффективных методов лечения, до 32% пациентов, страдающих АГ, не получают эффективных противогипертензивных препаратов [3].
Ренин–ангиотензин–альдостероновая система (РААС) играет ключевую роль в патофизиологии АГ, выступая первичным регулятором объема жидкости, водно–солевого баланса и объема крови. При повышении активности РААС ангиотензин–II вызывает вазоконстрикцию, повышение секреции альдостерона и активности симпатической нервной системы, что в совокупности способствует становлению и прогрессированию АГ. Блокаторы рецепторов ангиотензина–II (БРА) регулируют работу РААС, блокируя активацию рецепторов ангиотензина–II подтипа АТ1, что сопровождается вазодилатацией, уменьшением секреции вазопрессина, выработки и секреции альдостерона.
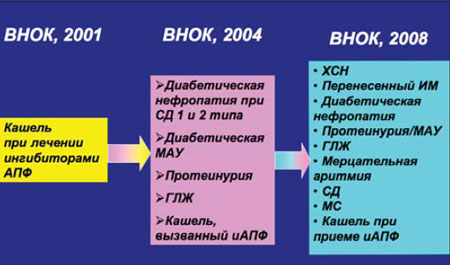
На протяжении ряда лет важную роль в лечении АГ играют БРА II, входящие в список основных антигипертензивных препаратов, которые практически сразу заявили о себе не только как о средствах для лечения АГ, но и о перспективных препаратах для предотвращения ряда ССО, лечения хронической сердечной недостаточности и заболеваний почек. Основания для их назначения при АГ значительно расширены (рис. 1), и сегодня совсем не обязательно иметь предшествующий печальный опыт применения ингибиторов АПФ в виде мучительного сухого кашля или ангионевротического отека для выбора сартанов как противогипертензивных препаратов, т.е. БРА II обрели самостоятельную ценность. Наработана серьезная доказательная база по применению этих препаратов, и, разумеется, появилась потребность провести сравнительную оценку эффективности и безопасности отдельных представителей класса сартанов. Этой цели служит мета–анализ Nixon R.M. с соавт. [4], посвященный оценке сравнительной эффективности валсартана в лечении АГ в ряду прочих БРА II. В настоящее время в России широко используются лозартан, валсартан, реже – эпросартан, ирбесартан, телмисартан, кандесартан. За каждым из этих препаратов значительная доказательная база, например лозартан доказал свои преимущества перед атенололом в лечении АГ с сопутствующей гипертрофией левого желудочка (исследование LIFE), ирбесартан доказал наличие у него мощного нефропротективного потенциала (исследования IDNT и IRMA–2), эпросартан эффективно предупреждал развитие повторного инсульта в исследовании MOSES. Что касается сравнения противогипертензивной активности различных сартанов, то в большинстве посвященных этому вопросу мета–анализов сообщалось о сопоставимой активности различных БРА [5], однако при этом либо не рассматривалась эффективность валсартана, либо он применялся в низкой дозе (до недавнего времени валсартан применялся в основном в дозе 80 мг/сут., в то время как с 2001 г. рекомендуемая стартовая доза валсартана для лечения АГ 160 мг/сут., максимальная – 320 мг/сут.).
| Рис. 1. Клинические ситуации в пользу применения БРА II в рекомендациях ВНОК |
 |
Валсартан поистине «препарат–многостаночник», доказавший свою эффективность при АГ (исследование VALUE), при хронической сердечной недостаточности (исследование Val–HeFT), при остром инфаркте миокарда (исследование VALIANT). Общее число включенных в эти исследования пациентов превысило 34 тыс. человек. Валсартан стал первым препаратом из класса БРА II, который был зарегистрирован для лечения больных ХСН. В исследовании Val–HeFT [7] в течение 2 лет наблюдали 5010 больных ХСН со II– IV ФК NYHA, которые получали рекомендуемую терапию, в составе которой могли назначать иАПФ, бета–блокаторы, диуретики и дигоксин. К проводимой терапии был добавлен либо валсартан в стартовой дозе 40–80 мг с последующим увеличением до 160 мг 2 раза/сут., либо плацебо. Добавление валсартана к проводимой терапии, включая иАПФ в 93% случаев, привело к снижению риска развития смертности и сердечно–сосудистой заболеваемости на 13,2% (р=0,009) в основном за счет снижения количества госпитализаций вследствие ХСН. В подгруппе пациентов, не получавших иАПФ, применение валсартана снижало риск общей смертности на 33,1 % (р = 0,017), а риск развития комбинированной точки (общая смертность + сердечно–сосудистые события) – на 44 % (р = 0,0002). В исследовании Val–HeFT было показано, что при лечении валсартаном наблюдается достоверное по сравнению с плацебо, снижение активности мозгового натрийуретического пептида, считающегося одним из важных маркеров прогрессирования сердечной недостаточности. При лечении валсартаном отмечалось и меньшее, по сравнению с группой плацебо, нарастание активности норадреналина – еще одного неблагоприятного прогностического маркера. В результате дополнительного анализа результатов исследования Val–HeFT была обнаружена способность этого препарата предупреждать развитие мерцательной аритмии. В исследовании VALIANT [8] изучалось применение валсартана у пациентов с острым инфарктом миокарда, осложненным сердечной недостаточностью и/или дисфункцией левого желудочка, с использованием БРА в сравнении с иАПФ на течение острого ИМ. В исследование включались больные в течение 0,5–10 дней после развития ИМ. По данным этого исследования, монотерапия валсартаном в дозе 160 мг 2 раза/сут оказалась такой же эффективной в лечении постинфарктных больных с дисфункцией левого желудочка и/или сердечной недостаточностью, как и монотерапия каптоприлом в дозе 50 мг 3 раза/сут., ценность применения которого в подобной ситуации была доказана ранее. Следует отметить лучшую переносимость валсартана. Вместе с тем комбинированная терапия ингибитором АПФ и БРА не давала дополнительного улучшения прогноза у больных после ИМ по сравнению с монотерапией иАПФ. По итогам VALIANT оба препарата можно в равной степени применять при остром инфаркте миокарда у пациентов с высоким риском сердечно–сосудистых осложнений. Выбор будет, очевидно, определяться переносимостью и стоимостью этих препаратов. В исследовании KYOTO HEART [9] оценивали у 3031 пациента эффективность валсартана, присоединенного к проводимой антигипертензивной терапии у больных с неконтролируемой АГ и высоким риском осложнений. Пациенты были рандомизированы в группу получающих дополнительно валсартан в дозе до 320 мг/сут. и группу получающих другие препараты за исключением БРА. В качестве первичной конечной точки была сумма всех фатальных и нефатальных сердечно–сосудистых событий. В среднем период наблюдения составил 3,3 года. В обеих группах был достигнут одинаковый контроль за уровнем АД: давление снизилось со 157/88 до 133/76 мм рт.ст. У больных группы валсартана по сравнению с другой группой достоверно снизился риск развития событий первичной конечной точки на 45%. Таким образом, присоединение валсартана к лечению недостаточно контролируемых больных АГ не только позволило добиться целевого уровня, но и значительно улучшило прогноз.
В исследовании VALUE (2004) также осуществлялось увеличение дозы валсартана с 80 мг до 160 мг/сут. [10], поскольку в этих исследованиях была продемонстрирована высокая эффективность валсартана, целесообразно сравнить эффект валсартана и других сартанов в сопоставимых дозах. Nixon R.M. с соавт. [4] при проведении в 2009 г. крупного мета–анализа (13 тыс. пациентов) учел недостатки проведенных ранее мета–анализов, отобрав для анализа исследования, в которых различные сартаны назначались в сопоставимых дозах, в том числе исследования с валсартаном, используемым в более высоких дозах (160–320 мг/сут.). Как уже сообщалось ранее, целью мета–анализа было изучение сравнительной эффективности разных сартанов в снижении систолического (САД) и диастолического (ДАД) АД у больных с эссенциальной АГ. Были проанализированы результаты краткосрочных проспективных рандомизированных двойных слепых контролируемых исследований, проведенных за период с октября 1997 г. по май 2008 г. (более 10 лет), в которых у больных АГ (лица старше 18 лет с 1 –2 степенью повышения АД, ДАД – 90–115 мм рт. ст.) применялся хотя бы один сартан. Были использованы англо– и германоязычные базы данных MEDLINE, EMBASE, EMBASE Alert, а также базы данных Кокрановских систематических обзоров и клинических исследований и научного цитирования (SciSearch). Всего в мета–анализ было включено 31 исследование (13110 больных), распределение по количеству исследований с применением различных сартанов приведено на рисунке 2. Авторы мета–анализа включали только те исследования, в которых титрование доз препаратов либо не проводилось, либо проводилось форсированно. При этом дозировки сартанов классифицировались как «низкие», «средние» и «высокие» (рис. 3).
| Препарат | Количество исследований |
| Лозартан | 13 |
| Валсартан | 12 |
| Кандесартан | 6 |
| Ирбесартан | 6 |
| Телмисартан | 5 |
| Олмесартан | 2 |
| Препараты | Низкие дозы, мг | Средние дозы, мг | Высокие дозы, мг |
| Лозартан | 50 | 100 | — |
| Валсартан | 80 | 160 | 320 |
| Кандесартан | 8 | 16 | 32 |
| Ирбесартан | — | 150 | 300 |
| Телмисартан | — | 40 | 80 |
| Олмесартан | 10 | 160 | 320 |
При оценке результатов мета–анализа авторы прежде всего отметили связь эффекта всех БРА с используемой дозой препаратов. На рисунке 4 приведены данные по снижению САД и ДАД при использовании различных доз валсартана. Причем валсартан в дозе 160 мг оказался эффективнее лозартана в дозе 100 мг и ирбесартана в дозе 150 мг/сут. Таким образом, валсартан снижал САД достоверно лучше, чем лозартан (на 3,31 мм рт.ст.) и ирбесартан (на 3,56 мм рт.ст.), и ДАД – лучше, чем лозартан (на 1,95 мм рт. ст.), ирбесартан (на 2,06 мм рт.ст.) и кандесартан (на 1,85 мм рт.ст. Других статистически достоверных различий в эффективности различных сартанов, при использовании их в эквивалентных дозах обнаружено не было.
Для уточнения этих данных авторы мета–анализа рекомендуют провести специально спланированные рандомизированные клинические исследования с прямым сравнением разных препаратов друг с другом.
В настоящее время на российском рынке появился препарат Валз (фармацевтическая компания Актавис). Отличительной особенностью Валза является наличие всех трех зарегистрированных показаний, как и у оригинального валсартана: АГ, ХСН и повышение выживаемости пациентов с острым инфарктом миокарда. Это может быть важно для практического врача при выборе назначаемого препарата. Следует отметить и наличие комбинированного препарата валсартан+гидрохлоротиазид Валз Н, более выраженно снижающего АД по сравнению с валсартаном. По результатам исследования на биоэквивалентность доказано, что Валз эквивалентен оригинальному валсартану. Валз сочетает высокую эффективность и сравнительно невысокую стоимость, что делает препарат доступным для большинства пациентов.
Литература:
1. Kearney PM, Whelton M, Reynolds K, Muntner P, Whelton PK, He J. Global burden of hypertension: analysis of worldwide data. Lancet 2005; 365: 217–23.
2. Whitworth JA. World Health Organization (WHO) International Society of Hypertension (ISH) statement on management of hypertension. J Hypertens 2003; 21: 1983–92.
3. Hyman DJ, Pavlik VN. Characteristics of patients with uncontrolled hypertension in the United States. N Engl J Med 2001; 345: 479–86.
4. Nixon R.M., Muller E., Lowy A., Falvey H. Valsartan vs. other angiotensin II receptor blockers in the treatment of hypertension: a meta–analytical approach. Int J Clin Pract 2009; 63 (5): 766–775.
5. Baguet JP, Legallicier B, Auquier P, Robitail S. Updated meta–analytical approach to the efficacy of antihypertensive drugs in reducing blood pressure. Clin Drug Investig 2007; 27: 735–53.
6. Conlin P.R., Spence J.D., Williams B. et al. Angiotensin II antagonists for hypertension: are there differences in efficacy? Am J Hypertens 2000; 13 (4 Pt 1): 418–26
7. Cohn J.N., Tognoni G. A randomized trial of the angiotensin_receptor blocker valsartan in chronic heart failure. N Engl J Med 2001;345: 1667–75
8. Pfeffer M.A., McMurray J.J., Velazquez E.J. et al. Valsartan, captopril, or both in myocardial infarction complicated by heart failure, left ventricular dysfunction, or both. N Engl J Med 2003; 349: 1893–906
9. Sawada, T. et al. Effects of valsartan on morbidity and mortality in uncontrolled hypertensive patients with high cardiovascular risks. KYOTO HEART Study. Eur Heart J 2009, Oct; 30 (20): 2461–9.
10. Julius S., Kjeldsen S.E., Weber M. et al. Outcomes in hypertensive patients at high cardiovascular risk treated with regimens based on valsartan or amlodipine: the VALUE randomised trial. Lancet 2004; 363: 2022–31.
11. Giles T.D., Oparil S., Silfani T.N. et al. Comparison of increasing doses of olmesartan medoxomil, losartan potassium, and valsartan in patients with essential hypertension. J Clin Hypertens (Greenwich) 2007; 9: 187–95.
