Определение целевых уровней артериального давления при гипотензивной терапии у больных с тяжелой, резистентной к терапии, артериальной гипертонией
СтатьиОпубликовано в журнале:
"Российский кардиологический журнал"
»» N 2 2008
Люсов В.А.1, Харченко В.И1, Какорин В.А.1, Корякин М.В.2, Вирин М.М.3, Потиевский Б.Г.4, Видьманова И.Е4
Российский государственный медицинский университет 1;
Лечебно-реабилитационный центр Росздрава 2;
Академия экономики, финансов и права3;
Центральная клиническая больница Гражданской авиации4, Москва
| “Лечить надо не болезнь, а больного”
М.Я.Мудров |
Артериальная гипертония (АГ) является одним из важнейших факторов, который существенно увеличивает смертность и ухудшает прогноз жизни [1]; адекватная терапия АГ, напротив, приводит к снижению риска осложнений и увеличению продолжительности жизни [2].Это положение является аксиомой и не имеет принципиальных возражений. Одним из важных моментов терапии АГ является снижение повышенного артериального давления (АД) и достижение в результате проводимого лечения так называемых “целевых уровней” (ЦУ) АД.
В Рекомендациях по диагностике и лечению артериальной гипертензии Европейского общества по артериальной гипертензии и Европейского общества кардиологов (2003) дается такое определение ЦУ АД: “Можно рекомендовать снижение как САД, так и ДАД менее 140/90 мм рт. ст. и даже до более низких цифр при хорошей переносимости у всех больных АГ и менее 130/80 мм рт. ст. у больных сахарным диабетом (СД)” [3].
Такие же критерии ЦУ АД даны и в “Седьмом отчете Совместной национальной комиссии по предупреждению, выявлению, оценке и лечению высокого артериального давления США” (JNC VII) – 2003 год [4–6], и в последних Российских рекомендациях (второй пересмотр): “Профилактика, диагностика и лечение артериальной гипертензии” (ВНОК, 2004), в которых сформулировано: “ЦУ АД при лечении АГ принят Подобной точки зрения придерживаются представители крупнейших кардиологических учреждений страны.
С.А. Шальнова и соавт., ссылаясь на авторитетных исследователей [3,4], пишет: “Полученные данные недвусмысленно свидетельствуют о том, что основным условием влияния на исходы АГ является достижение так называемых “целевых уровней” (ЦУ) АД, которые составляют для всех больных АГ Ценное и важное для лечения больных АГ разъяснение, определяющее ЦУ АД в зависимости от возраста, дано в статье И.Е. Чазовой и Л.Г. Ратовой: “Множество завершившихся в последние годы исследований наглядно продемонстрировали, что только “жесткий” контроль АД может достоверно снизить частоту ССО – ИМ, ОНМК, ХСН у пациентов с АГ. С учетом результатов этих исследований были определены желательные целевые уровни АД. Согласно рекомендациям экспертов ВОЗ и МОАГ (1999) [10,11], целевым уровнем АД для лиц молодого и среднего возраста, а также для больных СД признаны величины, не превышающие 130/85 мм рт. ст., а для лиц пожилого возраста – 140/90 мм рт. ст” [9].
К сожалению, разделение ЦУ АД для разных возрастных групп больных АГ “не прижилось” в научной российской литературе, в частности такого определения нет и в последних рекомендациях ВНОК, 2004 [9].
Ценные для клинической практики положения содержатся в “Рекомендациях по диагностике и лечению артериальной гипертензии Европейского общества по артериальной гипертензии и Европейского общества кардиологов”, 2003 [3]: “Цель, к которой следует стремиться, так же, как и реально достигнутая, может существенно зависеть от исходного уровня АД, особенно САД, тогда как снижение последнего менее 140 мм рт. ст. может оказаться сложной задачей, особенно у пожилых пациентов. Целевые уровни АД не являются столь жесткими, как это было представлено в предыдущих рекомендациях [12,13], настоящие рекомендации являются гибкими, оставляют врачу больше свободы и ответственности в принятии решения по конкретному пациенту” [3].
Мы считаем, что тезис об уровнях ЦУ АД требует весьма серьезного уточнения и разъяснения, исходя из особенностей клинического течения АГ у конкретных больных.
С помощью современной комбинированной терапии можно снизить АД до ЦУ Целевые уровни АД при лечении АГ различной степени тяжести
Целевые уровни АД в зависимости от особенностей клинического течения АГ.
Основной целью лечения больных АГ является максимальное снижение риска сердечно-сосудистой заболеваемости и смертности. Достижение этой цели требует коррекции всех модифицируемых факторов риска, включая курение, дислипидемию, диабет, а также адекватное лечение ассоциированных клинических состояний наряду с собственно снижением АД [3].
Согласно европейским рекомендациям 1994 и 1998 гг. и рекомендациям ВОЗ/МОАГ 1999 г. [10,11], рекомендовалось начинать лечение АГ у больных 1–2 степени тяжести. Однако в 2003 году в “Рекомендациях по диагностике и лечению артериальной гипертензии Европейского общества по артериальной гипертензии и Европейского общества кардиологов, 2003 г.” [3], заявлено, что “сохраняя уважение к вышеуказанным рекомендациям, нынешние не ограничиваются больными АГ степени 1–2, но распространяются на пациентов с высоким нормальным АД [5].
Однако в “Рекомендациях” подчеркнуто, что они созданы Комитетом экспертов, назначенных ЕОАГ и ЕОК на основе лучших имеющихся доказательств по всем основным пунктам и носят скорее образовательный, чем регламентирующий характер [3].
Целевые уровни АД при лечении мягкой АГ
Ю.А.Карпов приводит данные клинических исследований INVEST, 2003; EUROPA, 2003; ACTION, 2004; PEACE, 2004; CAMELOT, 2004 в которых изучалось снижение АД с помощью разных антигипертензивных препаратов (АГП) с плацебо-контролем у больных стабильной ИБС, которая в каждом исследовании сочеталась с АГ у 100-27% больных [14].
В этих исследованиях исходное АД в среднем по группам было 159/93-129/78 мм рт. ст.; достигнутое в результате лечения АД (верапамил, атенолол, периндоприл, и др. АГП с плацебо-контролем) снизилось до 31/77 – 124/75 мм рт. ст.; снижение на 19/10 – 4/4 мм рт. ст. [14].Как видим, у большинства больных отмечалось наличие мягкой гипертонии или даже нормальное АД (129/78 мм рт. ст.), поэтому закономерно, что во всех группах леченных больных удалось достичь в среднем по группе нормального уровня АД (т.е был достигнут целевой уровень Эти данные убедительно доказывают, что у больных мягкой АГ безопасным целевым уровнем АД являются показатели Мы считаем, что тезис об уровнях ЦУ АД требует весьма серьезного уточнения и разъяснения, исходя из особенностей клинического течения АГ у конкретных больных.
С помощью современной комбинированной терапии можно снизить АД до ЦУ В крупнейшем российском исследовании РОСА 2 [14а], в котором приняли участие 20 центров из 19 городов России, полностью завершили исследование 1181 больной (87,2 %). В группе больных А, которые получали ступенчатую комбинированную гипотензивную терапию, через 16 недель лечения ЦУ АД (<140/90 мм рт. ст.) достигли 97,2 % [14а]. Однако обращают на себя внимание исходные цифры АД у больных этой группы до начала лечения: 163,1±11,6/97,5±7,4 (135–208/60,0–126) мм рт. ст.; через 16 недель лечения был достигнут уровень АД 129,3±7,3/80.8 ±5,3 мм рт. ст.; дельта АД 0–16 = 33,8±11,8/-16,7±7,2 мм рт. ст. (р <0,0001) [14а]. Т.е., исходя из средних цифр исходного АД до лечения, большинство больных по тяжести АГ можно отнести к мягкой гипертонии или к АГ 1–2 степени по классификации ВНОК, 2004 [7].
Целевые уровни АД при лечении тяжелой АГ.
Более сложен вопрос о цифровых величинах целевого уровня АД у больных с тяжелой АГ (3–4 стадии по классификации JNS-5 и 3 степени по классификациям JNS-6 [15] и ВНОК, 2004) [7], что соответствует IIIII стадии ГБ по классификации, принятой Россздравом [15] и, тем более, у больных злокачественной АГ.
Немало больных ГБ, как правило, с длительным анамнезом гипертонии, у которых АД находится на высоких цифрах, например 180/120 мм рт. ст. или выше, которое может подниматься до еще более высоких цифр, если заболевание протекает с гипертоническими кризами.
В порядке дискуссии возникает вопрос: следует ли считать АД 140/90 мм рт. ст. целевым уровнем АД при лечении данного больного?
Теоретически у таких больных с помощью комбинированной многокомпонентной терапии АД может быть снижено до целевого уровня Возникает вопрос: следует ли считать указанное реально достигнутое минимальное АД, удовлетворительно переносимое больным АГ, целевым уровнем АД для данного больного при последующей его госпитализации в стационар с более высоким давлением?
Что касается злокачественной АГ, то ЦУ АД наиболее реально, по нашему мнению, устанавливать после операции пересадки почки.
Целевые уровни АГ при лечении ИСАГ
Как считает О.Д.Остроумова, целевой уровень САД для больных ИСАГ с сосудистой деменцией (СД) составляет менее 140 мм рт. ст., а для всех остальных пациентов независимо от возраста – менее 140 мм рт. ст. Необходимо помнить, что особенно у пожилых пациентов АД следует снижать медленно и достигать целевого уровня АД постепенно, в среднем в течение месяца (кроме ситуаций с гипертоническими кризами), в противном случае можно спровоцировать развитие ишемии головного мозга [16]. Нормализация уровня САД сопровождается у больных СД улучшением или стабилизацией показателей интеллектуальных функций, тогда как в аналогичных случаях без контроля АД эти показатели ухудшаются [16].
По мнению О.Д.Остроумовой, лечение ИСАГ – очень непростая задача, поскольку нормализовать уровень САД труднее, чем уровень ДАД. Так, при использовании одной и той же схемы лечения целевой уровень ДАД Предостережения об опасности неадекватно низкого для конкретного человека снижения АД.
Наличие и выраженность поражения органов мишеней (ПОМ) и ассоциированных клинических состояний (АКС) ограничивают уровни снижения АД у больных с тяжелой АГ.
ЦУ АД при окклюзирующем (стенозирующем) атеросклерозе коронарных артерий.
Ю.А. Карпов пишет: “Как показали результаты крупных клинических исследований с применением АГП, значительное снижение САД и ДАД не только не ухудшало, но и улучшало прогноз больных стабильной стенокардией как сопутствующей АГ, так и без нее. Но следует иметь в виду, что есть данные и о повышении риска коронарных осложнений при значительном снижении АД. В исследовании SHEP у пожилых больных с ИСАГ было показано, что ДАД менее 55–60 мм рт. ст. ассоциируется с увеличением частоты развития основных ССО, включая инфаркт миокарда [14, 17]. Больные с выраженным (окклюзирующим) поражением коронарных артерий и/или ГЛЖ имеют более высокий риск коронарных осложнений при низком ДАД. К аналогичным выводам пришли и авторы других крупнейших работ по данному вопросу [18-20].Существование J-образной зависимости между коронарными осложнениями и интенсивным снижением АД у курящих, больных АГ, было подтверждено в 2003 году в исследовании HOT [21].
Взаимосвязь уровня САД и перфузии головного мозга при различной патологии сосудов, питающих головной мозг, отмечена в работах неврологов [22] (подробное изложение ниже).
Согласно Европейским “Рекомендациям по диагностике и лечению артериальной гипертензии” [3], у большинства больных следует ожидать наличия других факторов риска, поражения органов-мишеней и ассоциированных состояний, что будет определять выбор препарата. Более того, большинству пожилых пациентов требуется проведение двухкомпонентной и более терапии, особенно в связи с трудностью достижения целевых значений САД менее 140 мм рт. ст.
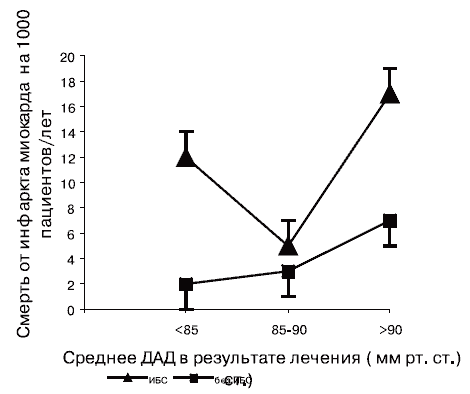
Рис. 1. Соотношение между уровнем смертности от инфаркта миокарда у больных с ишемической болезнью сердца (ИБС) и без ИБС с уровнем снижения АД под влиянием лечения (согласованные с возрастом) [ 20].
Оптимальный уровень ДАД менее понятен. При анализе историй болезней после выписки из стационара, группа исследователей SHEP оценивала роль ДАД на фоне терапии у больных с ИСАГ [17]. Они пришли к заключению, что достижение уровня АД менее 70 мм рт. ст. и особенно менее 60 мм рт. ст. сопровождается увеличением риска и имеет плохой прогноз. В связи с этим необходимы дальнейшие исследования, которые прояснили бы вопрос, насколько значимо может быть снижен уровень ДАД у пациентов с ИСАГ и трудностью нормализации САД [3].
Известный российский геронтолог Л.Б.Лазебник и соавт. пишут: “Если у пациента с артериальной гипертонией нет ишемической болезни сердца (ИБС), то в отношении такого больного верно утверждение – чем ниже АД, тем больше продолжительность жизни” [24]. То есть, возможно снижение АД до нормы. Значительное снижение АД при наличии ИБС может вызвать ухудшение коронарного кровообращения. Риск развития инфаркта миокарда наиболее низок при поддержании диастолического АД в пределах 90 мм рт. ст. и начинает расти при его более высоком или более низком уровне. Темп снижения АД также имеет важное значение. При неотложных состояниях следует стремиться к снижению АД в течение 24 часов. В остальных случаях обычно нет оснований принимать экстренные меры. Для больных пожилого и старческого возраста допустимо снижение АД до целевых значений в течение 3–4 недель, что уменьшает риск развития осложнений и улучшает переносимость лекарственных препаратов.
Лечение больных, страдающих одновременно ИБС и АГ, требует комплексного подхода, то есть одновременного воздействия на оба состояния. Первостепенной задачей лечения является максимальное снижение общего риска сердечно-сосудистых заболеваний и смертности за счет предупреждения ИМ, мозгового инсульта и хронической почечной недостаточности, обратного развития поражения органов-мишеней [3–6,25,26].
В качестве задач второго ряда следует рассматривать уменьшение клинических проявлений и улучшение качества жизни, а именно: уменьшение частоты и продолжительности приступов стенокардии, а также предотвращение ее прогрессирования [26].
Задачей собственно антигипертензивной терапии является достижение и стабильное поддержание АД на целевом уровне (ниже 140/90 мм рт.ст.) [25, 3-6], [24].
ЦУ АД при неврологической патологии
Мы считаем, что для лечения больных с ЦВБ, в том числе перенесших инсульт, оценки клинических особенностей течения заболевания, в частности поражения ЦНС и артерий, питающих головной мозг, и современной адекватной терапии нужны специальные знания.
Управлять артериальным давлением таких больных должны, в первую очередь, врачи-неврологи или неврологи совместно с кардиологами.
Это связано с тем, что, по данным Симоненко В.Б. и соавт., среди ассоциированных состояний у больных АГ, у которых в анамнезе не было инсульта (500 больных, средний возраст – 64,8 ± 6,2 года), ИБС отмечалась у 63 % исследованных; у больных, перенесших мозговой инсульт (467 больных, средний возраст – 66,2±4,3 года) ИБС была диагнасцирована в 82 % случаев [27].
Таким образом, для больных с ЦВБ в 63–82 % случаев характерно сочетание этого заболевания с ИБС, и этот факт необходимо учитывать кардиологам при определении оптимального ЦУ АД у таких больных.
Как пишет известный российский невролог В.И.Скворцова, АГ отмечается у большинства больных, перенесших мозговой инсульт (МИ): “Результаты эпидемиологического мониторирования МИ методом Национального регистра, проводившегося в 2001–2004 году в 25 регионах РФ под эгидой Национальной ассоциации по борьбе с инсультом, показали, что АГ представлена у 92,5 % больных, перенесших МИ. Достоверных различий в частоте выявления АГ при разных типах МИ не было: она составляет при ишемическом МИ 92,3 %, при геморрагическом – 92,6 %” [28].
По мнению академика РАМН Е.И.Гусева и члена-корреспондента РАМН В.И.Скворцовой, неадекватная агрессивная антигипертензивная терапия является вторым ведущим фактором риска развития МИ [29,28].
При наличии дисциркуляторной энцефалопатии (ДЭ) антигипертензивные препараты надо назначать индивидуально, с осторожностью, с постепенным подбором оптимальных доз (снижение САД на 15 % и ДАД на 10 %), иначе резко нарастает угроза развития гипоперфузии головного мозга. Особенно постепенно и осторожно следует снижать АД при вертебро-базилярной недостаточности и появлении очаговой неврологической симптоматики; при этом больной должен находиться в горизонтальном положении в связи с возможностью более резкого снижения АД в ортостазе [28].
Так, например, по данным Somes W. et al, при снижении ДАД ниже 50 мм рт. ст. у таких больных риск развития инсульта возрастает в два раза, а при еще большем снижении ДАД риск возрастает до опасных границ! (рис.2) [17].
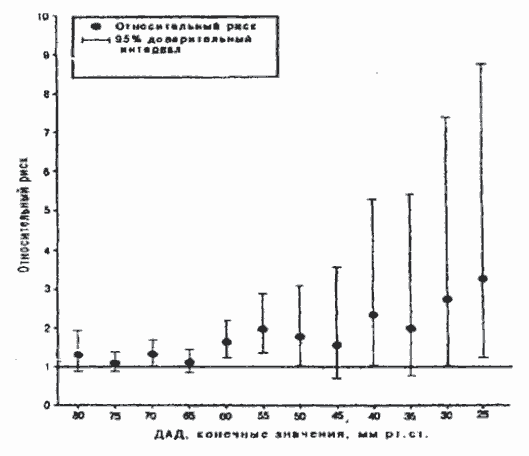
Рис.2. Скорректированные оценки величин относительного риска ССЗ по категориям принятых разделительных точек ДАД [17].
А.О.Конради, научные работы которой отличаются очень высоким качеством, в одной из своих последних работ делает два очень важных научно-практических вывода:
- Адекватная антигипертензивная терапия сопровождается существенным снижением риска развития деменции любой этиологии.
- Полная нормализация АД у пожилых пациентов с длительным анамнезом гипертонии может способствовать углублению хронической ишемии мозга и нарастанию выраженности когнитивных функций.
Чрезмерное снижение АД может провоцировать нарастание мнестикоинтеллектуальных нарушений, вызванных снижением мозгового кровотока вследствие нарушения его ауторегуляции. Это еще раз доказывает необходимость более осторожного отношения к назначению антигипертензивной терапии и достижению целевых значений АД у больных с цереброваскулярной патологией [30].
Академик РАМН Н.В.Верещагин и его сотрудники считают, что камнем преткновения в спорах о стратегии и тактике лечения АГ при ЦВБ между терапевтами и неврологами является вопрос о целевом уровне АД [22, 23, 23a]. Сегодня сложились два подхода к определению оптимального уровня снижения АД у больных АГ с целью профилактики развития ССО и цереброваскулярных осложнений. “Кардиологический подход” базируется на результатах контролируемых, многоцентровых исследований, включающих преимущественно лиц с неосложненной АГ, и рекомендует врачам достижение для всех больных единого “целевого уровня АД независимо от его исходных показателей; “неврологический подход” основан на клиническом изучении мозгового кровотока у лиц, страдающих АГ с церебральной патологией [31].
Резюмируя данные литературы, можно сделать вывод об отсутствии единого целевого уровня АД для больных, уже имеющих цереброваскулярную патологию.
Особенности лечения АГ у больных с церебральными осложнениями обусловлены тем, что эти пациенты имеют различные адаптационные возможности сосудистой системы мозга и мозгового кровотока.
Установлено [32], что инцидентность повторного инсульта и его сопряженность с величиной поддерживаемого АД различаются в зависимости от характера уже состоявшегося инсульта (инфаркт мозга или кровоизлияние). Выявлены особенности динамики риска повторного инсульта в зависимости от уровня ДАД при различных подтипах ишемического инсульта. Было обнаружено, что после атеротромботического инсульта наименьшая частота рецидива церебрального события отмечалась при ДАД 85-89 мм рт. ст., а после лакунарного – 80-84 мм рт. ст. Исследования последних лет показали, что уровень не ДАД (как считалось ранее), а САД является более значимым фактором риска ССО, в том числе и инсульта. У больных с окклюзией сонной артерии наименьший риск при САД 140–150 мм рт. ст. В случаях двустороннего стеноза сонных артерий риск инсульта > 70 %, наименьший риск развития инсульта отмечен при САД 160–170 мм рт. ст. [33].
Однако каких либо сведений о “целевых” уровнях АД для больных с окклюзирующим поражением позвоночных артерий, сифона сонной артерии и интракраниальных артерий пока не получено.
С целью оптимизации подходов к лечению АГ при цереброваскулярной патологии в НИИ неврологии РАМН определены маркеры церебральной гипоперфузии при неадекватном снижении АД. При сохранности адаптационного резерва церебральной гемодинамики САД допустимо снижать на 20 % и ДАД – на 15 %. При выраженных нарушениях в системе регуляции мозгового кровотока, т.е. при наличии у больного маркеров гипоперфузии головного мозга снижение САД не должно быть более 15 %, ДАД – 10 % от стартового уровня [23 а, 34].
Таблица 1
Нормативы для средних величин АД по данным СМАД (J. Staessen, 1998) [41].
| Артериальное давление | Нормотония | Гипертония |
|---|---|---|
| Суточное АД, мм рт. ст. | <130/80 | >135/85 |
| Дневное АД, мм рт. ст. | <135/85 | >140/90 |
| Ночное АД. мм рт. ст. | <120/70 | >125/80 |
Хотя, на первый взгляд, предлагаемая степень снижения АД незначительна, на практике она составляет ощутимую величину: например, при АД 200/120 мм рт. ст. достигает 30–40/12–19 мм рт. ст. В то же время известно, что снижение систолического АД на 12 мм рт.ст. а диастолического – на 5 мм рт. ст. обусловливает уменьшение риска повторного инсульта на 34 % [23 а, 34].
Особенности лечения АГ у больных с церебральными осложнениями обусловлены тем, что эти пациенты имеют различные адаптационные возможности сосудистой системы мозга и мозгового кровотока. Поэтому необходимость достижения единого уровня АД в результате антигипертензивного лечения представляется весьма сомнительной. По-видимому, речь должна идти об адекватной относительной редукции АД, которая соответствует возможностям ауторегуляии мозгового кровотока и не приведет к дальнейшему ухудшению церебральнй перфузии. Следовательно, у больных АГ даже в случае небольшого, но длительного (в течение 3–5 лет) и стабильного снижения АД можно ожидать значительного улучшения отдаленного прогноза [23 а, 34].
Суточное мониторирование артериального давления (СМАД) и уровни нормального и оптимального АД.
Необходима информация о ДАД и САД не только утром (после прихода врача к больному после утренней конференции в 9–11 часов, так называемое “офисное” измерение АД, но и мониторирование АД с целью установления его уровня, когда оно может быть самым низким, например в ранние утренние часы. Тем более это необходимо делать при подборе гипотензивного лечения с помощью новых гипотензивных препаратов, на которые реакция АД больного неизвестна.
М.С.Кушаковский считает, что, определяя давление, следует учитывать его суточные колебания, которые у больных ГБ и у здоровых людей имеют одинаковую направленность: наиболее низкое во время сна, АД отчетливо возрастает к утру; у некоторых лиц оно повышается более постепенно, достигая максимума в часы дневной активности. Разница между самыми высокими и самыми низкими цифрами давления в течение суток у здоровых людей редко превышает 33 мм рт. ст. для систолического и 10 мм рт. ст. для диастолического давления; при ГБ эти колебания выражены резче [35]. Нельзя забывать и о различных неточностях в определении АД. В идеальных условиях при нормотензии погрешность метода Короткова равняется ±8 мм рт. ст. [35].
Однако уровни (параметры) нижней и высшей границ АД у здоровых нормотоников, по данным СМАД, в дневные и ночные часы четко не установлены, особенно с учетом возраста.
В последние годы (2004, 2006 гг.) активно изучается вопрос о так называемой “стресс-индуцируемой гипертонии” [36,37]. Доказано, что проведение нагрузочных психоэмоциональных тестов позволяет выявить лиц с повышенной стресс-реактивностью в виде избыточного прироста САД и ДАД [37]. По данным СМАД, к “стресс-индуцируемой гипертонии” можно отнести не только “гипертонию белого халата”, но и “гипертонию на рабочем месте”. По данным И.В.Осиповой, различие в рабочие и в выходные дни у машинистов локомотивных бригад составило для САД 15 мм рт. ст., для ДАД – 20 мм рт. ст. [36].
Как пишет проф. Е.Е.Гогин, сделана попытка определить оптимальную норму АД [38]. На практике этот уровень оказался предельно сближенным с артериальной гипотонией, а при отсутствии оговоренной нижней границы нормального АД – даже не отделенным от небезопасных форм коллаптоидных реакций.
Только позднее в JNS-7 было указано, что не рекомендуется уменьшать ДАД ниже 55–60 мм рт. ст. из-за повышения (“J6образная” зависимость от уровня АД) риска развития осложнений.
Однако снижение ДАД до 55–60 мм рт. ст., как мы считаем, с помощью гипотензивных препаратов, когда давление может снизиться и до более низких значений, является небезопасным. Как писал в одной из своих последних работ известный кардиолог и исследователь артериальных гипертензий Г.Г. Арабидзе, нормальным является АД 140/90 мм рт. ст. и ниже; критический уровень АД составляет 60/40 мм [39].
Кроме того, следует вспомнить что артериальной гипотонией считают уровни АД 100/60 мм рт. ст. в возрасте до 25 лет и 105/65 мм рт. ст. у лиц старше 40 лет [40].
Определение ЦУ АД по данным только офисного измерения АД недостаточно обосновано. Необходим контроль АД по данным СМАД и других методов объективного контроля состояния перфузии в жизненно важных органах.
Использование СМАД позволяет более доказательно выявлять АГ и оценивать эффект антигипертензивной терапии [41–43].
Степень ночного снижения АД – важный прогностический и диагностический критерий. Оценивая суточный профиль АД, следует помнить, что у здоровых людей и большинства больных АГ в обычных условиях жизнедеятельности наиболее низкое АД отмечается во время ночного сна, приблизительно в 3 ч ночи. Ближе к утру АД начинает повышаться (особенно быстро между 5-ю и 7-ю часами) и к 10–11 часам достигает максимума. После полудня АД несколько снижается, а затем вновь возрастает, образуя второй “пик” в районе 16–18 часов. Дальше отмечается сначала плавное, а затем выраженное снижение АД, отражающее наступление ночного сна. Описанные изменения АД носят название суточного (циркадного) ритма и отражают циклическое изменение физиологической активности, связанное с чередованием периодов сна и бодрствования [41–43].
На суточном профиле АД отчетливо видны непериодические колебания различной амплитуды и продолжительности, связанные с изменением уровня физических и психоэмоциональных нагрузок в процессе повседневной деятельности человека. Эти колебания принято обозначать термином “вариабельность АД”.
Таким образом, визуальный анализ суточного профиля АД сводится к выделению и оценке трех его составляющих: среднего уровня АД, его суточного ритма и вариабельности [41–43]. Такой же подход используется и при количественной оценке результатов СМАД.
Расчет средних величин АД за все время исследования, а также отдельно для периодов сна и бодрствования, является стандартной процедурой обработки результатов СМАД. Средние величины АД могут использоваться как для диагностики АГ, так и для оценки проводимого лечения.
Верхней границей нормального уровня среднесуточного АД большинство авторов считают 135/85 мм рт. ст. Для среднедневных значений предложен уровень 129/84 мм рт. ст.; средненочных – 120/70 мм рт. ст. [41–43]. По данным Ohkubo T. et al., при среднесуточном АД более 135/80 мм рт. ст. увеличивается риск кардиоваскулярной смертности, а при АД менее 120/65 мм рт. ст. – риск смертности, не связанной с сердечно-сосудистыми заболеваниями [44].
Для анализа суточного ритма обычно рассчитывают показатель степени ночного снижения АД (СНСАД). Классификация больных АГ по степени СНСАД представлена в табл. 2.
Таблица 2
Классификация больных АГ по степени ночного снижения АД (СНСАД) [41].
| Название группы | Англоязычное название группы | СНСАД, % | Распространенность, % |
|---|---|---|---|
| Нормальная СНСАД | Dippers | 10–22 | 60–80 |
| Недостаточная СНСАД | Non-dippers | <10 | 20–25 |
| Избыточная СНСАД | Оvег-dippers | >22 | 15–20 |
| Устойчивое повышение ночного АД | Night-peakers | <0 | 3–5 |
Таблица 3
Показатели вариабельности артериального давления у здоровых лиц в течение суток [41]
| Показатель | Сутки | День | Ночь |
|---|---|---|---|
| СО САД мм рт. ст. | <15.2 | <15.5 | <14.8 |
| СО ДАД мм рт. ст. | <12.3 | <13.3 | <11.3 |
По степени ночного снижения АД выделяют следующие основные типы суточного ритма: “Dipper” – с нормальным снижением АД в ночное время на 10–20 %; “Non-dipper”– при недостаточном ночном снижении АД (менее 10 %); “Night-peaker” – с более высоким уровнем давления ночью и “Оvег-dipper” – при чрезмерном снижении ночного АД (более 20 %) [41–43]. Работы 90-х годов показали, что с поражением органов-мишеней коррелирует как недостаточное, так и чрезмерное ночное снижение АД. Доказано, что при чрезмерном ночном снижении АД увеличивается частота поражения головного мозга, а при недостаточном снижении АД в ночные часы у больных преобладает кардиальная симптоматика. Для определения степени снижения АД ночью чаще используют показатели САД.
Увеличение вариабельности АД у больных АГ является независимым фактором риска поражения органов-мишеней. В частности, большая вариабельность САД в дневные часы ассоциируется с увеличением риска развития атеросклероза и кардиоваскулярных событий. Нормальными показателями вариабельности САД считаются: менее 15,2 за сутки; менее 15,5 днем и менее 14,8 для ночного периода. Для ДАД – <12,3, <13,3, <11,3 соответственно [41–43].
По мнению экспертов Европейского общества артериальной гипертензии, в настоящее время суточное мониторирование АД становится обязательной методикой для выявления и лечения артериальной гипертензии, в том числе в клинико-фармакологических работах по оценке эффективности новых гипотензивных средств. Значение СМАД, по мере накопления данных, будет увеличиваться [45].
Колебания АД в течение суток у больных с начальными стадиями АГ по данным СМАД.
По данным Кадниковой Ю.В. и соавт., пограничная АГ (ПАГ) у пожилых больных характеризуется более высокой, нежели при других степенях АГ, распространенностью “гипертонии белого халата” (ГБХ), относительным преобладанием в ее структуре изолированной систолической гипертонии (ИСГ) (табл. 4) [46].
При ПАГ у пожилых больных наблюдается значительная, сравнимая с более высокими степенями АГ, “нагрузка давлением” за счет САД во все временные периоды.
У пожилых больных с ПАГ имеются выраженные разнообразные нарушения суточного ритма – как САД, так и ДАД. Пожилым больным с ПАГ присуща высокая вариабельность АД, преимущественно за счет САД. Обращает на себя внимание преобладание “Non-dippers” по САД, значительное число “Nondippers” по ДАД и “Night-peakers” по САД и ДАД. Анализ вариабельности АД показал, что 73 % больных ПАГ имели повышенную вариабельность АД, что незначительно ниже этого показателя при АГ 2 (82 %) и 3 степени (100 %), табл. 4 [46].
Таблица 4
Распределение пожилых больных по степени ночного снижения артериального давления при различных степенях артериальной гипертонии [46]
| Группы по СНС, % | Степень АГ | |||
|---|---|---|---|---|
| ПАГ | АГ I степ. | АГ II степ. | АГ III степ. | |
| Dippers | 29,4 | 41,7 | 36,3 | 0 |
| Non-dippers | 41,2 | 29,1 | 45,5 | 40 |
| Night-peakers | 21,6 | 16,7 | 18,2 | 20 |
| Оvег-dippers | 7,8 | 12,5 | 0 | 40 |
| Дипперы | 39,2 | 37,5 | 36,4 | 20 |
| Нон-дипперы | 33,3 | 33,4 | 54,5 | 40 |
| Найт-пикеры | 17,7 | 8,3 | 9,1 | 40 |
| Овер-дипперы | 9,8 | 20,8 | 0 | 0 |
По данным невролога Симоненко В.Б. и соавт., у больных АГ, угрожаемой развитием мозгового инсульта, отмечено перераспределение суточных профилей АД в пользу “Non-dippers” – “Оvег-dippers” и “Night-peakers” [27].
В работе невролога Машина В.В. и соавт., изучавшего СМАД при разных типах ишемического инсульта (ИИ), сделаны следующие выводы: 1. По степени снижения ночного АД к группе “Dippers” относилось 36,6 %, “Non-dippers” – 50 %,”Night-peakers” – 6,6 %, “Оvег-dippers” – 6,6 %; 2. ИИ чаще развивается в утренние часы. Статистически значимо развитие лакунарного ИИ в период с 4 до 10 часов. У всех больных ИИ отмечено недостаточное или чрезмерное снижение АД ночью. Для атеротромботического ИИ характерна высокая степень вариабельности САД в дневное время, для лакунарного – высокая степень утреннего подъема АД. Максимальная скорость утреннего подъема АД отмечена у больных с лакунарным ИИ в группах “Non-dippers” и “Оvег-dippers” [47]. Данные процитированных нами неврологов еще раз подтверждают наш тезис о том, что коррекцию АД у больных с нарушением мозгового кровообращения, в том числе и в анамнезе, должны проводить неврологи, так как для этого необходимы специальные знания, которыми не располагают терапевты и кардиологи.
До каких уровней снижают АД при лечении АГ под контролем СМАД.
Как видно из табл. 5, уровни ночного ДАД у больных даже с пограничной и мягкой АД не ниже 76 мм рт.ст.
Таблица 5
Диапазоны АД для классификации уровня гипертонии, используемые в программе Dabl [42]
| Нормотоники | Больные АГ | |||||
|---|---|---|---|---|---|---|
| низкое | нормальное | пограничное | мягкая | умеренная | тяжелая | |
| Уровни АД, мм рт. ст., день | ||||||
| САД | <100 | 100–135 | 136–140 | 141–155 | 156–170 | >170 |
| ДАД | <65 | 65–85 | 86–90 | 91–100 | 101–110 | >110 |
| Уровни АД, мм рт. ст., ночь | ||||||
| САД | <90 | 91–120 | 121–125 | 126–135 | 136–150 | >150 |
| ДАД | <50 | 51–70 | 76–85 | 76–85 | 86–100 | 100> |
Проанализируем до каких уровней снижают ДАД современные кардиологи при лечении АГ.
По данным A.F Sanjuliani. et al., полученным с помощью СМАД, снижение среднего дневного ДАД при лечении моксонидином (среднее АД) снижалось с 87,4±2,6 мм рт. ст. до 80,9 ± 2,6 мм рт. ст, среднее ночное ДАД при этом снижалось до 78,6 ± 3,2 мм рт. ст.; до такого же уровня снижали среднее дневное ДАД [48].
М.П.Савенков и С.В. Иванова проводили лечение АГ при патологии шейного отдела позвоночника под контролем СМАД. По данным авторов, до начало лечения ночное САД было 142± 8,5 мм рт. ст., ДАД – 84 ± 3,2; в результате фармакологической терапии САД составило 127±3,1 мм рт. ст,; ДАД – 75±3,0 мм рт. ст. [49].
В.Б Мычка, В.П. Масенко, И.Е.Чазова приводят данные СМАД при лечении больных АГ моксонидином на фоне избыточного веса [50]. По степени снижения АД были выделены три группы больных. В группе с минимальными значениями ДАД (дневные часы) было 64,8 ± 10,4 мм рт. ст до лечения и 60,8±7,0 мм рт. ст. после лечения; ночные показатели ДАД составили 56,±8,7 мм рт. ст. и 57,5±10,9 мм рт. ст. соответственно (отметим, что исходное АД было низким).
Определенный практический интерес представляют величины САД и ДАД в среднем за сутки, дневные и ночные показатели у детей и подростков по данным СМАД. Например, самые низкие показатели ДАД, которые отмечаются у здоровых детей и подростков в ночное время, у мальчиков колеблются в пределах 65–67 мм рт. ст., у девочек составляют 66 мм рт. ст. [51]. Как видим, у детей и подростков – и у девочек, и у мальчиков – показатели ДАД выше, чем рекомендуемые JNS-7 показатели ДАД (табл. 6).
Таблица 6
95-й процентиль средних уровней АД (мм рт. ст.) у детей и подростков в зависимости от роста (130–180 см) по данным СМАД [51]
| Время суток | АД (мм рт. ст.) | |||
|---|---|---|---|---|
| САД | ДАД | САД | ДАД | |
| Мальчики | Девочки | |||
| в среднем за сутки | 117–130 | 75–77 | 117–124 | 75–76 |
| день | 125–137 | 85–85 | 124–131 | 84–84 |
| ночь | 107–122 | 65–67 | 109–114 | 66–66 |
Известно, что показатели и САД и ДАД у здоровых взрослых выше, чем у детей и подростков.
СМАД позволяет оценить результаты влияния длительной гипотензивной терапии, например, на нормализацию вариабельности АД [52, 53].
Методы контроля перфузии жизненно важных органов при проведении гипотензивной терапии.
С целью оптимизации подходов к лечению АГ при цереброваскулярной патологии в НИИ неврологии РАМН определены клинические маркеры церебральной гипоперфузии при неадекватном снижении АД: “наличие клинических признаков экстрапирамидного и/или псевдобульбарного синдрома, окклюзирующего поражения экстра- и краниальных артерий, а также деформаций магистральных артерий головы. Очаговых (лакунарных) и диффузных (лейкоараоз) изменений вещества головного мозга, гипертрофии левого желудочка сердца, ИБС” [22, 27]. Необходимо доказать безопасность такого снижения, в первую очередь необходимо исключить возможность развития “синдрома обкрадывания” в жизненно важных органах, что чревато развитием инфаркта миокарда и мозгового инсульта, аритмической смерти и т.п.
Мы считаем, что рекомендации по снижению пожилым больным АГ с ПОМ, АКС, выраженными ФР снижать АД до целевого уровня необходимо под контролем СМАД и непосредственным контролем уровня перфузии жизненно важных органов, в первую очередь – сердца и головного мозга; одновременно со СМАД целесообразно проведение суточного мониторирования сердечного ритма и динамики сегмента СТ, УЗИ сердца (гемодинамика, зоны гипо- и дискинезии, ишемии), сцинтиграфия миокарда; допплерография сосудов шеи и интракраниальная допплерография, дуплексное сканирование с цветным картированием кровотока, компьютерная томография и ЯМР при необходимости.
Кроме того, мы считаем, что следует, помимо снижения АД в пределах нормальных величин, снижать выраженность и других ФР (например, гиперлипидемии), и проводить эффективное лечение АКС, например, сахарного диабета.
Помимо клинических критериев гипоперфузии мозга, очень ценную информацию об этом состоянии дают и новые объективные методы исследования [54–57]. К ним можно отнести перфузионную томосцинтиграфию головного мозга, однофотонную эмиссионную компьютерную томографию (ОЭКТ) головного мозга с 99Тс-гексаметилпропиленаминоксимом (ГМПАО) на гамма-камере “Омега 500” [54].
Для оценки и интерпретации результатов методом обратного проецирования формировали 12–16 поперечных срезов толщиной 12 мм, охватывающих последовательно весь головной мозг.
Для полуколичественной оценки мозгового кровотока выбирали 3 супратенториальных томосреза, на каждом из которых выделяли 6 симметричных зон интереса (ЗИ). Таким образом, у каждого пациента в общей сложности было проанализировано 36 ЗИ. В каждой ЗИ оценивали локальное поглощение РФП веществом мозга по отношению к скорости счета в исследуемой ЗИ к таковой по срезу в целом. За относительно гипоперфузируемые принимали сектора, в которых накопление индикатора составило менее 95 % по сравнению с симметричной ЗИ на контралатеральной стороне.
В контрольной группе достоверных данных за наличие асимметрии церебральной перфузии обнаружено не было, тогда как у всех пациентов с АГ были выявлены участки церебральной гипоперфузии (табл. 7).
Таблица 7
Топография гипоперфузируемых зон интереса (ЗИ) у больных АГ до и после 6 месяцев гипотензивной терапии [54]
| Анатомический регион | Число гипоперфузируемых ЗИ /общее число ЗИ в анатомическом регионе | ЗИ со сниженной перфузией (%) в анатомическом регионе | |||
|---|---|---|---|---|---|
| До лечения | После лечения | р | До лечения | После лечения | |
| Лобная доля | 14/180 | 10/180 | 0,036 | 8 | 6 |
| Теменная доля | 11/90 | 4/90 | 0,019 | 12 | 4 |
| Височная доля | 21/180 | 16/180 | 0,034 | 12 | 9 |
| Затылочная доля | 11/90 | 4/90 | 0,012 | 12 | 4 |
| Всего | 57/540 | 34/540 | 0,006 | 11 | 6 |
Наиболее часто обеднение кровообращения имело место в теменной (12 %), височной (12 %) и затылочной (12 %) долях головного мозга, реже участки гипоперфузии наблюдались в лобной доле (8 %) (табл.7) Патологические изменения микроциркуляции, наблюдаемые у пациентов с АГ, могут быть вызваны нарушением механизмов регуляции сосудистого тонуса, морфологическими изменениями прекапиллярных резистивных сосудов, а также разрежением микрососудистой сети.
После 6 месяцев лечения у больных АГ отмечалось достоверное снижение среднесуточных величин САД и ДАД, кроме того, гипотензивная терапия вызывала улучшение церебральной перфузии, о чем свидетельствовало уменьшение общего числа гипоперфузируемых секторов с 57 до 34.
Представленные данные согласуются с результатами работы И.Е. Чазовой, в которой приводятся данные об улучшении перфузии головного мозга у больных АГ после лечения периндоприлом [57].
Гипотензивная терапия в течение 6 месяцев оказывала положительное влияние на когнитивную функцию у обследованных больных.
Целевые уровни АД при лечении АГ – сложный вопрос. На научном симпозиуме, посвященном комбинированной терапии артериальной гипертонии, возникла дискуссия по этому вопросу.
Дискуссия о “целевом” и “рабочем” АД [58].
Профессор В.И.Подзолков “Одна из целей гипотензивной терапии хорошо известна – достигнуть нормального уровня АД. Эти цифры являются ориентировочными. И с каждым пациентом мы должны думать о том, какое АД для него является оптимальным, а какое – “рабочим” [58].
Профессор Б.А. Сидоренко: “Мне хотелось бы оспорить термин “рабочее” давление. Этот термин какой-то примеренческий. При “рабочем” АД больной себя хорошо чувствует, трудоспособен и врач с этим уровнем АД как бы смиряется. Этот термин пришел к нам с тех времен, когда мы не имели эффективных препаратов и точных представлений, к чему может привести мирное сосуществование с АД, например,160/100 мм рт. ст., а оно может быть мирным в течение 10 лет, а на 11-й год закончиться инсультом. Нужно ли нам мириться с этим “рабочим” давлением или это всего-навсего констатация временной ситуации, когда больной с этим АД живет и с ним примирился, а врач должен преодолевать такое состояние” [58].
Профессор В.И.Подзолков: “… Вопрос о “рабочем” давлении дискуссионен. Если говорить о рекомендациях добиваться “целевого” АД, то лучше не употреблять этот термин вообще. В исследовании НОТ было четко показано, что снижение ДАД до 80,6 мм рт. ст. – это профилактика нарушения мозгового кровообращения; от 82,6 до 90 мм рт. ст. – профилактика развития коронарных осложнений, а общая смертность уменьшается при достижении ДАД 86,5 мм рт. ст. Эти цифры являются ориентировочными, к которым мы должны стремиться в своей практической деятельности. Но ряд пациентов, когда мы достигаем этих замечательных цифр, чувствуют себя плохо. Наверное, врачу не хватает терпения адаптировать пациента к новым цифрам АД, не хватает мастерства убедить больного в том, что нужно подождать, пока организм адаптируется к новым цифрам АД [58].
Профессор Ж.Д. Кобалава, обращаясь к профессору В.И.Подзолкову: “Глубокоуважаемый Валерий Иванович, я извиняюсь, но одна из самых распространенных ложных концепций, которую мы должны искоренять – это концепция “рабочего” давления, так же, как концепция целесообразности курсового лечения и так же, как, к сожалению, очень распространенная концепция – предположение об опасности снижения АД у больных ИБС, почечной недостаточностью, цереброваскулярной болезнью и мифические опасения плохой переносимости препаратов в группе пожилых больных [58].
Целевое АД должно заменить в нашем сознании понятие “рабочего” АД. Для большинства больных это уровень 130 и 85 мм рт. ст. Для пожилых больных и для группы лиц с пограничной АГ – это уровень менее 140 мм рт. ст. для систолического АД. В группе минимального риска в качестве целевого АД определены значения менее 150 мм рт. ст. для САД и менее 95 мм рт. ст. – для ДАД.” [58].
Обращаясь к материалам приведенной нами дискуссии, мы считаем, что целевым уровнем АД при лечении АГ у большинства больных АГ является уровень 140/90 мм рт. ст. и менее.
Термин “рабочее” АД применяется, если больные с тяжелым и длительным высоким АД фактически не могут существовать при АД 140/90 мм рт. ст. (головокружение, слабость, потеря равновесия, возможны падения и т.п.). Мы считаем, что этот термин может рассматриваться как временное понятие, на что указывает и Б.А.Сидоренко, которое распространяется на отрезок времени, когда врачи стремятся достигнуть целевой уровень АД 140/90 мм рт. ст. и менее у таких больных, если его удастся достигнуть вообще. Напомним, например, что по данным О.Д.Остроумовой, при лечении больных ИСАГ, при использовании одной и той же схемы, целевой уровень ДАД Уважаемый профессор Б.А.Сидоренко выражает тревогу: “Мирное сосуществование с АД, например,160/100 мм рт. ст. может быть мирным в течение 10 лет, а на 11-й год год закончиться инсультом. Нужно ли нам мириться с этим?” Зададимся вопросом, если у этого больного имеет место стенозирование крупной артерии, питающей головной мозг, являющейся причиной плохой переносимости более низкого АД? Не приведет ли снижение АД у этого больного до 140/90 мм рт. ст. и менее к инсульту не через 10 лет, а гораздо раньше после такого снижения?
Уважаемой Жанне Давидовне Кобалава мы хотим ответить, что “рабочее” давление – это не цель лечения и не достижение лечащего врача, основанное на его убеждении, что именно таковым, а не ниже, оно должно быть. Достигнутое “рабочее” давление – это “беда” для больного, так как высокое АД – весомый фактор риска мозгового инсульта, инфаркта миокарда и т.п. и чувство глубокой неудовлетворенности у лечащего врача, так как рекомендованных в руководствах по лечению АГ цифр целевого АД в течение сравнительно длительного периода лечения не удалось достичь, так как больной отмечает резкое ухудшение качества жизни и категорически отказывается от снижения АД до такого уровня.
Отметим, что большинство кардиологов с помощью комбинации современных гипотензивных препаратов могут достигнуть АД 140/90 мм рт. ст. у большинства больных с высоким АД.
Мы согласны с Ж.Д.Кабалава, что курсовое применение гипотензивных препаратов – нонсенс, так как больной АГ должен быть ориентирован на пожизненный прием этих препаратов. Однако синдром обкрадывания у больных с выраженным стенозированием артерий в жизненно важных органах, при неадекватно низком для данного больного снижении АД, что нередко бывает при лечении, например, мощными вазодилятаторами и ведет при этом к значительному снижению перфузии – к сожалению, не миф, а суровая реальность.
Напомним, что иАПФ, например, противопоказаны больным со злокачественной АГ при стенозе почечной артерии, так как возможно резкое снижение АД и резкое ухудшение перфузии почки на стороне стенозированной артерии.
От чрезмерной напористости при назначении гипотензивных препаратов пожилым больным предостерегают ведущие руководства по лечению АГ и по геронтологии.
В статье академика А.П.Голикова сообщается, что при перепадах АД может наступить ухудшение коронарного или мозгового кровообращения, поэтому при внутривенном введении клофелина для купирования гипертонического криза необходим более строгий контроль за динамикой АД. Эналаприл оказывает более плавное гипотензивное действие, не приводя к гипотонии [59].
Причины, по которым не достигаются целевые уровни у больных АГ разной степени тяжести, зависят от многого.
Р.Г. Оганов и соавт., на основе анализа данных зарубежных исследований и собственных данных пишет, “Несмотря на достижения в лечении АГ, связанные с появлением современных антигипертензивных препаратов, контроль АД в популяции далек от идеального. По данным исследований, проведенных во многих странах, количество больных, у которых удается контролировать АД на уровне 140/90 мм рт. ст. и ниже, составляет меньше 1/3. Самые лучшие показатели получены во Франции – 27 %, Бельгии – 25 % и США – 24 %. Наихудшие показатели отмечаются в Великобритании – 6 % и в России – 5,7 %. Промежуточное положение занимают Чехия – 17,8 %, Шотландия –17,5 % и Канада –26 %” [60].
Причинами такого явления в популяции, где больные с мягкой АГ составляют основную часть этих больных, авторы считают недостаточную мотивацию к лечению больных мягкой гипертонией, низкую приверженность к лечению, преимущественное использование для лечения АГ монотерапии, отсутствие адекватного контроля АД и др. [59]. Мы также считаем, что в России одним из факторов достижения лишь у 6 % целевого уровня АД в популяции является низкий жизненный уровень населения. Старые препараты типа клофелина, адельфана, эффективны и недороги, но резко ухудшают качество жизни и обладают серьезными побочными явлениями, поэтому больные АГ, особенно молодого возраста, принимают их неохотно. Современные эффективные гипотензивные препараты, например, ренитек, норваск и др. эффективны, но дороги и фактически недоступны по этой причине для большинства неработающих пенсионеров и других малообеспеченных граждан России. Другим фактором является крайне нездоровый образ жизни значительной части россиян: чрезмерное потребление алкоголя, высокий уровень стрессового воздействия высокой интенсивности и т.п.
Что касается больных АГ с тяжелой, длительно существующей АГ, резистентной к лечению, то мы считаем, что необходимо на основе объективных данных ответить на вопрос, почему некоторые больные с тяжелой длительно существующей АГ хорошо себя чувствуют при достижении с помощью антигипертензивной терапии “рабочего” давления, например, 160/100 мм рт. ст., но плохо себя чувствуют, а иногда и теряют работоспособность при достижении “целевого” АД – менее 140/90 мм рт. ст.? Не лежит ли в основе плохого самочувствия при достижении целевого АД неадекватное снижение ниже потребности перфузии жизненно важных органов? Не следует ли еще до снижения АД от “рабочего” уровня до “целевого” объективно оценить у таких больных перфузию жизненно важных органов, в первую очередь головного мозга, сердца, почечных артерий? Не следует ли сначала восстановить перфузию этих органов (например, путем операции хирургического лечения стенозов), а после этого с уверенностью снижать АД до целевого уровня, не опасаясь синдрома обкрадывания в сосудистом бассейне дистальнее стеноза артерии (артерий)?
Мы согласны с Л.Б.Лазебником, что значительное снижение АД при наличии ИБС может вызвать ухудшение коронарного кровообращения. Риск развития инфаркта миокарда наиболее низок при поддержании диастолического АД в пределах 90 мм рт. ст. и начинает расти при его более высоком или более низком уровне. Темп снижения АД также имеет важное значение. При неотложных состояниях следует стремиться к снижению АД в течение 24 часов. В остальных случаях обычно нет оснований принимать экстренные меры. Для больных пожилого и старческого возраста допустимо снижение АД до целевых значений в течение 3–4 недель, что уменьшает риск развития осложнений и улучшает переносимость лекарственных препаратов [18].
Достигнутое целевое АД должно быть безопасным для больного АГ в плане развития “синдрома обкрадывания” с возможным ухудшением течения ЦВБ и ИБС вплоть до развития инфаркта миокарда, инсульта, может приводить к тяжелым нарушениям сердечного ритма вплоть до фибрилляции желудочков сердца.
Известные исследователи артериальной гипертонии, среди которых В.С. Моисеев и Ж.Д. Кобалава, считают, что целесообразно производить СМАД в течение 48 часов: “У большинства больных характеристики суточного ритма на протяжении 2-х суток остаются неизменными. Вариабельность АД не изменялась у всех больных, что свидетельствует о высокой стабильности этого показателя. Однако при 48-часовом мониторировании устойчиво недостаточное снижение ночного АД было обнаружено у 28 % больных. Если же относить больных к группе нон-дипперов по результатам мониторирования лишь за первые сутки, то численность этой группы высокого риска составит 43 %. Таким образом, 15 % больных могут быть ошибочно отнесены к группе высокого риска поражения органов мишеней и подвергнуты излишне “агрессивному” лечению” [61].
При достигнутом целевом АД должна быть наиболее адекватная перфузия жизненно важных органов. Качество жизни должно быть выше, чем до достижения ЦУ АД.
При лечении больных с высоким нормальным АД, как и при достижении ЦУ у больных с тяжелой АГ, особенно пожилого возраста, с наличием выраженных ФР, ПОМ, АКС целесообразно не допускать снижения ДАД ниже 85–90 мм рт. ст. В тяжелых случаях ИСАГ снижение САД может быть приостановлено на уровне 160 мм рт. ст., исходя из самочувствия больного. Кроме того, при проведении гипотензивной терапии таким больным необходим строгий объективный контроль адекватности перфузии жизненно важных органов: головного мозга, сердца с помощью СМАД, мониторирования сердечного ритма, сцинтиграфии головного мозга и т.п.
Приоритет в установлении целевых уровней АД у больных с выраженными окклюзирующими поражениями артерий, питающих головной мозг, у больных с транзиторными ишемическими атаками, у перенесших нарушение мозгового кровообращения и, особенно, при остром нарушении мозгового кровообращения, должен принадлежать неврологам.
Целевые уровни АД у больных АГ с сопутствующими ИБС и ЦВБ следует согласовывать с неврологами, исходя из объективных данных о состоянии артериального русла головного мозга.
Причиной невозможности достижения целевого уровня АД у многих больных АГ чаще всего является плохое самочувствие больного при АД 140/90 мм рт. ст. и ниже. Как правило, это больные с длительно существующим, плохо леченным или вовсе нелеченным заболеванием с высокими цифрами АД, что приводит к необратимым изменениям в головном мозге.
В цикле исследований, выполненных в НИИ неврологии РАМН [23а], а также по данным зарубежных исследований, приводимых известным российским неврологом Скворцовой, установлено, что
- АГ индуцирует процессы гипертрофии и ремоделирования, характеризующиеся уменьшением внутреннего диаметра сосудов. Возникает комплекс деструктивных, адапттивных и репаративных реакций, вовлекающих сосуды любого диаметра, что приводит к развитию очаговой ишемии мозга и формированию малых глубинных (лакунарных) инфарктов или зон неполного некроза ткани мозга в артериальных сосудах головного мозга
- по данным электронной и световой микроскопии, морфологическим признаком ремоделирования церебральных сосудов являются уменьшение их просвета, достоверное усыхание мышечного слоя, достоверное уменьшение ядер эндотелиальных клеток [23а,28].
АГ изменяет способность эндотелиальных клеток высвобождать вазоактивные вещества и повышает сократительный тонус системных и церебральных артерий, изменяет сосудисто-мозговую ауторегуляцию, которая является функцией артериол головного мозга, позволяющей поддерживать мозговой кровоток в относительном постоянстве, несмотря на колебания перфузионного давления в некоторых пределах (обычно от 70 до 150 мм рт. ст.).
Хроническая АГ смещает эти пределы в сторону более высокого давления, делая головной мозг более уязвимым к понижению перфузионного давления [23а, 28].
В результате происходят деструктивные изменения сосудистой стенки, к первичным из которых относят ее плазматическое пропитывание, которое может достигать степени массивных плазморрагий, приводящих к набуханию стенки с резким сужением или облитерацией просвета сосуда (гипертонический стеноз).
В бассейне стенозированного или облитерированного сосуда резко снижается кровоток, что приводит к развитию очаговой ишемии мозга и формированию малых глубинных (лакунарных) инфарктов или зон неполного некроза ткани мозга.
Дегенерация стенки артериол с отложением гиалина под базальной мембраной и в межклеточном веществе средней оболочки является проявлением необратимых системных изменений при АГ и может считаться признаком гиалинового артериолосклероза [23а, 28].
Повреждение нервного аппарата клетки происходит ранее и в большей степени, чем других структур сосудистой стенки. В результате денервации сосуда развиваются соответствующие функциональные нарушения, в частности повышение чувствительности к катехоламинам. Разрыв стенки денервированных сосудов может стать источником кровоизлияния в мозг [23а, 28].
Обнаружено значительное нарушение микроциркуляции у больных АГ, зависящее от давности и выраженности заболевания и связанное с ухудшением реологических свойств крови [62].
То есть, ведущие неврологи страны высказывают мнение, с которым нельзя не согласиться, что целевые уровни АД нельзя навязывать всем больным “по уставу” – 140/90 мм рт. ст. и ниже: “необходимость достижения единого уровня АД в результате антигипертензивного лечения представляется весьма сомнительной. По-видимому, речь должна идти об адекватной относительной редукции АД, которая соответствует возможностям ауторегуляции мозгового кровотока и не приведет к дальнейшему ухудшению церебральнй перфузии” [23а, 34].
Заключение
Исходя из вышеизложенного, мы считаем: чтобы снизить число больных с тяжелой АГ, которых выписывают из стационара или длительно наблюдают в поликлинике с “рабочим”, а не с рекомендуемым в руководствах по лечению АГ целевым АД, которого не удалось достигнуть, следует производить выявление больных АГ на ранних стадиях заболевания с последующим эффективным пожизненным управлением АД у этих больных.
Мы согласны с профессором В.И.Подзолковым, что определение целевого уровня АД у конкретного больного АГ является непростым дискуссионным вопросом [58], и призываем коллег к продолжению дискуссии на эту тему на страницах РКЖ.
Литература
1. Stokes J, Kannel W, Wolf P, et.al. Blood pressure, as a risc factor for cardiovascular disease/ The Framingham Study-30 years of followup // Hypertension1989;13 (Suppl.1):13–80.
2. Waeber B. Treatment strategy to control blood pressure optimally in hypertensivt patients // blood pressure 2001;10:62–73
3. Рекомендации по диагностике и лечению артериальной гипертензии. Европейское общество по артериальной гипертензии. Европейское общество кардиологов // Артериальная гипертензия - 2003, Том 10, № 2 с.65–90. (J. Hyhertens 2003;21:1011–53.)
4. The Seventh Report of the Joint National Committee on // NIH Publication, 2003; № 03–5233.
5. Шляхто Е.В., Конради А.О. Анализ “Седьмого отчета Совместной национальной комиссии по предупреждению, выявлению, оценке и лечению высокого артериального давления США” ((JNC V11).) // Сердце – 2005, том 4, № 3 (21), с. 154–155.
6. Chobanian A.V., Bakris G.L., Black H.R. et al. The seventh report of the joint national committee on prevention, detection, avaluation and treatment of high blood pressure. The JNS 7 report//JAMA, 2003; V.289; p.2560–2572.
7. Профилактика, диагностика и лечение артериальной гипертензии. Российские рекомендации (второй пересмотр). М.: ВНОК, 2004
8. Шальнова С.А. Марцевич С.Ю., Деев А.Д. и др. Исследование ПРОЛОГ: снижение риска сердечно-сосудистых заболеваний у больных артериальной гипертонией под влиянием антигипертензивной терапиии // Кардиоваскулярная терапия и профилактика.20052005,34 (4), с. 11–15.
9. Чазова И.Е. Ратова Л.Г. Комбинировнная терапия артериальной гипертонии. с 655–676. В кн. Руководство по артериальной гипертонии / Под ред. Е.И.Чазова и И.Е.Чазовой- М.:Медиа Медика, 2005.-с.784
10. WHOFISH Hypertension Guidelines Committee. 1999 World Health Organization – International Society of Hypertension Guidelines for the Management of Hypertension // J. Hypertens. 1999; 17: 151–83.
11. Рекомендации ВОЗ и Международного общества гипертонии (МОГ). Артериальная гипертония. практическое руководство для первичного звена здравоохранения / Под ред. Р.Г.Оганова, 1999, с.18.
12 Pyorala K, De Backer G, Grabam I et al. Prevtntion of coronary heart disease in clinical practise. Recommendations of the Task Force of the European Society of Cardiology; European Atherosclerosis Society and European Society of Hypertension //Eur. Heart. J. 1994;15:1300–1331.
13. Wood D, De Backer G, Faergeman O et al. Prevtntion of coronary heart disease in clinical practise.. Recommendations of the Second Joint Task Forse of European and other Societies on Coronary. Prevtntion // Eur. Heart. J. 199;19:1434–1503.
14. Карпов Ю.А. Ишемическая болезнь сердца в сочетании с артериальной гипертонией: особенности течения и лечения. с. 434–453. В кн. Руководство по артериальной гипертонии / Под ред. Е.И.Чазова и И.Е.Чазовой - М.: Медиа Медика, 2005.-с.784.
14а. Беленков Ю.Н.. Чазова И.Е., Ратова Л.Г. Российское исследование по оптимальному снижению артериального давления (РОСА-2) два года наблюдения. Что в итоге? // Кардиоваскулярная терапия и профилактика. 2005,4 (6) ч.1, с. 4–14.
15. Шляхто Е.В., Конради А.О. Классификация артериальной гипертензии: от болезни Брайта до сердечно-сосудистого континуума (обзор) // Артериальная гипертензия. 2004, том 10, № 2. с. 98–103.
16. Остроумова О.Д.Артериальная гипертония у пожилых. с.490–507. В кн. Руководство по артериальной гипертонии //Под ред. Е.И.Чазова и И.Е.Чазовой// М.: Медиа Медика, 2005.-с.784
17. Somes GW, Pabor M, Sborr RI et al. The role of diastolic blood pressure when treating isolated systolic hypertension // Arch Intern Med 1999;159:2004–9.
18. Zanchetti A. What Blood Pressure level Should Be treated? P. 1967–1983. In. Hypertension Pathophysiology, Diagnosis, and Management / Edited by J.H.Laragh and B.M.Brener. Raven Press, Ltd., New York,1990.
19. Zanchetti A. Systolic, diastolic and 24-hour blood pressure: which should be treated? In: Hansson L, ed. Hypertension annual. London: Gower Academic Journals, 1988;3–19.
20. Cruickhank JM, Thorp JM, Zacharias F.J. Benefits and potential harm of lowering high blood pressure// Lancet,1987;1:581–583
21. Zanchetti A., Hansson l, Clemеnt D et al. On behalf of the HOT Study Group/ Benefits anl riscs of the more intensive blood pressure lowering in hypertensive patients of the HOT Study with different risk profiles: does a J-shaped curve exist in smokers?// Hypertens. 2003;21: 797–804.
22. СуслинаЗ.А., Гераскина Л.А., Фонякин А.В. Актуальные вопросы и рациональный подход к лечению артериальной гипертонии при сосудистой патологии мозга// Кардиоваскулярная терапия и профилактика.2005,4 (3), ч.1, с.82–87.
23. Гераскина Л.А., Суслина З.А., Фонякин А.В. и др. Церебральная перфузия у больных артериальной гипертонией и хроническими формами сосудистой патологии головного мозга//Тер. Архив 2003; 12: 32–36.
23а. Верещагин Н.В., Суслина З.А., Максимова М.Ю. Артериальная гипертония и цереброваскулярная патология: современный взгляд на проблему// Кардиология 2004,№ 3,, с..4 –8.
24. Лазебник Л.Б., Комиссаренко И.А. Лечение артериальной гипертонии у больных старших возрастов с высоким риском развития сердечно-сосудистых осложнений// Росс. кардиол. ж. 2006, № 5 (61). С. 82–87.
25. Профилактика, диагностика и лечение первичной артериальной гипертонии в Российской Федерации. Первый доклад экспертов научного общества по изучению артериальной гипертонии, ВНОК и Межведомственного совета по сердечно-сосудистым заболеваниям (ДАГ-1) // Русский мед. ж., 2000, том 8, № 8, с.318–346.
26. ACC/AHA 2002 Guideline Update for the Management of Patients With Chronic Stable Angina: A Report of the American College of Cardiology/ American Heart Association Task Force on Practice Guidelines (Committee to Update the 1999 Guidelines for the Management of Patients With Chronic Stable Angina)// J. Am. Coll. Cardiol.2000;36;970–1062.
27. Симоненко В.Б., Фисун А.Я., Широков Е.А. и др. Артериальная гипертония с угрозой развития мозгового инсульта: клинические особенности, суточные профили артериального давления и терапия антагонистами рецепторов ангиотензина-11// Кардиоваскулярная терапия и профилактика. 2005,4 (3) ч.1, с. 29–34..
28. Скворцова В.И. Артериальная гипертония и церебро-васкулярные нарушения. с. 217–246 В кн. Руководство по артериальной гипертонии / Под ред. Е.И.Чазова и И.Е.Чазовой- М.: Медиа Медика, 2005.-с.784
29. Гусев Е.И., Скворцова В.И. Ишемия головного мозга. М.: Медицина, 2001.
30. Конради А.О. Артериальная гипертензия у больных, перенесших инсульт //Сердце. 2006, том5,;4, (28) с.184–186.
31. Суслина З.А., Варакин Ю.Я. артериальная гипертония и профилактика цереброваскулярных заболеваний. Позиция невролога - Атмосфера // Нервные болезни. 2004; 4:2–13.
32. Irie K, Yamaguchi T, Minetatsu K et al. The J-curve phenomenon in stroke recurrence // Stroke 1993; 24:1844–9.
33. Rothwell PM, Howard SC, Spence JD. Relationship between blood pressure and stroke risk in hatients with symptomatic carotil occlusive lisease // Stroke 2003;34:2583–92.
34. ШарыповаТ.Н., Гераскина Л.А., Суслина З.А. и др. Церебральная перфузия на фоне антигипертензивной терапии у больных с дисциркуляторной энцефалоратией. Материалы конференции “Современные возможности эффективной профилактики, диагностики и лечения артериальной гипертонии”. М.:2001; с.-209.
35. Кушаковский М.С. Гипертоническая болезнь. М.: Медицина 1977.
36. Осипова И.В. Зальцман А.Г. Воробьева Е.Н. и др. Распространенность факторов риска и особенности поражения органов-мишеней при стресс-индуцированной артериальной гипертонии у мужчин трудоспособного возраста // Кардиоваскулярная терапия и профилактика.2006,5 (2) ч.1, с. 10–14.
37. Шабалин А.В. Гуляева Е.Н. Веркршанская Э.М. и др. Клиническая значимость оценки стресс реактивности у больных эссенциальной артериальной гипертензией // Кардиоваскулярная терапия и профилактика.2004,3 (1) ч.1, с.28–35.
38. Гогин Е.Е. История изучения проблемы артериальной гипертонии и классификации гипертонической болезни. с.21–41. В кн. Руководство по артериальной гипертонии / Под ред. Е.И.Чазова и И.Е. Чазовой- М.: Медиа Медика, 2005.-с.784.
39. Арабидзе Г.Г. Основные принципы современной гипотензивной терапии // Ангиология и сосудистая хирургия.1996,31, с.130–139.
40. Сметнев А.С., Тополянский В.Д. Гипотензия артериальная. БМЭ / Под ред. Б.В.Петровского, М., “Сов. энциклопедия”.1977, том 5. с.633–634.
41. Артериальная гипертония: Практическое руководство для врачей Центрального федерального округа РФ. Москва,2003.с.112. В кн. Руководство по артериальной гипертонии / Под ред. Е.И.Чазова и И.Е. Чазовой- М.: Медиа Медика, 2005.с.784.
43. Кокорин В.А., Волов Н.А. Современные аспекты методики измерения артериального давления // Российский кардиологический журнал. Июнь 2006 г., (юбилейный номер), с.117–122.
44. Ohkubo T., Imai Y., Tsuiji I. et.al. Referense values for 24-hour ambulatory blood pressure monitoring based on a prognostic criterion. The Ohasama Study // Hypertension,1998;32;255–259.
45. World Health Organization – International Society of Hypertension. Guidelines for nhe management of hypertension/ J. Hypertens. 1999;17:151–183.
46. Кадникова Ю.В. Шутемова Е.А. Масленниковап О.А. и др. Суточный профиль артериального давления у пожилых больных с пограничной артериальной гипертонией // Кардиолог.2005,№ 6, с. 32–36.
47. Машин В.В. Белова Л.А., Грищук Д.В. и др. Характеристика суточного профиля артериального давления при различных подтипах ишемического инсульта // Кардиоваскулярная терапия и профилактика, 2005; 496), ч.11, с. 27–31.
48. Sanjuliani A.F., V.G.Abreu, J.U.Braga et al. Влияние моксонидина на симпатическую нервную систему, артериальное давление, активность ренина плазмы. Альдостерон плазмы, лептин и метаболический профиль препарата у больных артериальной гипертонией с ожирением. Обзоры клинической кардиологии. 2006,№ 3, с.48–59.
49. Савенков. М.П., Иванова С.В. Артериальная гипертензия при патологии шейного отдела позвоночника // Российский кардиологический журнал. 2006, июнь, (Юбилейный выпуск), с. 65–69.
50. Мычка, В.Б., Масенко В.П., Чазова И.Е. Артериальная гипертония на фоне избыточного веса: особенности терапевтического подхода / Обзоры клинической кардиологии. 2006,№ 5, с 13–20.
51. Soergel M., Kirschtein M, Busch c et.al. Oscillometric twenty four hour ambulatory blood pressure values in healthy children anl adolescents: multicenter trial including 1141 subjtcts // J. Pediatrics 1997;130:178–84.
52. Мухин Н.А.Фомина И.Г., Люсов В.А. и др. Динамика показателей суточного ритма артериального давления и вариабельности сердечного ритма у больных артериальной гипертензией на фоне лечения новой формой нифедипина-нифекарда ХL // Российский кардиологический журнал. 2003,№ 6, с.38–42.
53. Маркова Л.И., Евдокимова Е.В., Радзевич А.Э. и др. Суточный профиль артериального давления и мозговой кровоток у больных артериальной гипертонией на фоне длительной терапии рилминедином // Российский кардиологический журнал. 2004,№ 5, с.47–50.
54. Ефимова И.Ю., Ефимова Н.Ю., Трисс С.В., Лишманов Ю.Б. Влияние гипотензивной терапии на состояние мозгового кровообращения и когнитивной функции у больных артериальной гипертонией // Кардиолог, 2006,№ 1. с. 27–31.
55. Синицын В.Е. Лучевые методы обследования пациентов с артериальной гипертонией с.344–371. В кн. Руководство по артериальной гипертонии/ Под. ред. Е.И.Чазова и И.Е. Чазовой М.: Медиа Медика, 2005.-с.784
56. Евсиков Е.М., Байкова О.А., Отарова С.М. и др. Значимость изменений мозгового кровотока в патогенезе артериальной гипертонии у больных с метаболическим синдромом // Кардиолог, 2006,№ 6, с. 17- 25.
57. Чазова И.Е., Мычка В.Б., Горностаев В.В. и др. Цереброваскулярные осложнения у больных артериальной гипертонией: первичная и вторичная профилактика // Consilium Medicum/ репринт, 2003;5 (2):3–6.
58. Комбинированная терапия артериальной гипертонии. Научный симпозиум в рамках У1 Российского национального конгресса “Человек и лекарство” // Кардиология 1999,№ 8. с. 84–96
59. Голиков А.П. Сравнительная оценка купирования гипертонических кризов эналоприлом и клонидином // Кардиология 2004, № 11, с. 77–79.
60. Оганов Р.Г., Небиеридзе Д.В. Клиническая эффективность нолипрела при лечении артериальной гипертонии. Основные результаты исследования ЭТАЛОН // Кардиология 2004,№ 3, с.66–69.
61. Котовская Ю.В., Дмитриев А.А., Кобалава Ж.Д., Моисеев В.С. Устойчивость двухфазного ритма артериального давления при 48-часовом мониторировании // Кардиология 2002,№ 11, с.28–31.
62. Маколкин В.И., Подзолков В.И., Павлов В.И., Самойленко В.В. Состояние микроциркуляции при гипертонической болезни // Кардиология,2003,№ 5, с.67.
