Моксифлоксацин: настоящее и будущее в ступенчатой терапии
СтатьиОпубликовано в журнале: НИИ антимикробной химиотерапии, Смоленск, Россия
Клиническая микробиология и антимикробная терапия, № 1, 2003
Л.С. Страчунский, А.В. Веселов, В.А. Кречиков
Контактный адрес: 214019, Россия, Смоленск, а/я 5
Факс: (0812) 61 12 94
Эл. почта: str@antibiotic.ru
Абстракт
Моксифлоксацин – новый 8-метоксихинолон широкого спектра действия с высокой активностью в отношении как грам(+) и грам(-) аэробной микрофлоры, так и внутриклеточных возбудителей и анаэробов. Обладает активностью в отношении микроорганизмов, резистентных к другим классам антибактериальных препаратов, включая макролидо- и пенициллинорезистентные пневмококки и b-лактамазопродуцирующие штаммы Haemophilus influenzae.
Высокая активность против перечисленных возбудителей и хороший фармакокинетический профиль позволяют применять моксифлоксацин для терапии респираторных инфекций. Одним из подходов является ступенчатая терапия, при которой моксифлоксацин по данным многочисленных контролируемых клинических исследований продемонстрировал высокую клиническую эффективность и безопасность у пациентов с внебольничной пневмонией.
Несмотря на имеющиеся доказательные данные в отношении его высокой эффективности при респираторных заболеваниях, моксифлоксацин на сегодняшний день не нашел широкого применения при других инфекциях.
В данной статье представлен обзор результатов клинических исследований ступенчатой терапии моксифлоксацином при лечении внебольничной пневмонии и сделана попытка оценить возможные перспективы его дальнейшего применения.
Ключевые слова: моксифлоксацин, фторхинолоны, пневмония
Moxifloxacin: the Present and the Future in the Sequential Therapy
L.S. Stratchounski, A.V. Veselov, V.A. Kretchikov
Research Institute of Antimicrobial Chemotherapy, Smolensk, Russia
Abstract
Moxifloxacin – new broad spectrum 8-methoxiquinolon with high activity against Gram(+) and Gram(-) microorganisms as well as against anaerobes and intracellular pathogens. It is also active against microorganisms that are resistant to other classes of antimicrobials, including penicillin- and macrolide-resistant pneumococci and b-lactamase-producing Haemophilus influenzae.
An excellent activity against that pathogens and good pharmacokinetic profile allowed using moxifloxacin in the therapy of respiratory tract infections. High clinical efficacy and safety of moxifloxacin have been demonstrated for community-acquired pneumonia while using sequential therapy in the large number of controlled clinical trials. In spite of available evidence based data of moxifloxacin efficacy in respiratory infections he is not widely use in another types of infection processes.
In the article the literature review of clinical trials on sequential (IV/PO) moxifloxacin therapy in patients with community-acquired pneumonia is presented. An attempt to analyze the perspectives of moxifloxacin usage is made.
Key words: moxifloxacin, quinolones, pneumonia
Введение
В настоящее время хинолоны из небольшой группы препаратов, ранее использовавшихся исключительно для лечения инфекций мочевыводящих путей, превратились в один из доминирующих классов антимикробных препаратов (АМП). Вторая волна в развитии хинолонов связана с появлением фторированных производных, обладающих гораздо более высокой активностью в отношении широкого спектра микроорганизмов, включая грамположительных возбудителей (Staphylococcus aureus) и грамотрицательную флору, улучшенной фармакокинетикой, появлением форм для парентерального введения и, вследствие этого, расширением показаний для применения. "Золотым стандартом" хинолонов II поколения стал ципрофлоксацин, который с большим успехом используется для лечения многих инфекций. Существенным недостатком препаратов этого поколения является низкая активность в отношении пневмококков, внутриклеточных возбудителей (хламидий, микоплазм) и анаэробов. Эта проблема была разрешена с разработкой новых фторхинолонов III-IV поколений. Первым препаратом этой группы был левофлоксацин, который превосходил по активности против пневмококка и атипичных возбудителей предыдущие фторхинолоны, в связи с чем, данное поколение получило название «респираторные» или «антипневмококковые» фторхинолоны. Дальнейшие модификации химической структуры привели к появлению соединений активных и в отношении анаэробов. Ряд новых препаратов (темафлоксацин, тровафлоксацин, гатифлоксацин, гемифлоксацин) были потеряны, вследствие развития тяжелых нежелательных лекарственных реакций (НЛР). Единственным представителем фторхинолонов IV поколения применяющимся в настоящем времени является моксифлоксацин.
Хороший фармакокинетический профиль моксифлоксацина и наличие форм выпуска, как для парентерального применения, так и для приема внутрь, позволяют использовать данный препарат для ступенчатой антимикробной терапии (САТ) различных инфекций, включая инфекционные заболевания дыхательных путей.
Моксифлоксацин – характеристика препарата
Механизм действия
Моксифлоксацин, как и все фторхинолоны, оказывает бактерицидное действие за счет ингибирования ферментов класса топоизомераз – ДНК-гиразы (топоизомеразы II) и топоизомеразы IV. Основной мишенью моксифлоксацина в грамположительных микроорганизмах преимущественно является топоизомераза IV, а в грамотрицательных бактериях – ДНК-гираза [1].
Моксифлоксацин обладает высокой активностью против грамположительных и грамотрицательных микроорганизмов (включая микроорганизмы, устойчивые к другим классам АМП), атипичных возбудителей и анаэробов. Кроме того, в настоящее время отсутствуют данные о резистентности к моксифлоксацину основных возбудителей внебольничной пневмонии.
Спектр активности
Streptococcus pneumoniae. Моксифлоксацин высокоактивен в отношении S. pneumoniae. По данным одного из самых больших исследований, включавшем 5640 штаммов, 99,8% из них были чувствительны к препарату, 0,1% – умереннорезистентны, 0,1% – устойчивы; МПК90 составила 0,25 мг/л [2]. Также моксифлоксацин обладает высокой активностью в отношении полирезистентных пневмококков: МПК90 моксифлоксацина для 138 штаммов, устойчивых к пенициллину, эритромицину и тетрациклину, составила 0,5 мг/л [3].
По активности в отношении пневмококка моксифлоксацин превосходит другие фторхинолоны (за исключением ситафлоксацина и гемифлоксацина): он в 2 раза активнее спарфлоксацина [2] и гатифлоксацина [4], в 4-8 раз активнее левофлоксацина [2, 5], в 8 раз активнее ципрофлоксацина и офлоксацина [ 5]. По сравнению с бета-лактамами и макролидами активность моксифлоксацина в отношении полирезистентных S. pneumoniae значительно выше [2].
Streptococcus pyogenes. Значение МПК90 моксифлоксацина для S. pyogenes (b-гемолитический стрептококк группы А) составляет 0,06–0,25 мг/л. Моксифлоксацин в 2-4 раза активнее офлоксацина, ципрофлоксацина и левофлоксацина, обладает одинаковой активностью с гатифлоксацином [6, 7]. Наличие резистентности к макролидам не влияет на активность моксифлоксацина [ 7].
|
1 MRSA – метициллинорезистентный S. aureus 2 MSSA – метициллиночувствительный S. aureus |
Haemophilus influenzae, Moraxella catarrhalis. Моксифлоксацин имеет очень высокую активность по отношению к H. influenzae и M. catarrhalis, включая штаммы резистентные к аминопенициллинам вследствие продукции b-лактамаз.
Важно отметить, что у определенной категории пациентов, особенно пожилого возраста, высок риск развития внебольничной пневмонии, вызванной грамотрицательными возбудителями, в частности Klebsiella pneumoniae и Escherichia coli, которые также наряду с P. aeruginosa выступают этиологической причиной нозокомиальной пневмонии.
Escherichia coli. Как и все другие фторхинолоны моксифлоксацин обладает высокой активностью по отношению к E. coli, однако in vitro несколько уступает ципрофлоксацину, что, однако, не имеет клинического значения [10, 11].
Klebsiella spp. Моксифлоксацин более активен чем большинство b-лактамных АМП, близок по активности к офлоксацину и незначительно уступает ципрофлоксацину [10, 11]. На штаммы E. coli и K. pneumoniae, резистентные к ципрофлоксацину, моксифлоксацин не действует [12].
Pseudomonas aeruginosa. Моксифлоксацин уступает ципрофлоксацину по активности против синегнойной палочки. МПК90 моксифлоксацина по данным разных авторов находится в диапазоне от 8 до 32 мг/л и более, а МПК90 ципрофлоксацина – от 0,5 до 16 мг/л [4, 10, 11].
Neisseria gonorrhoeae. Для моксифлоксацина характерна очень высокая активность против N. gonorrhoeae, которая in vitro лишь несколько ниже, чем у ципрофлоксацина [11].
Таблица 1. Активность моксифлоксацина в отношении аэробных грамположительных и грамотрицательных микроорганизмов
| Микроорганизм [ссылка] | Диапазон МПК, мг/л | МПК90, мг/л |
| Грамположительные микроорганизмы | ||
| S. pneumoniae [2] | <0,002–4 | 0,25 |
| S. pyogenes [7, 11] | 0,06–0,25 | 0,25 |
| S. aureus (MSSA) [8, 11] | 0,03–0,12 | 0,12 |
| S. aureus (MRSA) [8, 9, 11] | <0,06–4 | 0,06-8 |
| Грамотрицательные микроорганизмы | ||
| H. influenzae [2] | <0,002–0,25 | 0,06 |
| M. catarrhalis [2] | <0,002–0,5 | 0,06 |
| E. coli [10] | 0,03-0,5 | 0,06 |
| Klebsiella spp. [11] | 0,06–4 | 0,5 |
| N. gonorrhoeae [11] | 0,004-0,125 | 0,015 |
| P. aeruginosa [4, 10, 11] | 0,12–64 | 8–>32 |
Chlamydia spp. В отношении C. trachomatis моксифлоксацин превосходит эритромицин, азитромицин, доксициклин и ципрофлоксацин, офлоксацин, что открывает перспективы для его применения в лечении урогенитальных инфекций.
По активности против C. pneumoniae моксифлоксацин находится на одном уровне с левофлоксацином и более активен по сравнению с ципрофлоксацином.
Mycoplasma pneumoniae. Моксифлоксацин обладает большей активностью чем тетрациклин (МПК90=0,25 мг/л), доксициклин, ципрофлоксацин и левофлоксацин, однако уступает кларитромицину и азитромицину [13, 14].
Mycoplasma hominis. По активности против M. hominis моксифлоксацин значительно превосходит доксициклин, кларитромицин, левофлоксацин и ципрофлоксацин [14].
Ureaplasma urealyticum. Моксифлоксацин незначительно уступает кларитромицину и проявляет высокую активность как в отношении чувствительных (МПК90 0,25 мг/л), так и резистентных к доксициклину штаммов (МПК90 0,5 мг/л). Моксифлоксацин активнее доксициклина, эритромицина, ципрофлоксацина и левофлоксацина [14, 15].
Legionella spp. Моксифлоксацин превосходит по активности ципрофлоксацин и такой классический АМП для лечения легионеллезной инфекции как эритромицин, но несколько уступает кларитромицину и рифампицину [16, 17].
Таблица 2. Активность моксифлоксацина в отношении внутриклеточных возбудителей
|
Микроорганизм |
МПК90, мг/л | Ссылка | ||||||
| Мокси- флоксацин |
Лево- флоксацин |
Ципро- флоксацин |
Азитро- мицин |
Кларит- ромицин |
Эрит- ромицин |
Докси- циклин |
||
| C. trachomatis | 0,06 | – | 1-2 | 0,06-0,125 | 0,015 | 0,25-0,5 | 0,25 | 21, 24, 26 |
| C. pneumoniae | 0,06-1 | 1 | 1-2 | 0,125-0,25 | 0,06 | 0,125 | 0,25 | 23, 24, 25 |
| M. pneumoniae | 0,063-0,125 | 0,5 | 1 | ≤0,008 | ≤0,008–0,06 | – | 0,12 | 27, 28, 29 |
| M. hominis | 0,06 | 1 | 4 | - | >32 | ≥16 | 4-16 | 28, 30 |
| U. urealiticum | 0,25 | 1 | 4 | - | 0,12 | 8 | 0,5-1 | 28, 30 |
| Legionella spp. | 0,016-0,06 | 0,016-0,03 | 0,06 | 0,5 | ≤ 0,004 | 0,12-0,5 | 8 | 31, 32 |
Mycobacterium spp. Моксифлоксацин активен в отношении как чувствительных, так и полирезистентных штаммов M. tuberculosis и превосходит ципрофлоксацин, офлоксацин и левофлоксацин. МПК90 моксифлоксацина для полирезистентных штаммов составляет 0,5 мг/л [18, 19].
По отношению к атипичным микобактериям (M. kansasii и M. avium-intracellulare) моксифлоксацин превосходит ципрофлоксацин и левофлоксацин [18].
Анаэробы. В отличие от фторхинолонов II-III поколений (ципрофлоксацина, офлоксацина, левофлоксацина) моксифлоксацин обладает высокой активностью против анаэробов, причем как неспорообразующих, так и спорообразующих. По своей антианаэробной активности моксифлоксацин сравним с имипенемом, метронидазолом и клиндамицином [20, 21].
Клиническая фармакология
Фармакокинетика
Моксифлоксацин практически полностью всасывается из желудочно-кишечного тракта при приеме внутрь, биодоступность составляет от 86% [22] до 91,8% [23]. При внутривенном введении 400 мг в течение 1 часа значения максимальной концентрации препарата в плазме (Cmax) и площади под фармакокинетической кривой (ПФК) незначительно больше чем при приеме 400 мг внутрь [22, 24].
Максимальная концентрация препарата в плазме (Cmax) в исследовании Stass и соавт. [22] составила 2,5 мг/л через 2 часа после приема внутрь 400 мг. В то же время в исследованиях Wise с соавт. [24] и Lubasch с соавт. [25] максимальные концентрации были 4,34-4,98 мг/л и достигались через 1 час. Прием пищи, включая молочные продукты, не влияет на всасывание моксифлоксацина [26, 27].
При приеме внутрь моксифлоксацин имеет большой объем распределения (Vd): 3,08–3,55 л/кг [22] и достигает высоких концентраций в тканях и жидкостях организма: в бронхиальном секрете, альвеолярных макрофагах, тканях верхнечелюстной пазухи и жидкости, покрывающей эпителий бронхов (табл. 3).
Таблица 3. Концентрации моксифлоксацина в жидкостях и тканях организма*
| Локус [ссылка] | Максимальная концентрация (соотношение ткань / плазма) |
Концентрация через 24 часа (соотношение ткань / плазма) |
| Слизистая верхнечелюстной пазухи [44] | 7,47 мг/кг (1,9) | 1,47 мг/кг (2,5) |
| Бронхиальный секрет [45] | 5,4 мг/кг (1,7) | 1,1 мг/кг (2,1) |
| Альвеолярные макрофаги [45] | 56,7 мг/л (18,6) | 35,9 мг/л (70,0) |
| Жидкость, покрывающая эпителий бронхов [45] | 20,7 мг/л (6,8) | 3,6 мг/л (1,4) |
* после приема 400 мг препарата внутрь
Концентрация моксифлоксацина в жидкостях дыхательных путей значительно превышает МПК90 для основных возбудителей респираторных инфекций.
Моксифлоксацин связывается с белками плазмы на 39,4–48%, что несколько выше, чем у ципрофлоксацина (35%). Метаболизируется в печени путем коньюгации с образованием двух метаболитов: М1 (ацетилглюкуронид) и М2 (сульфо-производное моксифлоксацина) [22].
При однократном приеме 400 мг моксифлоксацина внутрь более 96% дозы выводится через почки и ЖКТ, при этом с мочой экскретируется 15,1–35,4% препарата [22, 24]. В неизмененном виде через почки выводится 19,4% дозы, в виде метаболита М1 2,5% и в виде метаболита М2 13,6%. С фекалиями в неизмененном виде выводится 25,4% дозы и 35,5% в виде метаболита М1.
По данным большинства авторов период полувыведения составляет 12-13 час, что больше чем у ципрофлоксацина, офлоксацина и левофлоксацина. Длительный период полувыведения позволяет принимать препарат 1 раз в сутки [22, 24, 25].
Влияние возраста, заболеваний печени и почек
У взрослых возраст практически не влияет на фармакокинетические свойства моксифлоксацина, но значения максимальной концентрации препарата в плазме и площади под фармакокинетической кривой (ПФК) несколько выше у пожилых женщин по сравнению с молодыми и пожилыми мужчинами [28].
В отличие от офлоксацина и левофлоксацина при легкой почечной недостаточности (клиренс креатинина ³30 мл/мин/1,73 м2) период полувыведения остается неизменным и составляет 14,5 час [29]. Однако пока нет достаточной информации о применении моксифлоксацина при клиренсе креатинина <30 мл/мин/1,73 м2 или при гемодиализе, поэтому препарат не следует назначать этим категориям пациентов.
У пациентов с легкой и среднетяжелой печеночной недостаточностью (N=8) значения Cmax, ПФК и T1/2 оказались меньше, чем у здоровых добровольцев (N=10): Cmax – 2,55 и 3,02 мг/л; ПФК – 25,1 и 32,8 мг/л/час; T1/2 – 11,7 и 13,4 час соответственно [30]. В целом, на сегодняшний день мало данных о применении моксифлоксацина у пациентов с печеночной недостаточностью.
Существенных различий между фармакокинетическими параметрами при приеме моксифлоксацина внутрь и при внутривенном введении нет. Это позволяет использовать моксифлоксацин в САТ с ранним переходом на прием препарата внутрь.
Фармакодинамика
В настоящее время большее внимание уделяется фармакодинамическим свойствам АМП, которые значительно влияют на их эффективность. Считается, что для фторхинолонов условиями эффективности являются [31, 32]:
По результатам исследований с использованием in vitro моделирования с использованием респираторных патогенов значения ПФК/МПК и ПФК/МПКнесвяз для моксифлоксацина выше, чем для других фторхинолонов (табл. 4).
Таблица 4. Фармакодинамические свойства моксифлоксацина* [31]
|
Антибиотик |
Доза |
МПК, мг/л |
ПФК/МПК |
ПФК/МПКнесвяз |
|
Ципрофлоксацин |
500 мг/2 р/сут |
2 |
10 |
7 |
|
Ципрофлоксацин |
750 мг/2 р/сут |
2 |
14 |
10 |
|
Левофлоксацин |
500 мг/1 р/сут |
1 |
50 |
35 |
|
Моксифлоксацин |
400 мг/1 р/сут |
0,25 |
120 |
60 |
*Данные получены в in vitro модели с использованием полирезистентных штаммов S. pneumoniae
ПФК – площадь под фармакокинетической кривой
Понятие о ступенчатой антимикробной терапии
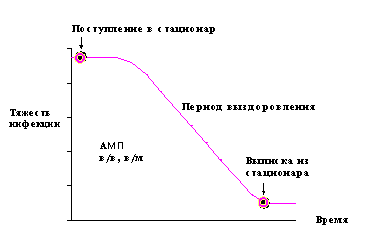
Расходы стационаров на приобретение лекарственных средств в среднем составляют 15-20% от бюджета, из них на долю АМП приходится 50-60%, что заставляет искать новые подходы к их применению [33, 34]. Одним из таких подходов является ступенчатая антибиотикотерапия (САТ). Применение подобной методики позволило снизить в США количество койко-дней на 440.000 в год, что привело к экономии порядка 440 млн $ за год [35]. В англоязычной литературе имеется несколько терминов с одинаковым содержанием: sequential therapy, streamline therapy, step-down therapy, switch therapy, follow-on therapy - двухэтапное применение АМП с переходом с парентерального на непарентеральный (как правило, пероральный) путь введения в возможно более короткие сроки с учетом клинических и лабораторных данных. Основная идея САТ заключается в сокращении длительности парентерального введения АМП, что может привести к значительному уменьшению стоимости лечения, сокращению срока пребывания в стационаре при сохранении высокой клинической эффективности терапии (рис. 1).
 |
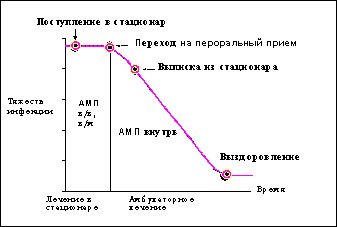 |
Рис. 1. Традиционный и ступенчатый подход к лечению тяжелой внебольничной пневмонии
(Ramirez J.A. Diagn Microbiol Infect Dis 1995; 22:219-223)
Несмотря на очевидные преимущества САТ, в силу разных причин (отсутствие пероральных АМП, сомнения в их эффективности, сложившиеся стереотипы и т.д.) она не всегда применяется на практике. По данным R.Quintiliani и соавт. [36], 75% госпитализированных пациентов с различными инфекциями могли быть переведены с парентерального на пероральный путь введения АМП. Перечень заболеваний, при которых проведены контролируемые клинические испытания САТ, включает пневмонию, инфекции урогенитального тракта, инфекции кожи и мягких тканей, остеомиелит, интраабдоминальные инфекции [37, 38]. Однако наибольшее число работ проведено по САТ внебольничной пневмонии.
Преимущества САТ
Для пациента:
Для стационара:
Ограничения ступенчатой терапии
Наряду с преимуществами можно выделить определенные клинические и экономические ограничения САТ. Первые из них связаны с тем, что существует риск клинической неэффективности вследствие снижения комплаентности пациента при приеме пероральных АМП (т.е. желания пациента выполнять рекомендации и назначения врача). Основными факторами, влияющими на этот показатель, являются свойства АМП, характер заболевания (острое, хроническое), индивидуальные особенности пациента, поведение медицинского персонала. Приверженность зависит от кратности приема препарата, длительности курса, лекарственной формы, связи с приемом пищи, переносимости. Показана прямая зависимость между частотой приема АМП и приверженностью пациента: при однократном приеме она составила 84%, двукратном - 75% и трехкратном – 59%. Поэтому предпочтение следует отдавать пероральным АМП, которые можно назначать 1-2 раза в сутки [40].
Лекарственные взаимодействия, существенно влияя на биодоступность отдельных пероральных АМП, могут быть причиной снижения их эффективности. Так, антациды, препараты железа и кальций (молочные продукты) снижают всасывание пероральных фторхинолонов, тетрациклина, поэтому пациенту, получающему эти препараты, следует делать двухчасовой интервал между ними и приемом вышеуказанных АМП.
Относительные экономические недостатки САТ связаны с ранней выпиской и продолжением лечения в амбулаторных условиях, что вынуждает самого пациента покупать препарат для завершения курса лечения. Однако это меньше касается пациентов, имеющих медицинскую страховку (полис) или льготы на приобретение лекарственных препаратов.
Таблица 5. Критерии перевода больного на пероральный АМП [41 с изменениями]
|
Основные (клинические) |
Дополнительные |
|
| Микробиологические | Фармакологические | |
| Температура тела <38°С в течение 24-48 ч Тенденция к нормализации клинического анализа крови, СРБ* Улучшение/стабилизация клинической картины Возможность перорального приема пищи и жидкости Отсутствие нарушения всасывания в ЖКТ Низкая вероятность лекарственных взаимодействий |
Возбудитель выделен или нет Известна чувствительность возбудителя к АМП Моно- или комбинированная терапия |
Наличие соответствующего АМП Достаточная биодоступность АМП Спектр активности АМП |
Сроки и условия перевода пациента на пероральный прием АМП
Важным фактором при ступенчатой терапии является срок перевода пациента на пероральный путь введения АМП; ориентиром могут служить стадии инфекции. R.Quintiliam и соавт. [42] выделяют три стадии инфекционного процесса у пациентов, находящихся на стационарном лечении: I стадия продолжается 2-3 дня и характеризуется нестабильной клинической картиной, возбудитель и его чувствительность к АМП, как правило, неизвестны, антибактериальная терапия носит эмпирический характер, чаще всего назначают препарат широкого спектра действия. На II стадии клиническая картина стабилизируется или улучшается, возбудитель и его чувствительность могут быть установлены, что позволяет провести коррекцию терапии. На III стадии (примерно через 7 дней от начала заболевания) наступает выздоровление и антибактериальная терапия может быть завершена. Оптимальным временем для перевода пациента на пероральную терапию является II стадия инфекционного процесса. Выделяют клинические, микробиологические и фармакологические критерии перевода пациента на второй этап ступенчатой терапии (табл. 5).
Требования к пероральным АМП
Выбирая пероральный АМП, необходимо учитывать его спектр активности, фармакокинетические характеристики, взаимодействие с другими препаратами, переносимость, а также достоверные данные о его клинической эффективности при лечении конкретного заболевания. Предпочтение следует отдавать препарату с наибольшей биодоступностью, ее необходимо учитывать и при определении дозы. При назначении АМП врач должен быть уверен, что его концентрация в очаге инфекции будет превосходить минимальную подавляющую концентрацию (МПК) для возбудителя. Наряду с этим, следует учитывать такие фармакодинамические параметры, как время сохранения концентрации выше МПК, площадь под фармакокинетической кривой, площадь под фармакокинетической кривой выше МПК и другие.
После выбора перорального АМП и перевода пациента на второй этап ступенчатой терапии необходимо продолжать динамический контроль за его клиническим состоянием, переносимостью АМП и приверженностью к проводимой терапии. Назначая пероральный АМП, следует всегда иметь в виду спектр его нежелательных реакций. Например, при использовании b-лактамов выше риск аллергических реакций, фторхинолоны не рекомендуют применять у детей, беременных и кормящих женщин вследствие их негативного влияния на развитие хрящевой ткани. В случае развития у пациента нежелательных явлений в первую очередь следует определить их связь с АМП, тяжесть и только потом принимать решение об отмене препарата.
Выбор оптимального АМП для ступенчатой терапии не является простой задачей. P.Jewesson [43] приводит характеристики "идеального" перорального АМП для второго этапа ступенчатой терапии (табл. 6).
Таблица 6. Характеристики “идеального” АМП [43]
| Характеристика | Моксифлоксацин |
|
Пероральный АМП тот же, что и парентеральный |
Да |
|
Доказанная клиническая эффективность при лечении данного заболевания |
Да |
|
Наличие различных оральных форм (таблетки, растворы и т.д.) |
Да |
|
Высокая биодоступность |
Да |
|
Отсутствие лекарственных взаимодействий на уровне всасывания |
с Ca2+, Mg2+, Fe2+ |
|
Хорошая переносимость при пероральном приеме |
Да |
|
Длительный интервал дозирования |
Да |
|
Низкая стоимость |
Нет |
Варианты ступенчатой терапии
В зависимости от орального АМП выделяют 4 варианта САТ [43]: (I) парентерально и внутрь назначают один и тот же АМП; пероральный АМП обладает хорошей биодоступностью; (II) парентерально и внутрь назначают один и тот же АМП; пероральный препарат имеет низкую биодоступность; (III) парентерально и внутрь назначают разные АМП; оральный АМП обладает хорошей биодоступностью; (IV) парентерально и внутрь назначают разные АМП; пероральный препарат имеет низкую биодоступность. Идеальным является первый вариант. Например, фторхинолон (ципрофлоксацин, пефлоксацин, левофлоксацин, моксифлоксацин) внутривенно, а далее – внутрь.
Таким образом, САТ является фармакоэкономически обоснованным режимом терапии, обеспечивающим преимущества как для пациента, так и стационара. САТ может применяться в любых лечебных учреждениях, она не влечет за собой дополнительных вложений и затрат, а требует лишь изменения привычных подходов врачей к проводимой антибактериальной терапии.
САТ при внебольничной пневмонии: данные клинических исследований
Эффективность моксифлоксацина в САТ
В нескольких клинических исследованиях были изучены клиническая и бактериологическая эффективность САТ моксифлоксацином при внебольничной пневмонии (табл. 7). В одном исследовании моксифлоксацин сравнивали с комбинацией амоксициллин/клавуланат ± кларитромицин. Клиническая эффективность в группе моксифлоксацина составила 93%, в контрольной - 85% [95% C.I. 2.9%, 13.2%]; уровень эрадикации для моксифлоксацина был равен 94%, в группе сравнения – 82% [95% C.I. 1.2%, 22.9%]. Время, необходимое для нормализации температуры было значительно ниже в группе моксифлоксацина. По сравнению с контрольной группой для моксифлоксацина требовался более короткий курс в/в терапии и меньшее время госпитализации пациентов [44].
В работе Choundhri S.H. и соавт. сравнивали САТ моксифлоксацином с другими фторхиноланами III-IV поколений, в частности с терапией алатрофлоксацином/тровафлоксацином, которые, после получения данных о потенциальной гепатотоксичности, были заменены на левофлоксацин. Уровень клинической эффективности в группе моксифлоксацина составил 86%, в группе сравнения – 89% [95% C.I. -8.9%, 4.2%]. Уровень бактериологической эффективности был равен 83% и 90%, соответственно [95% C.I. -21.4%, 3.6%]. Несмотря на большее число пациентов в группе моксифлоксацина с отягощенным анамнезом, тяжелым общим состоянием, септическим шоком и пневмонией, вызванными P.aeruginosa, эффективность моксифлоксацина была эквивалентна препаратам сравнения [45].
Grossman C. и соавт. сравнили вышеуказанные режимы терапии при тяжелой внебольничной пневмонии. Клиническая эффективность в группе моксифлоксацина была равна 79%, в группе сравнения – 80%. Уровень эрадикации в отношении S.pneumoniae составил 82% и 85%, а в отношении H.influenzae – 71% и 60%, соответственно [46].
Таблица 7. Эффективность моксифлоксацина при ступенчатой терапии внебольничной пневмонии (сводные данные)
| Автор, ссылка, дизайн | Препараты сравнения | Кол-во пациентов | Режим дозирования | Курс, дней | Эффективность, % | Примечания | |
| Клини- ческая |
Бактерио логическая |
||||||
| Finch R. и соавт.[44] ОИ |
МКС АМК±КЛР |
258 280 |
400/400 мг 1 р/сут 1,2 г в/в / 625 мг внутрь 3 р/сут ± 500 мг 2 р/сут | 7-14 7-14 |
93,4 85,5 |
93,7 81,7 |
Пациенты на стационарном лечении |
| Choundhri S.H. и соавт.[46] Р, ДС |
МКС АЛАТР/ТРО В или ЛФЦ |
249 258 |
400/400 мг 1 р/сут 200/200 мг 1 р/сут или 500/500 мг 1 р/сут |
7-14 7-14 |
86 89 |
83 90 |
Пациенты на стационарном лечении |
| Grossman C. и соавт. [47] Р, ДС |
МКС АЛАТР/ТРО В или ЛФЦ |
61 49 |
400/400 мг 1 р/сут 200/200 мг 1 р/сут или 500/500 мг 1 р/сут |
7-14 | 79 80 |
82 71† 85 60‡ |
Пациенты с тяжелой внебольничной пневмонии † S.pneumoniae ‡ H.influenzae |
| Drummond M. и соавт.[45] Р |
МКС АМК±КЛР |
306 322 |
400/400 мг 1 р/сут 1,2 г в/в / 625 мг внутрь 3 р/сут ± 500 мг 2 р/сут | 7-14 | 93 85 |
Уровень эрадикации не определялся | |
Заслуживают внимания данные относительно эффективности моксифлоксацина при внебольничной пневмонии, вызванной атипичными возбудителями. S. Larsen при анализе сводных данных, полученных при сравнении САТ моксифлоксацином с комбинацией амоксициллин/клавуланата ± кларитромицин или фторхинолонами (алатрофлоксацин/тровафлоксацин или левофлоксацин), показали, что частота эрадикации в отношении M. pneumoniae и C. pneumoniae составила для обеих групп 96%/97% и 93%/92%, соответственно. В отношении L. pneumophila моксифлоксацин превзошел по уровню эрадикации препараты сравнения – 100% и 83%, соответственно (табл. 8) [47].
Таблица 8. Эффективность ступенчатой терапии моксифлоксацином при внебольничной пневмонии, вызванной атипичными возбудителями (сводные данные)
|
Возбудитель |
Уровень эрадикации |
|
|
Моксифлоксацин 400/400 мг 1 р/сут |
Группа сравнения* | |
|
Mycoplasma pneumoniae |
96 |
97 |
|
Chlamydia pneumoniae |
93 |
92 |
|
Legionella pneumophila |
100 |
83 |
Алатрофлоксацин/Тровафлоксацин 200 мг 1 р/сут или Левофлоксацин 500 мг 1 р/сут
Переносимость моксифлоксацина при САТ
В клинических исследованиях частота НЛР при приеме моксифлоксацина была аналогична частоте при приеме препаратов сравнения: кларитромицина [48, 49, 50, 51], амоксициллина [52]. Только по данным Burke T. и соавт. при приеме моксифлоксацина чаще встречалась тошнота, чем при приеме цефуроксим аксетила (11% и 4% соответственно, p=0,003) [53]. Частота возникновения других НЛР оказалось аналогичной в группах сравнения.
При исследовании САТ для лечения тяжелой внебольничной пневмонии у 158 пациентов наиболее частые НЛР по данным Grossman C. и соавт. были представлены реакциями в месте введения препарата (6%) и диареей (6%) (табл. 9) [46].
Таблица 9. Нежелательные лекарственные реакции при ступенчатой терапии моксифлоксацином тяжелой внебольничной пневмонии [47]
|
НЛР |
Моксифлоксацин (n=83), |
Группы сравнения (n=75), |
|
Реакции в месте введения препарата |
5 (6) |
7 (9) |
|
Диарея |
5 (6) |
5 (7) |
|
Бессонница |
4 (5) |
1 (1) |
|
Головная боль |
3 (4) |
0 (0) |
|
Кандидоз ротовой полости |
3 (4) |
3 (4) |
Mandell L и соавт. показали, что наиболее частые НЛР были связаны с желудочно-кишечным трактом и включали: диарею (6%), отклонения в показателях функции печени (5%) и тошноту (3%), в то время как реакции в месте введения препарата имели место только у 2% пациентов. Не было зарегистрировано ни одного случая фото- и нефротоксичности [54].
Из 10,5 млн пациентов, которым был назначен моксифлоксацин (сегодня это число приближается к 19 миллионам), только у 2634 были подтверждены НЛР. Три из 4 описанных случаев пируэтной тахикардии были документально подтверждены и возникали у пациентов с заболеваниями сердечно-сосудистой системы, нарушениями электролитного состава крови и на фоне приема аритмогенных препаратов (табл. 10) [55].
Таблица 10. Профиль безопасности пероральной формы моксифлоксацина [56]
| Исследование | Количество пациентов | Частота НЛР | Наиболее частые НЛР | |||
| Тошнота | Диарея | Головокружение | Сыпь | |||
| IV фаза (США) | 18 374 | 14,3% | 5,3% | 2,2% | 2,0% | - |
| ПРН в амбулаторных условиях (Германия) | 16 007 | 2% | 0,5% | 0,4% | 0,2% | - |
| ПРН в стационарах (Германия) | 2 188 | 3% | 1% | - | 0,1% | 0,2% |
| Мета-анализ 30 клинических исследований моксифлоксацина | 7 368 | 25% | 7% | 5% | 3% | - |
| Препараты сравнения | 5 678 | 23% | 5% | 4% | 2% | - |
Влияние на сердечно-сосудистую систему
При исследовании безопасности САТ при внебольничной пневмонии у 550 пациентов группы моксифлоксацина не было зафиксировано ни одного эпизода развития нежелательной лекарственной реакции со стороны сердечно-сосудистой системы, связанного с удлинением интервала QT. После внутривенного введение моксифлоксацина изменения продолжительности QT составили 3 ± 29 мсек, причем коррегированный интервал QT не отличался от показателей при пероральном приеме моксифлоксацина. Корреляции между концентрацией моксифлоксацина в плазме и частотой развития аритмий, связанных с удлинением QT, отмечено не было [54].
Перспективы САТ моксифлоксацином
САТ моксифлоксацином уже доказала свою эффективность при лечении внебольничной пневмонии. Однако, учитывая широкий спектр активности данного препарата, который включает наряду с респираторными патогенами и другую флору, в частности возбудителей нозокомиальных инфекций, анаэробов, возбудителей инфекций кожи и мягких тканей, интраабдоминальных и гинекологических инфекций, проводятся дальнейшие клинические исследования с целью определить место моксифлоксацина в лечении данных заболеваний.
При лечении инфекций кожи и мягких тканей по данным трех рандомизированных двойных слепых исследований моксифлоксацин не уступал по клинической и бактериологической эффективности цефалексину и комбинации цефалексина с метронидазолом [56, 57, 58].
При терапии неосложненных воспалительных заболеваний органов малого таза у женщин моксифлоксацин (400 мг/1 р./сутки, 14 дней) был сравним по клинической эффективности (96,6% и 98,0%) с комбинацией ципрофлоксацина (500 мг однократно), доксициклина (100 мг/2 р./сутки) и метронидазола (500 мг/3 р./сутки) в течение 14 дней [59]. Бактериологическая эффективность моксифлоксацина была выше3 чем в группе сравнения (92,5% и 88,2% соответственно).
Естественно, что при тяжелых инфекциях требуется начальная терапия парентеральными препаратами с последующим переходом на прием внутрь. В связи с этим необходимо дальнейшее изучение моксифлоксацина как препарата потенциально способного оказать эффект при его ступенчатом использовании не только в отношении респираторных заболеваний, но и тяжелых инфекционных поражениях, включая сепсис, нозокомиальную пневмонию, интраабдоминальные инфекции.
|
3 Данных о статистической значимости различий нет |
Заключение
Моксифлоксацин является новым фторхинолоном IV поколения, обладающим высокой активностью в отношении большинства клинически значимых возбудителей, включая респираторные патогены, грамположительные и грамотрицательные микроорганизмы ответственные за развитие нозокомиальных инфекций, анаэробы.
Благодаря отсутствию существенных различий между фармакокинетическими параметрами моксифлоксацина при в/в и пероральном введении сегодня стало возможным применять его в САТ с ранним переходом на прием препарата внутрь. САТ позволяет снизить длительность пребывания пациента в стационаре, уменьшая как общую стоимость терапии, так и частоту НЛР, связанных с парентеральным применением АМП.
Обладая оптимальной фармакокинетикой, позволяющей принимать препарат 1 раз в сутки, хорошей переносимостью и высокой клинической эффективностью при лечении внебольничной пневмонии (более быстрое достижение апирексии, хорошая эффективность при тяжелом статусе пациента, включая эпизоды бактериемии) имеется большая перспектива использования моксифлоксацина для САТ при других инфекционных заболеваниях.
Литература
1. Ricci V., Piddock L. Characterization of the QRDR of gyrA of Bacteroides fragilis and role in fluoroquinolone resistance. Proceedings of the 38th ICAAC†; 1998 Sep 24-27; San Diego, USA. p. 121.
2. Jones M., Staple A., Critchley I., et al. Benchmarking the in vitro activities of moxifloxacin and comparator agents against resent respiratory isolates from 377 medical centers throughout the United States. Antimicrob Agents Chemother 2000; 44:2645-52.
3. Johnson A., Livermore D., Warner M., James D., George R. Activity of moxifloxacin against invasive and multiresistant pneumococci from England and Wales. Proceedings of the 39th ICAAC†; 1999 Sep 26-29; San Francisco, USA. p. 255.
4. Milatovic D., Schmitz F., Brisse S., Verhoef J., Fluit A. In vitro activities of sitafloxacin (DU-6859a) and six other fluoroquinolones against 8,796 clinical bacterial isolates. Antimicrob Agents Chemother 2000; 44:1102-7.
5. Buxbaum A., Straschil U., Moser C., Graninger W., Georgopoulos A. Comparative susceptibility to penicillin and quinolones of 1385 Streptococcus pneumoniae isolates. J Antimicrob Chemother 1999; 43 (Suppl B):13-8.
6. Souli M., Weneersten C., Eliopoulos G. In vitro activity of BAY 12-8039, a novel 8-methoxyquinolone, against species representative of respiratory tract infections. Proceedings of the 37th ICAAC†, 1997. Poster F126.
7. Blondeau J., Church D., Laskowski R., Borsos S. Comparative activity of moxifloxacin and other quinolones against macrolide sensitive and resistant Streptococcus pyogenes. J Antimicrob Chemother 1999; 44 (Suppl A):131.
8. Jones M., Visser M., Klootwijk M., Heisig P., Verhoef J., Schmitz F. Comparative activities of clinafloxacin, grepafloxacin, levofloxacin, moxifloxacin, ofloxacin, sparfloxacin, and trovafloxacin and nonquinolones linozelid, quinupristin-dalfopristin, gentamicin, and vancomycin against clinical isolates of ciprofloxacin-resistant and -susceptible Staphylococcus aureus strains. Antimicrob Agents Chemother 1999; 43:421-3.
9. Kretchikov V.A., Dekhnich A.V., Startchounski L.S. Comparative activity of old and new quinolones against nosocomial Staphylococcus aureus. Proceeding of 12th ECCMID¨; 2002 Apr 24-27; Milan, Italy. Abstract P1145.
10. Fass R. In vitro activity of BAY 12-8039, a new 8-methoxyquinolone. Antimicrob Agents Chemother 1997; 41:1818-24.
11. Woodcock J., Andrews J., Boswell F., Brenwald N., Wise R. In vitro activity of BAY 12-8039, a new fluoroquinolone. Antimicrob Agents Chemother 1997; 41:101-6.
12. Кречиков В., Эйдельштейн И. Активность левофлоксацина и моксифлоксацина в отношении ципрофлоксацин-нечувствительных нозокомиальных штаммов, продуцентов b-лактамаз расширенного спектра (ESBL). Клин Микробиол Антимикроб Химиотер 2001; 3 Приложение 1: 23.
13. Duffy L., Kempf M., Crabb D., Wall W., Herrington J. In vitro activity of moxifloxacin and six other new antimicrobials against Mycoplasma pneumoniae. Proceedings of the 39th ICAAC†; 1999 Sep 26-29; San Francisco, USA. p. 252.
14. Bebear C.M., Renaudin H., Boudjadja A., Bebear C. In vitro activity of BAY 12-8039, a new fluoroquinolone against mycoplasmas. Antimicrob Agents Chemother 1998; 42:703-4.
15. Ullmann U., Schubert S., Krausse R. Comparative in-vitro activity of levofloxacin, other fluoroquinolones, doxycycline and erythromycin against Ureaplasma urealyticum and Mycoplasma hominis. J Antimicrob Chemother 1999; 43 (Suppl C):33-6.
16. Schulin T., Wennersten C., Ferraro M., Moellering R. Jr, Eliopoulos G. Susceptibilities of Legionella spp. to newer antimicrobials in vitro. Antimicrob Agents Chemother 1998; 42:1520-3.
17. Gomez-Lus R., Adrian F., del Campo R., et. al. Comparative in vitro bacteriostatic and bactericidal activity of trovafloxacin, levofloxacin and moxifloxacin against clinical and environmental isolates of Legionella spp. Int J Antimicrob Agents 2001; 18:49-54.
18. Gillespie S., Billington O. Activity of BAY 12-8039 against mycobacteria. Proceedings of the 8th ICID‡; 1998 May 15-18; Boston, USA. p. 176.
19. Rivera-Martínez E., Pérez-González E., García M., Orrantia-Gradín R, Hernández-Oliva G, Torres-Gutierrez Rubro A. Determination of the in vitro susceptibility of different strains of M.tuberculosis to BAY 12-8039 and other antituberculosis agents. Proceedings of the 8th ICID‡; 1998 May 15-18; Boston, USA. p. 173-4.
20. Nord C., Edlund C. Susceptibility of anaerobic bacteria to BAY 12-8039, a new methoxyquinolone. Clin Microb Infection 1997; 3 (Suppl 2):285.
21. MacGowan A., Bowker K., Holt H., Wootton M., Reeves D. BAY 12-8039, a new 8-methoxy-quinolone: comparative in-vitro activity with nine other antimicrobials against anaerobic bacteria. J Antimicrob Chemother 1997; 40:503-9.
22. Stass H., Kubitza D. Pharmacokinetics and elimination of moxifloxacin after oral and intravenous administration in man. J. Antimicrob. Chemother. 1999; 43 (Suppl B):83-90.
23. Ballow C., Lettieri J., Agarwal V., Liu P., Stass H., Sullivan J. Absolute bioavailability of moxifloxacin. Clin Ther 1999; 21:513-22.
24. Wise R., Andrews J., Marshall G., Hartman G. Pharmacokinetics and inflammatory-fluid penetration of moxifloxacin following oral or intravenous administration. Antimicrob Agents Chemother 1999; 43:1508-10.
25. Lubasch A., Keller I., Borner K., Koeppe P., Lode H. Comparative pharmacokinetics of ciprofloxacin, gatifloxacin, grepafloxacin, levofloxacin, trovafloxacin and moxifloxacin after single oral administration in healthy volunteers. Antimicrob Agents Chemother 2000; 44:2600-3.
26. Lettieri J., Vargas R., Agarwal V., Liu P. Effect of food on the pharmacokinetics of a single oral dose of moxifloxacin 400 mg in healthy male volunteers. Clin Pharmacokinet 2001; 40 (Suppl 1):19-25.
27. Stass H., Kubitza D. Effects of dairy products on the oral bioavailability of moxifloxacin, a novel 8-methoxyfluoroquinolone, in healthy volunteers. Clin Pharmacokinet 2001; 40 (Suppl 1):33-8.
28. Sullivan J., Lettieri J., Liu P., Heller A. The influence of age and gender on the pharmacokinetics of moxifloxacin. Clin Pharmacokinet 2001; 40 (Suppl 1):11-8.
29. Stass H., Halabi A., Delesen H. No dose adjustment needed for patients with renal impairment receiving oral BAY 12-8039 (M). Proceedings of the 38th ICAAC†; 1998 Sep 24-27; San Diego, USA. p. 5.
30. Stass H., Kubitza D. No dose adjustment is needed for moxifloxacin (MOX) in subjects suffering from hepatic impairment (HI). Clin Microb Infection 1999; 5 (Suppl 3):291.
31. Zhanel G., Walters M., Karlowsky J., Laing N., Hoban D. Activity of free (unbound) fluoroquinolone serum concentrations versus multi-drug resistant Streptococcus pneumoniae using an in vitro pharmacodynamic model. Proceedings of the 40th ICAAC†; 2000 Sept 17-20; Toronto, Canada. p. 7.
32. Wright D., Brown G., Peterson M., Rotschafer J. Application of fluoroquinolones pharmacodynamics. J Antimicrob Chemother 2000; 46:669-83.
33. Jewesson P. Cost-effectiveness and value of an IV switch. PharmacoEconomics, 1994, 5 (Suppl 2), 20-26.
34. Jewesson P. Pharmaceutical, pharmacokinetic and other considerations for intravenous to oral stepdown therapy. Can. Infect. Dis. J., 1995, 6 (Suppl. A), 11-16.
35. Ramirez J.A. Managing antiinfective therapy of community-acquired pneumonia in the hospital setting: focus on switch therapy. Pharmacotherapy 2001; 21:79S-82S
36. Quintiliani R., Nightingale C., Crowe H. et al. Strategic antibiotic decision-making at the formulary level. Rev. Inf. Dis., 1991, 13, S770-S777.
37. Ramirez J. Advances in antibiotic use: switch therapy. Curr. Ther. Res., 1993, 55 (A), 30-34.
38. Janknegt R., van der Meer J. Sequential therapy with intravenous and oral cephalosporins. J. Antimicrob. Chemother., 1994, 33, 169—177.
39. Страчунский Л.С., Розенсон О.Л. Ступенчатая терапия: новый подход к применению антибактериальных препаратов. Клиническая фармакология и терапия 1997; 6:20-4
40. Eisen S., Miller D., Woodward R. et al: The effect of prescribed daily dose frequency on patient medication compliance. Arch. Intern. Med., 1990, 150, 1881-1884.
41. Nathwani D. Cost-effectiveness considerations for combination therapies. In: Antibiotic combination therapy - the role of ciprofloxacin. Cambridge Medical Publications, 1997, 19.
42. Quintiliani R., Cooper В., Briceland L. et al. Economic impact of streamlining antibiotic administration. Am. J. Med., 1987, 82 (Suppl. 4A), 391-394
43. Jewesson P. Economic impact of intravenous-to-oral antibacterial stepdown therapy. Clin. Drug Invest., 1996, 11 (Suppl 2), 1-9.
44. Finch R., Collins O., Kubin R. IV/PO Moxifloxacin (MXF) compared with IV/PO amoxicillin/clavulanate (AMC) +/- clarithromycin (CMP) in the treatment of community acquired pneumonia (CAP) admitted to hospital. Presented at the 11th ECCMID¨, Istanbul, Turkey, 1-4 April, 2001. Poster # P862
45. Choudhri S.H., Hollister A.S., Haverstock D., Weinstein D.M., Jackson P., Church D. Safety and efficacy of sequential (IV to PO) moxifloxacin for the treatment of community-acquired pneumonia in hospitalized patients. Presented at the 1st International Symposium on Resistant Gram-positive Infections, San Antonio, Texas, 3-5 December, 2000. Poster # I-14
46. Grossman C., Choudhri S., Haverstock D., Jackson P., Church D. Moxifloxacin intravenous-to-oral switch therapy for severe community-acquired pneumonia. Presented at CHEST 2001, Philadelphia, Pennsylvania, 4-8 November, 2001. Poster #187
47. Larsen S., Choudhri S., Haverstock D., Jackson P., Church D. Efficacy and safety of sequential (IV to PO) moxifloxacin for treatment of community-acquired pneumonia due to atypical pathogens. Presented at the 41st ICAAC†, Chicago, Illinois, 16-19 December, 2001. Poster # 865
48. Fogarty C., Grossman C., Williams J., Haverstock D., Church D. Efficacy and safety of moxifloxacin vs clarithromycin for community-acquired pneumonia. Infect Med 1999; 16:748-63.
49. Hoffken G., Meyer H., Sprenger K., Verhoef L. Efficacy and safety of moxifloxacin (MXF) vs clarithromycin (Кларитро) for the treatment of community-acquired pneumonia (CAP). J Antimicrob Chemother 1999; 44 (Suppl A):127.
50. Chodosh S., DeAvate C., Haverstock D., Aneiro L., Church D. Short-course moxifloxacin therapy for treatment of acute bacterial exacerbations of chronic bronchitis. Resp Med 2000; 94:18-27.
51. Wilson R., Kubin R., Ballin I., et al. Five day moxifloxacin therapy compared with 7 day clarithromycin therapy for the treatment of acute exacerbations of chronic bronchitis. J Antimicrob Chemother 1999; 44:501-13.
52. Petipretz P., Arvis P., Marel M., et. al. Oral moxifloxacin versus high-dosage amoxycillin in the treatment of mild-to-moderate, community-acquired, suspected pneumococcal pneumonia in adults. Chest 2001; 119:185-95.
53. Burke T., Villanueva C., Mariano H. Jr., et al. Comparison of moxifloxacin and cefuroxime axetil in the treatment of acute maxillary sinusitis. Clin Ther 1999; 21:1664-77.
54. Mandell L., Choudhri S.H., Kubin R. Safety assessment of sequential IV/PO moxifloxacin in the treatment of patients with community-acquired pneumonia (CAP). Presented at the 11th ECCMID¨, Istanbul, Turkey, 1-4 April, 2001. Poster # P863
55. P.B. Iannini, R. Kubin, C. Reiter. Over 10 million patient uses: An update on safety profile of oral moxifloxacin. Proceedings of the 42nd ICCAC†; 2002 Sep 27-30; San Diego, USA. p.346
56. Parish L., Heyd A., Haverstock D., Church D. Efficacy and safety of moxifloxacin versus cephalexin in the treatment of mild to moderate acute uncomplicated skin and skin structure infections. J Antimicrob Chemother 1999; 44 (Suppl A):137.
57. Leal del Rosal P., Martinez R., Fabian G., et al. Efficacy and safety of moxifloxacin vs cephalexin in the treatment of mild to moderate uncomplicated skin and soft tissue infections (uSSSI). J Antimicrob Chemother 1999; 44 (Suppl A):148.
58. Leal del Rosal P., Fabian G., Vick-Fragoso R. Efficacy and safety of moxifloxacin vs cephalexin (with or without metronidazole) in the treatment of mild to moderate uncomplicated skin and skin structures infections (uSSSI). Proceedings of the 39th ICAAC†; 1999 Sep 26-29; San Francisco, USA. p. 716.
59. Heystek M., Tellarini M., Schmitz H., Krasemann C. Efficacy and safety of moxifloxacin vs ciprofloxacin plus doxycycline plus metronidazole for the treatment of uncomplicated pelvic inflammatory disease (PID). J Antimicrob Chemother 1999; 44 (Suppl A):143.
†Interscience Conference on Antimicrobial Agents and Chemotherapy
¨ European Congress of Clinical Microbiology and Infectious Diseases
‡ International Congress on Infectious Diseases
Авелокс® (моксифлоксацин) - Досье препарата
Комментарии
ПРАКТИКА ПЕДИАТРА
