Оценка эффективности вакцины Акт-ХИБ у детей из групп риска
Статьи

АКТ-ХИБ
|
№2 (26) март/апрель 2003 г.
|
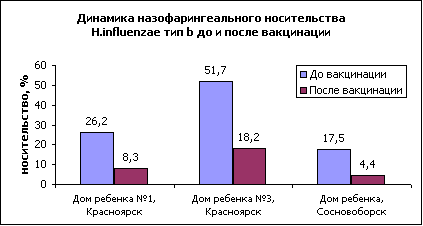
Оценка эффективности вакцины "Акт-ХИБ" у детей из группы риска Л.М. Куртасова2, Л.А. Рузаева1, А.А. Двоеконко1, Г.А. Зарянко1, Н.Н. Опейкина1, В.А. Третьякова1, Н.А. Шакина1, С.В. Ященко1 В настоящее время в России обоснованную озабоченность педиатров вызывает проблема гемофильной инфекции [3]. Это связано с ее повсеместным распространением, большим удельным весом тяжелых форм (менингиты, пневмонии, эпиглоттиты), высокой летальностью и многочисленными осложнениями [1,4,5]. По статистическим данным детской инфекционной больницы №1 г. Красноярска на протяжении последних 3-х лет Haemophilus influenzae тип b (ХИБ) является этиологическим фактором в формировании 30,4% гнойных менингитов и 29,8% крупов у детей, госпитализированных для стационарного лечения. При этом следует отметить, что возбудитель поражает в основном детей раннего возраста. Цель настоящего исследования - комплексное изучение реактогенности, клинической и эпидемиологической эффективности вакцины Акт-ХИБ (производство Авентис Пастер, Франция) у детей раннего возраста с поражениями ЦНС. Для реализации поставленной цели были проведены динамические наблюдения за 277 детьми с поражениями ЦНС в возрасте от 3-х месяцев до 4-х лет в специализированных домах ребенка (СДР) закрытого типа в городах: Ачинск, Красноярск, Минусинск, Сосновоборск Красноярского края. Все исследуемые пациенты вакцинировались в период клинической ремиссии. При наличии гипертензионно-гидроцефалического синдрома вакцина вводилась в стадии клинической компенсации. Вакцинацию Акт-ХИБ у 141 ребенка проводили отдельно, у 136 детей - в комбинации с другими вакцинами. В зависимости от сочетания получаемых в один день прививок сформировано 5 групп детей. Для изучения частоты встречаемости ХИБ-носительства было проведено бактериологическое исследование отделяемого из носоглотки у 201 наблюдаемого ребенка в период до вакцинации Акт-ХИБ и через 6 месяцев после иммунизации в 3-х СДР. Отделяемое из носоглотки отбирали с помощью стерильного ватного тампона из нижней носовой раковины обоих носовых ходов, а при необходимости и задней стенки глотки, доставляли в пробирках с "транспортной" средой. Бактериологическое исследование отделяемого из носоглотки проводилось с использованием шоколадного Haemophilus-агара, стрипов API-NH, латекс-теста H. influenzae b; чувствительность к антибактериальным препаратам определялась на стрипах ATB-NH с помощью автоматического анализатора Expression (Bio Merieux, Франция). Идентификация осуществлялась с помощью компьютерной программы APILAB [6]. Для оценки профилактической эффективности вакцины Акт-ХИБ использовали сравнительный анализ заболеваемости (менингит, пневмония, бронхит, отит, синусит, круп) у наблюдаемых детей с определением индекса эпидемиологической эффективности. Полученные результаты обрабатывали с помощью методов вариационной статистики с определением критерия достоверности Стьюдента t. Клиническая часть исследования включала динамический контроль за состоянием здоровья привитых детей. Особое внимание уделяли изучению переносимости детьми вакцины Акт-ХИБ. Реактогенность вакцины оценивалась по результатам активного динамического наблюдения за привитыми в течение 5 дней после вакцинации. При этом учитывались как местные (болезненность, гиперемия и инфильтрация в месте инъекции), так и общие реакции (повышение температуры тела, недомогание, слабость, миалгия и др.). Активное наблюдение за вакцинированными в течение 5 дней после прививки позволило у 9 (3,25%) детей выявить нетяжелые общие реакции, которые сохранялись в течение 1-2-х дней с последующим самостоятельным купированием без применения лекарственных препаратов. У 1 (0,36%) ребенка вакцинация Акт-ХИБ сопровождалась местной реакцией в виде легкой, локализованной в месте инъекции гиперемии, без инфильтрации и других признаков воспаления, не сопровождавшаяся жалобами и не требовавшая терапии. У остальных 267 (96,38%) привитых детей поствакцинальный период протекал гладко и не требовал обращения за медицинской помощью. Из 141 ребенка, привитого вакциной Акт-ХИБ вне сочетания с другими препаратами, у одного (0,71%) отмечалось кратковременное (менее суток) повышение температуры тела до 37,50 и недомогание. Из 136 детей, которые вакцинировались Акт-ХИБ в различных комбинациях с другими прививками, у 8 (5,8%) отмечались общие реакции. У одного ребенка (0,74%) отмечалось недомогание (менее суток) без повышения температуры, у 7 (5,1%) детей зарегистрировано повышение температуры тела до 37,60 в течение 24-36 часов. У двух детей в течение первого дня после вакцинации наблюдали раздражительность, у одного недомогание. При бактериологическом исследовании отделяемого из носоглотки в период до вакцинации было выделено 155 штаммов H. influenzae - от 201 обследованного (77,1%), в том числе типа b гемофильной палочки - 62 штамма. Уровень ХИБ-носительства в наблюдаемых закрытых детских учреждениях составил 30,8%, отдельно по каждому СДР -17,5%, 26,7% и 51,7% (рис. 1).
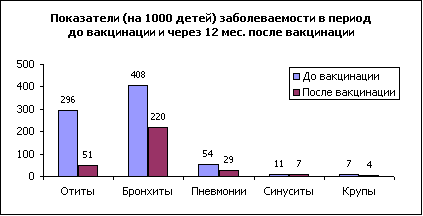
Через 6 месяцев после вакцинации АКТ-ХИБ у наблюдаемых детей было выделено 19 штаммов ХИБ. Уровень носительства составил 9,3%, что в 3,3 раза (р Некоторые биохимические свойства определялись с одинаковым постоянством у всех ХИБ-штаммов. Так, 100% штаммов разлагали глюкозу и образовывали фосфатазу, 100% не разлагали сахарозу, не образовывали липазу, бетагалактозидазу, пролинариламидазу, гаммаглутамилтрансферазу. Вариабельность ряда свойств ХИБ-штаммов свидетельствует о сложности идентификации культур рутинными методами и необходимости использования системы api-NH. На основании биохимических свойств (продукции индола, уреазы и орнитиндекарбоксилазы) H. influenzae дифференцируется на 8 биотипов, определение которых имеет эпидемиологическое значение. Среди изученных нами штаммов встречались все биотипы. Наиболее высокий удельный вес приходится на I-III биотипы. Соответственно, в довакцинальный период - 47,5%, в поствакцинальный период - 63,2%, за счет увеличения в 2,5 раза (р Чувствительность к антибиотикам была изучена к 17 препаратам на стрипах atb-NH. ХИБ-штаммы, выделенные в довакцинальный и поствакцинальный периоды, в 100% случаев чувствительны только к цефотаксиму, гентамицину, рифампицину. В поствакцинальный период увеличился до 100% удельный вес штаммов, чувствительных к следующим антибактериальным препаратам: амоксициллину/клавуланату, цефаклору, цефуроксиму, хлорамфениколу, тетрациклину, пристинамицину, розоксацину; значительно снизился удельный вес штаммов резистентных к амоксициллину (с 54,4% до 16,6%, р В довакцинальный период к эритромицину умеренно устойчивы 52,2% штаммов, все остальные чувствительны, а в поствакцинальный период соответственно 75% (рИ только к одному из 17 изученных препаратов - котримоксазолу выявлено увеличение доли резистентных штаммов с 21,7% до 41,7% (рНи у одного из выделенных штаммов на всем протяжении исследований не выявлена пенициллиназа. Таким образом, установлен высокий уровень ХИБ-носительства (30,8%) в закрытых детских учреждениях, сформированный популяцией полирезистентных к антибактериальным препаратам штаммов. После проведения полного курса вакцинации Акт-ХИБ уровень назофарингиального ХИБ-носительства резко снижается (с 30,8% до 9,3%, рС применением стандартной методики [2] по результатам ежемесячного учета и анализа случаев заболеваемости у наблюдавшихся пациентов была определена профилактическая эффективность вакцины Акт-ХИБ. Общее число случаев заболеваний за год до вакцинации у 277 привитых составило 228 (82%), из них на отиты приходилось 82 (36%) случая, бронхиты - 126 (55%) случаев, пневмонии - 15 (7%) случаев, синуситы - 3 (1%) случая, крупы - 2 (1%) случая (рис.2). Изучение спектра заболеваний через год после вакцинации показало, что общее число инфекционных заболеваний респираторного тракта и ЛОР-органов снизилось в 2,7 раза (с показателя 823,1 на 1000 детей до 310,3, р При сравнении показателей заболеваемости через 1 год у привитых после проведения полного курса вакцинации и в группе непривитых детей индекс эпидемиологической эффективности вакцинации Акт-ХИБ составил 2,2 (pТаким образом, результаты проведенного исследования показали хорошую переносимость, низкую реактогенность и высокую профилактическую эффективность вакцины Акт-ХИБ в группах детей с поражениями ЦНС.
Литература: © Л.М. Куртасова, Л.А. Рузаева, А.А. Двоеконко, Г.А. Зарянко, Н.Н. Опейкина, В.А. Третьякова, Н.А. Шакина, С.В. Ященко, 2003 |
Комментарии
ПРАКТИКА ПЕДИАТРА